空心锌铬铁氧体/二氧化钛复合物的制备及去污性能
2016-11-23孙代红刘华荣李睿哲
孙代红,刘华荣,李睿哲
(长江大学化学与环境工程学院,荆州434020)
空心锌铬铁氧体/二氧化钛复合物的制备及去污性能
孙代红,刘华荣,李睿哲
(长江大学化学与环境工程学院,荆州434020)
以葡萄糖溶液为原料,通过水热法制备了分散性良好的碳微球;以碳微球为模板,应用化学沉淀法和热处理技术除去碳核获得空心铬锌铁氧体;用钛酸四丁酯作为钛源,在空心铁氧体表面包覆二氧化钛制备了锌铬铁氧体/二氧化钛二元复合物.采用现代分析技术表征了制备样品的微观结构、形貌和电磁性能,并对其吸附和降解染料废水的性能进行了研究.结果表明,ZnCr0.25Fe1.75O4对染料废水具有较好的去污效果,对甲基橙和罗丹明B的去污效率分别为87%和83%;TiO2对铁氧体的包覆能提高复合物对染料废水的光催化降解性能,其中mT/ZCF=0.3的ZnCr0.25Fe1.75O4/TiO2复合物的去污效果最佳,几乎与纯二氧化钛相仿.
空心铁氧体;二氧化钛;光催化;甲基橙;罗丹明B
随着社会经济的快速发展,一系列环境问题也随之而来,其中,染料废水(主要源于染料生产、印刷及印染等产业)对水域环境造成了严重污染.通过高效的光催化剂降解有机物(染料)是解决此类问题的有效方法.研发效率高、能耗低、稳定性好、操作简单且易回收利用的催化剂是一项具有挑战性的工作.纳米磁性材料具有密度小、比表面大、在液体中分散性好及易分离回收等特点,尤其是空心球可容纳其它客体,从而产生一些新奇的特性,因此在催化、传感、药物传导、电磁屏蔽及电磁学等领域[1~7]具有广泛的应用前景.研究表明,Co或氧化钴空心球对反铁磁体的剩余磁化强度具有很强的冷却效应[8];CoFe2O4基复合物有较好的电磁波吸收效果[9];空心的Fe2O3粒子[10,11]和ZnFe2O4[12,13]作为光催化剂在环境保护领域具有潜在的应用前景.
纳米结构的半导体,尤其是锐钛矿相TiO2,因具有无毒副作用、稳定性好、成本低和优良的光催化效果等特性,而被广泛应用于染料[14,15]和其它有机污染物的降解,是目前颇具应用前景的光催化材料[16].制备稳定、催化活性高的纳米颗粒的关键因素之一是将其制成颗粒或胶质悬浮状,而这种稳定性也导致催化过程结束后难分离的问题[17].一种简单的解决方法是将TiO2与磁性物质复合,在光催化过程结束后通过磁分离技术回收催化剂.据文献[18,19]报道,由TiO2与磁性纳米颗粒形成的核⁃壳结构的复合物用作光催化剂具有较好的催化效果.基于上述研究结果,空心铁氧体除具有普通空心球类材料的吸附特性外,还因其特有的磁性在光催化领域将获得特殊的应用.如果将磁性的铁氧体空心球与光催化活性高的半导体氧化物复合,生成的复合物不仅具有优良的吸附与光催化活性,而且易于回收和重复使用.本文以碳微球为模板,通过共沉淀法制备了空心铁氧体ZnCrxFe2-xO4(x=0.25,0.50,0.75,1.00),并进一步制备二氧化钛复合物ZnCrxFe2-xO4/TiO2;表征了样品的结构、形貌、比表面积和磁性能;将其用于处理模拟染料废水,不仅处理效率较高,而且方便回收和重复利用.
1 实验部分
1.1 试 剂
葡萄糖、九水合硝酸铁、九水合硝酸铬、六水合硝酸锌、氨水、无水乙醇、十六烷基三甲基溴化铵
(CTAB)、环己烷、正戊醇、硝酸和钛酸正四丁酯均为分析纯,购于上海国药(集团)化学试剂有限公司.
1.2 样品的制备
1.2.1 碳微球的制备 取4.2 g葡萄糖溶于40 mL蒸馏水,超声5 min,搅拌溶液至透明;转移到50 mL内衬聚四氟乙烯不锈钢反应釜中,于180℃反应8 h.冷却至室温,离心,分别用蒸馏水和无水乙醇洗涤至滤液呈无色.于60℃真空干燥至恒重,得到棕黑色碳微球.
1.2.2 空心ZnCrxFe2-xO4的制备 取0.2975 g(1 mmol)Zn(NO3)2·6H2O,按ZnCrxFe2-xO4(x=0.25,0.50,0.75,1.00)的化学计量比称取相应量的Fe(NO3)3·9H2O和Cr(NO3)3·9H2O,溶于36 mL乙醇/水溶液(体积比为3∶1)中,强力搅拌至溶液透明,再加入0.3 g尿素和0.1 g自制的碳微球,超声30 min.于60℃回流24 h,冷至室温后,缓慢滴加0.1mol/L NaOH溶液至pH≈10,搅拌数小时,陈化3 h;离心分离,用蒸馏水和乙醇交替洗涤至滤液呈中性;于60℃真空干燥至恒重,于550℃煅烧3 h,得棕黑色目标产物.
1.2.3 ZnCr0.25Fe1.75O4/TiO2(ZCF/T)复合物的制备 将0.2401 g(1 mmol)空心ZnCr0.25Fe1.75O4分散到由0.6 g CTAB、6mL环己烷和0.5mL戊醇组成的微乳液体系中,转移至250mL三颈烧瓶中,再加入1mL蒸馏水,超声5~10min,用硝酸调节pH=5~6,搅拌均匀得混合溶液A;按TiO2∶ZnCr0.25Fe1.75O4质量比(mT/ZCF)分别为0.1(1∶10,下同),0.2,0.3,0.4和0.5称取一定质量的钛酸正四丁酯Ti(OBu)4,溶于20 mL乙醇溶液中得溶液B;将溶液B缓慢滴加至混合溶液A中,搅拌数小时,用磁铁分离,弃去上层清液;固相产物用乙醇洗涤至滤液呈中性,于60℃真空干燥至恒重,于500℃煅烧2 h,即得mT/ZCF为0.1~0.5的ZCF/T复合物.
1.3 样品表征
采用Philps⁃PW3040/60型X射线衍射仪(Cu Kα射线,λ=0.15418 nm)测定样品的物相结构;用Varian ICP⁃OES720型元素分析仪分析样品的元素含量;用Hitachi S⁃4800扫描电子显微镜(SEM,电压50 kV)和JEOL⁃2000型透射电子显微镜(TEM,电压200 kV)观察样品的表面形貌和粒子的尺寸分布;用NEXUS⁃670 FTIR红外光谱仪和Renishaw RM 1000显微共焦拉曼光谱仪测定样品的红外光谱(KBr压片,扫描范围400~4000 cm-1)和拉曼光谱(k=632.8 nm,扫描范围200~2000 cm-1);用Solidspec DUV⁃3700漫反射光谱仪记录样品的紫外光谱;用Lakeshore7404型振动样品磁强计检测样品的饱和磁化强度、矫顽力等电磁参数;用UV⁃2501PC型紫外分光光度计测试废水溶液处理前后的紫外吸收值,计算出处理剂的去污性能.
1.4 去污实验
取100mL一定浓度的待处理废液,加入25mg的催化剂,先避光搅拌0.5 h,然后在可见光(高压汞灯)照射下,持续搅拌,每隔一段时间取出3mL降解液,测试其浓度变化.过滤分离出催化剂,经水洗、干燥,回收备用.
甲基橙溶液的吸光度与浓度满足方程式:y=0.0761x+0.0055[R2=0.9999,y表示溶液的吸光度,x(mg/L)表示溶液的浓度,吸光度为1时该溶液浓度约为12.5 mg/L].罗丹明B溶液满足方程式:y=0.2007x+0.0085(R2=0.9991),吸光度为1时该溶液浓度约为5 mg/L.
为了便于比较,TiO2的光催化实验在紫外光照射下进行.
2 结果与讨论
2.1 X射线衍射分析
表1列出了所制备样品的化学组成,可见样品中元素含量的测定值与理论值(括号中)较吻合,误差≤1.5%,表明所制备样品的组成符合预期的化学计量.
图1为ZnCrxFe2-xO4,ZCF,TiO2和ZCF/T复合物的XRD谱图.图1(A)中,2θ=18.21°,30.17°,35.52°,43.17°,53.53°,57.06°和62.76°处的衍射峰与尖晶石型ZnFe2O4的标准谱图(JCPDSCARD No.22⁃1012)相吻合,并分别与(111),(220),(311),(400),(422),(511)和(440)晶面相对应,说
明所制备样品均为单一的尖晶石相.图1(B)中,除了有ZCF的衍射峰(方块标记)处,还观察到2θ=25.38°,37.82°,48.07°,53.94°,55.05°,62.74°,70.34°,75.16°和82.31°处TiO2的特征峰(三角形标记),分别对应于(101),(004),(200),(105),(211),(204),(220),(215)和(303)晶面(JCPDSCARD No.21⁃1272).此外,还可以观察到复合物中TiO2的衍射峰强度与其相对含量呈正相关,且其衍射峰略向2θ减小的方向移动,表明其晶面间距变大,这是由于TiO2最强峰对应的晶面间距约为0.351 nm,而铁氧体最强峰对应的晶面间距约为0.254 nm,故随着TiO2含量的增加,复合物的衍射峰向低角度偏移.

Table 1 Chem ical com ponent of as⁃prepared sam p les∗

Fig.1 XRD patterns of ZnCrxFe2-xO4(x=0.25,0.50,0.75,1.00)(A)and ZCF(a),TiO 2(b)and ZCF/T com positesw ith mT/ZCF=0.1,0.2,0.3,0.4,0.5(c—g)(B)
图2所示XPS谱图表明,ZCF/T复合物中存在Zn,Fe,Cr,Ti和O元素,而C元素则来自于仪器本身.位于1020.3和1043.1 eV处的峰归属于Zn2+的2p3/2和2p1/2;710.5和724.3 eV处的峰归属于Fe3+的2p3/2和2p1/2的结合能;573和584 eV处的峰归属于Cr3+的2p3/2和2p1/2的结合能,而458.7和464.3 eV处的峰则是Ti4+的2p3/2和2p1/2的结合能.
2.2 样品的微观形貌
图3为碳微球、ZnCr0.25Fe1.75O4和ZCF/T复合物的SEM和TEM照片.由图3(A)和(E)可见,碳微球表面略显粗糙,尺寸约为500~600 nm,有较好的均一性和分散性.由图3(B)和(F)可知,铁氧体粒子呈球形,其中大的粒子是由30~50 nm微粒构成的团聚体,部分空心结构清晰可见[见图3(B)插图].由图3(C)和(G)可见,复合物中ZnCr0.25Fe1.75O4粒子的颜色较深(其吸电子能力比TiO2强),浅色的TiO2对ZnCr0.25Fe1.75O4有较好的包覆效果;由于磁性粒子的相互作用,复合物有一定程度的团聚.由元素分布的Mapping图[图3(H—L)]可推测复合物中存在O,Ti,Cr,Zn和Fe元素,其含量与理论值基本相符,其中O的含量最大,Cr的含量最小.另外,由图3(D)可见,ZnCr0.25Fe1.75O4包覆碳微球的未烧结样品是由许多ZnCr0.25Fe1.75O4纳微米颗粒包覆在碳微球上,尺寸约为600~700 nm,表面比碳微球更粗糙,经烧结后部分粒子成空心球,也有部分粒子的发生了坍塌[图3(B)].
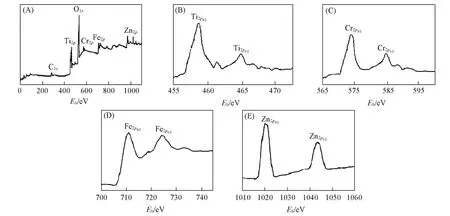
Fig.2 XPS spectra of the ZCF/T Composite

Fig.3 SEM and TEM images of carbon m icroballoons(A,E),ZnCr0.25Fe1.75O4(B,F)and ZCF/T composite with mT/ZCF=0.3(C,G),unsintered C/ZnCr0.25Fe1.75O4(D)and elem ent mapping of ZCF/T composite with mT/ZCF=0.3(H—L)
2.3 红外和拉曼光谱分析
ZnCr0.25Fe1.75O4和mT/ZCF=0.3的ZCF/T复合物的红外和拉曼光谱示于图4.由图4(A)可知,3430 和1630 cm-1处的峰对应于O—H的伸缩振动[20,21],表明样品含有少量的吸附水和残留羟基;尖晶石铁氧体通常有2个位于600~550和450~385 cm-1处的固有的M—O伸缩振动,分别与四面体位和八面体位的M—O相对应[22],因此570和416 cm-1处的2个峰应分别归属为ZnCr0.25Fe1.75O4中四面体位和与
八面体位M—O伸缩振动;位于466 cm-1处的峰对应于TiO2中Ti—O—Ti的伸缩振动;在ZCF/T复合物的IR谱图中,能观察到ZnCr0.25Fe1.75O4和TiO2的特征吸收,且略有蓝移,表明复合物中TiO2和ZnFe2O4存在一定的相互作用,并不是2个组分的简单混合.由图4(B)可知,ZnCr0.25Fe1.75O4在100~800 cm-1范围有5个峰,分别为204 cm-1(F2g),242 cm-1(Eg),324 cm-1(F2g),486 cm-1(F2g)和645 cm-1(A1g),其中,645 cm-1处的峰被指认为AO4四面体单元的特征峰,其余4个为BO6八面体单元的特征峰[23];位于145 cm-1(Eg),401 cm-1(B1g),519 cm-1(A1g)和629 cm-1(Eg)为锐钛型TiO2的4个特征吸收峰[24,25];这也能证实复合物是由ZnCr0.25Fe1.75O4和TiO2形成的.
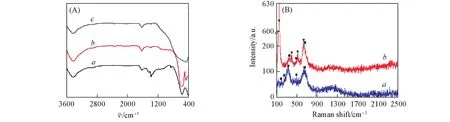
Fig.4 FTIR spectra(A)and Raman spectra(B)of ZnCr0.25Fe1.75O4(a),ZCF/T Composite with mT/ZCF=0.3(b)and TiO2(c)
图5为ZnCr0.25Fe1.75O4和mT/ZCF=0.3的ZCF/T复合物在室温及外加磁场为±2×106A/m下的磁滞回线.众所周知,饱和磁化强度Ms是代表样品磁性强弱的宏观物理量,它的大小与样品粒子的微观结构有关.Fe和Cr为磁性金属,Zn为非磁性金属,ZnCr0.25Fe1.75O4铁氧体的磁性强弱与原子(离子)中价层的单电子数、金属离子的占位、样品的微观形貌、结构和致密度等密切相关.由图5可知,ZnCr0.25Fe1.75O4的Ms比ZCF/T复合物的大,而矫顽力(Hc)变化不大.通常情况下,复合物的Ms主要取决于其中磁性组分的含量[26](Ms=φms,φ为磁性粒子的体积分数,ms为单个磁性粒子的饱和磁矩).复合物中ZnCr0.25Fe1.75O4的含量相对较小,TiO2的包覆对ZnCr0.25Fe1.75O4的磁性起到了稀释作用,故其饱和磁化强度比母体的低.复合物具有一定的磁性,为其在应用过程中的回收和循环使用提供了便利.
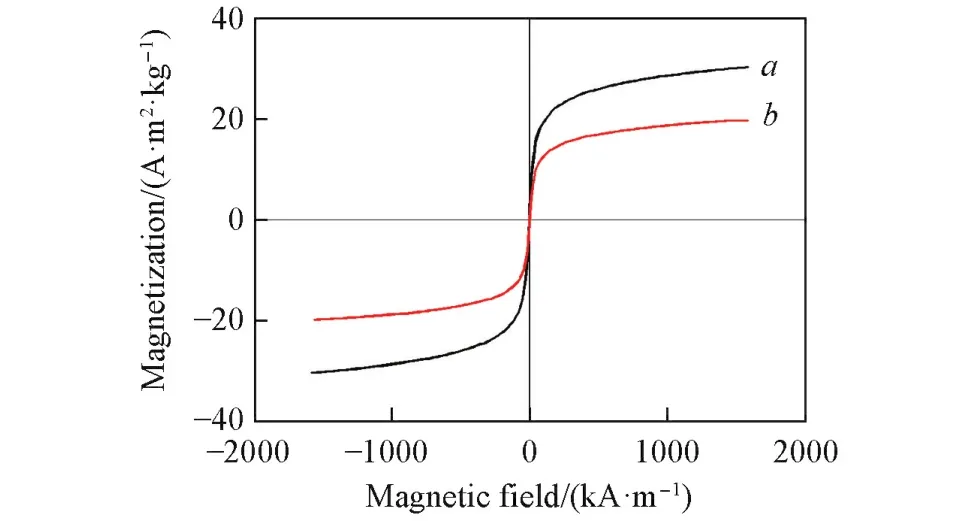
Fig.5 Hysteresis loop patterns of ZnCr0.25Fe1.75O4(a)and mT/ZCF=0.3 ZCF/T Composites(b)at room temperature
矫顽力Hc表示改变物质磁化方向所需要的场强,受各项异性常数、饱和磁化强度、晶粒尺寸、晶格应力、晶体表面和内部的缺陷等因素的影响.本实验样品的矫顽力变化不大,其中ZnCr0.25Fe1.75O4比复合物的略大,这可能与样品的磁晶各向异性有关.
2.4 样品的去污性能
样品的去污性能包括吸附污染物和光催化降解污染物的能力,前者与样品的空洞、孔隙和比表面积有关,而后者则与样品在光照下产生的光生电子、光生电子空穴、组分间的界面作用及其缺陷等有关.
2.4.1 ZnCrxFe2-xO4的去污性能 图6反映了ZnCrxFe2-xO4(x=0.25,0.50,0.75,1.00,样品1~4)对甲基橙(MO)和罗丹明B(RhB)溶液的去污性能.由图6可知,样品在0.5 h内(避光搅拌)的去污活性较大,主要表现为吸附作用;随着光照时间的增加,样品的去污活性逐渐减小,至3 h基本达到平衡,该阶段主要表现为对污染物的光催化降解.样品的去污效果的顺序为样品1>样品2>样品3>样品4,活性最好的是ZnCr0.25Fe1.75O4,其对甲基橙和罗丹明B的降解率分别达87%和83%.在ZnCrxFe2-xO4系
列样品中,ZnCr0.25Fe1.75O4对于2种染料都具有最佳的去污效果,这可能与其比表面积呈正相关(表2).因此,选用ZnCr0.25Fe1.75O4制备ZCF/T复合物.

Fig.6 Removal effect of ZnCrxFe2-xO4on time for MO(A)and RhB(B)solutions
图7示出了回收的ZnCr0.25Fe1.75O4对2种染料废水的去污性能.可见,当催化剂使用4次后,它们对甲基橙和罗丹明B的去污活性变化较小,分别保持在82%和75%左右,表明所制备的铁氧体是一种高效、稳定的催化剂.
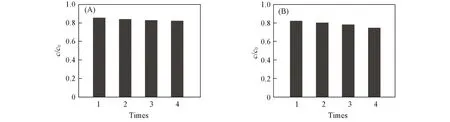
Fig.7 Removal effect of recyclable ZnCr0.25Fe1.75O4for MO(A)and RhB(B)solutions
2.4.2 ZCF/T复合物的去污性能 分别考察了TiO2含量、溶液pH、反应时间、煅烧温度和循环次数对ZCF/T复合物去污性能的影响.
图8给出了mT/ZCF=0.1~0.5的ZCF/T复合物(分别对应样品1~5,TiO2(6)和ZnCr0.25Fe1.75O4(7)对MO和RhB溶液的去污性能(复合物生成条件:水解反应12 h,pH=5~6,煅烧温度500℃).由图8可见,ZCF/T复合物的去污活性均比ZnCr0.25Fe1.75O4高,且随着TiO2含量的增加呈先增大后减小的变化趋势,其中mT/ZCF=0.3的ZCF/T复合物对MO和RhB溶液的去污效果最好,均大于93%,与纯TiO2的相当.这可能是由于随着TiO2含量的增加,复合物的光催化活性增强;而当TiO2含量继续增大,可能会部分堵塞铁氧体的空心孔,导致其平均孔径和比表面积减小(表2),综合各种因素,mT/ZCF=0.3 的ZCF/T复合物具有最好的去污效果.此外,在ZCF/T复合物的界面处ZnCr0.25Fe1.75O4和TiO2会生成异质结,进而生成的晶格缺陷(带电缺陷)具有稳定e和h+的作用,因而也能提高其光催化作用.界面处发生的缺陷反应如下:

生成的带电缺陷具有稳定光生e和h+的作用,同时空位缺陷能增加对光的传导和响应,因而能提高ZCF/T复合物的光催化活性.综合吸附和光催化降解作用,ZCF/T复合物的去污效果比
ZnCr0.25Fe1.75O4好,mT/ZCF=0.3的复合物具有最佳的去污效果.

Fig.8 Removal effect of ZnCr0.25Fe1.75O4,ZCF/T composites and TiO2on time for MO(A)and RhB(B)solutions

Table 2 Average pore size and specific surface area of samp les
图9示出了pH对mT/ZCF=0.3的ZCF/T复合物去污性能的影响.可见,反应溶液的pH对复合物的光催化活性影响不大;当pH=6时,复合物去污效果相对较好,Ti(OBu)4的水解更完全.
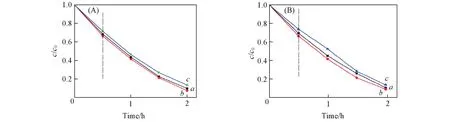
Fig.9 Removal effect of ZCF/T Composite with mT/ZCF=0.3 on pH value for MO(A)and RhB(B)solutions
Ti(OBu)4的水解时间对mT/ZCF=0.3的ZCF/T复合物去污效果的影响如图10所示.可见,水解时间为12 h的复合物的光催化活性最佳,这可能是因为反应12 h时Ti(OBu)4几乎完全水解,TiO2对ZnCr0.25Fe1.75O4的包覆较好,且异质结处的界面相互作用较大;随着反应时间的增长,可能会有部分TiO2粒子填充到ZnCr0.25Fe1.75O4的孔隙中,复合物的比表面积有所减小,导致去污性能反而会减弱.
不同烧结温度制备的mT/ZCF=0.3的ZCF/T复合物的去污性能如图11所示.当温度高于500℃,复合物去污活性几乎不变,这可能是因为当煅烧温度达到500℃时,复合物的晶型趋于完整,ZnCr0.25Fe1.75O4与TiO2间的界面相互作用可能达到最大,继续升高温度对复合物的晶型和界面相互作用影响不大,故其光催化活性也几乎不变.
图12给出了mT/ZCF=0.3的ZCF/T复合物对甲基橙和罗丹明B溶液的循环去污效果及复合物的回收示意图.可见,当复合物循环使用达到第4次时,其活性与第1次相比仅减小约10%,说明该催化剂不仅活性高,而且重复使用性能稳定.与TiO2相比,ZCF/T复合物的磁性为其回收和循环使用提供了极大的便利,不仅节省了回收时间,而且催化剂多次循环使用降低了处理废水的成本,减小了催化剂对环境的污染,其经济意义十分明显.
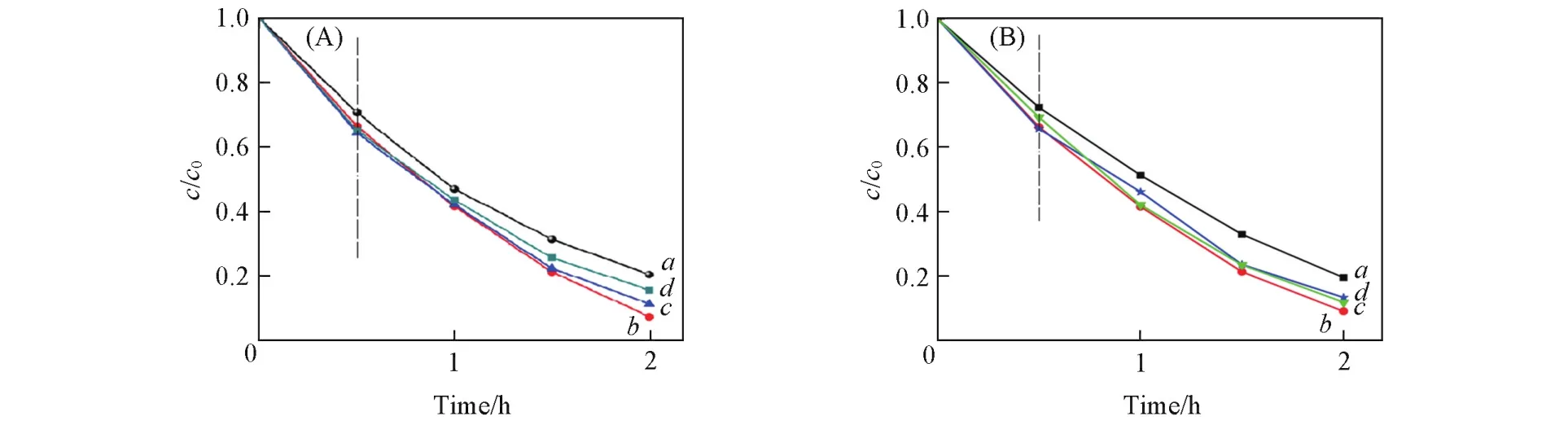
Fig.10 Removal effect of ZCF/T composite with mT/ZCF=0.3 on hydrolysis time for MO(A)and RhB(B)solutions

Fig.11 Removal effect of ZCF/T Composite with mT/ZCF=0.3 on sintering temperature for MO(A)and RhB(B)solutions

Fig.12 Removal effect of ZCF/T Composite with mT/ZCF=0.3 on cycle num bers for MO(A)and RhB (B)solutions and recycled schematic diagram[RhB solution before(C)and after(D)by ultraviolet treatm ent and recycled Composite by an externalm agnet(E)]
值得提及的是,与其它研究报道[[27~29]相比,本文的创新点主要表现在制备的样品具有空心球结构,并能在可见光下应用,且比海绵状ZnFe2O4[30]有更好的去污效果.
2.5 催化剂的去污机理
样品的去污机制包括吸附和光催化降解机制.吸附机制主要与样品的空洞、孔隙及比表面积等因
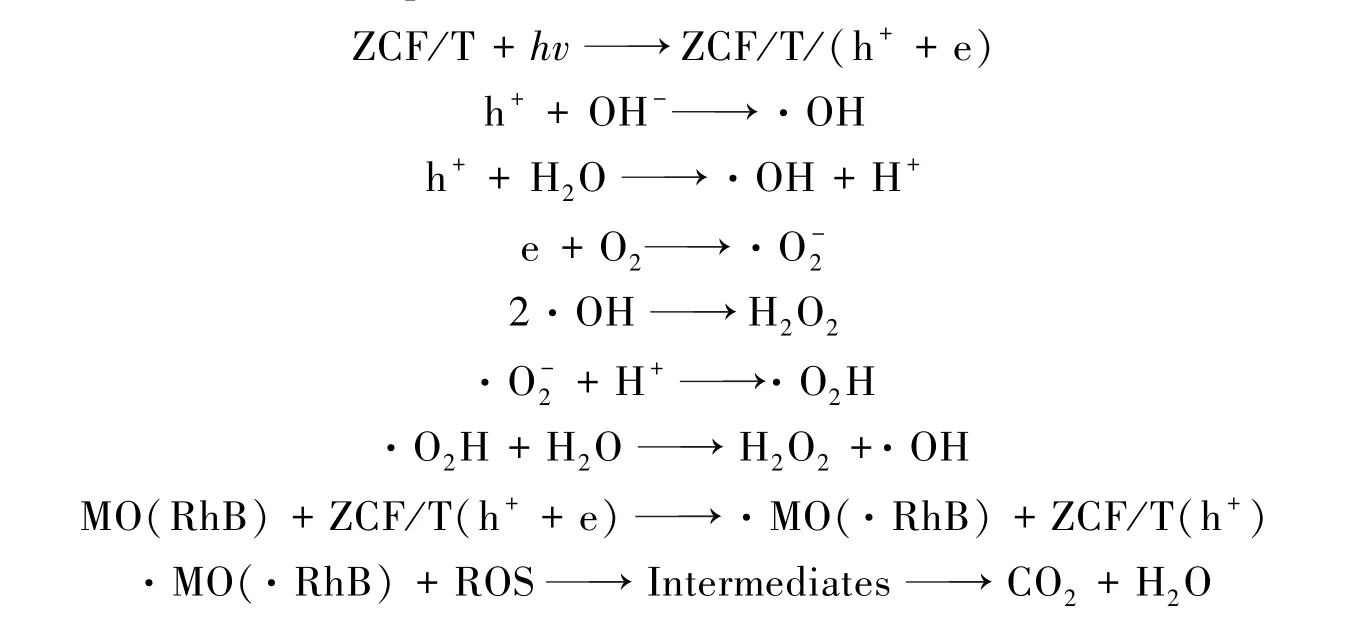
素有关;而光催化降解机制主要与样品产生的光生电子、光生电子与晶格缺陷等相关.样品的光催化机制可阐述如下:在可见光的作用下,ZnCrxFe2-xO4表面产生光生电子(e)和光生电子空穴(h+),e和h+与H2O和O2作用生成羟基自由基(·OH)、超氧阴离子(·O-2)和H2O2等活性氧微粒(ROS),这些强氧化性的 ROS能将 MO(RhB)逐渐降解,最终转化为 CO2和 H2O.在 ZCF/T复合物中,由于ZnCr0.25Fe1.75O4与TiO2之间的相互作用在其界面处产生晶格缺陷,这种缺陷可稳定光生电子e和光生空穴h+,因而会增强其光催化活性.尽管复合物中TiO2的含量小于纯TiO2,但由于复合物具有稳定e 和h+的作用,故其光催化活性和TiO2几乎相近.由此推断可能的光催化机理[31,32]为:
3 结 论
以葡萄糖为原料,制备了尺寸均一、分散性较好的碳微球,并以此微球为模板,应用化学沉淀法及热处理技术制备出一系列锌铬铁氧体ZnCrxFe2-xO4;用钛酸四丁酯作为钛源,合成了ZCF/T复合物.采用现代测试技术表征了样品的结构、形貌和磁性能.去污实验结果表明,ZnCr0.25Fe1.75O4和ZCF/T复合物对染料废水都具有较好的吸附和光催化降解活性;TiO2含量对ZCF/T复合物的光催化活性影响较大,而反应时间、溶液的pH值及煅烧时间的影响则相对较小.mT/ZCF=0.3的ZCF/T复合物的去污效果与纯TiO2相近,且回收方便、重复使用性能稳定,是具有较大潜在应用前景的废水处理剂.
[1] Hyuk I.S.,Jeong U.,Xia Y.,Nat.Mater.,2005,4,671—678
[2] LiM.J.,Xu X.,Tang Y.,Guo Z.N.,Zhang H.A.,Zhang H.,Yang B.,Colloid Interface Sci.,2010,346,330—336
[3] Chen X.Y.,Ma C.,Bao S.P.,Colloid Interface Sci.,2010,346,8—15
[4] Liu X.R.,Hou C.M.,Yuan L.,Liu S.K.,Qin Y.Y.,Huang K.K.,Feng S.H.,Chem.J.Chinese Universities,2013,34(2),277—283(刘宪瑞,侯长民,袁龙,刘绍孔,秦圆圆,黄科科,冯守华,高等学校化学学报,2013,34(2),277—283)
[5] Victor F.P.,Kannan M.K.,Paul A.,Science,2001,291,2115—2121
[6] Pan Z.W.,Dai Z.R.,Wang Z.L.,Science,2001,291,1947—1953
[7] Zhao H.T.,Wang Q.,Liu R.P.,Ma R.T.,Chem.J.Chinese Universities,2016,37(4),613—618(赵海涛,王俏,刘瑞萍,马瑞廷.高等学校化学学报,2016,37(4),613—618)
[8] Yoshikawa H.,Hayashida K.,Kozuka Y.,Horiguchi A.,Awaga K.,Bandow S.,Iijima S.,Appl.Phys.Lett.,2004,85,5287—2594
[9] Xu F.,Xiang C.,Li L.C.,Mao M.Y.,Zhou Y.,Ding Y.,Li J.B.,Chem.J.Chinese Universities,2013,34(10),2254—2261(许峰,向晨,李良超,毛梦怡,周琰,丁艳,李涓碧.高等学校化学学报,2013,34(10),2254—2261)
[10] Ohmori T.,Takahashi H.,Mametsuka H.,Suzuki E.,Chem.Chem.Phys.,2000,2,3519—3525
[11] Brown A.S.S.,Hargreaves J.S.J.,Rijniersce B.A.,Catal.Lett.,1998,53,7—10
[12] Xu X.J.,Zhou L.H.,Zhai Q.G.,Lu C.Z.,Am.Ceram.Soc.,2007,90,1959—1965
[13] Li Z.M.,Lai X.Y.,Wang H.,Mao D.,Xing C.J.,Wang D.,Phys.Chem.C,2009,113,2792—2799
[14] Libanori R.,Giraldi T.R.,Longo E.,Leite E.R.,Ribeiro C.,Sol⁃gel.Sci.Technol.,2009,49,95—101
[15] Malagutti A.R.,Mourao H.A.J.L.,Garbin J.R.,Ribeiro C.,Environ.,2009,90,205—212
[16] Tryk D.A.,Fujishima A.,Honda K.,Electrochim.Acta,2000,45,15—20
[17] Mourao H.A.J.L.,Malarutti A.R.,Ribeiro C.,Appl.Catal.A:General,2010,382,284—291
[18] Ung T.,Liz⁃Marzan L.M.,Mulvaney P.,Phys.Chem.B,2001,105,3441—3447
[19] Chang S.Y.,Liu L.,Asher S.A.,Am.Chem.Soc.,1994,116,6745—6751
[20] Bahout M.M.,Bertrand S.,Pena O.,J.Solid State Chem.,2005,178,1080—1086
[21] Maensiri S.,Masingboon C.,Boonchom B.,Eraphin S.,Scripta Mater.,2007,56,797—800
[22] Florea M.,AlifantiM.,Parvulescu V.I.,Tarabasanu D.M.,Diamandescu L.,Feder M.,Negrila C.,Frunza L.,Catal.Today,2009,141,361—366
[23] Wang Z.W.,Schiferl D.,Zhao Y.S.,O'Neill H.S.C.,J.Phys.Chem.Solids.,2003,64,2517—2523
[24] Saepurahman,Abdullah M.A.,Chong F.K.,J.Hazard.Mater.,2010,176,451—458
[25] Horikoshi S.,Abe M.,Sato S.S.,J.Photochem.Photobiol.,A:Chem.,2011,220,94—101
[26] Chen Y.Y.,Shen J.H.,KongW.Q.,Li L.C.,Chinese J.Inorg.Chem.,2015,31,243—252(陈瑶瑶,沈俊海,孔卫秋,李良超.无机化学学报,2015,31,243—252)
[27] Zhu C.Q.,Li Y.R.,Su Q.,Lu B.G.,Pan J.Q.,Zhang J.W.,Xie E.Q.,Lan W.,J.Alloys Compd.,2013,575,333—338
[28] Jiang Z.F.,Jiang D.L.,Yan Z.X.,Liu D.,Qian K.,Xie J.M.,Appl.Catal.B:Environ.,2015,170/171,195—205
[29] HabibiM.H.,Habibi A.H.,J.Ind.Eng.Chem.,2014,20,2964—2968
[30] Zhu X.D.,Zhang F.,Wang M.J.,Ding J.J.,Sun S.,Applied Surf.Sci.,2014,319,83—89
[31] Su M.H.,He C.,Sharma V.K.,AsiM.A.,Xia D.H.,LiX.Z.,Deng H.Q.,Xiong Y.,J.Hazard.Mater.,2012,211/212,95—103
[32] Casbeer E.,Sharma V.K.,Li X.Z.,Sep.Purif.Technol.,2012,87,1—14
Preparation and Decontam ination Capability of Hollow Zn⁃Cr Ferrite/Titanium Dioxide Composites†
SUN Daihong∗,LIU Huarong,LIRuizhe
(College ofChemistry and Environmental Engineering,Yangtze University,Jingzhou 434020,China)
Homogeneous and dispersive carbon nanosphere was synthesized by hydrothermal method using glucose as the material.Hollow Cr⁃Zn ferrite was prepared by coprecipitation method and thermal treatment technology using carbon sphere as template.Ferrite/titanium dioxide composites were obtained by coating titanium dioxide on the ferrite using tetrabutyltitanate as titanic source.The structure,morphology,electromag⁃netic performance of as⁃prepared samples and their absorptivity and degradability on dye wastewater were studied by modern analytical techniques.The results showed that the hollow ZnCr0.25Fe1.75O4has preferable photocatalytic property on dye wastewater,and its removal efficiency on methyl orange and Rhodamine B are about 87%and 83%,respectively.The coating of TiO2on the ferrite could improve photocatalytic activity of as⁃prepared sample,the ZnCr0.25Fe1.75O4/TiO2composite with 23.08%of TiO2content has excellent photo⁃catalytic activity,and is equivalent to pure TiO2.
Hollow ferrite;Titanium dioxide;Photocatalytic;Methyl orange;Rhodamine B
O647;TB34
A
10.7503/cjcu20160340
(Ed.:V,D,Z,K)
†Supported by the National Natural Science Foundation of China(No.21201023).
2016⁃05⁃16.
日期:2016⁃10⁃19.
国家自然科学基金(批准号:21201023)资助.
联系人简介:孙代红,男,副教授,主要从事污水处理等方面的研究.E⁃mail:sundaihong888888@163.com
