植物液泡膜Na+/H+逆向转运蛋白的研究与应用
2016-11-21任秀艳王宝增王聪艳侯志敏
任秀艳,王宝增,王聪艳,侯志敏
(1.廊坊师范学院 生命科学学院,河北 廊坊 065000; 2.河北省高校食药用菌应用技术研发中心,河北 廊坊 065000)
植物液泡膜Na+/H+逆向转运蛋白的研究与应用
任秀艳1,2,王宝增1,王聪艳1,侯志敏1
(1.廊坊师范学院 生命科学学院,河北 廊坊 065000; 2.河北省高校食药用菌应用技术研发中心,河北 廊坊 065000)
液泡膜Na+/H+逆向转运蛋白是植物体内广泛存在的一种跨膜转运蛋白,负责植物体内Na+、H+的交换。本文对Na+/H+逆向转运蛋白的克隆、分子结构、功能及应用等方面展开论述,旨在为研究者系统的理解Na+/H+逆向转运蛋白的研究进展,为调控该蛋白的表达来改进植物的生长发育及抗盐胁迫能力等方面的应用提供参考。
植物;液泡膜;Na+/H+逆向转运蛋白;耐盐性
当前农业生产所面临的逆境胁迫包括生物胁迫和非生物胁迫,其中非生物胁迫中最重要的是土壤的盐渍化。过多的盐分会对植物造成渗透压胁迫和离子胁迫[1]。植物在正常生长情况下,细胞质K+/Na+比例较高,其中K+浓度较高,可达100-200 mM,而Na+离子浓度相对较低,只有1-10 mM[2]。因此,细胞如何将胞质中多余的Na+有效的排出并将Na+积累到液泡中是植物适应盐胁迫的主要机制,这种机制称为Na+的区隔化,是植物在长期的进化过程中形成的。这种区隔化通常是由Na+/H+逆向转运蛋白 (Na+/H+antiporter or exchanger, NHX)通过和H+之间交换从细胞质中排除Na+,从而降低过多的Na+对细胞质的毒害,同时Na+也可作为一种有益的渗透调节剂来降低细胞的渗透压。大量研究表明,生物界普遍存在这种跨膜转运蛋白,主要负责植物体内Na+、H+的交换,维持细胞内外Na+浓度的相对稳定,调节胞内pH值,在植物抵抗盐胁迫中担负着重要角色[3]。
1 植物液泡膜Na+/H+逆向转运蛋白的发现及作用
1.1 植物Na+/H+逆向转运蛋白的发现
1985年,Blumwald和Poole在甜菜上发现了第一个植物液泡膜Na+/H+逆向转运蛋白[4],此后,该蛋白在不同类型植物上逐渐被报道,如盐生植物碱蓬[5](Suaedaheteroptera)、滨藜[6](Atriplexpatens)、冰叶日中花[7](Mesembryanthemumcrystallinum)、番杏[8](Tetragoniatetragonioides)、盐芥[9](Thellungiellasalsuginea)、车前[10](Plantagomaritime)等;较耐盐的甜土植物如大麦[11](Hordeumvulgare)、棉花[12](Gossypiumhirsutum)、玉米[13](zeamays)及拟南芥[14](Arabidopsisthaliana)等。可见,无论在原核生物、真核生物还是在高等动植物中均存在Na+/H+逆向转运蛋白,并且已经从多种生物中克隆到编码该蛋白的基因,同时对其结构和功能进行了深入研究。但Mennen[15]研究表明,并不是所有的耐盐植物细胞中都存在Na+/H+逆向转运蛋白,如在高度耐盐陆地棉(Gossipiumbirsutum)中没有检测到该蛋白活性。
1.2 液泡膜Na+/H+逆向转运蛋白在植物体内的主要功能
液泡是位于细胞中央的泡状结构,由膜包被。在细胞质中主要维持细胞内水分平衡,调节渗透压,是养料及多种代谢产物积累和贮存的场所,因此该细胞器具有避免有毒物质伤害细胞质的作用。同时,液泡也是植物成熟细胞中最大的细胞器,增加了细胞表面积与体积之比,可使细胞与环境之间进行充分的物质交换,有利于提高植物的耐盐性。
1.2.1 离子的区隔化及细胞质中离子稳态平衡的调节
植物维持自身正常生长发育过程中,体内Na+,K+和H+处于相对平衡的状态,保持一定的K+/Na+比例,Na+积累过多会对植物体造成伤害,因此,植物体必需将过多的Na+排除体外或区隔化到液泡中来减少对其自身的伤害。研究表明,植物细胞中多余Na+的区隔化到液泡主要由Na+/H+逆向转运蛋白来完成的[14,16,17],同时将H+从液泡转移到细胞质,具有调节细胞质内pH值和Na+浓度的功能[14,18],这个过程主要依靠液泡膜的两个质子泵H+-ATPase和H+-PPase产生的质子电化学势梯度来驱动完成[4,19]。植物体内Na+的区隔化不但避免了多的Na+对细胞内代谢相关酶类及膜系统造成伤害,而且区隔化到液泡的Na+可以促使细胞从外界环境中吸收水分来维持细胞的渗透平衡。可见,植物液泡膜Na+/H+逆向转运蛋白在离子区隔化及离子稳态平衡中发挥重要作用。
1.2.2 调节细胞液泡的pH
Na+区隔化到液泡的同时将液泡中的H+转运到细胞质中,增加了细胞质的pH。研究发现,日本牵牛(Ipomoeanil)中InNHX1基因的表达与液泡中pH及花的颜色密切相关,pH的改变直接影响花的颜色[20];当InNHX1基因发生突变时,液泡pH不变时,相应的花的颜色也没有变化。随后,对三色牵牛(Ipomoeatricolar)的研究发现,在花蕾阶段,其花瓣的pH为6.6,颜色为紫色,当花完全开放时,pH为7.7,颜色变为蓝色,而花瓣液泡膜H+-ATPase、H+-PPase和Na+/H+逆向转运蛋白的活性明显增强。这说明液泡膜pH变化和Na+/H+逆向转运蛋白有关的[21]。此外,Ohnishi等[22]2005年研究日本牵牛发现,InNHX2除了提高牵牛植株耐盐性外,对花瓣pH的调节也有一定作用。
1.2.3 影响植物组织器官的发育
Apse等2003年对拟南芥AtNHX1的缺失突变体nhx1研究发现,与野生型植株相比,突变体植株的总叶面积缩小、表皮细胞数量减少、Na+/H+和K+/H+交换活性降低,而将该基因转入突变体中并过量表达即可使植株基本恢复正常。可见,AtNHX1不但可以影响Na+/H+和K+/H+交换活性,还可以影响植物的生长发育[23]。
2 植物Na+/H+逆向转运蛋白的基因克隆及分子特征
2.1 植物Na+/H+逆向转运蛋白基因的克隆
高等植物中第一个克隆到的液泡膜Na+/H+逆向转运蛋白基因是拟南芥中的AtNHX1[14],此后,不断在其他高等植物中克隆到该基因(表1),但绝大多数来自甜土植物或盐生植物。对已克隆的液泡膜NHXs分析表明,在多数高等植物中,液泡膜Na+/H+逆向转运蛋白以家族形式存在,由多基因家族控制。而且在多种植物中都有该蛋白的同源基因(homologous gene)存在。如拟南芥中至少有6个(AtNHX1-AtNHX6)[24],水稻中至少有5个(OsNHX1-OsNHX5)[25],玉米中有6个(ZmNHX1-ZmNHX6)[13],大麦中至少有2个(HvNHX1-HvNHX2)[9],小麦中克隆到3个(TaNHX1-TaNHX3)[26],番茄中克隆到3个(LeNHX1-LeNHX3)[27],牵牛花中克隆到2个(InNHX1-InNHX2)[28],杨树中克隆到2个(PtNHX1,PtNHX6)[29]。对拟南芥中编码Na+/H+逆向转运蛋白基因的研究发现,这6个基因分别在不同的器官中发挥着各自不同的作用[24]。利用这些蛋白的保守序列设计简并引物,根据RT-PCR及RACE方法,从红小豆(Vignaangularis)幼苗中已成功克隆到液泡膜Na+/H+逆向转运蛋白的同源基因,命名为VaNHX1,作者待发表。
从表1的结果可以看出,大多数植物液泡膜Na+/H+逆向转运蛋白基因含有1410-1767个核苷酸的开放阅读框(Open Read Frame, ORF),编码470-589个氨基酸残基(表1),推测分子量从47kDa到179kDa不等。如拟南芥AtNHX1分子量为47kDa[14],而菊芋HtNHX1分子量可高达178.53kDa[30]。由此可见,不同植物由于种属不同,其液泡膜NHX蛋白的分子量具有不同程度的差异。说明植物液泡膜Na+/H+逆向转运蛋白NHXs在进化上可能具有多样性的特点。
利用DNAstar软件对表1所列出的植物NHXs进行氨基酸序列同源性分析,发现不同植物中Na+/H+逆向转运蛋白具有不同程度的同源性[13,16,35]。如盐生植物北滨黎AgNHX1、盐角草SeNHX1与番杏TtNHX1的同源性很高,而与水稻等甜土植物的NHXs同源性相对较低[25]。而有些植物中存在液泡膜Na+/H+逆向转运蛋白家族,如拟南芥,玉米及大豆等均克隆到不同的Na+/H+逆向转运蛋白,NHXs家族成员间的序列同源性也有所差异。到目前为止,所发现的植物液泡膜NHXs蛋白都属于细胞内模(Intra-cellular, IC)类的第一类(Class I),并在细胞内形成一个独立的转运子分支,拟南芥中AtNHX1-4属于Class I类,它们之间有56%-87%的相似性,而AtNHX5和AtNHX6属于Class II类,它们有79%的相似性,但Class II类与Class I类只有21%-23%的相似性。
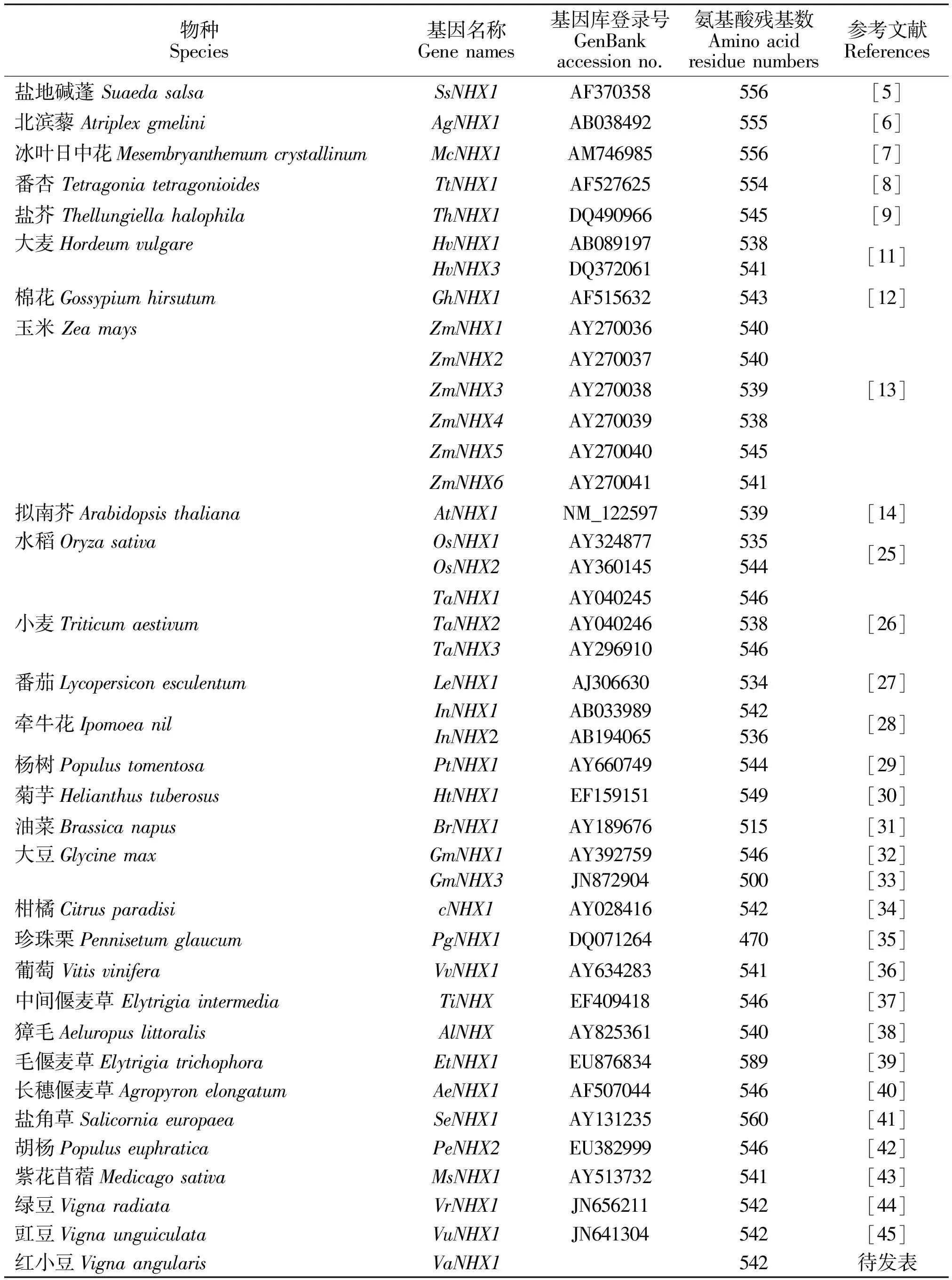
表1 已克隆的部分高等植物液泡膜Na+/H+逆向转运蛋白
不同植物的NHXs在氨基酸组成上具有一定的保守性,除了珍珠粟PgNHX1外,都具有相同的氨基酸序列LFFIYLL PPI。研究表明,该序列除了在番茄LeNHX1、玉米ZmNHX1及柑橘cNHX1中存在个别氨基酸的差别外,在其他所有植物NHX中都是高度保守的。通过氨基酸序列同源性的比较,分析了不同植物NHXs的进化关系(图1)。由图1的进化树分析可知,番茄LeNHX1与其他植物NHXs亲缘关系相对较远。其它植物液泡膜NHXs可以大致分为5大类群,第I类主要包括豆科植物,如紫花苜蓿MsNHX1、大豆GmNHX1,GmNHX3、绿豆VrNHX1、豇豆VuNHX1等;作者新分离鉴定的红小豆VaNHX1属于此群,且与绿豆和豇豆的亲缘关系最近。第II类以盐生植物为主,如盐角草SeNHX1、冰叶日中花McNHX1、盐地碱蓬SsNHX1、北滨藜AgNHX1、棉花GhNHX1等;第III类为木本植物,如杨树PtNHX1、柑橘cNHX1、胡杨PeNHX2等;第IV类为较耐盐植物如盐芥ThNHX1、拟南芥AtNHX1及玉米ZmNHX1-6等。第V类以禾本科植物为主,包括小麦TaNHX1-2、水稻OsNHX1-3、大麦HvNHX1、长穗偃麦草AeNHX1等。由此可见,从进化的角度来说,上述这几个类群的植物液泡膜Na+/H+逆向转运蛋白来自于相同祖先,具有共同的进化起源。

图1 植物液泡膜Na+/H+逆向转运蛋白氨基酸序列的系统进化分析
2.2 植物Na+/H+逆向转运蛋白的分子结构特征
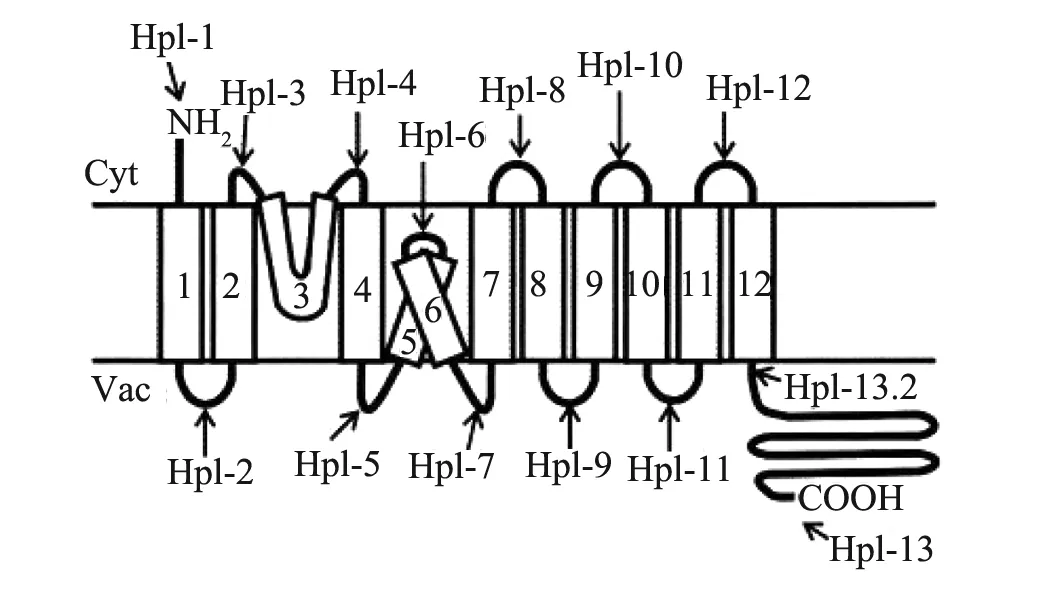
图2 AtNHX1的推测拓扑结构模型[46]
Yamaguchi等[46]分析了AtNHX1的拓扑学结构,结果如图2,AtNHX1由12个跨膜结构域和1个亲水的C末端“尾巴”组成,其中跨膜区TM3、TM5、TM6与膜相连,但并没有跨过液泡膜,而C末端几乎都位于液泡腔中。
大量分析表明,尽管不同生物中NHX的分子量、氨基酸数量、跨膜结构域数目有所不同,但都具有和拟南芥基本相似的结构特征。其N-端高度疏水,面向细胞质,且疏水区域较长,而C-端较短且高度亲水,形成亲水的C末端尾巴,且几乎全部位于液泡内。在该蛋白质家族中,N末端是高度保守的,其保守性对于NHXs的活性很重要;而亲水的C末端在不同植物的NHX中变化很大,可能起调节作用。从拓扑结构上分析表明,来自于不同植物的NHX在结构上极其相似,都由多个跨膜结构域和一个不跨膜的疏水区组成,在不同植物中该蛋白的跨膜结构域数量不同,一般为9-12个,其中TM5和TM6与Na+结合,是液泡膜NHXs活性的重要结构域。另外,不同植物的NHX氨基酸的高度保守序列LFFIYLLPPI都位于跨膜结构域上,是氨氯吡嗪咪蛋白的结合位点[47]。
3 Na+/H+逆向转运蛋白在植物耐盐性中的作用
3.1 植物Na+/H+逆向转运蛋白的表达与耐盐性的关系
盐胁迫下,高等植物液泡膜NHXs有两种表达形式:组成型表达和诱导表达。组成型表达是在无盐条件下蛋白在植株体内即可表达,但活性较低,而盐处理后其活性明显增加,多数盐生植物属于此类,如北滨藜、盐地碱蓬等。诱导表达是在盐诱导下该蛋白才表达显示其活性,某些耐盐植物多为此类,如大麦,向日葵等;如在甜菜悬浮细胞培养液中,随着NaCl浓度的升高NHX分子数增加[4];用高浓度的NaCl处理冰叶日中花及大麦,同样可诱导冰叶日中花及大麦根部液泡膜Na+/H+逆向转运蛋白活性上升[7,11]。Pitann等[48]研究表明,高盐下,抗盐杂交玉米品种中,ZmNHX表达明显上调。Kabala等[49]在200 mM NaCl处理的黄瓜根中也检测到了NHX蛋白的活性。Queirós等[50]发现在马铃薯细胞培养液,液泡膜NHX同样受盐的诱导表达。Silva等[42]研究表明胡杨细胞悬浮液能够在高达150mM的NaCl培养基中正常生长,而在300mM的盐浓度下,细胞虽不能生长但却能保持高度继代培养17天。大量研究表明,植物体内NHXs的有无及活性的高低与其耐盐性密切相关。
3.2 转Na+/H+逆向转运蛋白基因植物与耐盐性的关系
由于Na+/H+逆向转运蛋白在盐胁迫下能够诱导表达,利用基因工程手段对该蛋白进行转基因研究受到了人们的重视。研究表明,将Na+/H+逆向转运蛋白基因转到拟南芥中并过量表达,当用浓度为200 mM的NaCI处理时,拟南芥植株仍能正常生长发育,且液泡膜中Na+浓度AtNHX1活性成正相关,从而进一步证明了Na+在液泡膜中的区隔化在植物耐盐胁迫中的重要作用[14]。Zhang等[51]在番茄、油菜中过量表达AtNHX1,得到了世界上第一批真正意义上的耐盐作物。用200 mM的NaCl处理转基因植株发现植株可以正常生长发育,经检测,大量的盐分积累到转基因番茄的叶片,而果实中并未发现盐的积累,这保证了果实的品种[52,53]。同样,将AtNHX1基因转到甜菜、小麦、玉米及烟草中,其耐盐性都有不同程度的提高。此外,研究者对其他植物的液泡膜Na+/H+逆向转运蛋白的转基因进行了研究,发现该蛋白的过量表达同样能增强转基因植物的耐盐性。过量表达AgNHX1的转基因水稻中该蛋白活性是野生型植株的9倍,用高达300 mM的NaCl处理转基因植株,植株仍可存活[54]。Qiao等[55]研究发现,过量表达长穗偃麦草AeNHX1的拟南芥和油芥(Festuca),在250 mM NaCl条件下种子仍能正常发芽,而野生型则不发芽。Werma等[56]研究了过量表达珍珠栗PgNHX1基因的水稻,与野生型相比,增强耐盐性的同时促进了根系的生长发育。研究表明,植物的耐盐性是由多基因控制的,但在植物中转入单基因即可明显的改善提高植物对盐胁迫的耐受性,这说明在植物耐盐基因工程中,Na+/H+逆向转运蛋白基因具有巨大的潜在应用价值[57]。
由于植物在抵御盐胁迫过程中可诱导体内多种基因的表达,说明植物的耐盐性受多基因控制。那么同时过量表达多个基因可能比单个基因能更好的赋予转基因植物的耐盐性。Zhao等[58]研究了过量表达盐地碱蓬SsNHX1及拟南芥AVP1双基因的水稻,结果发现,与转二者之一的单基因相比,转双基因的植株具有更强的耐盐性。Gouiaa等[59]研究表明,在烟草中过量表达小麦TNHX1和TVP1双元基因,与转单基因及野生型相比,明显增强了植株耐盐性。Brini等[60]在拟南芥中同时过量表达小麦的TNHX1和TVP1,同样证明了转双基因植株获得了更高的耐盐性,该结果与文献[56]的研究结果一致。另外,Zhou等[61]将盐角草SeNHX1和菠菜(Atriplexhortensis)的甜菜碱合成酶基因BADH构建成双元表达载体转入烟草,研究转基因植株的抗盐性。结果表明,与转单一基因的植株相比,盐胁迫下双价转基因植株具有更高的生物量、Na+以及甜菜碱积累量。这些研究结果进一步证明了液泡膜Na+/H+逆向转运蛋白和H+-PPase在植物耐盐性中的重要作用。
4 展望
植物在长期的进化过程中形成了复杂的适应盐胁迫的机制,液泡膜Na+/H+逆向转运蛋白在植物抵御盐胁迫中发挥着十分重要的作用。该蛋白将细胞质中过多的Na+外排进入液泡,同时通过质子泵的作用将H+排到细胞质中,这种作用不但减少过多Na+对细胞质中各类代谢酶的毒害, 而且调节了细胞渗透势、维持了细胞内的离子稳态平衡。随着基因工程技术的迅猛发展,应用基因工程手段,无论转单基因还是双元基因都能不同程度的提高转基因植物的耐盐性,这进一步说明了Na+/H+逆向转运蛋白在植物抗盐基因工程中的重要作用。目前对该蛋白的研究还不够深入,至于该蛋白在提高植物耐盐性过程中,是否和植物体内某些代谢网络及信号分子有关,还有待进一步研究。今后对液泡膜Na+/H+逆向转运蛋白的研究可以从下面几个方面进行考虑: 首先,为了全面阐明该蛋白在植物抗逆性和植物生长发育的调控机制,可以从细胞和分子水平上深入研究此类蛋白的调控网络、不同调控网络之间的交叉调控以及其中涉及到的某些重要调控蛋白的功能;其次,通过比较研究不同植物和极端生境下生存的野生植物,来研究液泡膜Na+/H+逆向转运蛋白在植物适应盐胁迫中的特殊作用,为抗逆基因资源的发掘奠定基础;最后,是否能将已有的某些优良抗逆基因与Na+/H+逆向转运蛋白基因共同转入某些重要的农作物或牧草中,而获得一批抗逆性强的优良转基因新品种。这将有利于大面积盐碱地的改良和利用,对于某些极端环境下的农业发展尤为重要。
[1] Blumwald E,Aharon GS,Apse MP.Sodium transport in plant cells[J].Biochimica et Biophysica Acta,2000,1465:140-151.
[2] Higinbotham N.Electropotential of plat cells[J].Annual Review of Plant Physiology and Plant Molecular Biology,1973,24:25-46.
[3] 曾华宗,罗利军.植物抗旱、耐盐基因概述[J].植物遗传资源学报,2003,4:270-274.
[4] Blumwald E,Poole RJ.Na+/H+antiport in isolated tonoplast vesicles from storage tissue of Beta vnlgaris[J].plant physiol,1985,78:163-167.
[5] Ma XL,Zhang Q,Shi HZ,et al.Molecular cloning and different expression of a vacuolar Na+/H+antiporter gene inSuaedasalsaunder salt stress[J].Biologia Plantarum,2004,48(2):219-225.
[6] Hamada A,Shono M,Xia T,et al.Isolation and characterization of a Na+/H+antiporter gene from the halophyteAtriplexgmelini[J].Plant Molecular Biology,2001,46:35-42.
[7] Chauhan S,Forsthoefel N,Ran Y,et a1.Na+/myo-inositol symporters and Na+/H+-antiport inMesembryanthemumcrystallinum[J].The Plant Journal,2000,24:511-522.
[8] 吕慧颖,李银心,陈华,等.番杏Na+/H+逆向转运蛋白的克隆及特性分析[J].高技术通讯,2004,14:26-31.
[9] Wu C,Gao X,Kong X,et al.Molecular cloning and functional analysis of a Na+/H+antiporter gene ThNHXl from a halophytic plantThellungiellahalophila[J].Plant Molecular Biology Reporter,2009,27:1-12.
[10] Staal M,Maathuis FJM,Elzenga JTM,et al.Na+/H+antiporter activity in tonoplast vesicles from roots of the salt-tolerantPlantagomaritimeand the salt sensitiveplantagomedia[J].Physiologia Plantarum,1991,82(2):179-184.
[11] Fukuda A,Chiba K,Maeda M,et al.Effect of salt and osmotic stresses on the expression of genes for the vacuolar H+-pyrophosphatase,H+-ATPase subunit A,and Na+/H+antiporter from barley[J].Journal of Experimental Botany,2004,55(397):585-594.
[12] Wu CA,Yang GD,Meng QW,et a1.The cottonGhNHXlgene encoding a novel putative tonoplast Na+/H+antiporter plays an important role in salt stress[J].Plant Cell Physiology,2004,45:600-607.
[13] Zörb C,Noll A,karl S,et al.Molecular characterization of Na+/H+antiporters (ZmNHX) of maize (ZeamaysL) and their expression under salt stress[J].Journal of Plant Physiology,2005,162:55-66.
[14] Apse MP,Aharon GS,Sneddon WA,et al.Salt tolerance conferred by overexpression of a vacuolar Na+/H+antiport inArabidopsis[J].Science,1999,285:1256-258.
[15] Mennen H,Jacoby B,Marschner H.Is sodium proton antiport ubiquitous in plant cells[J].J Plant Physio,1990,137:180-183.
[16] Pardo JM,Cubero B,Leidi E,et al.Alkali cation exchangers: roles in cellular homeostasis and stress tolerance[J].J Exp Bot,2006,57:1181-1199.
[17] Sottosanto JB,Gelli A and Blumwald E.DNA array analyses of Arabidopsis thaliana lacking vacuolar Na+/H+antiporter: impact ofAtNHX1 on gene expression[J].Plant J,2007,40:752-771.
[18] Blumwald E.Tonoplast vesicles as a tool in the study of ion transport at the plant vacuole[J].Physiologia Plantarum,1987,69:731-734.
[19] Yamaguchi T and Blumwald E.Developing salt-tolerant crop plant:Challenges and opportunities[J].Trends Plant Sci,2005,10:615-620.
[20] Yamaguchi T,Fukada-Tanaka S,Inagaki Y,et al.Genes encoding the vaeuolar Na+/H+exehanger and flower coloration[J].Plant Cell Physiol,2001,42:451-461.
[21] Yoshida K,Kawachi M,Mori M,et al.The involvement of tonoplast proton pumps and Na+(K+)/H+exehangers in the change of petal color during flower opening of morning glory,Ipomoeatricolorcv.Heavenly blue[J].Plant Cell Physiol,2005,46:407-415.
[22] Ohnishi M,Fukada-Tanaka S,Hoshino A,et al.Characterization of a novel Na+/H+antiporter gene InNHX2 and comparison of InNHX2 with InNHX1,which is responsible for blue flower coloration by increasing the vacuolar pH in the Japanese morning glory[J].Plant Cell Physiol,2005,46: 259-267.
[23] Apse M P,Sottosanto JB,Blumwald E.Vacuolar cation/H+ exchange,ion homeostas is,and leaf development are altered in a T-DNA insertion almutant of AtNHX1,theArabidopsisvacuolar Na+/H+an tiporter[J].Plant J,2003,36:229-239.
[24] Yokoi S,Quintero FJ,Cubero B,et al.Differential expression and function ofArabidopsisthalianaNHX Na+/H+antporters in the salt stress response[J].Plant J,2002,30:529-539.
[25] Fukuda A,Nakamura A,Tanaka Y.Molecular cloning and expression of the Na+/H+exchanger gene inOryzasativa[J].Biochimicaet Biophysica Acta,1999,1446:149-155.
[26] Yu JN,Huang J,Wang ZN,et al.A vacuolar Na+/H+antiporter from wheat plays an important role in stress tolerance[J].J Biosci,2007,32:1153-1161.
[27] 范晶.番茄LeNHX3基因的克隆与植物过量表达载体的构建[J].江苏农业科学,2010,(6):47-49.
[28] Ohnishi,M,Fukada-Tanaka S,Hoshino A,et al.Characterization of a novel Na+/H+antiporter geneInNHX2 and comparison ofInNHX2 withInNHX1,which is responsible for blue flower coloration by increasing the vacuolar pH in the Japanese morning glory[J].Plant Cell Physiol,2005,46 (2):259-267.
[29] 张德强,赵淑堂,卢孟柱,等.杨树Na+/H+反向运输蛋白基因(PtNHX1、PtNHX6) 的克隆和检测[J].林业科学,2006,42(11) :29-36.
[30] 严一诺,孙淑斌,徐国华,等.菊芋Na+/H+逆向转运蛋白基因的克隆与表达分析[J].西北植物学报,2007,27(7):1291-1298.
[31] Wang J,Zuo K,Wu W,et al.Molecular cloning and characterization of a new Na+/H+antiporter gene fromBrassicanapus[J].DNA Seq,2003,14:351-358.
[32] Sun YX,Wang D,Bai YL,et al.Studies on the overexpression of the soybeanGmNHX1 inLotuscorniculatus:The reduced Na+level is the basis of the increased salt tolerance[J].Chinese Science Bulletin,2006,51:1306-1315.
[33] 张继星,王晓宇,陈永胜,等.大豆GmNHX3基因的克隆机遗传转化载体的构建[J].吉林大学学报(理学版),2012,50(2):365-370.
[34] Porat R,Pavoncello D,Ben-Hayyim G,et al.A heat treatment induced the expression of a Na+/H+antiport gene (cNHX1) incitrusfruit[J].Plant Sci,2002,162:957- 963.
[35] Rajagopal D,Agarwal P,Tyagi W,et al.PennisetumglaucumNa+/H+antiporter confers high level of salinity tolerance in transgenicBrassicajuncea[J].Mol Breeding,2007,19:137-151.
[36] Hanana M,Cagnac O,Yamaguchi T,et al.A grape berry (VitisviniferaL.) cation/proton antiporter is associated with berry ripening[J].Plant Cell Physiol,2007,48(6):804-811.
[37] 张耿,王赞,关宁,等.中间偃麦草Na+/H+逆向转运蛋白的分子克隆及生物信息学分析[J].遗传,2007,29(10) :1263-1270.
[38] Zhang GH,Su Q,An LJ,et al.Characterization and expression of a vacuolar Na+/H+antiporter from the monocot halophyteAeluropuslittoralis[J].Plant Physiol Biochem,2008,46:117-126.
[39] 关宁,李聪,王涌鑫,等.毛偃麦草Na+/H+逆向转运蛋白的分子克隆及生物信息学分析[J].分子植物育种,2009,7(1):169-176.
[40] Qiao WH,Zhao XY,Li W,et al.Overexpression of AeNHX1,a root-specific vacuolar Na+/H+antiporter fromAgropyronelongatum,confers salt tolerance toArabidopsisand Festuca plants[J].Plant Cell Rep,2007,26(9):1663-1672.
[41] Wu GX,Wang G,Ji J,et al.Hydrophilic C terminus ofSalicorniaeuropaeavacuolar Na+/H+antiporter is necessary for its function[J].J Genet,2014,93(2):425-430.
[42] Silva P,Facanha AR,Tavares RM,et al.Role of tonoplast proton pumps and Na+/H+antiporter system in salt tolerance ofPopuluseuphraticaoliv[J].J Plant Growth Regul,2010,29:2-34.
[43] 安宝燕,罗琰,李加瑞,等.紫花苜蓿Na+/H+逆向转运蛋白基因在拟南芥中表达提高转基因植株的耐盐性[J].作物学报,2008,34(4):557-564.
[44] Mishra S,Alavilli H,Lee B,et al.Cloning and functional characterization of a vacuolar Na+/H+antiporter gene from Mungbean (VrNHX1) and its Ectopic expression enhanced salt tolerance inArabidopsisthaliana[J].PLos One,2014,9(10):1-14.
[45] Mishra S,Alavilli H,Lee B,et al.Cloning and characterization of a novel vacuolar Na+/H+antiporter gene (VuNHX1) from drought hardy legume,cowpea for salt tolerance[J].Plant Cell,Tissue and Organ Culture (PCTOC),2015,120(1):19-33.
[46] Yamaguchi T,Apse MP,Shi HH,et al.Toplogical analysis of a plant vacuolar Na+/H+antiporter reveals a luminal C terminus that regulates antiporter cation selectivity[J].Proc Natl Acad Sci USA,2003,100(2):12510-12525.
[47] Screpanti E,Padan E,Rimon A,et al.Crucial steps in the structure determination of the Na+/H+antiporter NhaA in its native conformation[J].J Mol Bio,2006,362:192-202.
[48] Ptiann B,Mohamed AK,Neubert AB,et al.Tonoplast Na+/H+antiporter of newly developed maize (Zea mays) hybrids contribute to salt resistance during the second phase of salt-stress[J].J Plant Nutr Soil,2013,176:148-156.
[49] Kabala K,Janicka-Russak M.Na+/H+antiporter activity in plasma membrane and tonoplast vesicles isolated from NaCl-treated cucumber roots[J].Biologia Plantarum,2012,56(2):377-382.
[50] Queirós F,Fontes N,Silva P,et al.Activity of tonoplast proton pumps and Na+/H+exchange in potato cell cultures is modulated by salt[J].J of Expe Botany,2009,60(4):1363-1374.
[51] Zhang HX,Blumwald E.Transgenic salt-tolerant tomato plants accumulate salt in foliage but not in fruit[J].Nature Biotechnology,2001,19:765-768.
[52] Guo Y,Ursula Halfter,Manabu Ishitani,et al.Molecular characterization of functional domains in the protein kinase SOS2 that is required for plant salt tolerance[J].The Plant Cell,2001,13:1383-1399.
[53] Gösta Lilius,Niklas Holmberg,Leif Bülow.Enhanced NaCI stress tolerance in transgenic tobacco expressing bacterial choline dehydrogenase[J].Nature Biotecnology,1996,14:177-180.
[54] Ohta M,Hayashia Y,Nakashima A,et al.Introduction of a Na+/H+antiporter gene fromAtriplexgmeliniconferssalt tolerance to rice[J].FEBS Letters,2002,532(3):279-282.
[55] QiaoWH,Zhao XY,Li W,et al.Overexpression ofAeNHX1,a root-specific vacuolar Na+/H+antiporter fromAgropyronelongatum,confers salt tolerance toArabidopsisandFestucaplants[J].Plant Cell Rep,2007,26(9):1663-1672.
[56] Verma D,Singla-Pareek SL,Rajagopal D,et al.Functional validation of a novel isoform of Na+/H+antiporter fromPennisetumglaucumfor enhancing salinity tolerance in rice[J].J Biosci,2007,32(3):1-7.
[57] Zhang HX,Hodson JN,Williams JP,et al.Engineering salt-tolerant Brassica plants:characterization of yield and seed oil quality in transgenic plants with increased vacuolar sodium accumulation[J].Proceedings of the National Academy of Sciences of the United States of America,2001.98:12832-12836.
[58] Zhao FY,Zhang XJ,Li PH,et al.Co-expression of theSuaedasalsaSsNHX1 andArabidopsisAVP1 confer greater salt tolerance to transgenic rice than the singleSsNHX1[J].Mol Breeding,2006,17(4):341-353.
[59] Gouiaa S,Khoudi H,Leidi EO,et al.Expression of wheat Na+/H+antiporter TNHXS1 and H+-pyrophosphatase TVP1 genes in tobacco from a bicistronic transcriptional unite improves salt tolerance[J].Plant Mol Biol,2012,79:137-155.
[60] Brini F,Hanin M,Mezghani I,et al.Overexpression of wheat Na+/H+antiporter NHX1 and H+-pyrophosphatase TVP1 improve salt-and drought-stress tolerance inArabidopsisthalianaplants[J].J Exp Bot,2007,58:301-308.
[61] Zhou S,Chen X,Zhang X,et al.Improved salt tolerance in tobacco plants by co-transformation of a betaine synthesis gene BADH and a vacuolar Na+/H+antiporter geneSeNHX1[J].Biotechnol Lett,2008,30:369-376.
Research and application of plant vacuolar Na+/H+antiporter
REN Xiu-yan1,2, WANG Bao-zeng1, WANG Cong-yan1, HOU Zhi-min1
(1.CollegeofLifeScience,LangFangTeachersUniversity,LangfangHebei065000,China;2.EdibleandMedicinalFungiResearchandDevelopmentCenterofHebeiUniversities,LangfangHebei065000,China)
Vacuolar membrane Na+/H+antiporter is transmembrane transporter protein which exists widely in plant and is responsible for plants Na+, H+exchange.In this review, we reviewed recent progress on the cloning, molecular structure, function and their uses in plant salt tolerance of Na+/H+antiporter, designed to enable researchers to understand systematically the research progress of Na+/H+antiporter and provided
to improve plant growth and development salt-tolerant through regulating the expression of Na+/H+antiporter.
Plant; Vacuolar; Na+/H+antiporter; Salt tolerance
2016-07-05
河北省科技厅项目(12222902);廊坊师范学院重点项目(LSZZ201203);河北省高等学校遗传学重点发展学科项目;廊坊师范学院微生物学重点学科项目
任秀艳(1977-),女,博士,副教授,研究方向:生物化学及分子生物学.
1001-9383(2016)03-0039-010
Q943
A
