陶行知“教学做合一”在化学教学中的实践——以“镁的提取及应用”为例
2016-11-18郑璇廖思彬
郑璇 廖思彬
陶行知“教学做合一”在化学教学中的实践——以“镁的提取及应用”为例
郑璇*廖思彬
(龙岩第一中学福建龙岩364000)
文章以“镁的提取及应用”的教学设计为例,实践陶行知“教学做合一”的教学方法论。学生通过阅读信息、自学课本、探究流程和练习巩固提高等自主活动来“学”和“做”,以实现教师的“教”。
教学做合一;自主学习;镁
陶行知先生是我国著名教育家,毕生致力于教育改革。他提出的“教学做合一”是生活教育论的方法论。他指出“教学做是一件事,不是三件事。我们要在做上教,在做上学”[1]。“教学做合一”方法论的提出不仅推进了当时的教育改革,也符合当下的新课程理念,指导着我们更新教学方式,将“教”“学”与“做”结合起来,与实际的生活联系起来。从生活中寻找教育切入点,注重教学与实践相结合。那么,如何在化学教学中践行陶行知的教学主张呢?本文以鲁科版高中《化学1》中第3章第4节“镁的提取及应用”为例。
本节的学习重点是如何从海水中获取人类需要的物质。“镁的提取及应用”作为本专题第2课时内容,着重介绍镁的工业提取步骤,而镁及其化合物(如氯化镁和氢氧化镁等)的性质渗透在镁的提取过程中,成为解决从海水中提取镁的辅助信息。本课时内容分为从海水中提取镁的流程和镁的性质两个部分,新教材把如何获取物质放在重要位置,旨在培养学生发现问题和解决问题的能力。[2]
在新课程的背景下,不少教师已经改变传统讲授式的教学方法,在课堂中注重以学生为主体,常常把该课内容设计为工业生产流程模式。教师心中已有完整的教学设计,在课堂上只是根据预想的教学过程设置若干个有梯度问题,再给予信息,引导学生提出解决方案。基本的教学模式是:讲解背景知识:认识镁→引出主题:如何从海水提镁→信息提供:镁中海水中的含量图→提出问题:如何实现镁离子的分离→学生回答:加沉淀剂。在这样的设计中,学生只要顺着教师的思路,逐一解决梯度问题,便可完成整个工业生产路线。这样的教学虽比传统教学更进步,但仍有局限:学生缺乏工业流程的整体设计思想,只会逐一解决当前问题;学生在课堂中还是被动地解决教师设置的问题,而不会带着主人翁的意识去发现问题、提出问题、解决问题。
本文的教学设计则努力实践了陶行知先生“教学做合一”的教育理念,教师将课堂让给学生,整个工业流程设计由学生自主、合作和探究完成。教师将所有可能用到的信息全部呈现出来,只提出最核心的问题:“如何提取镁”,不再有阶梯性引导过程。学生面对这一主题,需要从宏观角度分析获取源,获取手段及获取需要的材料,还要选择最佳合成路线,甚至要评价过程及方法。学生需要阅读理解信息、自学课本、自主探究流程,才能提出方案。每一环节的设计都要思考“是否需要”“为什么需要”“这么做的理由”。完成方案设计后,学生不仅从工业流程设计中掌握镁及其化合物的主要性质,也体验到工业生产过程的实际性和严谨性。更有价值的是,学生在实践中培养了自身的大局观,这对将来处理工业流程和实验大题是有很大帮助的,可以跳出局部问题,从整个局面来考虑问题。教师在课堂中的作用是引导学生积极地通过“自读、自疑、自做、自释”来达到学习的目的。这样的教学从真正意义上实现了在“做”中“学”,“做”中“教”,“做”中求进步的目标。
教学过程的实施:
(1)教师设置教学情景,引入新课,并提出问题:请你提取镁,你的设计方案是怎么样?在提取过程中又可能会面临怎样的困难,如何解决?
(2)学生根据学案,小组合作探究,完成海水提镁方案。教师在巡视过程中对合作小组学习和个别特殊问题给予指导,收集学生在设计探究方案时存在的问题,组织学生讨论、形成实验方案。
(3)学生总结此方案优点,评价实验方案,教师
点评学生的活动或方案、解决学生的疑难。学案及设计思想如下:
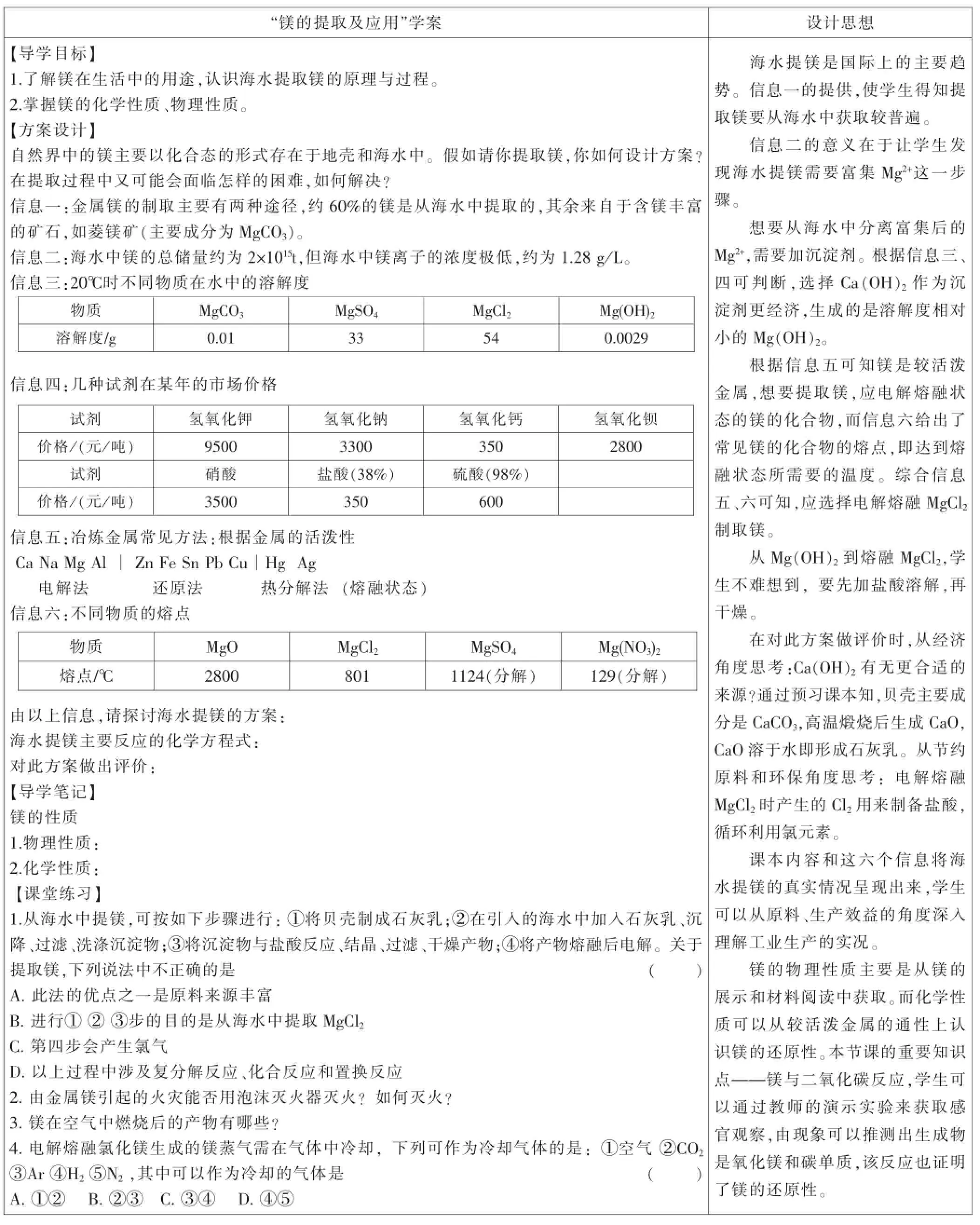
“镁的提取及应用”学案设计思想【导学目标】1.了解镁在生活中的用途,认识海水提取镁的原理与过程。2.掌握镁的化学性质、物理性质。【方案设计】自然界中的镁主要以化合态的形式存在于地壳和海水中。假如请你提取镁,你如何设计方案?在提取过程中又可能会面临怎样的困难,如何解决?信息一:金属镁的制取主要有两种途径,约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,如菱镁矿(主要成分为MgCO3)。信息二:海水中镁的总储量约为2×1015t,但海水中镁离子的浓度极低,约为1.28g/L。信息三:20℃时不同物质在水中的溶解度物质MgCO3MgSO4MgCl2Mg(OH)2溶解度/g0.0133540.0029信息四:几种试剂在某年的市场价格试剂氢氧化钾氢氧化钠氢氧化钙氢氧化钡价格/(元/吨)950033003502800试剂硝酸盐酸(38%)硫酸(98%)价格/(元/吨)3500350600信息五:冶炼金属常见方法:根据金属的活泼性CaNaMgAl∣ZnFeSnPbCu∣HgAg电解法还原法热分解法(熔融状态)信息六:不同物质的熔点物质MgOMgCl2MgSO4Mg(NO3)2熔点/℃28008011124(分解)129(分解)由以上信息,请探讨海水提镁的方案:海水提镁主要反应的化学方程式:对此方案做出评价:【导学笔记】镁的性质1.物理性质:2.化学性质:【课堂练习】1.从海水中提镁,可按如下步骤进行:①将贝壳制成石灰乳;②在引入的海水中加入石灰乳、沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应、结晶、过滤、干燥产物;④将产物熔融后电解。关于提取镁,下列说法中不正确的是()A.此法的优点之一是原料来源丰富B.进行①②③步的目的是从海水中提取MgCl2C.第四步会产生氯气D.以上过程中涉及复分解反应、化合反应和置换反应2.由金属镁引起的火灾能否用泡沫灭火器灭火?如何灭火?3.镁在空气中燃烧后的产物有哪些?4.电解熔融氯化镁生成的镁蒸气需在气体中冷却,下列可作为冷却气体的是:①空气②CO2③Ar④H2⑤N2,其中可以作为冷却的气体是()A.①②B.②③C.③④D.④⑤海水提镁是国际上的主要趋势。信息一的提供,使学生得知提取镁要从海水中获取较普遍。信息二的意义在于让学生发现海水提镁需要富集Mg2+这一步骤。想要从海水中分离富集后的Mg2+,需要加沉淀剂。根据信息三、四可判断,选择Ca(OH)2作为沉淀剂更经济,生成的是溶解度相对小的Mg(OH)2。根据信息五可知镁是较活泼金属,想要提取镁,应电解熔融状态的镁的化合物,而信息六给出了常见镁的化合物的熔点,即达到熔融状态所需要的温度。综合信息五、六可知,应选择电解熔融MgCl2制取镁。从Mg(OH)2到熔融MgCl2,学生不难想到,要先加盐酸溶解,再干燥。在对此方案做评价时,从经济角度思考:Ca(OH)2有无更合适的来源?通过预习课本知,贝壳主要成分是CaCO3,高温煅烧后生成CaO,CaO溶于水即形成石灰乳。从节约原料和环保角度思考:电解熔融MgCl2时产生的Cl2用来制备盐酸,循环利用氯元素。课本内容和这六个信息将海水提镁的真实情况呈现出来,学生可以从原料、生产效益的角度深入理解工业生产的实况。镁的物理性质主要是从镁的展示和材料阅读中获取。而化学性质可以从较活泼金属的通性上认识镁的还原性。本节课的重要知识点——镁与二氧化碳反应,学生可以通过教师的演示实验来获取感官观察,由现象可以推测出生成物是氧化镁和碳单质,该反应也证明了镁的还原性。
教学反思与评价:
本教学设计是笔者教学公开周的教学实践尝试,旨在践行陶行知先生的“教学做合一”,从生活生产中提出课题——“镁的提取”。教学设计中学生的角色不再只是学习者,而是企业的领导者,如何解决生产的现实问题会激发学生的学习热情。学生可将之前学习的“钠及其化合物的性质”的学习思路运用到新的学习中。学生再通过查阅资料、分析讨论如何运用资料解决现实问题。相信这节课的尝试会教会学生如何运用已学知识和查阅未知资料来解决问题。
从教学手段来看,本节课将学生认知建构与情感激活、教学控制与情境创设融为一体,灵活地将教材知识点设计成探究性问题,创设了学生能够独立探索的情境,给学生创造“做”的机会,让学生在思考中解决问题,实现从“做”中“学”的目标。
从教学过程来看,本节课以学生的活动为基础,在动态、开放、主动、合作的学习环境中“解放了学生头脑、双手、眼睛、嘴巴”[3],发挥了学生主体作用,使他“能想、能干、能看、能谈”[3],能从中感受到将所学知识运用于生产实际中的乐趣。
从教学效果来看,本节课让学生认识了丰富的海水资源,树立了保护和合理利用资源的意识,培养了学生的学习能力,挖掘了学生的潜力,使学生综合素质得到提高。
陶行知先生说:“先生的责任不在教,而在教学生学。”[4]因此,教师能在教学中用“教学做合一”的理论指导实践,根据具体的教学内容、学生特征和教学条件为学生策划适合的学习资源,创新学习活动,让学生在真实的情境中去发现问题、解决问题,真正做到联系生活、学以致用,那么“教是为了不教”离我们的教学也将不远了。
[1]周逸先.“教学做合一”加强课堂教学的实践性——陶行知生活教育方法论对课堂教学改革的启示[J].学科教育,2001(5):14-17
[2]陈艳.基于“镁的提取与应用”的教学设计课例探究[J].数理化学习,2014(2):62-64
[3]童宝安.六大解放与综合实践——陶行知教育思想学习心得交流[J].福建陶研,2010(4):40-42
[4]李庆.在中学化学教学中实践“教学做合一”[J].化学教与学,2012(9):19-20
1008-0546(2016)11-0011-02
G633.8
B
10.3969/j.issn.1008-0546.2016.11.004
*通信联系人,E-mail:yuchan28@qq.com
