偶联试剂SMCC的一锅法合成
2016-11-15王新增吴忠伟
王新增, 任 重, 宋 颖, 吴忠伟
(浙江海正药业股份有限公司,浙江 台州 318000)
偶联试剂SMCC的一锅法合成
王新增, 任 重, 宋 颖, 吴忠伟
(浙江海正药业股份有限公司,浙江 台州 318000)
SMCC是一类含有N-羟基琥珀酰亚胺(NHS)活性酯和马来酰亚胺的双功能偶联剂,可以分别将含有巯基和氨基的化合物键接在一起,在生物及化学领域应用广泛。本文采用一锅法将反式氨甲环酸、马来酸酐在 DMF作溶剂的条件下反应生成反式氨甲环酸的马来酰胺,再与三氟乙酸酐、N-羟基丁二酰亚胺、三甲基吡啶等反应生成SMCC,对合成SMCC的工艺进行了简单优化,得出了最佳合成条件,总收率可达92%,纯度可达99%以上。
SMCC;一锅法;合成;偶联试剂
SMCC(琥珀酰亚胺4-(N-马来酰亚胺甲基)环己胺-1-羧酸)是一类含有N-羟基琥珀酰亚胺(NHS)活性酯和马来酰亚胺的双功能偶联剂,可以分别将含有巯基和氨基的化合物键接在一起,可作为链接子将抗体与毒素分子连接起来,在免疫实验、肿瘤成像的放射性标记中广泛应用[1-2],其最早由Yoshitake及其团队合成出[3],以氨甲环酸为原料,与马来酸酐反应生成氨甲环酸的马来酰胺,在乙酸酐及醋酸钠作用下环合,与N-羟基丁二酰亚胺经酯化反应得到SMCC,收率仅21%。1991年,Nielsen 和 Buchardt报道了一锅法合成SMCC的方法[4],氨甲环酸与马来酸酐反应生成氨甲环酸的马来酰胺,然后再加入DCC和NHS,反应完后经提取浓缩结晶得到SMCC,收率75%,Paterson 和 Eggleston 采用TFA-NHS作为酯化试剂,合成出SMCC,马来酸酐与氨甲环酸反应生成氨甲环酸的马来酰胺,然后一锅环合酯化生成SMCC,此方法得到的SMCC收率为89%[5],但需要分离出氨甲环酸的马来酰胺, TFA-NHS试剂在使用之前需要单独配制好,操作步骤较繁琐。Nicholas 和 Jarmila在对SMCC的合成优化过程中[6],发现采用TFA-NHS试剂能有效地促进羧酸转化为丁二酰亚胺酯及马来酸环合转化为马来酰亚胺,采用一锅法反应后,水洗及乙醚打浆后,可以分离得到SMCC,总收率超过90%。
本文采用Nicholas和 Jarmila所述的方法,一锅法反应生成SMCC,然后水洗,浓缩,得到SMCC固体后,用二氯甲烷和正庚烷重结晶得到SMCC,收率92%,纯度大于99%。
1 实验
1.1 主要仪器及试剂
Bruker 400兆核磁共振仪,Bruker microTOF-QII质谱仪,BRUKER VECTOR22红外光谱仪,SHIMADZU UV240PC紫外光谱仪。
反式氨甲环酸,常州市尚科医药化工材料有限公司;马来酸酐,国药集团化学试剂有限公司;2,4,6-三甲基吡啶,Alfar Aesar试剂公司;三氟乙酸酐,上海亿日化工科技有限公司;N-羟基丁二酰亚胺,国药集团化学试剂有限公司。
1.2 合成方法
往2L四口圆底烧瓶中加入15.72 g(100 mmol)反式氨甲环酸、9.80 g(100 mmol)马来酸酐,加入500 mL DMF,室温搅拌6 h,在搅拌过程中,溶液逐渐变澄清。然后将反应液用冰盐浴冷却至0~-5℃,用100 mL滴液漏斗将27.8 mL(210 mmol)2,4,6-三甲基吡啶加入至反应液中,滴加过程保持反应液温度在0~-5℃,再另一1 000 mL四口烧瓶中,加入46g(400 mmol)N-羟基丁二酰亚胺、500 mL DMF,搅拌,冰盐浴冷却至0~-5℃之间,量取55.6 mL(400 mmol)三氟乙酸酐,通过滴液漏斗滴加至1 000 mL烧瓶中,滴加过程保持温度在0~-5℃,滴加完毕后,此温度下搅拌反应10 min,再量取2,4,6-三甲基吡啶52.8 mL(400 mmol),通过滴液漏斗滴加到1 000 mL烧瓶反应液中,搅拌10 min,将1 000 mL烧瓶中液体慢慢加入到2L烧瓶中,保持两烧瓶中液体温度在0~-5℃,1~2 h内加完,加完后,撤去冰盐浴,室温搅拌过夜,反应混合物用600 mL二氯甲烷稀释,冰水浴冷却,加入1N盐酸500 mL,分去上层水相,下层有机层再用1N盐酸500 mL洗涤二次,有机相用无水硫酸镁干燥,过滤,滤液浓缩至干,得到固体约33 g,用250 mL二氯甲烷溶解,在布氏漏斗上面垫约2 cm厚的硅胶,将SMCC二氯甲烷溶液过滤,滤液搅拌下加入500 mL的正庚烷,析出白色固体,过滤,真空干燥得到SMCC纯品约31.0 g,收率92%。
1H-NMR( CDCl3)δ:1.05 ( m, 2H);1. 39( m, 2H);1. 59 ( m, 1 H);1. 63( m, 2H);2.01( m, 2 H);2. 10~2. 33( m, 4H);2. 67( m, 1H);2.80( s, 4H) Hz);3. 27( d, 2 H, J=6.93);7. 00 (s, 2H),13C-NMR:δ25.89,28.26,29.5,36.15,39.91,43.22,134.83,170.65,171.30,171.70. MS:m/z=335.1241 [M+H]+。
2 结果与讨论
2.1 反应方程式

图1 合成SMCC的反应方程式

图2 SMCC合成反应机理图
试剂和条件,i)马来酸酐,DMF,室温,6 h;ii)三氟乙酸酐4eq,N-羟基丁二酰亚胺4eq,2,4,6-三甲基吡啶6.1eq,DMF,0℃到室温
该反应机理为氨甲环酸与马来酸酐先反应生成氨甲环酸的马来酰胺,然后与TFA-NHS作用,生成酯化中间态5,5在TFA-NHS作用下环合,得到SMCC,在氨甲环酸的马来酰胺与TFA-NHS反应时,也会有副产物4生成,4不能转化为SMCC。
2.2 滴加NHS-TFA溶液温度对反应的影响
如果酯化反应温度过高,或者滴加速度太快,则会生成副产物4,而4不能转化为SMCC,温度低可以抑制此副反应,在0℃几乎没有该副产物,因此,在滴加TFA-NHS试剂时,反应温度为0℃左右,滴加速度要慢,滴加速度快,温度高。生成的副产物多,得到的产物较难以提纯纯化。
2.3 反应配比对产率的影响(NHS-TFA)配比对反应影响
该反应根据反应机理,先是氨甲环酸与马来酸酐1∶1的反应生成氨甲环酸的马来酰胺, TFAA与NHS反应定量生成TFA-NHS,TFAA与NHS配比为1∶1,在TFA-NHS和2,4,6-三甲基吡啶作用下,然后得到SMCC。分别考察了TFA-NHS、2,4,6-三甲基吡啶与氨甲环酸配比对收率的影响,结果如图3、图4所示。

图3 TFA-NHS与氨甲环酸配比对收率的影响

图4 2,4,6-三甲基吡啶配比对收率的影响
根据上述数据,NHS-TFA与氨甲环酸配比为4,2,4,6-三甲基吡啶为 6当量时,收率最高。因此选择配比为氨甲环酸∶马来酸酐∶TFA-NHS/2,4,6-三甲基吡啶=1∶4∶6。
2.4 反应时间对转化率的影响
随着反应时间增加,产率逐渐增加,当反应10 h后,转化率不再增加,此时反应完全。反应时间选择10 h。
优化后的工艺为:反应物配比为马来酸酐/反式氨甲环酸∶TFAA/NHS∶2,4,6-三甲基吡啶=1∶4∶4∶6,反应时间为10 h。滴加TFA-NHS时的温度为0℃。
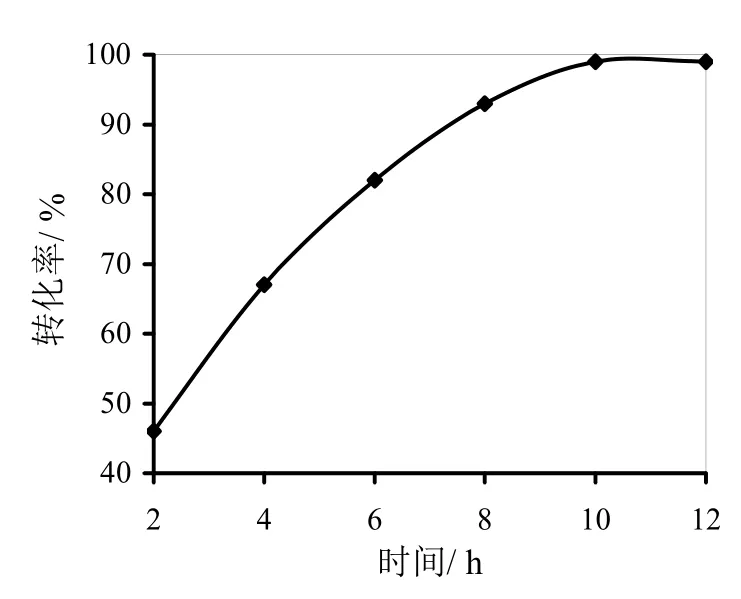
图5 反应时间对转化率的影响
3 结论
以反式氨甲环酸、N-羟基丁二酰亚胺、马来酸酐为原料,一锅法合成出SMCC,对合成工艺进行了优化,收率达92%,产物纯度99%以上,操作简单,收率高。采用质谱及1H-NMR和13C-NMR对SMCC结构进行了表征。反应物配比为马来酸酐/反式氨甲环酸∶TFAA/NHS∶2,4,6-三甲基吡啶=1∶4∶4∶6,反应时间为10 h,滴加TFA-NHS时的温度为0℃。
[1] Bieniarz C, Husain M, Barnes G, et al. Extended length heterobifunctional coupling agents for protein conjugations[J]. Bioconjugate Chem, 1996, 7(1): 88-95.
[2] Shreve P, Aisen A M. Monoclonal antibodies labeled with polymeric paramagnetic ion chelates[J]. Magn Reson Med, 1986(3): 336-340.
[3] Yoshitake S, Yamada Y, Ishikawa E, et al. Conjugation of glucose oxidase from Aspergillus niger and rabbit antibodies using N-hydroxysuccinimide ester of N-(4-carboxycyclohexylmethyl)-maleimide[J]. Eur J Biochem, 1979, 101(2): 395-399.
[4] Nielsen O, Buchardt O. Facile synthesis of reagents containing a terminal maleimido ligand linked to an active ester[J]. Synthesis, 1991(10): 819-821.
[5] Paterson M J, Eggleston I M. Convenient preparation of N-maleoyl amino acid succinimido esters using N-trifluoroacetoxysuccinimide[J]. Syn Comm. 2008, 38(2): 303-308.
[6] Nicholas M Leonard, Jarmila Brunckova. In situ formation of N-trifluoroacetoxy succinimide (TFA-NHS): one-pot formation of succinimidyl esters, N-trifluoroacetyl amino acidsuccinimidyl esters, and N-maleoyl amino acid succinimidyl esters[J]. The Journal of Organic Chemistry, 2011, 76(21): 9169-9174.
One-pot Synthesis of Conjugate Agent Succinimidyl-4-(N-maleimidomethyl)cyclohexane-1 -carboxylate (SMCC)
WANG Xin-zeng, REN Zhong, SONG Ying, WU Zhong-wei
(Zhe Jiang Hisun Pharmaceutical CO., LTD. Taizhou, 318000 China)
SMCC was used as a heterobifunctional linker, containing N-hydroxy succinimidyl active ester and maleimide,could crosslink amino group and mercapto group, had found utility in numerous areas of chemistry and biotechnogoly. SMCC was synthesized by one-pot with trans-4-(aminomethyl)cyclohexane carboxylic acid, maleic anhydride to give maleamino of trans-4-(aminomethyl)cyclohexane carboxylic acid, then reactived with N-hydroxysuccinimide, trifluoroacetic anhydride and sym-collidine to yield SMCC. The syntheisis process of SMCC was optimized. And the better process parameters was got, the yield was about 92%,the purity was beyond 99%.
SMCC; one-pot synthesis; conjugate agent
TQ421.2
A
1009-220X(2016)05-0050-04
10.16560/j.cnki.gzhx.20160514
2016-05-27
王新增(1976~),男,浙江台州人,硕士;主要从事药物合成的研究。xzwang@hisunpharm.com
