乳酸菌盐溶性蛋白培养物中血管紧张素转化酶抑制活性肽的测定及分离
2016-11-14赵俊良卢海鹏
赵俊良,卢海鹏,芒 来,金 山,*
(1.内蒙古农业大学兽医学院,农业部动物疾病临床诊疗技术重点实验室,内蒙古 呼和浩特 010018;2.内蒙古农业大学动物科学学院,内蒙古 呼和浩特 010018)
乳酸菌盐溶性蛋白培养物中血管紧张素转化酶抑制活性肽的测定及分离
赵俊良1,卢海鹏1,芒 来2,金 山1,*
(1.内蒙古农业大学兽医学院,农业部动物疾病临床诊疗技术重点实验室,内蒙古 呼和浩特 010018;2.内蒙古农业大学动物科学学院,内蒙古 呼和浩特 010018)
将16 株乳酸菌用MRS液体培养基3 代继代培养后,离心,并用灭菌的生理盐水制成乳酸菌悬浮液,接种于远东多线鱼肉盐溶性蛋白溶液(salt-soluble protein,SSP),对其代谢产物进行血管紧张素转化酶(angiotensin converting enzyme,ACE)抑制活性测定,筛选出ACE抑制活性较高的Pediococcus acidilactici ID7菌株(ACE抑制率为47.6%)和Lactobacillus plantarum 6214菌株(ACE抑制率为40.6%)。利用高效液相色谱(high performance liquid chromatography,HPLC)对Pediococcus acidilactici ID7的盐溶性蛋白培养代谢物进行色谱分析,获得了两个峰,其相应成分对ACE抑制的IC50分别为1.21 μg/mL和1.07 μg/mL,利用凝胶过滤HPLC法对出现较高的ACE抑制活性峰的成分进行色谱纯化,获得了ACE抑制率为26.67%,分子质量为586.7 D以下的ACE抑制多肽。
乳酸菌;血管紧张素转化酶;盐溶性蛋白;高效液相色谱法
近几年研究表明乳酸菌代谢产物和乳酸菌菌体具有提高机体营养成分的吸收[1-2]、调节肠胃和乳糖不耐受、降低胆固醇[3-6]、消除致癌因子、抗肿瘤[7-8]、提高机体免疫力[9]、抗高血压、预防动脉硬化[10-13]、抗酸化和抗衰老等作用,尤其是人们对乳酸菌的抗高血压作用越来越关注。机体血压受很多因素的调节作用,其中最重要的因素是肾素——血管紧张素系统(renin angiotensin system,RAS)和激肽释酶——激肽系统(kallikrein kinin system,KKS)之间的平衡,而系统中存在的血管紧张素转化酶(angiotensin converting enzyme,ACE)则是影响两个系统平衡的重要因素。ACE将RAS系统中的血管紧张素Ⅰ(angiotensinⅠ,AngⅠ)转换为血管紧张素Ⅱ(angiotensinⅡ,AngⅡ),而AngⅡ是活性很强的血管收缩剂,导致血压升高;另一方面,ACE也能作用于KKS系统中的降血压物质缓激肽而使其失活,从而使KKS系统处于抑制状态,同样导致了血压的升高,因此,抑制血浆和血管内皮细胞的ACE活性,不仅能够抑制具有升高血压作用的血管紧张素Ⅱ的产生,同时也能抑制降血压作用的缓激肽的分解,从而达到降血压的目的。食源性ACE抑制肽具有安全性、无副作用的优点,在食品与医药领域中具有广阔的应用前景。
1978年Cheung等[14]首次报道食物蛋白源ACE抑制多肽的研究后,相继报道了鱼肉、肉类、蔬菜、水果、发酵食品[15]等蛋白源ACE抑制多肽的研究。到目前为止,从天然蛋白酶分解物中分离到400多种ACE抑制肽,而且也具有能够使肠道充分吸收的短链多肽[15],特别是已经证明了奶酪[11]、酱油[16]、发酵大豆食品[17]及酸奶[18-19]中含有ACE抑制肽。
本实验通过对接种乳酸菌的远东多线鱼肉盐溶性蛋白(salt soluble protein,SSP)的代谢产物进行分析,研究了乳酸菌的SSP溶液代谢产物与ACE抑制活性的关系,并用高效液相色谱(high performance liquid chromatography,HPLC)对Pediococcus acidilactici ID7 SSP溶液培养物进行了色谱分析和ACE抑制多肽的分离纯化。
1 材料与方法
1.1 材料
1.1.1 材料与菌种
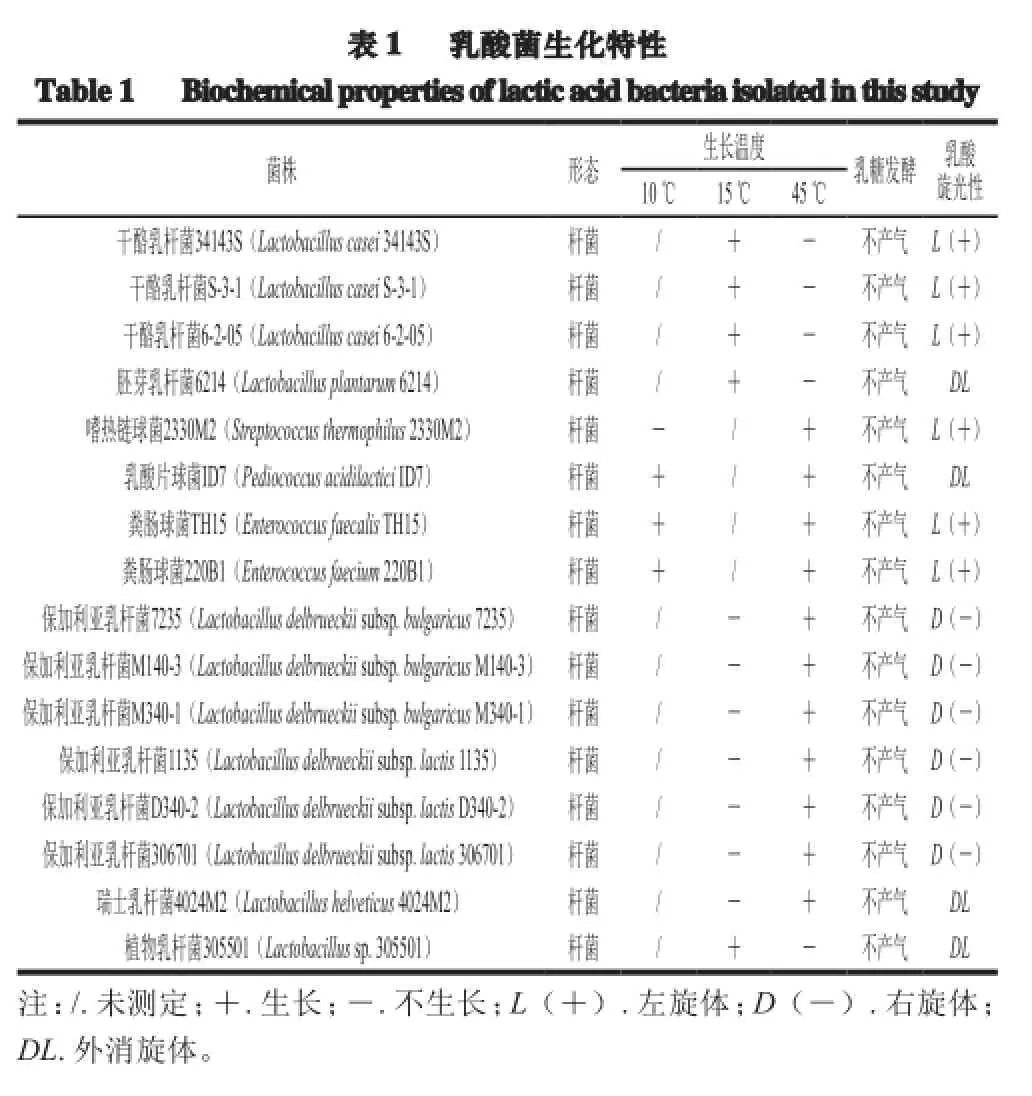
实验所用16 株乳酸菌及其生化特性如表1所示,由内蒙古农业大学微生物学实验室保存。
1.1.2 培养基
MRS液体培养基 北京陆桥有限责任公司;TYLG液体培养基:蛋白胨1.0 g/L、酵母粉0.50 g/L、葡萄糖0.50 g/L、吐温-80 0.1 g/L、L-盐酸盐0.01 g/L、蒸馏水1 000 mL,pH 6.8。
1.1.3 试剂与仪器
氢氧化钠、盐酸、硼酸、葡萄糖 北京化工厂;乳糖 天津市永大化学试剂有限公司;醋酸乙酯、乙氰美国SMA公司;三氟乙酸 北京合力开拓化工有限公司;Bradford试剂 北京博凌科为生物科技有限公司。
HPS-160恒温生化培养箱 哈尔滨市东联电子技术开发有限公司;U-1800型紫外-可见分光光度计 日本岛津公司;Sigma 2-16PK高速低温冷冻离心机、高效液相色谱仪、凝胶过滤高效液相色谱仪 德国Sigma公司;色谱柱5C18-AR-300 日本Nacalai Tesque公司;色谱柱Superdex Peptide HR 10/30 美国通用电气公司;旋转蒸发仪 东京理化器械有限公司。
1.2 方法
1.2.1 SSP溶液的制备
远东多线鱼肉(75 g)加食盐(1.5 g)后,再加蒸馏水(300 mL)、乳糖(2.0 g)、葡萄糖(2.0 g)及食盐(1.1 g),用绞肉机研磨。将这个混合液用高速离心机离心(10 000×g,10 min,4 ℃),取上清液进行过滤除菌(0.22 μm)制成SSP溶液(蛋白质质量浓度为8.0 mg/mL,pH 6.9)。测定蛋白质浓度用紫外检测方法[20],即使用牛血清白蛋白为标准蛋白质,测定280 nm波长处的吸光度之后换算为蛋白质质量浓度。
1.2.2 乳酸菌的培养方法以及菌体浓度测定
分别将供试16 株乳酸菌用MRS液体培养基或TYLG液体培养基3 代继代培养后,离心(13 000×g,20 min)取乳酸菌菌体,加5 mL灭菌生理盐水制成菌体悬浮液。将菌体悬浮液1.0%接种于SSP溶液,L. casei 34143S、L. casei S-3-1、L.casei 6-2-05、L. plantarum 6214在30 ℃条件下培养24 h,其他菌株在37 ℃条件下培养24 h。
1.2.3 ACE抑制活性测定方法
将培养乳酸菌的SSP溶液加热灭菌(100 ℃,10 min)后,离心(13 000×g,20 min)取上清液,用氢氧化钠调至pH值为8.3,作为样品溶液,用Cheung等[14]的方法测定ACE抑制活性。将50 μL样品溶液和50 μL ACE溶液(0.06 U/mL)在37 ℃条件下反应10 min后,加入150 μL 200 mmol/L硼酸缓冲液(含6.7 mmol/L Bz-Gly-His-Leu,500 mmol/L NaCl,pH 8.3),在37 ℃条件下反应30 min,然后用250 μL 1.0 mol/L的盐酸停止反应,再加醋酸乙酯0.5 mL充分搅拌后离心(800×g,15 min)抽提游离马尿酸,并用移液管吸取上部醋酸乙酯层0.2 mL,在120 ℃烘箱内烘干醋酸乙酯,再加入蒸馏水1.0 mL,混匀溶解马尿酸后,用分光光度计在228 nm波长处测定吸光度,ACE抑制率计算公式如下。
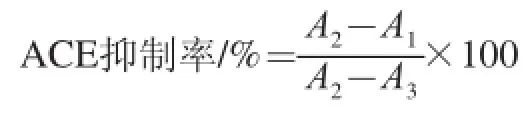
式中:A1为反应中ACE和样品同时存在的吸光度;A2为反应中蒸馏水代替样品的吸光度;A3为加1.0 mol/L盐酸停止ACE与马尿酰-组氨酰-亮氨酸(N-Hippuryl-His-Leu hydrate,HHL)的空白反应的吸光度。
1.2.4 ACE抑制多肽分离方法
1.2.4.1 样品前处理
用MRS液体培养基3 代继代培养Pediococcus acidilactici ID7后,13 000×g离心20 min取乳酸菌菌体,加5 mL灭菌生理盐水制成菌体悬浮液。将菌体悬浮液按接种量1.0%接种于SSP溶液(过滤除菌,0.22 μm),在37 ℃条件下培养72 h。培养后,100 ℃加热处理10 min,10 000×g离心20 min取上清液,与乙醇以体积比1∶9缓慢混合沉淀蛋白(在10 ℃以下的环境进行),离心(10 000×g,20 min),分别回收乙醇可溶性成分和乙醇不可溶性成分,用旋转蒸发仪进行浓缩,加与样品同体积蒸馏水溶解后,过滤除菌(0.22 μm)。pH值调至为8.3后用于测定ACE抑制率。
1.2.4.2 P. acidilactici ID7 SSP溶液培养物的乙醇可溶性成分分析
将P. acidilactici ID7 SSP溶液培养物的乙醇可溶性成分作为分析对象,以未接种乳酸菌SSP溶液为对照。用逆相-HPLC分离乙醇可溶性成分。色谱柱为5C18-AR-300(4.6 mm×250 mm,5 μm),进样量:80 μL;流动相:A为0.05%三氟乙酸(tri fluoroacetic acid,TFA),B为80%乙腈(含0.05% TFA),流速1.0 mL/min。收集移动相B:0~35%(40 min)线性梯度洗脱出的峰。
1.2.4.3 凝胶过滤HPLC分离
爸爸把矜持和骄傲种到了易非的骨子里。这些过眼云烟一样的尊贵和富足,让易非不听任何得道高僧的教诲,就明白一切皆是流水。那些在她面前显摆和卖弄的人,易非打从心眼儿里可怜他们。——尽管他们不知道,他们甚至在想:我倒要看看她到底有多大的定力?
用凝胶过滤HPLC分析逆相-HPLC中高ACE抑制率的洗脱峰。色谱柱为Superdex Peptide HR 10/30,流速为0.8 mL/min,测定波长为220 nm,用0.01% TFA作为移动相收集溶出的峰。收集ACE抑制率较高的峰在同样条件下再次利用凝胶过滤HPLC进行ACE抑制物质的纯化。
1.2.5 分子质量测定方法
对凝胶过滤HPLC纯化得到的峰进行分子质量测定。标准曲线绘制:流动相为0.01% TFA,流速为0.8 mL/min。以已知分子质量的胰岛素A链蛋白(2 532 D)、放线菌素C(1 280 D)及致癌蛋白(586.70 D)为标准品,以已知分子质量的蛋白质溶出时间为横坐标,蛋白质的分子质量为纵坐标绘制标准曲线,得到回归方程为y=-136.02x+4 066.70(R2=0.995 2)。将待测组分溶出时间代入回归方程计算其分子质量。
1.2.6 SSP溶液质量浓度测定
用Bradford法[21]测定。取100 μL ACE抑制溶液,加1 mL Bradford试剂,振动搅拌后,放置5~30 min,用分光光度计在595 nm波长处测定吸光度。以牛血清白蛋白作为标准品,以牛血清白蛋白质量浓度为横坐标,吸光度为纵坐标绘制标准曲线,得到回归方程为y=0.003 6x+ 0.004 6(R2=0.998 7)。将待测组分吸光度代入回归方程计算其质量浓度。
2 结果与分析
16 株乳酸菌SSP溶液培养物的ACE抑制率结果如表2所示。S. thermophilus 2330M2、P. acidilactici ID7、E. faecalis TH15、L. delbrueckii subsp. bulgaricus 7235、L. casei 34143S、L. casei S-3-1、L. casei 6-2-05及L. plantarum 6214等8 株乳酸菌SSP溶液培养物的ACE抑制率为20%以上,其中菌株ID7、6214及TH15的ACE抑制率达到40%以上。E. faecium 220B1、L. helveticus 4024M2、Lactobacillus sp. 305501、L. delbrueckii subsp. bulgaricus M340-1、L. delbrueckii subsp. lactis D340-2的ACE抑制率为10%以下,几乎没有ACE抑制活性,这可能与这些乳酸菌的SSP溶液培养物pH值下降到4.0时,ACE抑制活性物质在酸性环境下被破坏有关。该结果表明,不同乳酸菌SSP溶液培养物ACE抑制活性具有差异,而且,未接种乳酸菌的SSP溶液未检测到ACE抑制活性,证明了乳酸菌SSP溶液培养物的ACE抑制物质是乳酸菌分解SSP溶液而产生的乳酸菌代谢产物。

2.2 P. acidilactici ID7 SSP溶液培养物ACE抑制活性测定结果
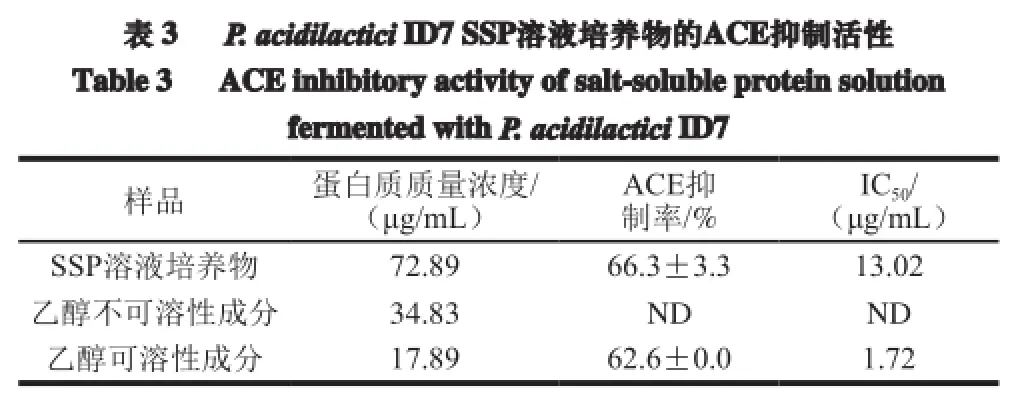
对接种P. acidilactici ID7的SSP溶液培养物分别进行乙醇可溶性成分和乙醇不可溶性成分回收,测定其ACE抑制活性,结果如表3所示。未检测到乙醇不可溶性成分的ACE抑制活性,乙醇可溶性成分的IC50值为1.72 μg/mL,表明ACE抑制物在乙醇可溶性成分中,而且具有较高的ACE抑制活性,因此对乙醇可溶性成分进行了ACE抑制多肽的分离。
2.3 P. acidilactici ID7 SSP溶液培养物乙醇可溶性成分逆相-HPLC分离及ACE抑制活性
将P. acidilactici ID7菌的SSP溶液培养物用95%乙醇进行纯化,对乙醇可溶性成分用逆相-HPLC进行色谱分离,结果如图1所示,获得了2 个峰(峰Ⅰ、峰Ⅱ)。P. acidilactici ID7的SSP溶液培养物和空白对照组的色谱峰完全不一样,说明随着乳酸菌代谢活动,SSP溶液被分解产生新的多肽,而且所有的多肽溶出在30%以下乙腈中,测定其ACE抑制活性结果,峰Ⅰ、峰Ⅱ的IC50值分别为1.21、1.07 μg/mL,说明分离到较高的ACE抑制活性肽,峰Ⅰ、峰Ⅱ蛋白质质量浓度分别为3.17、0.67 μg/mL,说明峰ⅡACE抑制活性更显著。

2.4 凝胶过滤HPLC分离
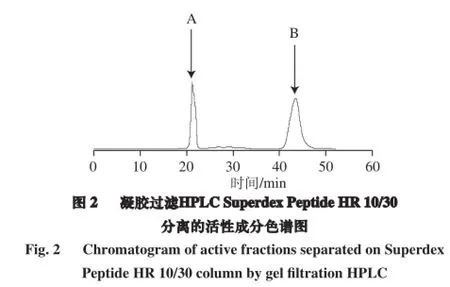
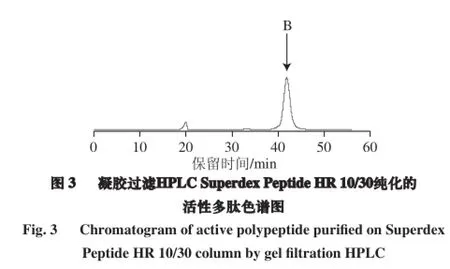
对采用逆相-HPLC分离获得的具有较高ACE抑制活性峰Ⅱ(IC50值为1.07 μg/mL)用凝胶过滤HPLC进行色谱分析,结果如图2所示,在21.30、43.72 min出现2 个峰(A和B),ACE 抑制率分别为3.33%、26.67%,说明ACE抑制活性物在峰B上。用已知分子质量的胰岛素A链蛋白(2 532 D)、放线菌素C(1 280 D)及致癌蛋白(586.70 D)的凝胶过滤HPLC检量线推算出分子质量,分别为1 170 D(峰A)、586.7 D以下(峰B)。将具有ACE抑制活性的峰B再次利用凝胶过滤HPLC进行纯化,获得了单一的ACE抑制活性多肽的色谱(图3)。已有报道证明,酸奶ACE抑制多肽(Ile-Pro-Pro,Val-Pro-Pro)[19]、发酵大豆食品Tofuyo的ACE抑制多肽(Ile-Phe-Leu,Tro-Leu)[17]及鱼肉蛋白水解物的ACE抑制多肽(Met-Tyr,Lys-Trp,Arg-Val-Tyr)[22]对轻度高血压患者具有降压作用。因此,从P. acidilactici ID7菌代谢SSP溶液培养物中分离到的ACE抑制多肽可能与以上报道的一样,具有较高的ACE抑制活性。
3 结 论
通过对16 株乳酸菌代谢SSP溶液培养物中ACE抑制活性的测定,获得了具有较高ACE抑制活性的P. acidilactici ID7(ACE抑制率为47.6%)和L. plantarum 6214(ACE抑制率为40.6%)。从出现较高的ACE抑制活性的P. acidilactici ID7 SSP溶液培养物中进行ACE抑制物分离,结果表明,ACE抑制物在乙醇可溶性成分中。用逆相-HPLC对乙醇可溶性成分进行分离,收集到2 个ACE抑制活性峰(Ⅰ、Ⅱ)。对其中具有较高ACE抑制活性峰Ⅱ(IC50值为1.07 μg/mL)用凝胶过滤HPLC色谱进行分离,得到了ACE抑制率为26.67%,分子质量为586.7 D以下的ACE抑制多肽,说明乳酸菌能分解SSP溶液产生ACE抑制活性多肽。
[1] 光冈知足. 双岐杆菌的研究[M].东京: 日本双歧杆菌研究中心,1994: 23.
[2] VOLLAARD E J, CLASENER H A L. Colonization resistance[J]. Antimicrob Agents Chemother, 1994, 38: 409-414. DOI:10.1128/ AAC.38.3.409.
[3] RAO D R, CHAWAN C B, PULUSIN S R. Influence of milk and thermophilus milk on plasma cholesterol and hepatic cholester genesis in rats[J]. Journal of Food Science, 1981, 46(5): 1339-1341. DOI:10.1111/j.1365-2621.1981.tb04168.x.
[4] PEARCE J. Effects of milk and fermented dairy products on the blood cholesterol content and profile of mammals in relation to coronary heart disease[J]. International Dairy Journal, 1996, 6(7): 661-672. DOI:10.1016/0958-6946(95)00011-9.
[5] WALKER D K, GILLILAND S E. Relationship among bile tolerance bile salt deconjugation, and assimilation of cholesterol by Lactobacillus acidophilus[J]. Dairy Science, 1993, 76: 956-961. DOI:10.3168/jds.S0022-0302(93)77422-6.
[6] 铃木丰, 梅津浩美, 山内吉彦. 发酵乳对摄取高胆固醇饲料大鼠的血清胆固醇浓度的影响[J]. 日畜会报, 1991, 62: 565-571. DOI:10.2508/chikusan.62.565.
[7] 伊藤敞敏. 发酵乳中乳酸菌的功能性[J]. 日本畜产学会报, 1992,63(12): 1276. DOI:10.2508/chikusan.63.1276.
[8] 横仓辉男. 乳酸菌的抗肿瘤效果及免疫活性作用[J]. 酪农科学·食品研究, 1994, 43: 141-150.
[9] SHU Q, BIRD S H, GILL H S, et al. Immunological cross-reactivity between the vaccine and other isolates of Streptococcus bovis and Lactobacillus[J]. FEMS Immunology and Medical Microbiology,1999, 26(2): 153-158. DOI:10.1111/j.1574-695X.1999.tb01383.x.
[10] JIN Shan, OGAWA Y, WATANABE T, et al. Angiotensin I-converting enzyme inhibitory activity of fermented surimi by lactic acid bacteria[J]. Journal of the Japanese Society for Food Science and Technology, 2007, 54: 160-166. DOI:10.3136/nskkk.54.160.
[11] ROBERTS P R, BURNEY J D, BLACK K W, et al. Effect of chain length on absorption of biologically active peptides from the gastrointestinal tract[J]. Digestion, 1999, 60: 332-337. DOI:10.1159/000007679.
[12] NAKAMURA Y. Studies on anti-hypertensive peptides in milk fermented with Lactobacillus helveticus[J]. Bioscience of Microbiota,Food and Health, 2004, 23: 131-138. DOI:10.12938/bifidus.23.131.
[13] YAMAMOTO N, AKINO A, TAKANO T. Antihypertensive effect of different kinds of fermented milk in spontaneously hypertensive rats[J]. Bioscience, Biotechnology, and Biochemistry, 1994, 58(4):776-778. DOI:10.1271/bbb.58.76.
[14] CHEUNG H S, WANG Fenglai, ONDETTI, et al. Binding of peptide substrates and inhibitors of angiotensin-converting enzyme[J]. Biological Chemistry, 1980, 255(2): 401-407.
[15] 松井利郎. 肾素-血管紧张素系统及降血压肽: 以前和以后[J]. 新食品工业, 2005, 47: 11-17.
[16] ICHIMURA T, HU J, AITA D Q, et al. Angiotensin I-converting enzyme inhibitory activity and insulin secretion stimulative activity of fermented fish sauce[J]. Journal of Bioscience and Bioengineering,2003, 96(5): 496-499. DOI:10.1016/S1389-1723(03)70138-8.
[17] KUBA M, TANAKA K, TAWATA S, et al. Angiotensin I-converting enzyme inhibitory peptides isolated from tofuyo fermented soybean food[J]. Bioscience, Biotechnology, and Biochemistry, 2003, 67: 1278-1283. DOI:10.1271/bbb.67.1278.
[18] JAUHIANEN T, COLLIN M, NARVA M, et al. Effect of long-term intake of milk peptides and minerals on blood pressure and arterial function in spontaneously hypertensive rats[J]. Milchwissens Chaft,2005, 60(4): 358-363.
[19] NAKAMURA Y, YAMAMOTO N, SAKAI K, et al. Purification and characterization of angiotensin I-converting enzyme inhibitors from sour milk[J]. Dairy Science, 1995, 78: 777-783. DOI:10.3168/jds. S0022-0302(95)76689-9.
[20] 陈声明, 张立钦. 微生物学研究技术[M]. 北京: 科学出版社,2006: 255.
[21] 冈田雅人, 宮崎香. 蛋白质的基本实验操作, 蛋白质实验手册(上)[M]. 3版. 东京: 羊土社, 2004: 30-31.
[22] MATSUFUJI H, MATSUI T, SEKI E, et al. Angiotensin I-converting enzyme inhibitory peptides in an alkaline protease hydrolyzate derived from sardine muscle[J]. Bioscience, Biotechnology, and Biochemistry,1994, 58: 2244-2245. DOI:10.1271/bbb.58.2244.
Separation and Determination of Angiotensin Converting Enzyme Inhibitory Peptide from Salt-Soluble Protein Solution Fermented with Lactic Acid Bacteria
ZHAO Junliang1, LU Haipeng1, MANG Lai2, JIN Shan1,*
(1. Key Laboratory of Clinical Diagnosis and Treatment Technology in Animal Disease, Ministry of Agriculture,College of Veterinary Medicine, Inner Mongolia Agricultural University, Hohhot 010018, China;2. College of Animal Science, Inner Mongolia Agricultural University, Hohhot 010018, China)
Sixteen lactic acid bacteria (LAB) strains were cultured for 3 generations in MRS liquid medium, centrifuged,prepared into LAB suspension with sterilized physiological saline, and then inoculated in salt-soluble protein (SSP) solution from arabesque greenling. Through determining angiotensin converting enzyme (ACE) inhibitory peptide from metabolites,Pediococcus acidilactici ID7 and Lactobacillus plantarum 6214 displayed high ACE inhibitory activity, with a percentage inhibition of 47.6% and 40.6%, respectively. Higher ACE inhibitory activity in SSP solution fermented with Pediococcus acidilactici ID7 was determined by high performance liquid chromatograph (HPLC). Meanwhile, two peaks after HPLC purification were achieved, which showed IC50of 1.21 μg/mL and 1.07 μg/mL, respectively. The peak with higher ACE inhibitory activity was purified by gel filtration. The obtained ACE inhibitory peptide showed percentage inhibition of 26.67% and molecular weight less than 586.7 D.
lactic acid bacteria (LAB); angiotensin converting enzyme (ACE); salt-soluble protein (SSP); high performance liquid chromatography (HPLC)
10.7506/spkx1002-6630-201609032
Q939.99
A
1002-6630(2016)09-0170-05
赵俊良, 卢海鹏, 芒来, 等. 乳酸菌盐溶性蛋白培养物中血管紧张素转化酶抑制活性肽的测定及分离[J]. 食品科学,2016, 37(9): 170-174. DOI:10.7506/spkx1002-6630-201609032. http://www.spkx.net.cn
ZHAO Junliang, LU Haipeng, MANG Lai, et al. Separation and determination of angiotensin converting enzyme inhibitory peptide from salt-soluble protein solution fermented with lactic acid bacteria[J]. Food Science, 2016, 37(9): 170-174.(in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201609032. http://www.spkx.net.cn
2015-06-24
内蒙古自治区自然科学基金项目(2012MS0405);国家国际科技合作专项(2011DFR30860)
赵俊良(1990—),男,硕士研究生,研究方向为兽医微生物与免疫学。E-mail:13484711238@163.com
*通信作者:金山(1968—),男,副教授,博士,研究方向为兽医微生物与免疫学。E-mail:jinshan@imau.edu.cn
