水镁石-碱法制备重质氧化镁的研究
2016-11-14黄春晖
翟 俊,黄春晖,张 琴,赵 娜,宗 俊
(华东师范大学化学与分子工程学院,上海200241)
水镁石-碱法制备重质氧化镁的研究
翟 俊,黄春晖,张 琴,赵 娜,宗 俊
(华东师范大学化学与分子工程学院,上海200241)
以水镁石和氢氧化钠为原料制备重质氧化镁。探究了原料配比、煅烧温度对氧化镁的表观密度、活性和形貌的影响。研究发现:通过控制原料配比和煅烧温度,可以制备出表观密度达到1 g/mL以上的胶囊状重质氧化镁,这是其他方法很难达到的。在氯化镁与氢氧化钠物质的量比为1∶(1.2~1.8)、煅烧温度为600~750℃条件下,制得氧化镁的表观密度最大,最高可达1.15 g/mL以上。而且制得的氧化镁晶型结构稳定,含杂质较少。
水镁石;重质氧化镁;表观密度;胶囊状;晶型结构
水镁石主要成分为Mg(OH)2·xH2O。就目前世界上已经发现的矿物中氧化镁的含量而言,水镁石是氧化镁含量最高的矿物,氧化镁质量分数高达65%以上。水镁石有害杂质含量少,热分解后产生的是水,而不是CO、CO2或其他对环境有害的气体,有益于环境保护[1]。中国水镁石矿主要分布在陕西、吉林、辽宁等省,总储量达1×107t,仅陕西就占7.8× 106t。水镁石可以露天开采,很有开发利用价值[2]。
重质氧化镁是一种无毒、无臭、无味的白色或米黄色粉末,难溶于水及有机溶剂,但容易吸潮,与空气中的水分及二氧化碳反应形成镁复盐,相对密度为3.58,熔点为2 800℃。商业重质氧化镁比表面积只有35 m2/g左右,在一定温度下水解改性得到氧化镁的比表面积也只有100 m2/g左右[3]。目前,国内外对重质氧化镁的研究相对于其他种类的氧化镁而言还远远不足,对重质氧化镁的定义也没有明确的限定,一般来说表观密度大于0.5 g/mL的氧化镁即可称为重质氧化镁[4]。菱镁矿石或水镁石经轻烧也可得到重质氧化镁[5],例如直接煅烧水镁石就可得到表观密度大于0.8 g/mL的氧化镁。但是,这种方法得到的重质氧化镁为初级产品,品质较差、含杂质较多,无法满足精细化工生产的要求[6]。尽管人们对重质氧化镁的研究较少,但是不能忽视它在工业上的重要用途。重质氧化镁在磁性材料行业用于彩色电视机的偏转线圈(铁氧体软磁)和其他铁氧体磁性材料,在钢球抛光行业做抛光剂,在电器行业做酚醛树脂(俗称电木粉)的原料,另外在饲料、玻璃、陶瓷、工业催化剂、环保行业也有很大的用途[7]。最新发现,重质氧化镁在节能灯的灯座或灯丝里作为添加型材料,具有导热性能良好且阻燃的特性,能提高灯泡的使用寿命,具有很大的应用价值[8]。
笔者采用水镁石-碱法制备重质氧化镁,不仅克服了直接煅烧水镁石带来的杂质含量高的问题,还可以提高氧化镁的表观密度,使其表观密度从0.75 g/mL提高到1.0 g/mL以上,甚至可以达到1.2 g/mL。
1 实验部分
1.1 原料、试剂和仪器
原料与试剂:水镁石矿粉(上海实业振泰化工有限公司),氢氧化钠、盐酸、碘、四氯化碳、可溶性淀粉、五水合硫代硫酸钠、碘化钾均为分析纯,去离子水。仪器:马弗炉、85-2A数显恒温磁力搅拌器、Bruker D8型X射线衍射仪、减压循环真空泵、日立S-4800型扫描电镜。
1.2 重质氧化镁制备
取一定量水镁石粉末,加入HCl溶解,过滤得滤液。向滤液中加入少量H2O2,静置1 d,过滤得滤液。按照n(MgCl2)∶n(NaOH)分别为1∶1.00、1∶1.25、1∶1.50、1∶1.75、1∶2.00、1∶2.25、1∶2.50、1∶2.75、1∶3.00向滤液中加入NaOH,沉淀得到Mg(OH)2,过滤后干燥,在不同温度下煅烧制得MgO。对MgO进行表观密度、活性测定,以及XRD、SEM表征,得出制备MgO的最佳条件。另外,与水选后水镁石直接煅烧制得的MgO相比较。
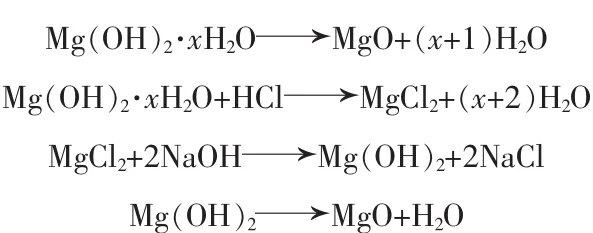
1.3 重质氧化镁性能测定
1)表观密度测定[9]。MgO样品表观密度测定采用轻敲模式。称量10 mL干燥量筒的质量,记为m1;向量筒中倒入MgO粉末,轻轻敲击量筒,直到粉末体积不再改变,再次称量量筒质量,记为m2;记下粉末体积,记为V。则MgO样品表观密度计算公式为(m2-m1)/V,单位为g/mL。
2)碘吸附值测定[10]。精确称取一定质量的MgO加入一定体积的I2-CCl4标准溶液中,超声震荡后过滤,将滤液加入0.1 mol/L的KI-乙醇溶液中,用0.1 mol/L的Na2S2O3标准溶液滴定至终点,计算单位质量MgO的碘吸附值(单位:mg/g)。碘吸附值越大说明MgO的活性越高。
3)柠檬酸活性测定(CAA值)[11]。参照国标法,量取0.1 mol/L的柠檬酸溶液100 mL于烧杯中,滴加3滴酚酞试剂。准确称取1.999 0~2.000 9 g MgO,在30℃下将MgO加入烧杯中,并立刻开始计时,待溶液变红时停止计时,记下时间(即为CAA值)。时间越长说明MgO活性越低。
4)采用Bruker D8型X射线衍射仪对氧化镁粉末进行表征,分析氧化镁的晶体结构。采用日立S-4800型扫描电镜观察MgO的形貌。
2 结果与讨论
2.1 不同工艺条件制得MgO的表观密度
表1列出不同n(MgCl2)∶n(NaOH)以及不同煅烧温度制得MgO的表观密度。从表1不难发现:不论是直接煅烧还是先以不同n(MgCl2)∶n(NaOH)制得Mg(OH)2再经煅烧制得MgO,其表观密度都可达到0.7 g/mL以上,基本都符合重质氧化镁的简单范畴。但同时发现,n(MgCl2)∶n(NaOH)和煅烧温度对最终产物表观密度的影响比较明显。

表1 不同n(MgCl2)∶n(NaOH)以及不同煅烧温度制得MgO的表观密度
以煅烧温度分别为650、7 00、750℃为例,不同n(MgCl2)∶n(NaOH)制得MgO的表观密度见图1a。由图1a看出,随着NaOH用量增加,MgO表观密度在n(MgCl2)∶n(NaOH)=1∶1.25处首先出现一个峰值,MgO表观密度在1.00 g/mL左右。分析其原因是由于Mg2+过量,在沉淀过程中引起吸留和包夹引起的。随着NaOH用量继续增加,MgO表观密度在n(MgCl2)∶n(NaOH)=1∶1.50处有小幅下降(MgO表观密度在0.9 g/mL左右),然后在n(MgCl2)∶n(NaOH)= 1∶1.75处又出现一个峰值,MgO表观密度在1.1 g/mL左右,甚至在煅烧温度为700℃时MgO表观密度达到1.15 g/mL。随后,继续增加NaOH用量,MgO表观密度变化不明显。
以n(MgCl2)∶n(NaOH)分别为1∶0.00、1∶1.00、1∶1.75、1∶2.00、1∶3.00为例,不同煅烧温度制得MgO的表观密度见图1b。由图1b可以看出,随着煅烧温度升高,MgO表观密度先小幅减小后增大。这是由于,450℃的煅烧温度不能使氢氧化镁完全分解,造成刚开始煅烧时MgO的表观密度较大;随着煅烧温度升高,氢氧化镁分解越来越充分,MgO表观密度小幅减小;随着煅烧温度继续升高,MgO表观密度逐渐增大,在煅烧温度为650~700℃时达到最大值,最高值达到1.15 g/mL以上。从图1b还可以看出,直接煅烧和n(MgCl2)∶n(NaOH)=1∶1.00条件制得MgO的表观密度相差不大。但是,在活性方面,直接煅烧制得MgO的活性要比NaOH沉淀再煅烧制得MgO的活性高很多,而且白度也较白,但其纯度不太好。
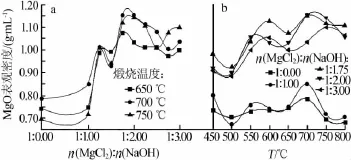
图1 不同n(MgCl2)∶n(NaOH)和不同煅烧温度制得MgO表观密度
2.2 MgO表观密度对活性的影响
表2列出不同n(MgCl2)∶n(NaOH)制得Mg(OH)2在700℃煅烧制得MgO的表观密度、CAA值、碘吸附值。从表2可以看出,MgO的CAA值很高,几乎都在500 s以上,说明MgO的活性很低;从MgO的碘吸附值数据也能说明这一点。

表2 MgO表观密度对CAA值及碘吸附值的影响
图2给出MgO表观密度与CAA值的关系。从图2看出,MgO的CAA值与其表观密度呈正相关性,相反产物的活性与表观密度呈负相关性。因为MgO表观密度大,说明MgO晶体颗粒排列紧密、孔面积小,而且晶体缺陷小、比表面积也较小,这样晶体表面及内部的活性位点也相对较少,从而活性就较低。
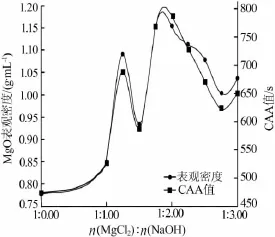
图2 MgO表观密度对CAA值的影响
2.3 MgO的XRD表征
图3为n(MgCl2)∶n(NaOH)=1∶1.75、煅烧温度为700℃制得MgO的XRD谱图。由图3可以看出,在2θ为37.0、43.0、62.4、74.8、78.7°处有衍射峰,与标准卡片氧化镁的衍射峰位置一致,说明制得的产物是氧化镁。另外,样品XRD谱图峰宽很窄且峰强很高,说明产物结晶度好,晶型结构稳定。
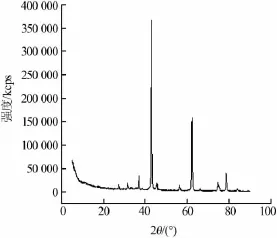
图3 MgO的XRD谱图
2.4 MgO的SEM表征
图4为n(MgCl2)∶n(NaOH)=1∶1.75、煅烧温度为700℃制得MgO的SEM照片。从图4可以看出,MgO颗粒为近似椭球状,或者称为胶囊状。颗粒内部堆积较为紧密、比表面积小、活性位点少,所以活性低,但是表观密度大。

图4 MgO的SEM照片
3 结论
以水镁石和氢氧化钠为原料,通过控制原料配比和煅烧温度等条件,制备出表观密度达到1 g/mL以上的胶囊状重质氧化镁,这是其他方法很难达到的。在n(MgCl2)∶n(NaOH)=1∶(1.2~1.8)、煅烧温度为600~750℃条件下,制得MgO的表观密度最大,最高可达1.15 g/mL以上,而且产物晶型结构稳定、含杂质较少。本方法不仅适用于实验室制备重质氧化镁,也可在工业生产中推广应用。另外,MgO制备过程中不需要添加其他反应物,制备过程简便、环保。所以,该方法制备的氧化镁具有很大的应用价值。
[1] 胡庆福.镁化合物生产与应用[M].北京:化学工业出版社,2004.
[2] 胡庆福,宋丽英,胡晓湘.水菱镁石开发与利用[J].无机盐工业,2005,37(11):44-46.
[3] 董静.高比表面氧化镁催化剂的制备与性能[J].化学反应工程与工艺,2013,29(4):327-331.
[4] 赵娜.纳米氢氧化镁的卤水-碱法合成与分析及重质氧化镁的制备[D].上海:华东师范大学,2015.
[5] 郭如新.水菱镁石和斜方云石的开发与应用[J].盐湖研究,2009,17(3):63-67.
[6] 许荣辉.高纯氧化镁制备原理初探[J].盐湖研究,2003,11(4): 39-41.
[7] 戴淑平,于景坤.电熔氧化镁对镁铬耐火材料致密化的影响[J].材料与冶金学报,2003,2(1):42-44.
[8] 陶道敏.高纯氧化镁用于等离子显示屏涂层[J].无机盐工业,2006,38(6):60.
[9] 彭浩,黄琼珠,路贵民,等.水氯镁石煅烧制备活性氧化镁研究[J].盐业与化工,2010,39(6):7-11.
[10] 张琴,赵娜,翟俊,等.卤水-氨水制备超细Mg(OH)2及超声处理对其影响[J].盐业与化工,2014,43(10):12-15.
[11] 金艳花,潘旭杰,代如梅,等.碳酸铵直接沉淀法制备纳米氧化镁的研究[J].无机盐工业,2014,46(7):33-35.
联系方式:1002880692@qq.com
Research on preparation of heavy MgO by brucite-alkali method
Zhai Jun,Huang Chunhui,Zhang Qin,Zhao Na,Zong Jun
(School of Chemistry and Molecular Engineering,East China Normal University,Shanghai 200241,China)
Heavy MgO was prepared by brucite and sodium hydroxide as raw materials.The influences of the material mix ratio and calcination temperature on bulk density,activity,and morphology of MgO products were investigated.The study found that by controlling the material mix ratio and calcination temperature,capsule shaped heavy magnesium oxide with bulk density of 1 g/mL could be prepared,which was hard by other ways.When amount-of-substance ratio of MgCl2to NaOH was 1∶(1.2~1.8)and calcination temperature at 600~750℃,the prepared MgO′s bulk density could as high as 1.15 g/mL and the crystal structure stability and purity were both well.
brucite;heavy MgO;bulk density;capsule shape;crystal structure
TQ132.2
A
1006-4990(2016)09-0033-03
2016-03-23
翟俊(1989— ),男,硕士,研究方向为无机新材料及纳米材料的制备表征。
