PEG/α-环糊精准聚轮烷水凝胶与BSA相互作用的光谱学研究
2016-11-12林集端赵珺
林集端,赵珺,2
(1华侨大学化工学院生物工程与技术系,福建 厦门 361021;2华侨大学油脂及天然产物研究所,福建 厦门 361021)
PEG/α-环糊精准聚轮烷水凝胶与BSA相互作用的光谱学研究
林集端1,赵珺1,2
(1华侨大学化工学院生物工程与技术系,福建 厦门 361021;2华侨大学油脂及天然产物研究所,福建 厦门 361021)
聚乙二醇(PEG)与环糊精(CD)自组装形成的准聚轮烷水凝胶可作为蛋白缓释载体。在此三元体系中,PEG、CD和蛋白质之间可能存在一定的相互作用。本文以牛血清白蛋白(BSA)为模型蛋白,通过紫外-可见吸收光谱,荧光光谱,X射线粉末衍射(XRD)和NOESY谱分析等技术,研究BSA在PEG/α-CD准聚轮烷水凝胶中结构的变化。结果表明BSA对水凝胶的生成速率具有显著的影响。通过荧光光谱和同步荧光光谱分析可知,BSA在水凝胶中其三级结构发生轻微变化,致使最大荧光发射波长发生红移,而Trp和Tyr残基在水凝胶中其微环境发生了微小变化。这些变化随着BSA浓度的提高而趋于显著。对比XRD谱图发现,水凝胶在加入BSA前后,2θ = 6.56°、11.54°、12.06°、20.56°、22.04°、26.04°这些衍射角位置的谱峰发生明显变化,说明BSA对PEG/α-CD准聚轮烷的晶型有一定的改变,反映了BSA与水凝胶不只是单纯的混合,而且存在形成复合物而改变蛋白质结构的可能性。2D NOESY谱图也表明BSA与PEG/α-CD准聚轮烷之间存在氢原子的相互耦合作用,证明了两者之间的相互作用。
准聚轮烷水凝胶;牛血清白蛋白;环糊精;聚乙二醇;光谱;X射线粉末衍射
自从HARADA等[1-2]首次报道了基于聚乙二醇(polyethylene glycol,PEG)和环糊精(cyclodextrin,CD)的超分子组装体以来,此类超分子组装体在纳米器件、传感器、分子转换器、体内给药释放系统、基因释放载体以及组织工程支架材料等方面得到了多方面的应用[3-4]。在这一组装体中,PEG穿过α-CD的空腔,形成准聚轮烷[5],并依靠氢键、疏水相互作用等次级键形成亚稳态的凝胶状物。这类水凝胶可作为蛋白质或酶的缓释载体,例如HIGASHI等[6-7]将PEG修饰胰岛素或溶菌酶,而后分别与α-或γ-CD混合,制备出一种固相载药缓释体系。他们还报道了PEG/α-CD水凝胶对血清免疫球蛋白IgG分子具有稳定化作用[8]。
到目前为止,尽管PEG/α-CD准聚轮烷水凝胶的合成与应用方面有很多研究,但在研究三元体系中蛋白质空间构象的变化及其影响方面却鲜有报导。探索准聚轮烷水凝胶与蛋白质形成的复合物结构,以及PEG/α-CD对蛋白质结构及活性的影响,对其在缓释给药方面的应用具有重要意义。白蛋白是血浆中最丰富的蛋白质,其蛋白质结构早已为人们所知,它可作为许多内源性和外源性化合物的存放和转运蛋白,对生命活动有着十分重要的作用,因此本研究将牛血清白蛋白(bovine serum albumin,BSA)作为模型蛋白,通过紫外吸收光谱、荧光光谱、X射线粉末衍射(XRD)等技术,研究PEG/α-CD准聚轮烷水凝胶和BSA之间的相互作用。
1 实验部分
1.1主要原料
聚乙二醇(PEG),相对分子质量1000,分析纯,西亚试剂有限公司;α-环糊精(α-CD),分析纯,南京奥多福尼生物科技有限公司;牛血清白蛋白(BSA),阿拉丁试剂有限公司;二水合磷酸二氢钠、十二水合磷酸氢二钠,分析纯,国药集团化学试剂有限公司;去离子水为实验室自制。
1.2主要仪器设备
UV1800型紫外/可见分光光度计,上海美谱达仪器有限公司;FLS920型全功能荧光光谱仪,英国Edinburgh公司;X射线粉末衍射仪,日本理学株式会社;冷冻干燥机,日本爱朗公司;500MHz/AVANCE Ⅲ型高分辨率核磁共振波谱仪,瑞士Bruker公司。
1.3准聚轮烷水凝胶生成动力学考察
用pH7.4的磷酸盐缓冲液配制浓度为0.02g/mL的PEG溶液和0.09g/mL的α-CD溶液,并将1.6 mL α-CD溶液和0.8mL PEG溶液相混合(A液);用上述PEG溶液配制浓度为6mg/mL的BSA溶液(B液),按一定配比加入A液混匀,并控制溶液中BSA浓度分别为0、0.33mg/mL、0.66mg/mL、1.00mg/mL、1.33mg/mL、1.66mg/mL、2.00mg/mL,用UV1800型紫外/可见分光光度计在600nm波长下测定准聚轮烷水凝胶生成过程中浊度随时间的变化曲线,即动力学曲线,检测时间为20min。对数据点进行曲线拟合,而后求导,取拐点处的导数值为最大生成速率vmax,并将此点对应的时刻记为临界时间tc。
1.4水凝胶中BSA的荧光光谱分析
用上述磷酸盐缓冲液配制浓度为8×10-6mol/L的BSA溶液。在25℃下,将PEG/α-CD准聚轮烷水凝胶与BSA混合,常温放置2h,测定溶液的荧光光谱。其中,BSA溶液2mL,准聚轮烷的加入量分别为0、10μL、20μL、40μL、80μL、160μL、320μL。以290nm为激发波长,在FLS920型全功能荧光光谱仪上记录300~500nm波长范围内的发射光谱。同时测定溶液的同步荧光光谱,即激发和发射单色器同时进行扫描,保持发射波长λem与激发波长λex之间的波长差Δλ=20nm,测定不同浓度水凝胶中BSA的发射峰强度和峰位的变化。
1.5X射线粉末衍射分析
取0.09g/mL的α-CD溶液和0.02g/mL的PEG按体积比2∶1混合,静置2h,生成准聚轮烷水凝胶后,冷冻干燥24h,制得粉末状样品。按同样方法,在准聚轮烷水凝胶中加入BSA,控制BSA浓度为5mg/mL,静置2h后冷冻干燥制样。XRD测试条件为:发射源CuKα(λ=0.154056 nm,40kV,30mA),步长0.02°,扫描速度(2θ)为5°/min。
1.6NOESY谱分析BSA结构的变化
用D2O配置0.09g/mL的α-CD和0.02 g/mL的PEG溶液按体积比2∶1混合,加入BSA,使其浓度为60mg/mL,静置2h,生成准聚轮烷后,测NOESY谱。另外,测准聚轮烷BSA的NOESY谱。2D NOESY谱采用90°脉冲序列(90°-T1-90°-Tm-90°-T2),混合时间为200ms,采样数据点阵2048×256;实验温度为30℃。
2 结果与讨论
2.1准聚轮烷水凝胶生成动力学及BSA的影响
准聚轮烷水凝胶形成过程的动力学曲线如图1所示。PEG与α-CD混合后,经过一段时间后,浊度快速上升,而在达到拐点后浊度上升的速率逐渐减缓,最终达到极值,表现出“S”形曲线。图1表明,随着水凝胶中BSA浓度的增加,达到同样浊度所需的时间逐渐变长,表明水凝胶的生成速率下降。通过曲线拟合及求导而得不同BSA浓度下vmax和tc的值及其变化情况,如图2所示。从图2中可看出,随着BSA浓度的提高,vmax逐渐下降,而tc逐渐延长。这一现象说明BSA与水凝胶之间存在一定的相互作用,BSA的存在将延缓PEG与α-CD的自组装。这一方面可能是由BSA与α-CD的相互作用所致,主要表现为BSA的局部疏水性区域的芳香族氨基酸残基(如苯丙氨酸Phe、色氨酸Trp、酪氨酸Tyr等)被未反应的α-CD所占据,导致BSA与PEG的竞争反应致使反应速率降低[9-10]。另一方面,BSA与PEG也存在相互作用,当PEG分子量大到一定程度时,会与蛋白质相互缠绕,将蛋白质包裹住,使BSA无形中阻碍了PEG的自由度,导致PEG与CD的碰撞概率降低[11]。

图1 BSA对准聚轮烷形成的影响

图2 不同BSA浓度下准聚轮烷形成的Vmax与tc
2.2准聚轮烷水凝胶对BSA荧光强度的影响
BSA是一种荧光较强的蛋白质,每个BSA分子含有26个Phe残基,19个Tyr残基和2个Trp残基,这3种氨基酸残基自身都具有荧光性。在测定蛋白质的荧光光谱时,通常Phe和Tyr的能量会转移到Trp上,因此,大多数蛋白质(包括BSA)所显现的荧光几乎都是Trp的荧光。在BSA中,2个Trp残基分别位于134位和213位,而荧光主要是由213位的Trp残基引起的[12]。在2.1节中提到BSA与准聚轮烷发生了相互作用,为了进一步的说明这种相互作用的存在,测定了在不同量的准聚轮烷存在下的BSA的荧光光谱。图3为在加入不同量的准聚轮烷水凝胶时BSA的荧光光谱。从图3可知,水凝胶自身并不具有荧光性,但是当加入量增大到一定程度时,BSA的荧光强度随着水凝胶浓度的增加逐渐降低。作者认为这可能是由于准聚轮烷水凝胶形成的过程中,逐渐把蛋白质包裹在其中,当凝胶的量大时,在物理结构上会显得比较硬,使得蛋白质分子被束缚在其中,空间上变得“拥挤”,分子运动受到一定限制,甚至会造成三级结构的改变,导致Trp残基周围微环境的变化,从而使BSA的荧光强度降低。但是在水凝胶浓度比较低时,其结构较松软,对BSA的束缚程度小,所以荧光强度的降低并不明显。另外,据RAWAT等[13]的报道,聚乙二醇会和BSA发生相互作用,当BSA分子的三级结构在溶液中稍微发生解折叠时,Trp残基会逐渐暴露在溶液中并与聚乙二醇发生相互作用,致使BSA荧光强度降低并红移。在本实验中,BSA的荧光光谱也发生了5nm的轻微红移,这与RAWAT等的结论一致。
由以上的分析可以得到BSA的三级结构发生了轻微的变化,至少蛋白质的部分部位发生了变化。为进一步说明这种变化的存在,测定了BSA的同步荧光光谱,设定Δλ=20nm,考察另一种氨基酸残基Tyr残基微环境的变化,结果如图4所示。从图4中可以看到,随着加入的水凝胶量的增加,荧光强度会逐渐降低,并且发生轻微的蓝移现象,说明Tyr残基的微环境也发生了微小的变化。由此可以基本确定当BSA中加入准聚轮烷水凝胶时,蛋白结构会有一定的变化,但变化幅度很小。HIGASHI等[6,12]所做的缓释体系的研究结果也间接证明这一结论。
2.3BSA与PEG/α-CD准聚轮烷在固相时的XRD衍射图谱分析
为了探讨BSA与PEG/α-CD体系在固相状态下的相互作用,可采用XRD图谱进行比较分析。图5为BSA与准聚轮烷相互作用前后,BSA、准聚轮烷及其三元水凝胶体系的XRD图谱。比较准聚轮烷与BSA/水凝胶的XRD图,可以看到两者的峰形大体上一致,但在6.56°、11.54°、13.16°、20.56°这些2θ值的位置,BSA/水凝胶具有一些新的峰,而在11.36°、13.08°、22.04°等处BSA/水凝胶不具有准聚轮烷的衍射峰。比较BSA与BSA/准聚轮烷的XRD图可以看到,BSA在与准聚轮烷混合前后峰形发生了很大的变化,BSA除了在22°和32°~34°的峰与BSA/水凝胶比较一致外,其余角度的BSA衍射峰在与准聚轮烷混合后均消失。由此可以得出结论,BSA与准聚轮烷不只是单纯的混合,它们在溶液中会发生一定的相互作用,甚至可能生成复合物,致使水凝胶的晶型结构发生变化。

图3 不同准聚轮烷浓度下BSA的荧光光谱

图4 不同准聚轮烷浓度下BSA的同步荧光光谱
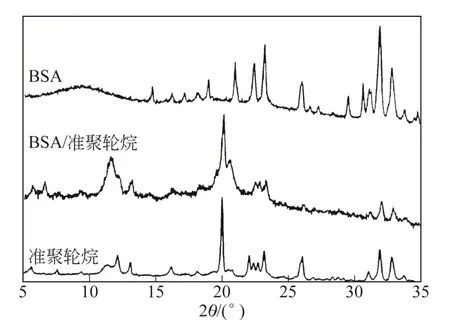
图5 X射线粉末衍射图
2.4BSA与PEG/α-CD准聚轮烷相互作用的NOESY谱
二维核磁共振中的NOESY谱是研究蛋白结构变化的一种常用手段,可用于分析化合物内所有空间距离相近的氢原子对。图6为BSA与PEG/α-CD准聚轮烷相互作用前后的NOESY谱。从图中可以看出BSA与PEG/α-CD结合前后两者部分基团的化学位移都发生的一定的变化。比较图6(a)和图6(b),在BSA与准聚轮烷结合前后,在化学位移1.3附近,BSA的氢原子发生了偏移,可归属为BSA中脂肪族氨基酸(缬氨酸、亮氨酸、异亮氨酸等)侧链氢原子的峰[14],说明BSA中脂肪族氨基酸侧链与准聚轮烷的空间距离近,可以发生一定的相互作用。BSA中芳香族氨基酸氢原子的特征峰出现在3~4.5附近,但与PEG/α-CD准聚轮烷的峰存在交叠。比较图6(a)和图6(c)在3.4~4和5附近的峰,可以看出PEG/α-CD准聚轮烷的峰发生了明显的变化,说明PEG/α-CD准聚轮烷氢原子与BSA中的氢原子之间产生了相互耦合作用。基于以上讨论可以认为,BSA与PEG/α-CD准聚轮烷之间存在相互作用。
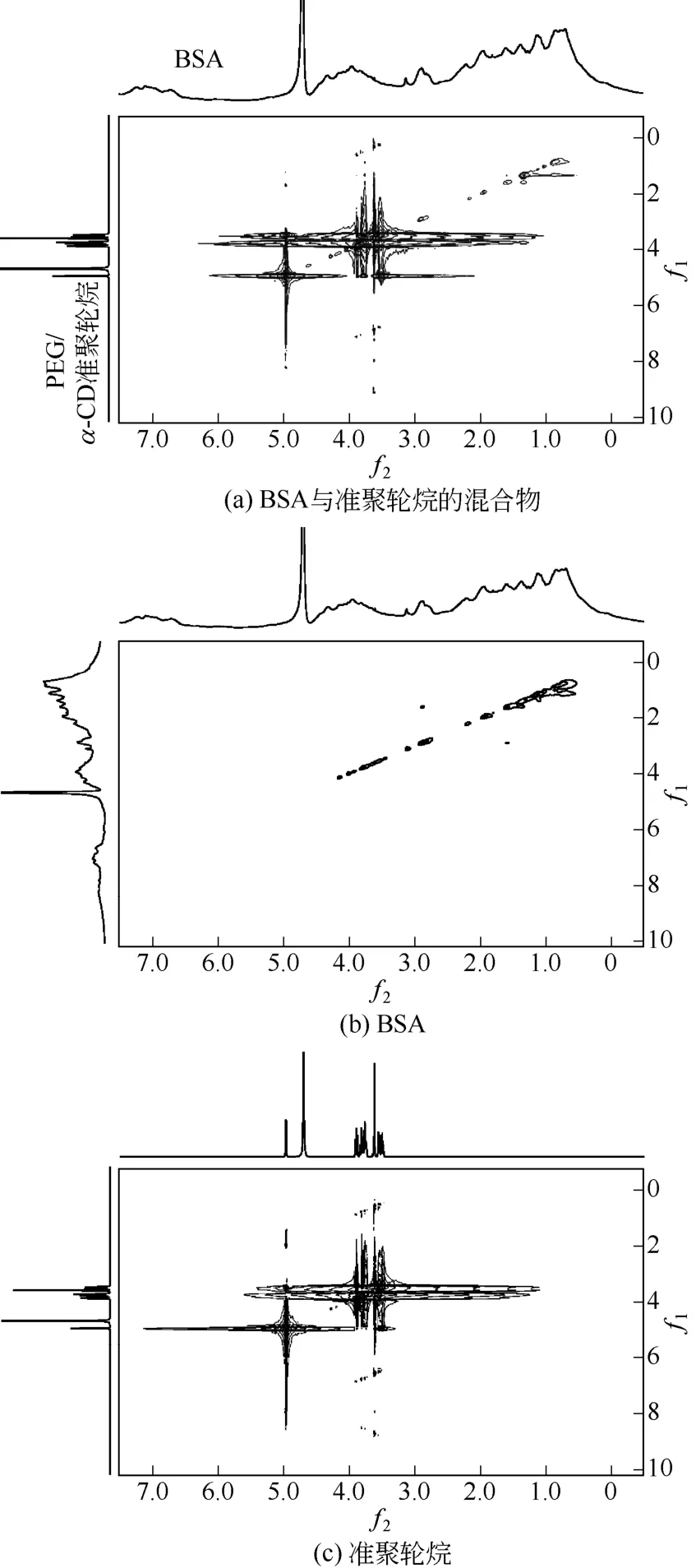
图6 BSA与PEG/α-CD准聚轮烷相互作用的NOESY谱
3 结 论
通过紫外-可见吸收光谱、荧光光谱、XRD、NOESY谱分析等技术对BSA和准聚轮烷水凝胶混合物的分析,可以得出以下主要结论。
(1)在准聚轮烷水凝胶体系中,随着BSA浓度的提高,BSA会抑制PEG和α-CD的穿环反应而使水凝胶的形成速率减缓。
(2)BSA与准聚轮烷形成的三元体系中,它们的作用是相互的,不仅是BSA会影响准聚轮烷的形成速率和晶型结构,而且当准聚轮烷浓度逐渐增大时,BSA的构象也会受到准聚轮烷的影响而发生变化。
[1] HARADA A,KAMACHI M. Complex formation between poly(ethylene glycol) and α-cyclodextrin[J]. Macromolecules,1990,23(10):2821-2823.
[2] HARADA A,LI J,KAMACHI M. The molecular necklace:a rotaxane containing many threaded α-cyclodextrins[J]. Nature,1992,356(6367):325-327.
[3] HARADA A. Cyclodextrin-based molecular machines[J]. Acc. Chem. Res.,2001,34(6):456-464.
[4] WENZ G,HAN B H,MULLER A. Cyclodextrin rotaxanes and polyrotaxanes[J]. Chem. Rev.,2006,106(3):782-817.
[5] GIBSON H W,BHEDA M C,ENGEN P T. Rotaxanes,catenanes,polyrotaxanes,polycatenanes and related materials[J]. Prog. Polym. Sci.,1994,19(5):843-945.
[6] HIGASHI T,HIRAYAMA F,MISUMI S,et al. Polypseudorotaxane formation of randomly-pegylated insulin with cyclodextrins:slow release and resistance to enzymatic degradation[J]. Chem. Pharm. Bull.,2009,57(5):541-544.
[7] HIGASHI T,HIRAYAMA F,YAMASHITA S,et al. Slow-release system of pegylated lysozyme utilizing formation of polypseudorotaxanes with cyclodextrins[J]. Int. J. Pharm.,2009,374(1/2):26-32.
[8] HIGASHI T,TAJIMA A,OHSHITA N,et al. Design and evaluation of the highly concentrated human IgG formulation using cyclodextrin polypseudorotaxane hydrogels[J]. AAPS Pharm. Sci. Tech.,2015,16(6):1290-1298.
[9] ROGOZEA A,MATEI I,TURCU I M,et al. EPR and circular dichroism solution studies on the interactions of bovine serum albumin with ionic surfactants and beta-cyclodextrin[J]. J. Phys. Chem. B,2012,116(49):14245-14253.
[10] LIU Y,LIU Y,GUO R. Insights into cyclodextrin-modulated interactions between protein and surfactant at specific and nonspecific binding stages[J]. J. Colloid Interface Sci.,2010,351(1):180-189.
[11] WU J,ZHAO C,LIN W,et al. Binding characteristics between polyethylene glycol(PEG)and proteins in aqueous solution[J]. J. Colloid Interface Sci.,2014,2(20):2983-2992.
[12] HIGASHI T,HIRAYAMA F,MISUMI S,et al. Design and evaluation of polypseudorotaxanes of pegylated insulin with cyclodextrins as sustained release system[J]. Biomaterials,2008,29(28):3866-3871.
[13] RAWAT S,RAMAN S C,SAHOO D K. Molecular mechanism of polyethylene glycol mediated stabilization of protein[J]. Biochem. Biophys. Res. Commun.,2010,392(4):561-566.
[14] OI W,ISOBE M,HASHIDZUME A,et al. Macromolecular recognition:discrimination between human and bovine serum albumins by cyclodextrins[J]. Macromol. Rapid Comm.,2011,32:501-505.
Spectroscopic study of the interaction between PEG/α-cyclodextrin pseudopolyrotaxane hydrogel with BSA
LIN Jiduan1,ZHAO Jun1,2
(1Department of Bioengineering and Biotechnology,College of Chemical Engineering,Huaqiao University,Xiamen 361021,Fujian,China;2Institute of Oil and Natural Products,Huaqiao University,Xiamen 361021,Fujian,China)
Self-assembled pseudopolyrotaxane hydrogel formed by polyethylene glycol(PEG)and cyclodextrin(CD)can be used as a slow-release carrier for proteins. In this ternary system,there may be certain interactions between PEG,CD and proteins. With bovine serum albumin(BSA)as the model protein,the structure changes of BSA in the PEG/α-CD pseudopolyrotaxane hydrogel was studied by ultraviolet-visible absorption spectrum,fluorescence spectrum,powder X-ray diffraction(XRD)techniques,and NOESY spectra. The results showed that BSA had a significant effect on the formation rate of the hydrogel. The fluorescence and synchronous fluorescence spectrum analysis showed that the ternary structure of BSA had minor changes in the hydrogel,which led to red-shift of the maximum fluorescence emission wavelength,and the microenvironment of Trp and Tyr residues also changed slightly in the hydrogel. These changes became more significant with the increasing of BSA concentration. Moreover,when BSA was added,the diffraction angles in XRD spectra at 2θ = 6.56°,11.54°,12.06°,20.56°,22.04°and 26.04°showed remarkable changes compared with those of the pure pseudopolyrotaxane,demonstrating that the crystalline pattern of PEG/α-CD pseudopolyrotaxane was changed in the presence of BSA. The results reflected that BSA was not simply physically mixed with the PEG/α-CD pseudopolyrotaxane hydrogel,but that it might prefer to form complexes with the hydrogel. 2D NOESY spectra also showed that the presence of mutual coupling of hydrogen atoms between BSA and PEG/α-CD,demonstrated the interaction between them.
pseudopolyrotaxane hydrogel;bovine serum albumin;cyclodextrin;polyethylene glycol;spectroscopy;powder X-ray diffraction
O 636.1
A
1000-6613(2016)11-3590-05
10.16085/j.issn.1000-6613.2016.11.031
2016-01-28;修改稿日期:2016-06-15。
福建省自然科学基金(2013J05028)、华侨大学引进人才科研启动项目(11BS408)及华侨大学研究生科研创新能力培育计划项目。
林集端(1990—),男,硕士研究生,研究方向为环糊精水凝胶。联系人:赵珺,博士,讲师。E-mail zhaojun@hqu.edu.cn。
