新型水溶性咪唑基硅量子点制备及用于果蔬中痕量铜的荧光检测
2016-11-09王佳佳连曼熊杰李在均
王佳佳连曼熊杰李在均*,2
(江南大学化学与材料工程学院1,食品胶体与生物技术教育部重点实验室2,无锡214122)
新型水溶性咪唑基硅量子点制备及用于果蔬中痕量铜的荧光检测
王佳佳1连曼1熊杰1李在均*1,2
(江南大学化学与材料工程学院1,食品胶体与生物技术教育部重点实验室2,无锡214122)
硅量子点因其极佳的亲生物性和光学性能成为纳米材料新宠,但传统硅量子点水溶性差限制了它的广泛应用。本实验以三甲基硅咪唑为硅前驱体采用水热法制备水溶性咪唑基硅量子点。相对于硼氢化钠、抗坏血酸、牛血清蛋白、半胱氨酸和柠檬酸,柠檬酸钠作为还原剂和稳定剂制得的硅量子点荧光发射最强。合成反应于220℃下可在2 h内完成,所制备的硅量子点水溶性好,平均粒径为2.6 nm,红外分析证实其表面存在游离的咪唑基。研究表明,硅量子点能与铜离子相互作用导致荧光强度的明显下降。考察不同温度下Cu2+对硅量子点荧光的猝灭行为,发现荧光猝灭程度随温度升高而增大。这说明荧光下降属于静态猝灭,即Cu2+与硅量子点上的咪唑基作用形成稳定配合物。此外,共振光散射分析还揭示荧光猝灭过程伴随着粒子团聚。基于硅量子点的荧光猝灭行为,建立了痕量铜的荧光检测方法。当Cu2+浓度在0.04~2400μmol/L之间,硅量子点的荧光强度随Cu2+浓度的增加而线性下降,检出限(S/N=3)达1.29×10-8mol/L。本方法具有高的灵敏度、选择性和重现性,已应用于果蔬中痕量铜的荧光检测。
三甲基硅咪唑;硅量子点;水热法;荧光检测;铜离子
1 引言
自20世纪70年代,半导体量子点因特殊的光电性能、优良的生物相容性和卓越的稳定性,替代了传统有机染料,应用于荧光探针、生物成像和医疗诊断等领域[1~3]。随着量子点理论和应用技术的迅速发展,各种新型量子点不断涌现,包括CdS,CdSe,CdTe,InP,InAs,GaAs,PbS,PbSe和ZnS[4~12]。然而,重金属的毒性限制了半导体量子点在生物医学尤其是活体中的应用。Derfus等[13]的研究表明,CdSe量子点在紫外线照射下对活体细胞有巨大的生物毒性。此外,重金属的使用还可能带来环境污染。近年来,硅量子点作为一种新的纳米材料备受关注[14]。尽管硅量子点具有极佳的亲生物性和光学性能,但传统硅量子点水溶性差给它的应用带来诸多不利。
水溶性硅量子点的制备可分为物理和化学两种方法。物理法能方便地调控硅量子点粒径,但它需要使用昂贵仪器。更重要的是,物理法不能从根本上解决硅量子点水溶性差的难题。相对于物理法,化学法得到了更快发展。目前,主要的化学法是电化学刻蚀法、微乳液法、溶液还原法和水热法。Kang等[15]采用电化学刻蚀法,以磷钼酸为催化剂,通过控制电流密度制备了不同尺寸分布的硅纳米晶。电化学刻蚀法是目前硅量子点合成较为常用的化学方法。虽然电化学刻蚀法简单易行,生产成本低,但大量合成硅量子点时难以控制粒子的尺寸分布,且需要使用剧毒化学试剂HF。Warner等[16,17]在甲苯和四辛基溴化铵溶液中采用LiAlH4还原SiX4(X=Cl,Br或I)制备硅量子点,该微乳液法避免了使用HF,但体系含水量较少,内部胶束单分性不易控制,所得纳米晶体产量较低,产品质量良莠不齐。Health等[18]在非极性有机溶剂中采用金属钠还原SiCl4和R-SiCl3制到硅量子点。Bley等[19,20]采用溶液还原法以Na4Si4还原NH4Br,制得表面带硅氢键的硅量子点,并进一步修上氨基,以增强水溶性。溶液还原法制得的硅量子单分散性好,采用微波辅助后,反应速率明显加快。尽管溶液还原法制备硅量子点取得了重要进展,但仍存在一些共同的缺点。首先,通过溶液还原法合成的量子点表面布满Si H键,导致硅量子点水溶性和稳定性差,因此需要进一步硅烷化,将亲水基团连接在硅量子点表面,以增强其水溶性和稳定性[21~27]。但是,硅量子点表面硅烷化修技术较为复杂,例如,铂催化反应效率高,但后续分离困难,且催化剂易吸附在硅量子点表面带来一定的生物毒性。同时,硅烷化修还提高了生产成本;光催化反应能够避免杂质引入,但反应时间较长,效率不高。此外,硅量子点包覆前后长时间和大剂量的紫外光辐射还可能导致光学性能下降;热反应法合成时间长,易引起量子点荧光效率降低。最近,Zhang等采用水热法一步合成表面氨基修的水溶性硅量子点[28],避免了使用硅烷化反应,使水溶性硅量子点的制备变得十分简单,为它的广泛应用奠定了坚实基础。
本实验以三甲基硅咪唑为硅前驱体,采用水热法制备水溶性咪唑基硅量子点。此硅量子点水溶性好,具有强而稳定的荧光发射。基于硅量子点与Cu2+作用产生显著的荧光猝灭,建立了测定铜的荧光分析方法。本方法具有高的灵敏度、选择性和重现性,已成功应用于果蔬中痕量铜的荧光检测。
2 实验部分
2.1仪器与试剂
Cary Esclipse荧光光度计(美国瓦里安公司);JEM-2100(HR)透射电子显微镜(日本JEOL公司); Nicolet iS50 FT-IR傅立叶红外光谱仪(美国赛默飞世尔科技公司);S-4800场发射扫描电子显微镜(日本日立株式会社);FLS920稳态/瞬态荧光光谱仪(英国Edinburgh Instruments公司);YLD-2000烘箱(南京万能加热设备厂);DZF-6020真空干燥箱(上海新苗医疗器械制造有限公司);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司)。
三甲基硅咪唑、柠檬酸三钠、浓HNO3、HClO4和CuSO4(分析纯,国药集团化学试剂公司)。BR缓冲溶液(H3PO4、乙酸和H3BO3的浓度均为0.04 mol/L,NaOH浓度为0.02 mol/L,pH 10.38)。实验用水均为二次蒸馏水(由一次蒸馏水经石英亚沸蒸馏器蒸馏制得)。铜标准溶液配制:称取适量CuSO4,配成Cu2+溶液,然后用EDTA标定准确浓度。
2.2硅量子点的合成
将0.3 g柠檬酸三钠溶于8 mL水,搅拌下滴加2 mL三甲基硅咪唑,转入高压反应釜,于220℃下水热反应120min,然后冷却至室温,用1 kDa透析袋透析除去固体杂质得到硅量子点。将硅量子点于4℃储存,待用。使用时,准确移取0.5mL此储备液,采用二次蒸馏水稀释至10 mL,得到硅量子点工作液[29]。
2.3荧光测定
移取0.25mL硅量子点工作液于离心管中,加入0.5mL BR缓冲溶液,加二次蒸馏水至总体积为1 mL (激发波长和发射波长分别为360和422 nm),摇匀,然后在荧光光度计上测定荧光光谱或荧光强度。
2.4Cu2+的测定
移取0.25mLCu2+标准溶液或样品溶液于离心管中,依次加入0.5mL BR缓冲溶液(pH 10.38)和0.25 mL硅量子点工作液,摇匀,然后在荧光光度计上测定荧光光谱或荧光强度。
2.5果蔬样品预处理
果蔬样品收集于当地市场。样品经洗涤、烘干,并研磨成粉末。将粉末样品置于真空干燥箱中,于105℃干燥至恒重,取出,冷却至室温,存储于干燥器中备用。称取1 g粉末样品于100 mL小烧杯中,加入10 mL浓HNO3,盖上表面皿浸泡24 h后,置于电炉上低温加热至颗粒熔化,再加8 mL浓HNO3和5 mL HClO4,摇匀,在电炉上加热。当溶液颜色转变为棕红色时,加入5 mL浓HNO3,继续加热至溶液澄清透明,降温蒸发至近干,冷却,用二次蒸馏水定容至10 mL。
3 结果与讨论
3.1硅量子点合成
硅量子点合成包括两个过程。第一个过程是三甲基硅咪唑水解生成二氧化硅纳米粒子。第二个过程是二氧化硅被还原生成硅量子点。前者的反应速率取决于体系酸度。碱性越强,三甲基硅咪唑水解越快,形成的二氧化硅粒子较大,不利于它在后期的还原,从而导致大量副产物产生。酸性越强,三甲基硅咪唑水解被抑制的程度也越大,这将造成硅量子点生成速率显著下降,甚至硅量子点合成失败;后者的反应速率取决于还原剂的还原能力。还原能力越强,形成硅粒子越快。由于硅粒子形成过快,并不利于硅晶体生长,产品中含有较多无定形硅,使硅量子点的荧光量子产率降低。还原剂的还原能力较弱生成硅纳米粒子的速率较小,这有利于形成结晶度高的硅粒子,硅量子点的荧光量子产率得到提高。然而,采用较弱的还原剂合成硅量子点,客观上要求一个更高的反应温度和更长的反应时间。大量的实践证明,水溶性硅量子点合成中的还原剂必须具备3个功能:还原剂应具有适当的还原能力,以确保形成的硅量子点是量子产率较高的硅晶体粒子;还原剂是硅纳米粒子的稳定剂,它的组成和结构决定了硅量子点的水溶性和稳定性;还原剂还是体系的酸度调节剂。它为三甲基硅咪唑水解提供一个适当的酸度,以确保二氧化硅的生成与后期的还原速率大致相当,不会造成硅源的大量浪费。可见,还原剂的选择对水溶性硅量子点的合成是至关重要的。
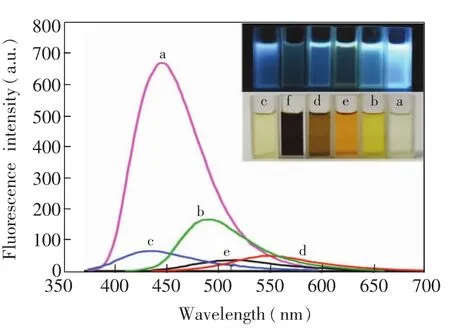
图1 不同还原剂所制备的硅量子点的荧光光谱。柠檬酸三钠(a)、柠檬酸 (b)、半胱氨酸 (c)、牛血清蛋白(d)、硼氢化钠(e)和抗坏血酸 (f)。插图:不同还原剂制得硅量子点的紫外(上)和可见光(下)照片Fig.1 Fluorescence spectra of silicon quantum dots prepared by using different reducing reagent.Sodium citrate(a),citric acid(b),cysteine(c),bovine serum albumin(d),sodium boron hydride(e)and ascorbic acid(f).Inset:Photographs of the silicon quantum dots prepared by using different reducing reagent under UV light(upper)and visible light(under)
实验分别尝试了以硼氢化钠、抗坏血酸、牛血清蛋白、半胱氨酸、柠檬酸和柠檬酸钠为还原剂合成水溶性咪唑基硅量子点。所得产物先在分光光度计上于200~900 nm波长范围内扫描得到紫外-可见吸收光谱,然后在荧光光度计上选择最大吸收波长为激发波长进行荧光扫描。从图1可见,抗坏血酸作为还原剂得到的产品几乎没有任何荧光发射,这是因为抗坏血酸弱的酸性和还原性。弱酸性抑制了三甲基硅咪唑的水解,而弱的还原性使硅量子点形成速率极慢,上述因素造成产品中硅量子点数量少,因此表现为极弱的荧光发射。尽管硼氢化钠具有超强的还原能力,但它极易与H+结合产生H2,在水中存在时间仅为数分钟。如此短的作用时间,它还原二氧化硅所产生的硅量子点数量非常少。另外,硼氢化钠没有稳定硅纳米粒子的功能,所得到的硅量子点水溶性和稳定性差。因此,采用硼氢化钠作还原剂的硅量子点荧光强度较弱;相对于抗坏血酸,牛血清蛋白、半胱氨酸和柠檬酸还原能力较强,硅量子点荧光发射明显增强;作为水溶性硅量子点合成的还原剂,柠檬酸三钠最为理想。一方面,柠檬酸三钠的水溶液呈碱性,可为三甲基硅咪唑水解提供适当的碱性环境,生成二氧化硅的速率明显高于采用酸作为还原剂的体系;另一方面,柠檬酸三钠具有强的还原能力,导致二氧化硅转变为硅晶体粒子的速率较快。柠檬酸三钠体系中二氧化硅的生成和还原实现了一个最佳匹配。由于硅源被完全转化为硅量子点,得到的产品为透明无色溶液。该产品不仅具有最强的荧光,而且稳定性和水溶性俱佳。因此,柠檬酸三钠被选择为合成硅量子点的还原剂。
图2A是不同柠檬酸三钠加入量下所制备硅量子点的荧光峰强度。当柠檬酸三钠用量少于0.3 g时,体系的荧光强度随着柠檬酸三钠用量的增加而迅速增大。因为使用一个高浓度的柠檬酸三钠带来一个更强的还原能力,使二氧化硅还原为硅晶体的速度加快,形成的硅量子点数量增多,从而导致了体系荧光强度的明显增加。当柠檬酸三钠用量超过0.3 g时,体系荧光强度随柠檬酸三钠用量的增加而迅速下降。这是因为柠檬酸三钠具有较强的碱性,它的用量增加使体系碱性迅速增大,这加快了三甲基硅咪唑水解,使二氧化硅的生成速率快于它在后期的还原,将造成二氧化硅粒子的大量累积而发生沉淀,导致形成的硅量子点数量减少和荧光强度减弱。图2B是不同柠檬酸三钠用量下制备的硅量子点的紫外-可见吸收光谱。所有紫外吸收光谱的形状和最大吸收波长基本相同,这表明不同柠檬酸三钠用量下所制备的硅量子点具有相似的粒径大小及粒径分布。然而,还观察到不同柠檬酸三钠用量下硅量子点的吸光度存在明显差异。当柠檬酸三钠用量超过0.3 g时,硅量子点的吸光度随柠檬酸三钠用量的增加而增大,显示硅量子点的数量增长。继续增加柠檬酸三钠用量,硅量子点吸光度反而下降,显示硅量子点的数量减少。为了得到强的荧光发射,柠檬酸三钠用量确定为0.3 g。
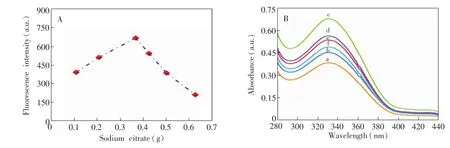
图2 (A)柠檬酸三钠用量的影响,(B)0.1,0.2,0.3,0.4,0.5和0.6 g的柠酸酸三钠用量制备的硅量子点紫外-可见吸收光谱(从a到f)Fig.2 (A)Effect of the amounts of sodium citrate and(B)ultraviolet-visible absorption spectra of the silicon quantum dots prepared by using 0.1,0.2,0.3,0.4,0.5 and 0.6 g of sodium citrate(from a to f)
图3A是不同反应时间合成硅量子点的荧光强度。随着反应时间增加,体系荧光强度将迅速增大,这是因为硅量子点数量增多所致。当反应时间增加到120min,增势趋缓,最后保持基本不变,说明合成反应达到平衡。图3B是不同反应时间制得的硅量子点的吸收光谱。从图3B可知,随着反应时间延长,硅量子点吸光度迅速增加,这说明延长反应时间产生的硅量子点数量增加,这将导致荧光强度的增加。此外,从图3B还可见,量子点吸光度增加的同时最大吸收波长逐步向长波方向移动,表明随着反应时间延长,硅量子点的粒径将缓慢增大。反应时间为150 min时,硅量子点的吸收光谱发生较大变化。它的吸收峰变高变宽,表明粒子的粒径分布更宽。为了节省时间和得到粒径分布较窄的硅量子点,的硅量子点合成反应时间选择120 min。

图3 (A)反应时间的影响,(B)不同反应时间制得的硅量子点的吸收光谱。反应时间分别为25,50,75,100,120和150min(由下到上)Fig.3 (A)Effect of reaction time and(B)absorption spectra of silicon quantum dots prepared by using different reaction time.Here,the reaction times are 25,50,75,100 120 and 150 min,respectively(from bottom to top)
3.2结构表征
透射电镜、扫描电镜和红外光谱分析被用于硅量子点的结构表征。由图4a可见,硅量子点为规整的球形,分散性较好,没有发现明显的团聚。硅量子点粒径在1~5 nm之间,经统计软件计算表明,硅量子点的平均粒径为2.6 nm。由产品中硅元素的能量色散光谱图(EDS,图4c)可见,硅量子点中存在C,O,Si和Na元素。其中,Si来自硅晶体,形成了硅纳米粒子。C,O和Na源于柠檬酸三钠,表明硅量子点上存在少量柠檬酸钠。图4d是量子点的红外光谱。在红外光谱中,1053.26 cm-1处有一个很强的吸收峰,说明了存在Si O键;1261.89 cm-1处较强的吸收峰是CO伸缩振动引起的,表征了CO键的存在;1667.75 cm-1处是NC的伸缩振动,说明了NC 键的存在;3124.69,3097.33和3011.50 nm处的3个峰说明了体系中存在3个不同的sp2杂化的CH。从上述红外分析结果可以得出一个结论:硅量子点表面存在咪唑基。
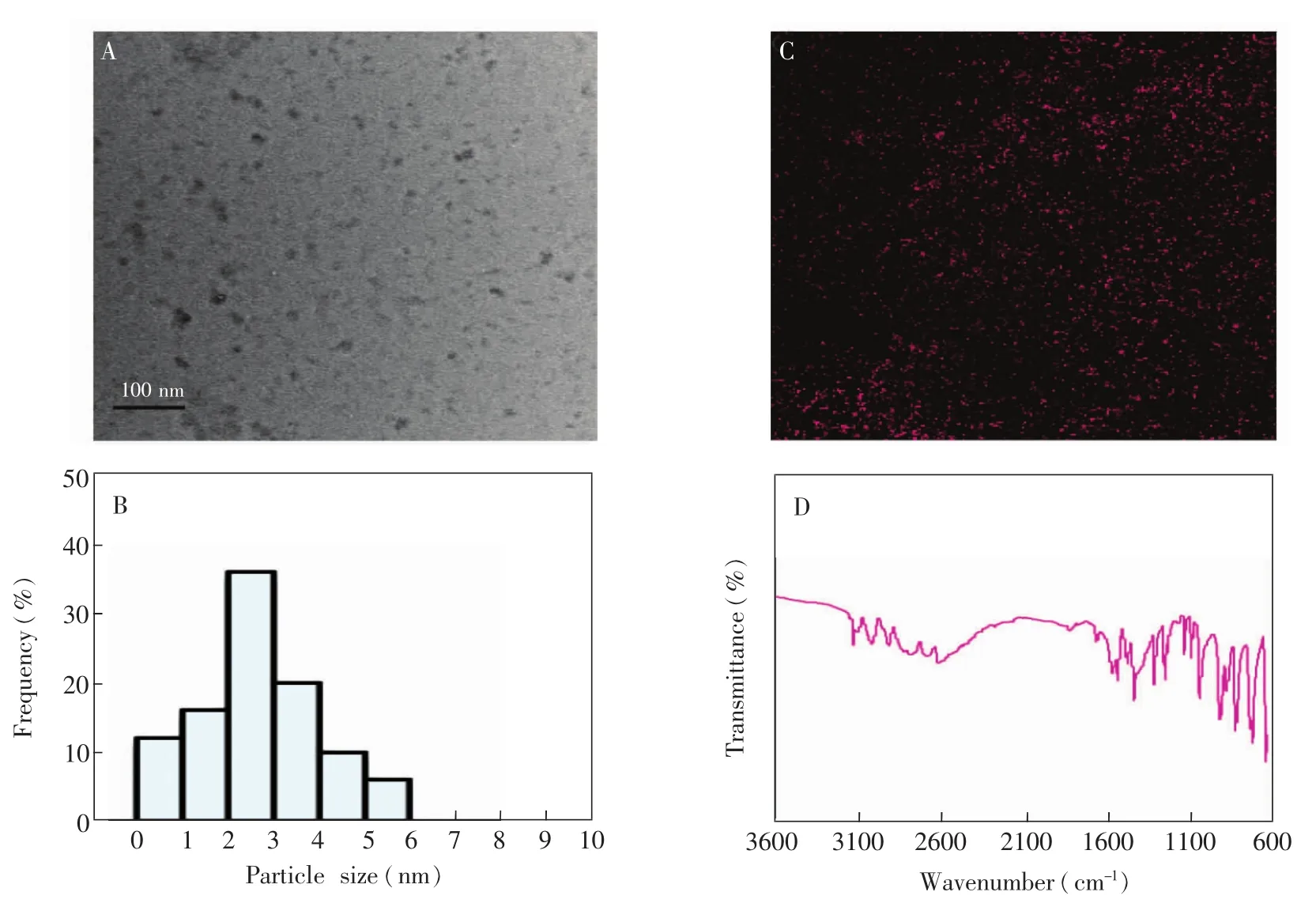
图4 硅量子点的透射电镜(A)、粒径分布(B)、EDS(C)和红外光谱图(D)Fig.4 TEM image(A),particle size distribution(B),energy dispersive spectroscopy(EDS)(C)and FTIR spectrum of silicon quantum dots(D)
3.3光学性质
咪唑基硅量子点具有良好的水溶性,产品为无色透明溶液,它的激发光谱和发射光谱见图5。图5显示,硅量子点的最大激发波长位于360 nm。在此波长激发下,硅量子点的荧光发射峰位于422 nm,比其它波长激发下的荧光强度更大。图5插图为合成反应前后体系在紫外灯照射下的光学照片。由于反应前的溶液基本没有荧光发射,而反应后的溶液发出明亮的蓝光,说明荧光来自反应产生的硅量子点。此外,硅量子点的荧光量子产率达到29.77%,呈示高的发光效率。
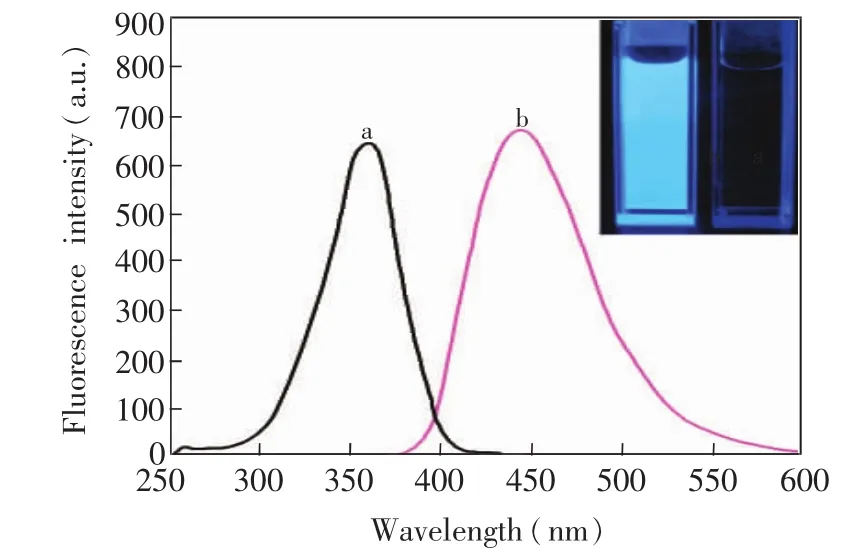
图5 硅量子点的激发光谱 (a)和发射光谱 (b)。插图:反应前(右)后(左)溶液在紫外灯辐射下的光学照片。Fig.5 Fluorescence excitation(a)and emission spectra (b)of silicon quantum dots.Inset:photographs of the solution before(right)and after(left)the reaction completed.
为考察咪唑基硅量子点的光稳定性,将硅量子点置于500W氙灯下照射,每隔一定时间测定其荧光强度的变化,结果列于图6。在光辐射开始的一段时间内,硅量子点的荧光强度略有下降,但继续延长光照时间,硅量子点的荧光基本保持不变,说明所合成的硅量子点具有良好的光稳定性。由于咪唑基稳定的硅量子点具有较好的光稳定性,它作为荧光探针用于金属离子的定量分析可获得好的重现性。
硅量子点在不同酸度条件下的荧光强度见图7。在酸性条件下,硅量子点的荧光强度较低,且酸性越强荧光强度越弱。在pH 2~7之间,硅量子点的荧光强度随pH值增加而线性增长;在pH 7~14之间,硅量子点的荧光较为稳定,改变pH并不影响荧光强度。这种荧光强度随pH值的变化规律表明硅量子点表面存在咪唑基。咪唑基对于H+较为敏感,在酸性条件下,咪唑基上未参与共轭的N易结合质子发生电荷传递,同时诱导硅量子点发生团聚,使得荧光淬灭。因此,pH值越小,荧光淬灭越完全。由于在中性及碱性条件下咪唑基稳定的量子点较为稳定,硅量子点可用于生物活体的细胞成像或生物医学分析等。
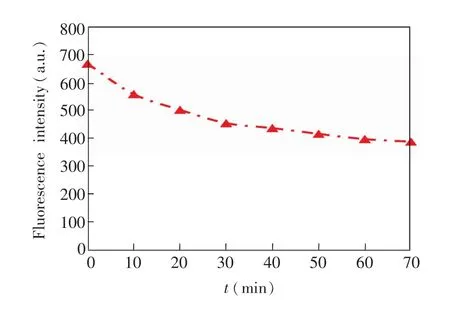
图6 不同光照时间的硅量子点荧光强度Fig.6 Fluorescence intensity of silicon quantum dots under ultraviolet lightwith different irradiation time
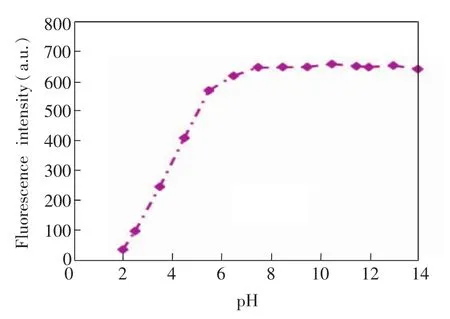
图7 介质pH值的影响Fig.7 Effect of pH value ofmedium
3.4对Cu2+的荧光响应
图8A加入铜离子前后硅量子点的荧光光谱。从图8A可知,加入Cu2+后,硅量子点的荧光强度明显下降,表明Cu2+能对硅量子点的荧光产生显著的猝灭作用。为了研究此荧光猝灭的机理,测定了不同浓度Cu2+存在下硅量子点荧光强度随温度变化的情况。图8B表明,荧光猝灭程度与Cu2+浓度为良好的线性关系,且随温度升高,荧光猝灭的程度加大,说明Cu2+对硅量子点的荧光猝灭可能属于静态猝灭,即Cu2+与硅量子点作用形成了非荧光的基态化合物。
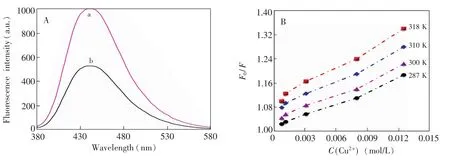
图8 硅量子点加入2.4mmol/L Cu2+前(a)后(b)荧光光谱(A),不同温度下和不同浓度的Cu2+硅量子点荧光猝灭情况(B)Fig.8 (A)Fluorescence spectra of silicon quantum dots before(a)and after(b)addition of 2.4mmol/L of Cu2+.(B)Fluorescence quenching of different concentration of Cu2+towards silicon quantum dots under different temperature
图9A是硅量子点、Cu2+溶液和含有Cu2+的硅量子点溶液的紫外可见吸收光谱和光学照片。Cu2+溶液为浅蓝色,它在650~900 nm之间有较小的吸收。硅量子点为无色溶液,在可见区基本上没有吸收,但在紫外区有较强的吸收。然而,当Cu2+加入到硅量子点后,溶液颜色立即加深,在650 nm附近出现较强的吸收。由于它的吸收峰明显不同于单独的Cu2+溶液,说明Cu2+的加入导致形成了新的化合物。由不同浓度Cu2+下的硅子点的共振光散射光谱(图9B)可见,共振光散射的强度随Cu2+浓度的增加而增大,这说明Cu2+与硅量子点作用导致了粒子的聚集发生。基于以上分析,荧光猝灭机理是Cu2+与硅量子点咪唑基上的氮原子结合形成配合物(图10)。限于空间位阻,Cu2+与咪唑基上.氮原子的配位主要是发生在不同硅量子点之间。
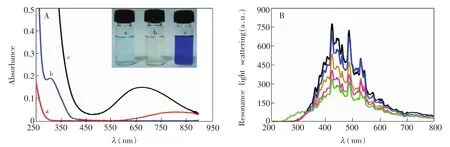
图9 A:Cu2+(a)、硅量子点(b)和含2.4 mmol/L Cu2+的硅量子点(c)的紫外可见吸收光谱和光学照片(插图)。B:硅量子点在含有不同浓度Cu2+下的共振光散射光谱。铜离子浓度:0.0,1.4,2.4,3.0和3.2mmol/L(从下到上)Fig.9 (A)Absorption spectra and photographs(Inset)of Cu2+solution(a),silicon quantum dots(b)and silicon quantum dots containing 2.4 mmol/L of Cu2+(c);(B)Resonance light scattering spectra of the silicon quantum dots in the presence of 0.0,1.4,2.4,3.0 and 3.2 mmol/L of Cu2+(from down to top).
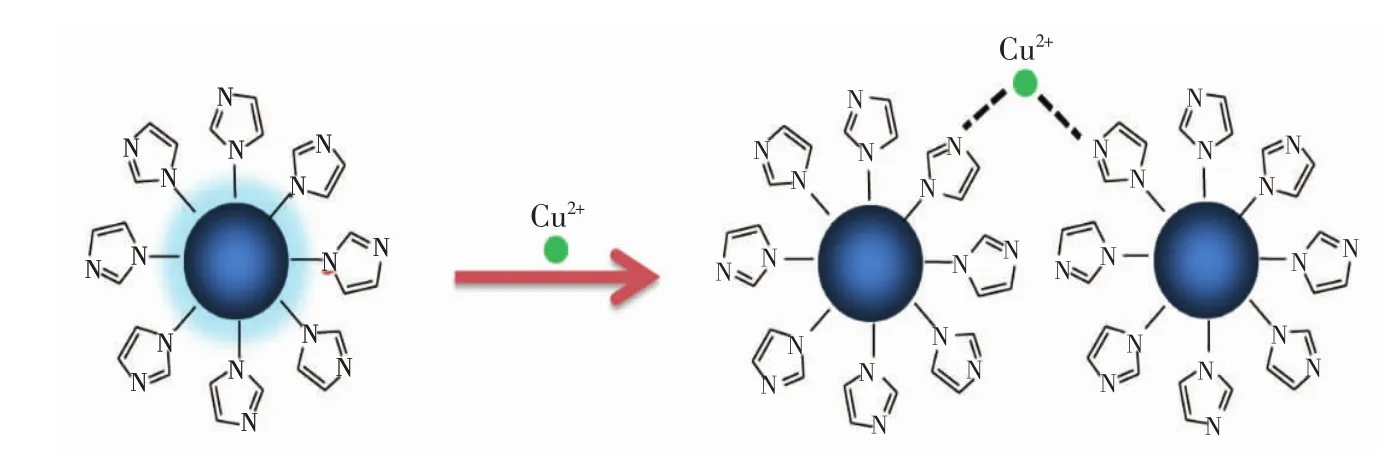
图10 荧光猝灭机理示意图Fig.10 Mechanism for fluorescence quenching
3.5分析特性
为进一步考察Cu2+对硅量子点荧光猝灭的动力学特征,研究了Cu2+加入量对荧光强度的影响。图11显示,Cu2+浓度不影响荧光发射峰的形状,它们的最大发射波长均在422 nm,表明Cu2+与量子点作用并不改变其晶体结构。然而,体系荧光强度随着Cu2+加入量增加而迅速下降。当Cu2+浓度在0.04~2400μmol/L之间,荧光强度(F)与 Cu2+浓度(C,μmol/L)呈良好的线性关系,线性方程为F=N0.1404C+961.95,相关系数R为0.997,方法检出限达到1.29×10N8mol/L(S/N=3)。基于Cu2+对硅量子点的荧光猝灭响应,建立了测定Cu2+含量的荧光分析方法。采用此方法测定20份0.2 mmol/L Cu2+,检测结果标准偏差为1.6%,表明方法具有良好的重现性。将硅量子点储备液在4℃储存一定时间,然后用于检测0.2mmol/LCu2+。结果表明,储备液储存3个月后测定结果相对偏差小于2.4%,表明硅量子点有较好的稳定性。
各种金属离子对硅量子点荧光的影响结果列于图12。在所有测试对象中,仅有Cu2+的引入导致了硅量子点荧光的显著猝灭,显示对Cu2+的测定具有较好的选择性。由于Cu2+和咪唑基上的氮有很强的配合能力,它们的作用导致形成稳定的基态配合物;Ca2+和Mn2+与咪唑基上的氮原子配合能力差,它们与硅量子点作用较弱,且不能形成稳定的配合物。因此,Ca2+和Mn2+的引入,硅量子点的荧光强度基本不变;尽管Ag+,Co2+,Hg2+,Zn2+,Al3+,Fe3+,Fe2+,Pb2+,Cr3+和Ni2+也能与咪唑基上的氮具有一定的配合能力,但它们与硅量子点的作用仅造成小幅度荧光下降,说明它们所形成的配合物不稳定。由于果蔬样品中上述金属离子极少,它们对Cu2+测定不会产生明显影响。
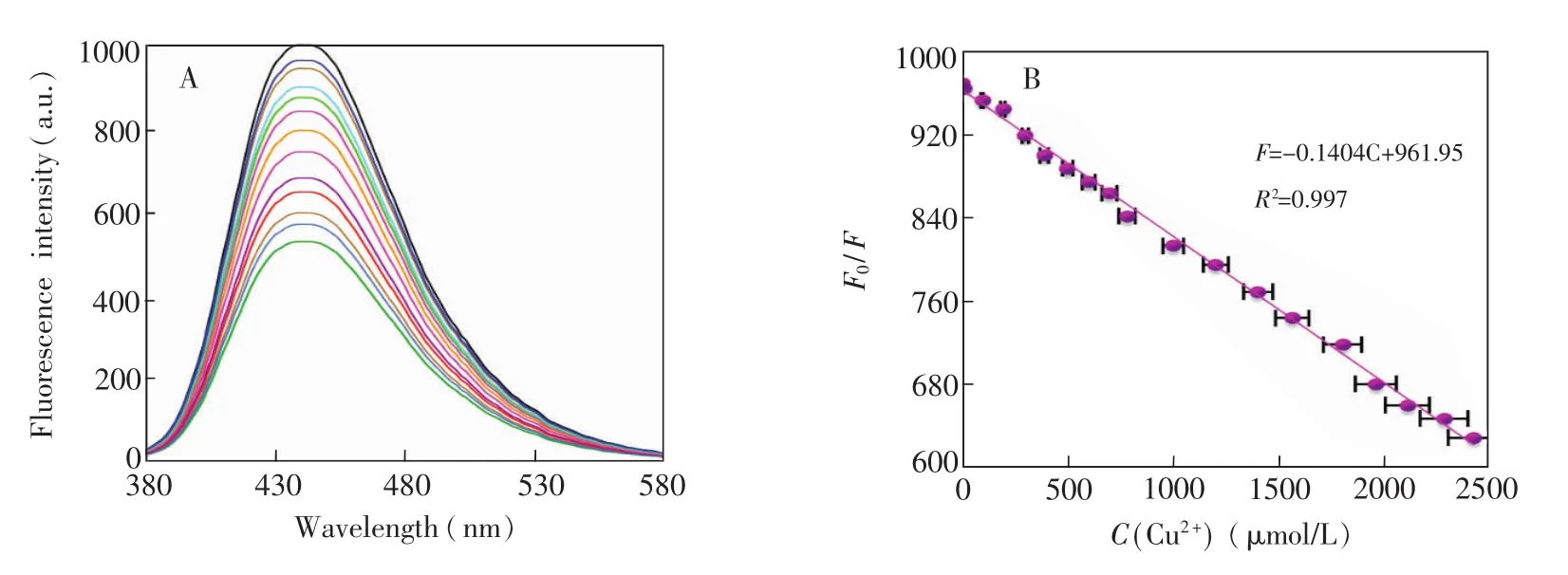
图11 不同浓度Cu2+存在下硅量子点的荧光光谱(A),B:硅量子点荧光强度与Cu2+浓度线性关系曲线Cu2+浓度:0.0,0.04,0.19,12.2,97.7,195,300,390,500,600,699,781,1000,1200,1400,1562,1800,1956,2106,2279,2419,2512,2640,2755,2895和3125μmol/L。Fig.11 A:Fluorescence spectra of silicon quantum dots in the presence of0.0,0.04,0.19,12.2,97.7,195,300,390,500,600,699,781,1000,1200,1400,1562,1800,1956,2106,2279,2419,2512,2640,2755,2895 and 3125μmol/L of Cu2+.B:The relationship curve of the fluorescence intensity with Cu2+concentration.
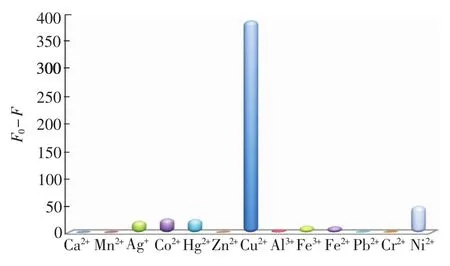
图12 不同金属离子对硅量子点荧光强度的影响。F0为不存在金属离子时硅量子点的荧光强度值,F为存在金属离子时硅量子点的荧光强度值Fig.12 Effect of differentmetal ions on fluorescence intensity of silicon quantum dots.F0and F is the fluorescence intensity of silicon quantum dots in the absence and presence ofmetal ion,respectively
3.6果蔬中痕量铜的测定
将所建立的分析方法用于果蔬中痕量铜的测定。从表1可知,测定结果与原子吸收法测定结果相一致,相对标准偏差(RSD)都在0.86%~1.8%之间,表明方法具有较好的精密度和准确性。
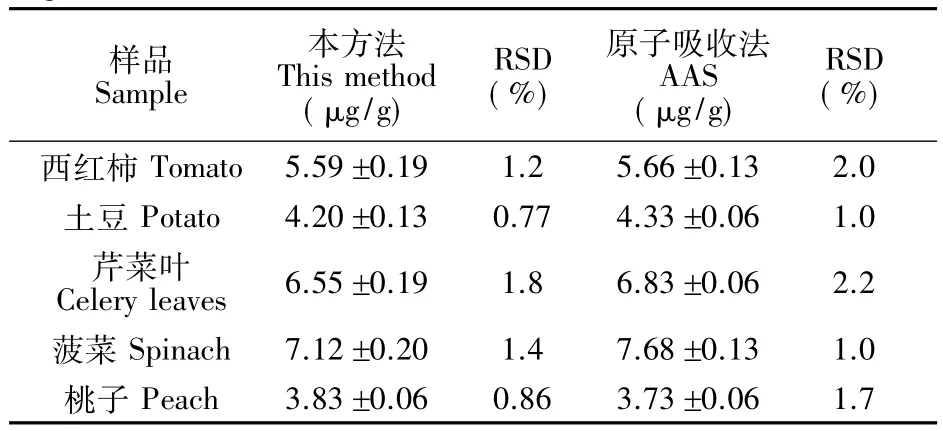
表1 果蔬中铜含量测定结果Table 1 Detection results of Cu2+in 5 kinds of fruits and vegetables
4 结论
采用一步水热合成水溶性的咪唑基硅量子点。所得到的硅量子点荧光发射强,光稳定性好,对Cu2+有灵敏和选择的荧光响应。基于Cu2+对硅量子点的荧光猝灭,建立了检测痕量Cu2+的荧光分析方法。方法具有高的灵敏度和选择性,已成功地应用于果蔬中Cu2+含量测定。此外,研究工作还可用于功能性硅量子点的设计与合成。
References
1Li J,Hong X,LiD,Zhao K,Wang L,Wang H,Du Z,Li J,Bai Y,Li T.Chem.Commun.,2004,4(15):1740-1741
2Hong X,Li J,Wang M,Xu J,GuoW,Li J,Bai Y,Li T.Chem.Mater.,2004,16(21):4022-4027
3WANG Zong-Hua,GAO Yan-Li,ZHANG Fei-Fei,XIA Yan-Zhi,LI Yan-Hui.Journal of Analytical Science,2012,28(1):119-125王宗花,高艳丽,张菲菲,夏延致,李延辉.分析科学学报,2012,28(1):119-125
4Peng X G,Manna L,Yang W D,Wickham J,Scher E,Kadavanich A,Alivisatos A P.Nature,2000,404(6773): 59-61
5LIN Zhang-Bi,SU Xing-Guang,ZHANG Hao,MOU Ying,SUN Ye,HU Hai,YANG Bai,YAN GANG-Lin,LUO Guimin,JIN Qin-Han.Chem.J.Chinese Universities,2003,24(2):216-220林章碧,苏星光,张皓,牟颖,孙晔,胡海,杨柏,闫岗林,罗贵民,金钦汉.高等学校化学学报,2003,24(2): 216-220
6Yu W W,Qu L H,Guo W Z,Peng X G.Chem.Mater.,2003,16(3):2854-2860
7Liu W Y,Lee JS,Talapin D V.J.Am.Chem.Soc.,2013,135(4):1349-1357
8Liu Z P,Kumbhar A,Xu D,Zhang J,Sun Z Y,Fang JY.Angew.Chem.Int.Ed.,2008,47(19):3540-3542
9Talapin D V,Rogach A L,Shevchenko E V,Kornowski A,Haase M,Weller H.J.Am.Chem.Soc.,2002,124(20): 5782-5790
10Ellingson R J,Beard M C,Johnson JC,Yu P R,Micic O I,Nozik A J,Shabaev A,Efros A L.Nano Lett.,2005,5(5):865-871
11Qin Jun-Jie,Cao Li-Xin,Liu Wei,Gao Rong-Jie,Su Ge,Qu Hua,Xia Cheng-Hui.Chin.J.Lumin.,2014,35(7): 858-865秦俊杰,曹立新,柳伟,高荣杰,苏革,曲华,夏呈辉.发光学报,2014,35(7):858-865
12Sun Lin,Zhang Qiu-Yan,Li Zhen-Zhen,Pan Yu-Jin,Wang Qing,Zhao Qiang.Chin.J.Lumin.,2015,36(3):339-347孙琳,张秋艳,李珍珍,潘玉瑾,王青,赵强.发光学报,2015,36(3):339-347
13Derfus A M,Chan W CW,Bhatia SN.Nano Lett.,2004,4(1):11-18
14Feng Y L,Liu Y F,Su C,Ji X H,He Z K.Sens.Actuators B,2014,203:795-801
15Cao L,Wang X,MezianiM J,Lu F S,Wang H F,Luo PG,Lin Y,Harruff B A,Veca LM,Murray D,Xie SY,Sun Y P.J.Lumin.,1998,80(1):159-162
16Warner JH,Hoshino A,Yamamoto K,Tilley R D.Angewandte Chemie,2005,117(29):4626-4630
17Warner JH,Rubinsztein-Dunlop H,Tilley R D.J.Phys.Chem.B,2005,109(41):19064-19067
18Heath JR.Science,1992,258(5085):1131-1133
19Bley R A,Kauzlarich SM.J.Am.Chem.Soc.,1996,118(49):12461-12462
20Yang C S,Bley R A,Kauzlarich SM,Lee HW H,Delgado G R.J.Am.Chem.Soc.,1999,121(22):5191-5195
21Somogyi B,Zolyomi V,Gali A.Nanoscale,2012,4(24):7720-7726
22Choi J,Wang N S,Reipa V.Bioconjugate Chem.,2008,19(3):680-685
23Sudeep P K,Page Z,Emrick T.Chem.Commun.,2008,46:6126-6127
24Shiohara A,Hanada S,Prabakar S,Fujioka K,Lim TH,Yamamoto K,Northcote P T,Tilley R D.J.Am.Chem.Soc.,2010,132(1):248-253
25Alsharif N H,Berger C EM,Varanasi SS,Chao Y,Horrocks B R,Datta H K.Small,2009,5(2):221-228
26Choi JK,Jang S,Sohn H,Jecong H D.J.Am.Chem.Soc.,2009,131(49):17894-17900
27Erogbogbo F,Yong K T,Roy I,Xu G X,Prasad P N.ACSNano,2008,2(5):873-878
28Zhang J,Yu SH.Nanoscale,2014,6(8):4096-4096
29Feng Y L,Liu Y F,Su C,Ji X H,He Z K.Sens.Actuators B,2014,203:795-801
This work was supported by the National Natural Science Foundation of China(No.21176101)
Synthesis of NovelW ater-Soluble Silicon Quantum Dots with Im idazole Groups and Its Application in Fluorescent Detection of Trace Copper in Fruits and Vegetables
WANG Jia-Jia1,LIAN Man1,XIONG Jie1,LIZai-Jun*1,2
(School of Chemical and Materials Engineering1; Key Laboratory of Food Colloids and Biotechnology,Ministry of Education2,Jiangnan University,Wuxi214122,China)
Silicon quantum dot has become an attractive nanomaterial due to their excellent biocompatibility and optical performance.However,poor water-solubility of the traditional silicon quantum dot limits its wide application.In this study,we reported the synthesis of water-soluble silicon quantum dots with imidazole groups by using hydrothermalmethod,in which N-trimethysilylimidazole was used as a precursor of silicon.Compared with sodium borohydride,ascorbic acid,bovine serum protein,cysteine and citric acid,the as-prepared silicon quantum dots offered the strongest fluorescence intensity when sodium citrate was used as the reducing agent and stabilizer for the synthesis.The reaction could complete within 2 h at 220℃.The obtained silicon quantum dots showed good water-solubility with an average particle size of 2.6 nm,and the result of infrared spectroscopic analysis verified the existence of free imidazole groups on the surface.Bymeans of the investigation of the fluorescence quenching behavior of copper ions towards the silicon quantum dots at different temperatures,we found that the degree of fluorescence quenching increased with the increase of temperature.There results proved that the fluorescence decrease belongs to static quenching.Namely,the interaction of Cu2+with imidazole groups on the surface of silicon quantum dots formed stable complex.In addition,the resonance light scattering analysis also showed that the fluorescence quenching process was accompanied by the agglomeration of particles.Based on the fluorescence quenching behavior of silicon quantum dots,we established amethod for the fluorescent detection of Cu2+.When the concentration of Cu2+was in the range of 0.04-2400μmol/L,the fluorescence intensity would linearly decreasewith the increase of Cu2+concentration,and the detection limit(S/N=3)reached 1.29×10-8mol/L.The method provided high sensitivity,selectivity and reproducibility,and was successfully applied to the determination of trace copper in fruits and vegetables.
N-trimethysilylimidazole;Silicon quantum dots;Hydrothermal method;Fluorescent detection; Copper
7 October 2015;accepted 8 November 2015)
10.11895/j.issn.0253-3820.150778
2015-10-07收稿;2015-11-08接受
本文系国家自然科学基金资助项目(No.21176101)
*E-mail:zaijunli@jiangnan.edu.cn
