瓦斯水合物诱导时间影响因素实验研究
2016-11-03张保勇刘金华周泓吉
张保勇, 刘金华, 周泓吉
(1.黑龙江科技大学 安全工程学院, 哈尔滨 150022;2.黑龙江科技大学 瓦斯等烃气输运管网安全基础研究国家级专业中心实验室, 哈尔滨 150022)
瓦斯水合物诱导时间影响因素实验研究
张保勇1,2,刘金华1,2,周泓吉1,2
(1.黑龙江科技大学 安全工程学院, 哈尔滨 150022;2.黑龙江科技大学 瓦斯等烃气输运管网安全基础研究国家级专业中心实验室, 哈尔滨 150022)
为探究多因素条件下瓦斯水合物诱导时间及其规律,利用自主设计的高压可视水合实验装置,由成核动力学实验确定了气体组分、NaCl质量分数及驱动力三种因素对瓦斯水合物诱导时间影响的程度,采用极差法和方差法对实验数据进行分析。结果表明:随着瓦斯中甲烷减少、丙烷增加,水合物的平均诱导时间先减少后增加;随着NaCl质量分数或驱动力Δp增加,水合物平均诱导时间逐渐减少;气样G2、NaCl质量分数3.5%、驱动力1.5 MPa条件下瓦斯水合物诱导时间最短;驱动力Δp较气体组分对水合物诱导时间影响显著性强,NaCl质量分数的显著性较弱。
瓦斯水合物; 成核动力学; 诱导时间; 影响因素; 显著性
0 引 言
加快煤矿瓦斯抽采利用,是贯彻落实科学发展观,推进煤矿安全发展、清洁发展、节约发展的必然要求[1]。2012年,我国煤矿瓦斯抽采量114亿m3,利用量38亿m3,排放量76亿m3,在污染环境的同时也浪费了清洁瓦斯能源。瓦斯利用率不高的主要原因是抽采瓦斯中甲烷浓度较低,直接利用技术稀缺,远距离输送困难。因此,亟须一种瓦斯分离提纯安全高效的新方法。2005年,文献[2-3]中提出利用瓦斯水合技术进行瓦斯分离,与其他传统分离方法相比,其具有分离条件温和、适用瓦斯气源浓度范围广等特性[4-5]。
水合分离技术是利用瓦斯混合气中主要组分(CH4、N2、O2等)形成水合物相平衡温压条件差异,使CH4尽可能高效率地发生水合固结,从而实现从瓦斯混合气中分离提纯的目的。瓦斯气体水合物生成过程包括水合物晶体成核和生长两个阶段[6],诱导时间是水合物成核动力学中的重要参数,针对诱导时间影响规律开展研究,有助于筛选出显著改善瓦斯水合工艺条件,对分离技术的工业应用具有重要科学意义。
目前,国内外学者针对气体水合物诱导时间影响开展了研究工作。对不同组分混合气水合物研究发现[7-9],气样组分差异不仅影响水合物形成的热力学条件,同时影响水合物的诱导时间;对NaCl溶液体系水合物研究发现[10-14],相比纯水体系水合物生成压力较高,是一种常见的热力学抑制剂,当NaCl质量分数较低时,其抑制效果并不明显,反而导致更多的水合物晶体析出,在一定程度上促进了水合物的生成,缩短了水合物的诱导时间;对不同压力条件下水合物研究发现[15-18],生成水合物的推动力一般是气体在气相和水合物相的逸度差,当温度一定时,体系压力越高,气相和水合物相逸度差越大,推动力越大;当压力增大至“极大值”时,将抑制气体水合物晶核的形成和生长。综上所述,三种因素对水合物生成均有一定的促进作用,而多因素条件下瓦斯水合物诱导时间影响的研究及各影响因素间显著性比较鲜见报道。
据此,笔者拟利用高压可视瓦斯水合实验装置开展NaCl溶液中多元瓦斯气体水合物成核动力学实验,以期获得气体组分、NaCl质量分数以及驱动力Δp对诱导时间的影响以及显著性规律。
1 实验原理
瓦斯水合物生成过程根据气相压力变化可以分为四个部分,如图1所示。
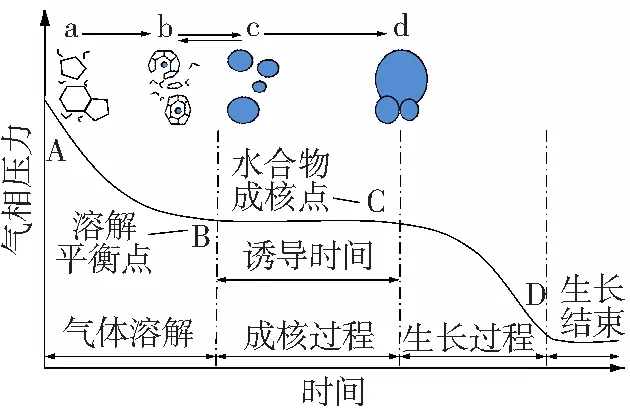
图1 瓦斯水合过程
初始状态溶液中无客体分子(a),随着瓦斯气的溶解(AB),气体逐渐消耗,气相压力降低,溶解的气体分子与水分子形成不稳定簇(b1)。当气体溶解至平衡点,水合物进入成核过程(BC),压力趋于稳定,不稳定簇通过共享表面聚集,同时聚集会起到抑制作用(b2),当不稳定簇聚集的大小达到临界值时(c),达到水合物成核点。水合物进入生长阶段(CD),气体消耗量迅速增加,压力降低,直至水合物生长结束。
瓦斯水合物诱导时间是出现一定数量可探测体积水合物相所需要的时间,是水合物形成过程中重要参数。截取实验所获得的压力-时间曲线中气相压力较为平缓的一段时间即为诱导时间。文中采用正交实验研究在三因素三水平不同体系下瓦斯水合物的诱导时间,该方法与传统全面实验相比具有实验次数少、数据点分布均匀和结论可靠等优点,可以通过较少的实验对结果进行极差和方差分析得出结论[19-23]。
2 材料与装置
瓦斯水合动力学实验所用瓦斯气样据煤矿抽采瓦斯组分配比,由哈尔滨通达特种气体有限公司提供。其中,G1:φ(CH4)=85%,φ(CO2)=5%,φ(C3H8)=5%、φ(N2)=2%、φ(O2)=3%;G2:φ(CH4)=70%、φ(CO2)=5%、φ(C3H8)=10%、φ(N2)=12%、φ(O2)=3%;G3:φ(CH4)=55%、φ(CO2)=5%、φ(C3H8)=15%、φ(N2)=22%、φ(O2)=3%。试剂NaCl质量分数不少于99.5%,由哈尔滨试剂化工厂提供。实验用水为自制蒸馏水。实验各因素水平如表1所示。

表1 瓦斯水合动力学影响因素与水平
自主研制煤矿瓦斯水合高压实验装置,如图2所示。实验装置主要包括:可视高压反应釜,用于水合物在不同体系中生成实验,容积为150 mL,最高承受压力20 MPa;恒温空气浴控制箱,为反应釜内水合物生成提供稳定的环境温度;压力系统,包括气瓶、气体增压泵、空气压缩机等;数据采集系统,包括温度/压力传感器、CCD摄像系统、数据采集器组件等。

图2 瓦斯水合动力学高压实验装置
3 实验设计与结果分析
3.1实验设计及结果
基于实验室前期所完成在三种NaCl质量分数溶液中不同瓦斯气样的水合物相平衡实验,确定在不同因素及水平下的正交实验初始热力学条件(表2),排除各因素对相平衡条件的影响。气体组分、NaCl质量分数、驱动力Δp均对水合物诱导时间有一定影响,其中单一因素水平发生变化时,其余两因素水平值并未随之变化,三种因素间并无交互作用,因此,可以设计三因素三水平的瓦斯水合物生成动力学正交实验表格L9(34)。正交实验方案中D列为空白列,用以估计实验误差。根据实验方案完成瓦斯水合物成核动力学实验,获取九组实验的水合物诱导时间,正交实验见表2。

表2 瓦斯水合动力学实验方案及结果
3.2水合物诱导时间影响因素分析
3.2.1极差分析
极差分析是通过计算和比较目标参数极差进行处理和分析实验数据的方法。计算因素x(A,B,C)在各水平的诱导时间之和及其平均数:

(1)



表3 瓦斯水合物影响因素极差表
极差是在因素x中的最大水平和均值与最小水平和均值的差值。因素x的极差较大,表明因素x在实验范围内对瓦斯水合物诱导时间影响显著。将上述所求得的数据,以各因素及水平为横坐标,平均诱导时间为纵坐标,绘制柱状图,见图3。

图3 瓦斯水合物平均诱导时间柱状图
根据图3可知,因素A、B、C的极差分别为119.67、82.00、160.67 min。驱动力Δp的极差最大,说明驱动力Δp在实验范围内变化时,水合物平均诱导时间变化最大。三种因素影响强弱顺序依次为:C(驱动力Δp)>A(气体组分)>B(NaCl质量分数)。进一步分析确定:其一,气样G1和G3的水合物平均诱导时间长于G2,三种气样对瓦斯水合物平均诱导时间影响程度依次为G2>G3>G1;第二,随着NaCl质量分数的升高,水合物平均诱导时间逐渐缩短,当质量分数达到3.5%时,诱导时间最短, 三种NaCl质量分数对瓦斯水合物平均诱导时间影响程度依次为:3.5%>2.0%>0.5%;第三,驱动力Δp对水合物平均诱导时间的影响接近线性,驱动力越大,平均诱导时间越短;三种驱动力对瓦斯水合物平均诱导时间影响程度依次为1.5 MPa>1.0 MPa>0.5 MPa。基于对三种因素的极差分析,在实验范围内确定瓦斯水合物生成的最佳实验体系:瓦斯气样G2、NaCl质量分数为3.5%、驱动力Δp为1.5 MPa。
通过极差分析可以较为直观分析各因素对水合物诱导时间的影响,并优选实验条件。但不能顾及实验过程和实验结果测定中必然存在的误差,且各因素对瓦斯水合物诱导时间影响的重要程度也不能给出准确的数量估计,为了弥补其不足,进一步进行方差分析。
3.2.2方差分析


(3)
以计算实验中各因素及误差的离差平方和

(4)
表示因素x水平变化时所引起的实验结果的差异。计算正交实验各因素的自由度fF以及实验误差的自由度fE,fF=fE=2。因素及误差的离差平方和分别除以各自的自由度,得到平均离差平方和,因素与误差的平均离差平方和相比后得方差比Fx,Fx值的大小反映了因素x对实验结果影响程度强弱,方差比Fx越大,表明因素x对诱导时间的影响越显著。方差比服从自由度为(2,2)的F分布,选取显著水平为0.20和0.25,查表得到F0.20及F0.25的临界值,计算结果如表4所示。因素A、B、C的方差比分别为3.02、1.46、5.26,因素C大于F0.20时的临界值,因素A大于临界值F0.25,表明因素A、C(气体组分、驱动力Δp)对水合物诱导时间影响相比于因素B(NaCl质量分数)更显著,且因素C为最显著因素。

表4 瓦斯水合动力学影响因素分析
3.2.3机理分析
通过极差和方差分析表明,驱动力Δp在实验范围内的增加,可以显著缩短水合物诱导时间。根据亨利定律,在等温等压下,气体在溶液中的溶解度与液面上该气体的平衡压力成正比。随着压力的增加,气体分子在溶液中的数量也逐渐增加,分子间距离减少,为水合物迅速成核提供物质基础。瓦斯水合物成核所需能量可由气-液界面的偏摩尔Gibbs自由能体现[6]:

VH(pexp-peq),
(5)
式中:VL、VH——分别表示水相和水合物相的体积;
pexp、peq——分别表示实验和相平衡压力;
fi,exp、fi,eq——分别为实验和相平衡时的逸度值;
xi——组分i(包括水)在混合气体水合物中的摩尔分数。
随着驱动力Δp的增加,偏摩尔Gibbs自由能变梯度逐渐增大,推动瓦斯水合物加快成核。Δp的增加提高了气体分子与液面碰撞的次数,导致水合物成核几率增加,从而缩短了诱导时间。
气体组分是影响水合物诱导时间的次要因素,且诱导时间随着组分浓度变化先减少后增加。由于气体组分中包含一定的丙烷,通过对多元气体水合物生成条件的预测[25]以及研究相关参考文献[26-30],分析认为实验中仅生成Ⅱ型水合物。基于Chen-Guo水合物生成过程动力学机理[6],非极性的气体分子溶解在水相中,水分子通过氢键相连将气体分子包围形成胞腔,由于氢键的作用力远大于范德华力,胞腔的氢键基本上是饱和的,且胞腔的大小由气体分子的直径决定,因此,一定大小的不同气体分子仅能形成一种体积大小的胞腔。由于瓦斯气体生成Ⅱ型水合物,溶解的丙烷最先形成51264十六面体结构的胞腔,当这些多面体结构胞腔在水溶液中的浓度达到一定程度时,它们才将彼此联结起来,而它们的几何结构以及水合物的稳定性决定了甲烷分子通过形成正十二面体胞腔,将正十六面体的胞腔相连。三种气样中G1中丙烷含量较少,丙烷的溶解以及胞腔的形成均是随机的,导致丙烷胞腔分布不均匀且间隔较大,联结较为困难,因此G1气样的水合物诱导时间最长。
竞争结构(Competing Structures)为影响Ⅱ型水合物诱导时间的另一个因素,水合物Ⅱ型结构要求晶胞中8个十六面体(51264)孔穴中32个六边形以固有的方式连接在一起,但对于两个独立的非对称结构的51264孔穴,水合物形成过程中,不同配位数的不稳定簇聚集时除形成Ⅱ型水合物,还有可能形成其他两种竞争结构(篮球结构和HSⅡ结构)[27],如图4所示。三种气样中气样G3中丙烷的浓度最大,溶液中丙烷形成的胞腔数量最多,相比前两种气样竞争更为明显。竞争结构的存在延缓了水合物生成过程,从而增加了诱导时间。三种气样的瓦斯水合物平均诱导时间呈先减少再增加的趋势。

图4 Ⅱ型水合物51264孔穴两种不同连接方式
分析认为,NaCl对水合物生成有一定促进作用,但相比其他两种因素影响效果并不显著。纯水不是以单个分子形式存在,而是在分子氢键作用下以水分子团簇(五聚体或六聚体)的形式存在[31-33]。Näslund等[34]利用X射线吸收光谱(XAS)和X射线拉曼散射光谱(XRS),发现在纯水中加入NaCl后,NaCl电离后的阴离子Cl-对水分子间氢键影响较小,而受阳离子Na+的影响较大,促进液态水形成团簇结构,提高了溶液中水分子团簇的密度。与纯水相比由于仅增加了水分子团簇的数量,略微提高了瓦斯水合物笼型结构形成的几率,从而缩短水合物成核所需的诱导时间。因此,NaCl质量分数越高,溶液中水分子团簇结构越多,对瓦斯水合物生成促进作用越强,但显著性较弱。
4 结 论
(1)利用正交实验可以从多因素中优选瓦斯水合分离条件。基于极差分析实验所选三种影响因素对瓦斯水合物诱导时间影响程度为驱动力Δp>气体组分>NaCl质量分数。气样G2、NaCl质量分数3.5%、驱动力1.5 MPa条件下瓦斯水合物诱导时间最短。
(2)方差分析表明驱动力Δp和气体组分对水合物诱导时间影响显著。Δp的增加不仅加速气体溶解,为水合物成核提供基础,而且增大了水合物成核的推动力。气样中甲烷及丙烷含量决定影响水合物诱导时间的微观因素。
(3)NaCl质量分数相比于驱动力Δp以及气体组分对诱导时间的影响并不显著,但其溶液电离出阴、阳离子形成的水合离子可一定程度影响水分子团簇的数量,从而促进瓦斯水合作用。
[1]张德江. 大力推进煤矿瓦斯抽采利用[J]. 求是, 2009, 24: 3-5.
[2]李智峰, 张强, 吴强, 等. 驱动力对瓦斯气体水合物成核诱导时间的影响[J]. 黑龙江科技学院学报, 2013, 23(4): 329-332.
[3]吴强. 煤矿瓦斯水合化分离试验研究进展[J]. 煤炭科学技术, 2014, 42(6): 81-85.
[4]张强, 吴强, 张保勇, 等. 干水对瓦斯混合气水合分离动力学影响研究[J]. 中国矿业大学学报, 2014, 43(4): 593-599.
[5]吴强, 张强, 张保勇, 等. 蒙脱石对瓦斯水合分离过程的影响[J]. 煤炭学报, 2013, 38(8): 1392-1396.
[6]吴强, 周竹青, 高霞, 等. NaCl溶液中多组分瓦斯水合物的成核诱导时间[J]. 煤炭学报, 2015, 40(6): 1396-1401.
[7]宋琦. 多元复杂体系水合物生成的实验及热动力学模型研究[D]. 常州: 常州大学, 2010: 41-68.
[8]周诗崇, 张锦, 徐涛, 等. 天然气水合物生成促进因素的研究进展[J]. 石油化工, 2015, 44(1): 127-132.
[9]NAEIJI P, MOTTAHEDIN M, VARAMINIAN F. Separation of methane-ethane gas mixtures via gas hydrate formation[J]. Separation and Purification Technology, 2014, 123: 139-144.
[10]YANG MINGJUN, SONG YONGCHEN, LIU YU, et al. Effects of halogen ions on phase equilibrium of methane hydrate in porous media[J]. International Journal of Thermophysics, 2012, 33(5): 821-830.
[11]张强, 吴强, 张保勇, 等. NaCl-SDS复合溶液中多组分瓦斯水合物成核动力学机理[J]. 煤炭学报, 2015, 40(10): 2430-2436.
[12]张保勇, 于跃, 吴强, 等. NaCl对瓦斯水合物相平衡的影响[J]. 煤炭学报, 2014, 39(12): 2425-2430.
[13]KOMATSU H, OTA M, SMITH R L, et al. Review of CO2-CH4clathrate hydrate replacement reaction laboratory studies - Properties and kinetics[J]. Journal of the Taiwan Institute of Chemical Engineers, 2013, 44(4): 517-537.
[14]王志海, 叶美芳, 董会, 等. 流体包裹体盐度低温拉曼光谱测定方法研究[J]. 岩矿测试, 2014, 33(6): 813-821.
[15]臧小亚, 梁德青, 吴能友. 多孔介质中甲烷水合物的生成特性研究进展[J]. 新能源进展, 2015, 3(2): 131-138.
[16]霍洪俊, 任韶然, 王瑞和, 等. 气体水合物动力学和热力学抑制剂复合作用试验[J]. 中国石油大学学报:自然科学版, 2012, 36(5): 110-113.
[17]李金平, 杨文洁, 梁海雷, 等. 压力对气-液水合反应驱动力的影响[J]. 兰州理工大学学报, 2009, 35(3): 47-50
[18]丁艳明, 陈光进, 孙长宇, 等. 水合物法分离甲烷-乙烷体系相关相平衡的研究[J]. 石油学报:石油加工, 2005, 21(6): 75-79.
[19]孙国庆. THF和TBAB对煤层气水合物相平衡影响的实验及理论研究[D]. 太源: 太原理工大学, 2015.
[20]刘海红, 李玉星, 王武昌, 等. 水合物聚集影响因素及正交试验研究[J]. 油气储运, 2013, 32(11): 1232-1236.
[21]刘厚平, 韩博, 张凌, 等. 基于正交试验法的天然气水合物地层钻井液配方设计[J]. 地质科技情报, 2013, 32(6): 202-206.
[22]LIU JIAN, WANG QUANBAO, ZHAO HAITAO, et al. Optimization design of the stratospheric airship’s power system based on the methodology of orthogonal experiment[J]. Journal of Zhejiang University SCIENCE A, 2013, 14(1): 38-46.
[23]江国业, 王晓娅, 孙鹏. 基于正交试验设计的水合物浆液流动特性流动特性数值模拟[J]. 科技导报, 2014, 32(13): 23-27.
[24]张秀成, 赵彬侠. 化工基础实验[M]. 西安:西北大学出版社, 2006: 165-174.
[25]陈光进, 孙长宇, 马庆兰. 气体水合物科学与技术[M]. 北京: 化学工业出版社, 2008: 68-69.
[26]雷晓, 邓建强, 张早校. 海底沉积物层CO2封存中水合物研究进展[J]. 化工进展, 2012, 31(6): 1338-1346.
[27]CHRISTIANSEN R, SLOAN E D. Mechanisms and kinetics of hydrate formation[J]. Annals of New York Academy of Sciences, 1994, 715(1): 283-305.
[28]HANSEN S B, BERG R W. Raman spectroscopic studies of methane gas hydrates[J]. Applied Spectroscopy Reviews, 2009, 44(2): 168-179.
[29]HESTER K C, DUNK R M, WALZ P M, et al. Direct measurements of multi-component hydrates on the seafloor: pathways to growth[J]. Fluid Phase Equilibria, 2007, 261(1): 396-406.
[30]SUM A K, BURRUSS R C, SLOAN E D. Measurement of clathrate hydrates via Raman spectroscopy[J]. The Journal of Physical Chemistry B, 1997, 101(38): 7371-7377.
[31]杨明军, 宋永臣, 刘瑜. 多孔介质及盐度对甲烷水合物相平衡影响[J]. 大连理工大学学报, 2011, 51(1): 31-35.
[32]顾锋, 赵会军, 王树立. 盐类体系中天然气水合物相平衡条件的研究[J]. 石油与天然气化工, 2008,37(2): 149-151.
[33]宋立群, 李玉星, 陈玉亮, 等. 影响水合物形成条件因素敏感性分析[J]. 科学技术与工程, 2011, 11(21): 5075-5079.
[34]MASLUND D C, EDWARDS D C, WERNET P. X-ray absorption spectroscopy study of the hydrogen bond network in the bulk water of aqueous solutions[J]. J Phys Chem A, 2005, 109(27): 5995-6002.
(编辑徐岩)
Experimental study on influence factors for induction times of gas hydrates
ZHANGBaoyong1,2,LIUJinhua1,2,ZHOUHongji1,2
(1.School of Safety Engineering, Heilongjiang University of Science & Technology, Harbin 150022, China;2.National Central Laboratory of Hydrocarbon Gas Transportation Pipeline Safety, Heilongjiang University of Science & Technology, Harbin 150022, China)
This paper is motivated by the need to explore the impact factor of induction time for gas hydrate. The exploration consists of investigating the effects of the gas component, NaCl concentration and driving force Δpon the induction time of gas hydrate using the independently designed visual high-pressure experimental hydration apparatus; determining the influential intensity and significance levels of the three factors on the induction time by nucleation kinetics experiments; and analyzing the experimental data by range and variance methods. The study demonstrates that the decreased methane and increased propane leads to an initial increase and subsequent decrease in the induction times of the gas mixtures; an increase in NaCl concentration or the driving force Δpis accompanied by a gradual reduction in the average induction times of hydrates; gas hydrate has the shortest induction time in the case of G2gas sample, 3.5% NaCl concentration and 1.5 MPa driving force Δp; and the driving force Δpexerts a more significant effect on the induction time than does the gas component, while NaCl concentration has a weaker significance.
gas hydrate; nucleation kinetics; induction time; influence factor; significance level
2016-02-29
国家自然科学基金重点项目(51334005);国家自然科学基金项目(51274267;51404102)
张保勇(1982-),男,安徽省霍邱人,副教授,博士,研究方向:瓦斯水合物理论及应用,E-mail:zhangbaoyong2002@163.com。
10.3969/j.issn.2095-7262.2016.02.002
TD712
2095-7262(2016)02-0122-06
A
