注射用炎琥宁不良反应报告分析
2016-11-01韦敬土班炳坤李二平
韦敬土 班炳坤 孙 蓉 周 黎 李二平
贵州省黔南州药品不良反应监测与评价中心,贵州 都匀 558000
注射用炎琥宁不良反应报告分析
韦敬土 班炳坤 孙 蓉 周 黎 李二平
贵州省黔南州药品不良反应监测与评价中心,贵州 都匀 558000
目的:了解注射用炎琥宁不良反应的发生特点及规律,为临床合理用药提供参考。方法:对贵州省黔南州上报的129例注射用炎琥宁不良反应(ADR)报告进行统计分析。结果:注射用炎琥宁ADR患者以儿童居多,占38.76%;以累及皮肤及其附件的报告最多,占57.36%;其中发生睾丸肿大1例。结论:注射用炎琥宁不良反应的发生与患者年龄、药物因素、药物配伍等因素有关。
注射液炎琥宁;药品不良反应;分析
随着抗菌药物的不断使用,临床上出现越来越来多的耐药菌种,由于中药注射剂疗效好、见效快、毒副作用小的优点,在临床抗菌、抗病毒治疗上得到了广泛运用,中药注射剂的品种也逐渐增多。炎琥宁是从传统中药穿心莲中提取的穿心莲内酯经酯化、脱水、成盐精制而成的脱水穿心莲内酯琥珀酸半酯钾钠盐,具有消炎、杀菌、抗病毒,促进肾上腺皮质功能及镇静作用,临床上常用于治疗病毒性肺炎和上呼吸道感染[1],取得良好的治疗效果,但随着临床的普遍使用,其不良反应也日益增多,引起了社会的广泛关注。本文通过对贵州省黔南州上报的129例注射用炎琥宁不良反应报告进行统计分析,探索其不良反应发生的特点及规律,为临床合理用药提供参考。
1 资料与方法
1.1 资料来源 收集贵州省黔南州2015年有关注射用炎琥宁不良反应报告129例。1.2 方法 利用国家药品不良反应监测系统检索方法和常规办公软件进行统计分析。对129例有关注射用炎琥宁不良反应报告的来源、类型、患者一般情况、出现不良反应时间、不良反应累及的系统-器官和临床表现、用药情况等进行统计与分析。
2 结果
2.1 报告来源及类型 129例注射用炎琥宁不良反应报告全部来自医疗机构,其中,来自乡镇卫生院最多,共65例,占50.39%,详细情况见表1。在不良反应报告类型中,一般报告120例,占93.02%;新的一般报告7例,占5.43%;新的严重报告1例,占0.78%,严重报告1例,占0.78%。

表1 报告来源
2.2 患者一般情况 男性68例,占52.71%;女性61例,占47.29%。年龄最大者78岁,最小者1岁,年龄段分布情况见表2。

表2 患者年龄段分布
2.3 药物过敏史 既往药品不良反应/事件史3例,占2.32%;无既往药品不良反应/事件史48例,占37.21 %;既往药品不良反应/事件史不详78例,占60.47%。家族药品不良反应/事件史不详者99例,占76.74%;无家族药品不良反应/事件史30例,占23.26%。2.4 不良反应发生时间 不良反应发生在静脉滴注过程中有119例,占92.25%,其中最早发生时间仅为静脉滴注后3 min,在30min内发生的有77例,占59.69 %;发生在静脉滴注完成后有6例,占4.65%,其中不良反应发生最晚时间为静脉滴注后2d;不良反应发生时间不详有4例,占3.10%。
2.5 原患疾病及用药情况 原患疾病为上呼吸道感染而使用注射用炎琥宁的有73例,占56.59%,其次是支气管炎24例,占18.61%,详细情况见表3。所使用的溶媒主要为生理盐水、5%葡萄糖注射液。单独使用注射用炎琥宁治疗原患疾病有115例,占89.14%;合并用药使用有14例,占10.85%,合并使用的药物主要有维生素C、青霉素、左氧氟沙星等。注射用炎琥宁一次最小使用剂量为5mg,最大剂量为480mg。
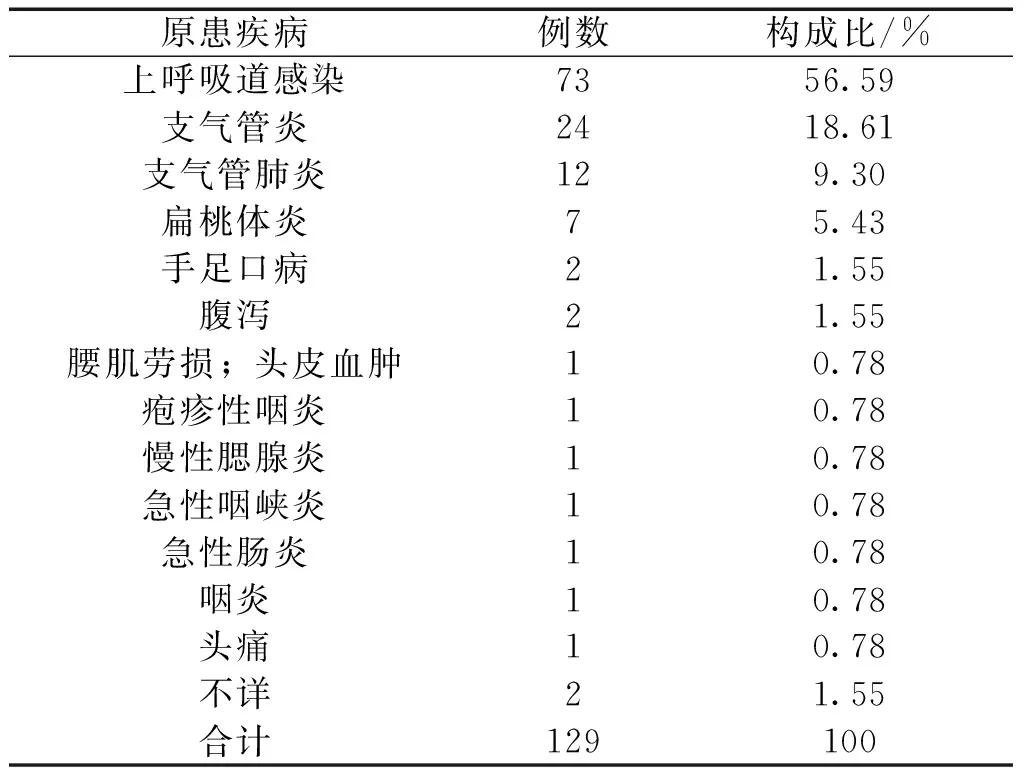
表3 ADR原患疾病统计情况
2.5 累及的系统-器官及临床表现 不良反应累及系统-器官最多的是皮肤及其附件,共74例,占57.36%,主要表现为皮疹、斑丘疹和瘙痒;其次是全身损害和消化系统,各有23例,分别占17.83%,主要表现为发热、寒战、过敏反应、恶心、呕吐、腹痛。详细情况见表4。

表4 不良反应累及的系统-器官及临床表现
2.6 不良反应因果关系及转归 按照《国家药品不良反应监测管理办法》中的评定标准分析,对注射用炎琥宁不良反应发生的因果关系进行评价,属于肯定的39例,占30.23%;属于很可能的25例,占19.38%;属于可能的46例,占35.66%;可能无关1例,占0.78%;无法评价1例,占0.78%;待评价17例,占13.18%。
在129例注射用炎琥宁不良反应报告中,经过医护人员及时处理,不良反应症状痊愈94例,占72.87 %,好转35例,占27.13%。
3 讨论
3.1 不良反应与年龄关系 从表1 ADR报告来源分析显示,注射用炎琥宁不良反应报告主要来自乡镇卫生院,共65例,占50.39%,这可能与乡镇卫生院大量使用注射用炎琥宁,而又未完全掌握其适应症以及配伍禁忌等因素有关。从患者年龄分布分析显示,小于14岁的患者共50例,占38.76%,明显多于各年龄阶段的报告数。儿童使用注射用炎琥宁发生不良反应较高可能与儿童生理功能发育还未健全,药物在体内代谢慢,容易蓄积等因素有关,另外,儿童在进行静脉滴注药品时,针刺的刺激,心里紧张,甚至会引起血管收缩、肌肉痉挛等因素也是导致不良反应发生的一个重要原因,儿童的不良反应报告较多也可能与该人群为注射用炎琥宁适应症疾病易感人群有关[2]。因此,在给儿童用药时,宜选择低量、低速静滴,同时要考虑儿童在静脉给药时紧张心理,尽量使其放松,并尽量使用口服制剂。
3.2 不良反应与药物使用情况的关系 为减少药品不良反应的发生,临床使用药品时应首先注意用药方法和剂量,因其给药速度、药物剂量及药物浓度都与不良反应发生具有一定的关系[3]。注射用炎琥宁在临床使用时,其静脉滴速过快、剂量过大、浓度过高均可使瞬间进入静脉的药物过多,导致不良反应出现的时间较早,也较为严重[3]。在129例注射用炎琥宁不良反应报告中,静脉滴注给药128例,占99.23%。静脉给药使药品迅速进入人体血液循环,容易使人体血液循环的pH值、渗透压发生激烈变化,导致人体各组织器官功能发生改变,从而易发生不良反应的损害。很多医务工作者误认为中药注射剂使用安全系数大,治疗范围广,从而导致超剂量、超适应症范围使用注射用炎琥宁的问题较为严重,尤其是在很多乡镇卫生院较为突出,在分析的病例报告中,有的单次使用量高达480mg。注射用炎琥宁主要适用于上呼吸道感染和病毒性肺炎,在本次病例报告分析中一些头痛、腰肌劳损等病例,也使用注射用炎琥宁进行治疗,超出了该药品的用药范围,从而增加了不良反应的发生率。在129例注射用炎琥宁不良反应报告中,注射用炎琥宁合并用药共14例,主要并用药有维生素C、青霉素、左氧氟沙星,而注射用炎琥宁说明书明确指出该药不宜与氨基苷类、喹诺酮类药物配伍使用,因为中药注射剂与化学药注射剂配伍后,会引起溶液pH值改变,甚至发生氧化、聚合等化学反应而形成不溶性微粒,使用后患者变态反应发生率增高,严重时会引起过敏性休克,甚至导致死亡[4]。所以在使用注射用炎琥宁时应尽量不要与其他化学药品同时使用,避免药物间化学反应,导致不良反应的发生。3.3 临床表现特点 从表3可以看出,注射用炎琥宁不良反应主要累及皮肤及其附件,其次是引起全身和消化系统损害,其不良反应的发生可能与其制剂本身成分有关,炎琥宁与穿琥宁在体内活性代谢物质为同一物质(穿琥宁为穿心莲内酯半酯单甲盐),能抑制早期毛细血管通透性增高与炎性渗出和水肿,能特异性地兴奋垂体一肾上腺皮质功能,促进ACTH释放,增加垂体前叶中ACTH的生物合成,有清热解毒和抗病毒作用,但也具有致敏原的作用。另外,注射用炎琥宁为中药注射剂,其成分复杂,在生产过程中也有可能其杂质成分未除尽等原因而引起不良反应的发生。值得注意的是有1例新的严重不良反应是引起儿童睾丸肿大,导致患者住院时间延长,发生不良反应的原因可能为患者生理功能不健全所致,给患者造成了严重的伤害,应该引起广大医务工作者的注意,避免类似的不良反应发生。
3.4 合理用药,减少不良反应发生 随着中药现代化的发展,各种中药注射剂不断应用于临床,中药注射剂不良反应发生率也逐年升高,在国家药品不反应监测中心病例数据库中,注射用炎琥宁所致的严重不良反应较为突出[5],由于很多中药注射剂不良反应还未研究明确,医务人员应严格按照药品说明书使用,根据患者病情,合理使用药品,保障药品使用安全、有效。
[1]黄秀纯, 吴雪荣. 门诊处方点评与不合格处方分析[J]. 医药导报, 2009,28(7): 961.
[2]吴斌. 98例注射用炎琥宁不良反应分析[J].安徽医药, 2007,(11)5: 473-474.
[3]梁雁, 鲁云兰. 159例中药注射剂不良反应分析[J]. 中国药物警戒, 2008, 5(5): 298-303.
[4]陈楠. 论中药注射剂的风险成因及风险管理措施[J]. 中国药物警戒, 2008, 5(5): 279.
[5]国家食品药品监督管理局. 关注穿琥宁、炎琥宁注射剂的安全性问题. 药物不良反应信息通报[EB/OL]. 2009-09-01.
(编辑:陶希睿)
Analysis of Adverse Drug Reactions Reports of Potassium Sodium Pehydroandroandrographolide Succinate for Injection
WEI Jingtu BAN Bingkun SUN Rong ZHOU Li LI Erping
Center for ADR Monitoring of Qiannan,Duyun 558000, China
objective To explore the features and regulation of adverse drug reactions reports of Potassium Sodium pehydroandroandrographolide Succinate for Injection.so as to provideinformation for rational clinical use of drug. Methods Making a statistical analysis of 129 adverse drug reactions (ADR)reports of Potassium Sodium pehydroandroandrographolide Succinate for Injection from Qiannan. Results Patients in the majority with children, accounting for 38.76%, mainly nvolving the skin and its accessories, accounting for57.36% One of them was diagnosed with swelling of testis. Conclusion Adverse drug reactions reports of Potassium Sodium pehydroandroandrographolide Succinate for Injection was significantly associated with patients’ age, drug, compatibility of drugs and others.
Potassium Sodium Pehydroandroandrographolide Succinate for Injection; Adverse Drug Reaction; Analysis
2016-07-18
韦敬土,主管药师,医学硕士,主要从事药品不良反应监测研究。E-mail:346690169@qq.com
R969
A
1007-8517(2016)18-0100-03
