富硒阿胶-菊粉咀嚼片的制备及降血糖活性研究
2016-10-31史雪洁朱晓振衣悦涛
史雪洁,朱晓振,衣悦涛
(1.中国科学院烟台海岸带研究所,山东烟台 264003;2.中国科学院大学地球科学学院,北京 100049)
富硒阿胶-菊粉咀嚼片的制备及降血糖活性研究
史雪洁1,2,朱晓振1,2,衣悦涛1,*
(1.中国科学院烟台海岸带研究所,山东烟台 264003;2.中国科学院大学地球科学学院,北京 100049)
以阿胶、菊粉、富硒卡拉胶等为原料,依次经过原料的干燥、混匀、制软材、干燥、过筛、压片后制得富硒阿胶-菊粉咀嚼片。本文概述了富硒阿胶-菊粉咀嚼片的制备工艺流程并对优化过程进行描述,研究了其降血糖活性功能。研究结果表明:阿胶、菊粉、富硒卡拉胶、硬脂酸镁的添加量分别为24.5%、73.5%、1%、1%,以95%的乙醇溶液为黏合剂,可制得表面光滑、色泽均匀,独特风味的富硒阿胶咀嚼片。小鼠降血糖实验结果表明,样品组小鼠在灌胃处理30 d后随机血糖有显著降低,与二甲双胍作用相当,因而该产品具有显著降低血糖水平功效。
阿胶,菊粉,咀嚼片,工艺,降血糖活性
阿胶(AsiniCoriiColla)为马科动物驴的干皮或鲜皮经煎煮浓缩制成的固体胶[1],主要成分为蛋白质[2],对血虚动物具有良好的补血作用。阿胶含有丰富的铁元素和大量的动物蛋白,是一种极易吸收的铁补充剂,能够有效控制缺铁性贫血[3]。
由于现存制作工艺的局限性,新制阿胶总带有火毒,进服新鲜阿胶会引起喉咙干痛及大便秘结等症状[4]。此外,为调和阿胶的口感,通常加入大量的蔗糖或其他造成人体血糖升高的糖类,使糖尿病人无法服用,限制了阿胶的使用范围。菊粉,又名菊糖,由果糖分子通过β(1→2)糖苷键连接[5],末端是葡萄糖[6],是一类天然果聚糖的混合物。人体摄入后几乎不被胃酸水解,具有益生素的特点[7]。同时,还具有控制血脂[8]、不引起血糖波动[9]、促进矿物质吸收[10]、防治便秘[11]、预防结肠癌[12]等生理功能。将菊粉加入到阿胶中,不仅可以使阿胶具有更佳的口感,而且能够促进肠道有益菌的生长,促进肠道蠕动[13],防止便秘的发生,有效解决阿胶存在的副作用问题。
硒作为一种生物体必需的微量元素,具有抗氧化[14]、降血糖、抗衰老[15]及解毒[16]等功能。我国有30%的地区严重缺硒,生活在缺硒地区的人口达4亿之多[17]。补硒时以有机硒为最安全最有效的方法,通常在食品中添加有机硒。膳食硒最高安全摄入量400 μg∕日。
目前阿胶已经有口服液、颗粒剂等多种剂型出现在保健品行列,但还没有阿胶咀嚼片出现。与普通片剂相比,咀嚼片具有口感良好、食用方便、无需崩解过程、生物利用度高等优点。
本实验旨在以阿胶、菊粉为主要原料,配以适量的富硒卡拉胶以实现富硒目的,采用湿法制粒压片工艺研制出食用方便、口感合适、具有保健功能的富硒阿胶-菊粉咀嚼片,并对产品的降血糖活性进行评价。
1 材料与方法
1.1材料与仪器
阿胶山东东阿修元阿胶生物集团有限公司;硒化卡拉胶(含硒量1%)青岛鹏洋科技有限公司;菊粉荷兰Sensus公司;链脲佐菌素(Streptozotocin,STZ)美国Sigma公司;硬脂酸镁国药集团化学试剂有限公司;SPF级昆明种小鼠60只,雄性,3周龄,体重18~23 g,北京华阜康生物科技股份有限公司,合格证号:SCXK(京)2014-0004。
真空干燥箱、鼓风干燥箱上海一恒科学仪器有限公司;TDP-5单冲压片机中南制药机械厂;JJ-1电动搅拌器金坛市科析仪器有限公司;DH252B川井除湿机深圳市纳美特科技有限公司;水分测定仪奥豪斯仪器有限公司;ACCU-CHEK Performa血糖仪、血糖试纸瑞士Roche公司;20目、80目标准检验筛。
1.2实验方法
原料的干燥→混匀→制软材→干燥→过筛→压片→感官评价→咀嚼片
1.3操作要点
1.3.1原料的干燥将咀嚼片制备过程中需要的原料先研磨成粉末,后过40目筛,置于40 ℃真空干燥箱中,干燥过夜后置于干燥器内密封保存以备用。
1.3.2软材的制作与造粒利用除湿机将室内湿度降至30%以下,按配方将不同的原料混合均匀,边搅拌边喷入黏合剂,制成软硬适中的软材,将软材置于托盘中于40 ℃鼓风干燥箱中干燥6 h。干燥后的软材分别经过80目和20目的标准检验筛,以除去较大的结块和较细的粉末,得到体积适中的颗粒。
1.3.3压片为使咀嚼片表面光滑,易从模具上脱落,需在混合后的物料中加入一定量的润滑剂-硬脂酸镁,利用单冲压片机进行压片。
1.4感官评定
对各成分含量不同的咀嚼片进行评分,评分小组由具有一定感官评价经验的15人组成,每人各自打分后取平均值。评价指标为嗅觉、味觉、甜度、酸度、苦味和嚼劲。品尝一个配方后须漱口,并间隔1 min后对下一处方进行评价,感官质量评分标准见表1,对每个因素的评价采用3分制,分值越高,表明该特征指标越好[18]。

表1 咀嚼片感官评分标准
1.5 单因素实验
1.5.1乙醇浓度对造粒效果的影响湿法造粒中常使用的润湿剂是水和乙醇[19]。预实验表明,由于菊粉的吸湿性,造粒困难,难以进行压片操作,因此选用乙醇作为润湿剂。在预实验基础上,选择配方:阿胶24.5%、菊粉73.5%、硒化卡拉胶1%(含硒量为1%)、硬脂酸镁1%。将原料混合均匀,边搅拌边喷洒乙醇溶液,乙醇溶液的体积分数分别为100%、95%、90%、85%、80%,乙醇溶液添加量为配方质量的25%,按照上述造粒的操作步骤进行造粒。以得粒率为评价指标,对乙醇溶液不同浓度的造粒效果进行评价。定义得粒率(DLL)为颗粒制剂干燥后,依次经过20目和80目标准筛过筛之后,得到20目与80目之间的颗粒质量占总颗粒的比例。

式中,m1表示干燥后过20目和80目筛后剩余的颗粒质量;m2表示配方的总质量。
1.5.2乙醇添加量对造粒效果的影响在预实验基础上,选择配方:阿胶24.5%、菊粉73.5%、硒化卡拉胶1%(含硒量为1%)、硬脂酸镁1%。将原料混合均匀,边搅拌边喷洒体积分数为95%乙醇溶液,乙醇溶液的添加量分别为原料总质量的10%、20%、30%、40%、50%,按照上述操作步骤进行造粒。以得粒率为评价指标,对乙醇溶液不同添加量的造粒效果进行评价。
1.5.3润滑剂的加入量对菊粉咀嚼片压片效果的影响为了使咀嚼片表面光滑,在混合后的物料中通常加入一定质量的润滑剂。本实验采用硬脂酸镁作为润滑剂。硬脂酸镁加入量为0.5%、1%、1.5%、2%、2.5%。在预实验基础上,选择配方:阿胶24.5%、菊粉73.5%、硒化卡拉胶1%(含硒量为1%)。将原料混合均匀,边搅拌边喷洒体积分数为95%乙醇溶液,乙醇溶液的添加量为原料总质量的25%。按照上述造粒的操作步骤进行造粒并对其评价。

表3 乙醇体积分数对得粒率的影响
注:▲p<0.05,与体积分数为80%组比较。

表4 乙醇溶液添加量对得粒率的影响
注:▲p<0.05,与添加量为10%组比较。1.6阿胶-菊粉咀嚼片最佳配方的确定
在单因素实验的基础上,应用Design Expert 7.0.0软件,采用Box-Behnken Design设计实验方案,以乙醇浓度(A)、乙醇添加量(B)、硬脂酸镁添加量(C)为影响因素,以咀嚼片的感官评分为响应值,设计了三因素三水平的正交实验,正交实验因素与水平表见表2。配方中阿胶、硒化卡拉胶、菊粉含量保持不变,以咀嚼片的感官评分为指标,对嚼味剂和填充剂的含量进行优化,以期得到口感最佳的咀嚼片配方。
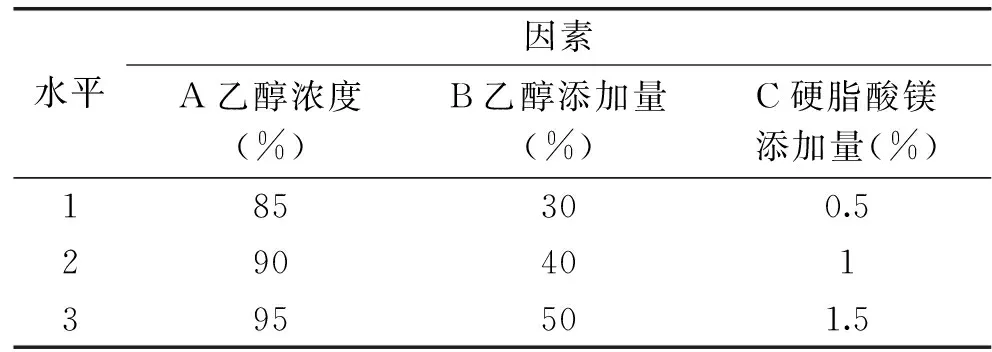
表2 正交实验因素与水平表
1.7咀嚼片功能成分降血糖实验
1.7.1糖尿病模型建造SPF级雄性昆明小鼠60只,3周龄,体重18~23 g,适应性饲养一周后,随机分为正常对照组和模型组,正常对照组10只,模型组50只。正常对照组普通饲料喂养,模型组高脂高糖饲料喂养。4周后检测体重及血糖,模型组单次腹腔注射120 mg/kg的STZ(STZ用灭菌的0.1 mmol/L、pH4.4的柠檬酸-柠檬酸钠缓冲液配成2%的溶液,冰上避光操作,现配现用),用于诱导动物糖尿病模型。正常组只注射等量的生理盐水。10 d后取尾静脉血,测得空腹血糖高于7.0 mmol/L 和餐后血糖高于11.1 mmol/L的作为糖尿病模型。一次注射未成模,立即按原剂量补注一次STZ,未成者淘汰,成模但缓解者淘汰。
1.7.2动物分组及药物处理建模成功小鼠40只。对小鼠进行如下分组:正常对照组(10只)、糖尿病模型组(10只)、样品+糖尿病组(10只)和二甲双胍+糖尿病组(10只)。
除正常对照组外其余各组小鼠均给予相应治疗:样品组(饲料为最佳原料配比制成的咀嚼片,溶解后灌胃给药,26 g/kg·d);二甲双胍组(150 mg/kg·d,灌胃给药);糖尿病组(等量生理盐水,灌胃给药);除正常对照组外其他小鼠给予高脂高糖饲料喂养,每日灌胃1次,连续灌胃8周,于第4周结束时分别检测体重及血糖值[20]。
1.8产品质量指标检测
1.8.1感官指标采用感官分析进行评定。
1.8.2物理指标脆碎度用脆碎度检查仪测定,硬度用硬度仪进行测定。
1.8.3微生物指标的检测微生物指标按照GB/T4789-2008《食品卫生微生物学检测》的规定执行。
1.8.4硒含量的测定硒含量按照GB 5009.93-2010 《食品安全国家标准 食品中硒的测定》的规定进行测定。
2 结果与分析
2.1单因素实验结果
2.1.1润湿剂对造粒效果的影响由表3可以看出,乙醇体积分数在80%~95%范围内,随着乙醇体积分数的增加,得粒率不断上升,当乙醇体积分数为95%时,得粒率达到了90.63%±2.92%,这主要是由于原料中的菊粉易吸水形成大的粘块,水分含量越高形成的粘块越多,干燥后不易通过标准筛,难以形成颗粒。当乙醇的体积分数为100%时,得粒率反而下降,这主要是由于无水乙醇对原料的粘结作用不够,软材干燥后经过标准筛剩余了大量的粉末,因此得粒率出现下降。因此,在后续实验中选择体积分数为95%的乙醇作为润湿剂。
2.1.2润湿剂添加量对造粒效果的影响由表4可以看出,当乙醇溶液添加量由原料总质量的10%增加到20%时,得粒率由25.34%±3.67%增加到了74.45%±4.38%;乙醇溶液添加量由20%增加到30%时,得粒率增加幅度较小;当乙醇溶液添加量由30%增加到50%时,得粒率开始迅速下降。造成这种现象的原因主要是由于乙醇溶液添加量较低时,粘合剂不够,有大量的粉末不能相互粘结形成颗粒;当乙醇溶液添加量过高时,

表5 硬脂酸镁加入量对压片效果的影响
原料中含有大量的水分,原料间的粘结作用过度形成大的结块,同样不利于颗粒的形成,因此,在后续实验中乙醇溶液添加量确定为30%。
2.1.3润滑剂的加入量对菊粉咀嚼片压片效果的影响由表5可以看出,当硬脂酸镁的加入量为1%时,制得的咀嚼片脱模效果好,而且具有很好的流动性以及润滑性,黏度低。因此,本实验采用加入量为1%的硬脂酸镁作为制备咀嚼片的润滑剂。
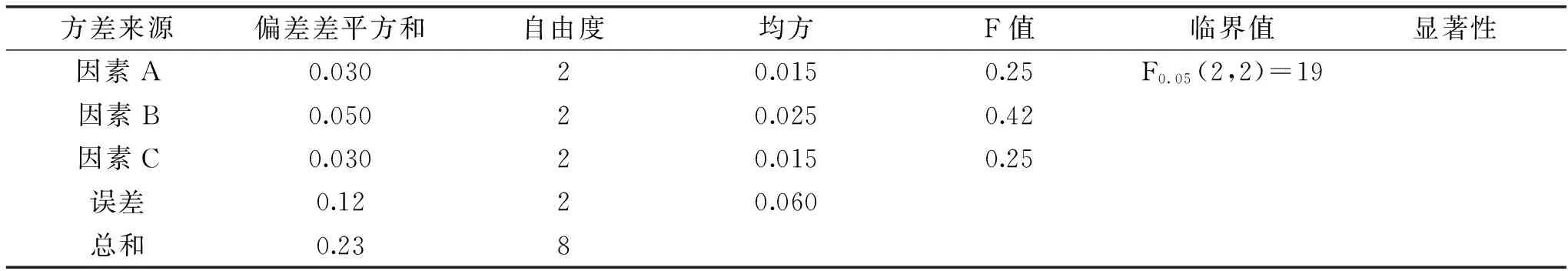
表7 方差分析表
2.2正交实验结果
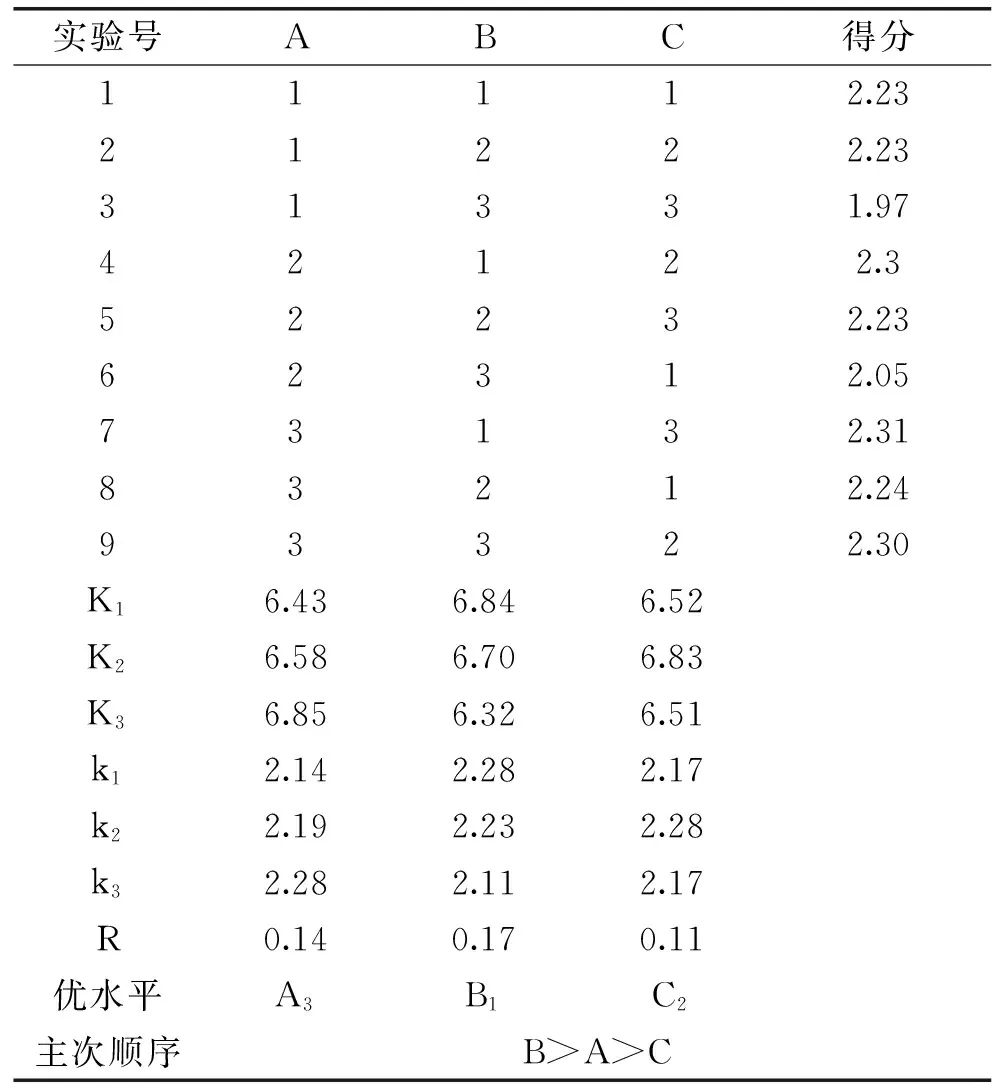
表6 咀嚼片配方优化实验结果
由表6可以看出,RB>RA>RC,在实验设计的范围内,乙醇浓度对咀嚼片口感的影响程度最大,其次为乙醇的加入量及硬脂酸镁的加入量。由直观分析可以看出A3>A2>A1,B1>B2>B3,C2>C1=C3。因而较好的组合为A3B1C2,即乙醇浓度为95%、乙醇加入量为原料总质量的30%、硬脂酸镁加入量为1%。由方差分析可知,三个因素对产量的影响都不是很大,可能是由于本实验误差自由度较小(仅为2),使检验灵敏度低,从而掩盖了考察因素的显著性。选择平均数较大的水平A3,B1,C2组合成最优水平组合A3B1C2。采用与实验方法相同的工艺,对制备的咀嚼片进行感官评价。三次平行实验得到的感官评价平均分为2.35分,制备的咀嚼片呈淡黄色,色泽均匀,表面光滑,具有阿胶-菊粉的独特风味、酸甜协调、崩解性好,在25 min内全部溶解,硬度及其质量差异限度等均符合中国药典规定。
2.3咀嚼片功能成分降血糖实验结果
表8实验数据表明,小鼠经过药物处理饲养30 d后,与正常组相比较体重显著降低。但样品组小鼠体重在灌胃处理30 d后可见明显增加,与糖尿病模型组相比有统计学意义,因此可以推测样品组饲料对糖尿病小鼠体重的下降具有减缓作用。

表8 各组小鼠药物处理前后体重变化±s)
注:▲p<0.05,与糖尿病模型组比较,表9同。
表9实验数据表明,正常对照组小鼠在灌胃30 d后血糖水平基本稳定,糖尿病模型组血糖水平具有较大幅度的增加。模型组血糖显著高于正常对照组,具有显著性差异。与糖尿病模型组比较,样品组与二甲双胍组小鼠在灌胃处理30 d后随机血糖均有降低,差异具有统计学意义,样品组降低糖尿病小鼠血糖和减缓糖尿病小鼠体重的作用显著,与二甲双胍作用相当。与正常对照组相比较,样品组与二甲双胍组小鼠的血糖偏高。

表9 各组小鼠药物处理前后随机血糖变化±s)
2.4产品质量指标检测
2.4.1感官指标本品为淡黄色片,外观完整,表面光滑,色泽均匀,具有菊粉、阿胶特有的香味,酸甜可口、入口柔顺、无异味,崩解性好,能在25 min内全部崩解。
2.4.2物理指标片重0.55 g±5.0%;脆硬度≤0.6%;硬度60 N±5%。
2.4.3微生物指标细菌总数≤1000 个/g;大肠杆菌未检出;致病菌未检出。
2.4.4硒含量指标硒含量为0.01%,在咀嚼片中稳定存在。
3 结论
与普通片剂相比,咀嚼片具有携带方便、质量稳定、口感良好等优点,片剂经过咀嚼后进入肠道,可减少药剂对胃肠道的负担,特别适用于小儿、老人、吞咽困难或胃肠功能较差的患者。本实验对富硒阿胶咀嚼片的制备工艺及配方进行了优化,并对咀嚼片中功能成分的降血糖效果进行了研究,得到如下结论:
按照配方:阿胶、菊粉、富硒卡拉胶、硬脂酸镁的添加量分别为24.5%、73.5%、1%、1%。将原料混合均匀,边搅拌边加入体积分数为95%的乙醇溶液,加入量为原料总质量的30%,在40 ℃的鼓风干燥箱中干燥6 h,制得富硒阿胶咀嚼片。采用此方法制得的咀嚼片表面光滑、色泽均匀,口感良好。
小鼠降血糖实验结果表明,该产品能够显著降低小鼠的血糖水平,并对其体重的减少具有缓解作用,与二甲双胍作用相当。因此,用阿胶、菊粉等原料制成的富硒阿胶咀嚼片具有降血糖活性的功效。
[1]陈慧慧,冯明建,朱海芳,等. 阿胶药理研究进展[J]. 国药物评价,2014,31(1):23-26.
[2]霍光华,阿胶氨基酸矿物成分分析与评价[J]. 氨基酸和生物资源,1996,18(4):22-24.
[3]高景会,王蕊,范峰. 阿胶现代研究进展[J]. 中国药事,2011,25(4):396-401.
[4]程博琳,苗明三. 阿胶的现代研究及特点[J]. 中医学报,2015,30(3):67-69.
[5]Gibson G R,Roberfroid M B. Dietary modulation of the human colonic microbiota-introducing the concept of prebiotics[J]. Journal of Nutrition,1995,125(6):1401-1412.
[6]彭英云,郑清,张涛. 菊粉的功能与利用[J]. 食品研究与开发,2012,33(10):236-240.
[7]Li W C,Zhang J,Yu C W. Extraction,degree of polymerization determination and prebiotic effect evaluation of inulin from Jerusalem artichoke[J]. Carbohydrate Polymers,2015,121(1):315-319.
[8]Canzi E,Brighenti F B,Casiraghi M C,et al. Effect of consumption of a ready-to-eat breakfast cereal containing inulin on the intestinal milieu and blood lipids in healthy male volunteers[J]. European Journal of Clinical Nutrition,1999,53(9):726-733.
[9]Niness K R,Inulin and oligofructose:what are they[J]. Journal of Nutrition,1999,129(7):1402-1406.
[10]Remesy C,Behr S R,Levrat M A,et al. Fiber fermentation in the rat cecum and its physiological consequences[J]. Nutrition Research,1992,12(10):1235-1244.
[11]Hond E D,Geypens B,Ghoos Y. Effect of high performance chicory inulin on constipation[J]. Nutrition Research,2000,20(5):731-736.
[12]Qian S Q,Lu H D,Meng P P. Effect of inulin on efficient production and regulatory biosynthesis of bacillomycin D in Bacillus subtilisfmbJ[J]. Bioresource Technology,2015,179(3):260-267.
[13]王金刚,杜宁娟. 菊粉的工业化生产技术与发展前景[J]. 食品工业科技,2008,29(11):308-312.
[14]安丽霞,温伟业,王俊东,等. 硒的生物学作用与生物转化[J]. 上海畜牧兽医通讯,2006,01(2):55-56.
[15]陈必链. 我国富锌和富硒功能食品研究现状[J]. 食品研究与开发,1999,20(1):33-37.
[16]马卓,刘宗平,张白银,等. 绵羊铅镉联合中毒与硒解毒的实验病理学研究[J]. 中国兽医科技,1997,27(3):12-14.
[17]董海兴. 硒与疾病[J]. 中国疗养医学,2006,15(2):113-114.
[18]陈武,邹盛勤,伍晓春,等.绞股蓝无糖口含片的制备工艺研究[J].食品科学,2008,29(3):245-248.
[19]冯大伟,冀晓龙,王敏,等. 菊粉咀嚼片制备工艺研究[J]. 食品研究与开发,2013,34(14):46-49.
[20]李耀冬,叶静,肖美添. 复方海藻膳食纤维对糖尿病小鼠降血糖作用的研究[J]. 食品工业科技,2014,35(10):341-345.
Preparation and hypoglycemic activity of selenium-enrichedasinicorricolla-inulin chewable tables
SHI Xue-jie1,2,ZHU Xiao-zhen1,2,YI Yue-tao1,*
(1.Yantai Institute of Coastal Zone Research,Chinese Academy of Sciences,Yantai 264003,China; 2.College of Earth Sciences,University of Chinese Academy of Sciences,Beijing 100049,China)
AsiniCoriiColla,inulin and selenium-enriched carrageenan were used as the main raw materials,and a kind of selenium-enrichedAsiniCoriiColla-inulin chewable tablets were prepared through drying,mixing,making granules,drying,compression. The manufacturing process and main point of the operation were described detailedly. Besides,hypoglycemic activity was studied. Accoding to the research,whenAsiniCoriiColla,inulin,selenium-enriched carrageenan,and magnesium stearate were 24.5%,73.5%,1%,1%,with 95% ethanol solution as a adhesive,a kind of selenium-enrichedAsiniCoriiColla chewable tablets with smooth surface,identical color and special flavor can be obtained. The results of hypoglycemic tests in mice indicated that blood sugar levels of mice which were feed withAsiniCoriiColla contained inulin and selenium-enriched carrageenan were decreased significantly after treatment for 30 d.
AsiniCoriiColla;inulin;chewable tables;processing technology;hypoglycemic activity
2016-03-03
史雪洁(1990-),女,硕士研究生,研究方向:资源生物与化学,E-mail:shixuejie@126.com。
衣悦涛(1974-),男,博士,副研究员,研究方向:海岸带资源化学,E-mail:ytyi@yic.ac.cn。
863计划(2012AA021205-1);山东省科技重大专项(2015ZDJS03002)。
TS201.1
B
1002-0306(2016)17-0242-05
10.13386/j.issn1002-0306.2016.17.039
