参麦注射液活性成分在正常和心肌缺血Beagle犬体内的药动学研究Δ
2016-10-26张世良董晓茜李国信夏素霞朱婉玲辽宁省中医药研究院临床药理实验室沈阳0034辽宁中医药大学药学院沈阳003
唐 思,杨 瑞,张世良,董晓茜,李国信#,夏素霞,朱婉玲(.辽宁省中医药研究院临床药理实验室,沈阳 0034;.辽宁中医药大学药学院,沈阳 003)
参麦注射液活性成分在正常和心肌缺血Beagle犬体内的药动学研究Δ
唐 思1*,杨 瑞1,张世良1,董晓茜1,李国信1#,夏素霞1,朱婉玲2(1.辽宁省中医药研究院临床药理实验室,沈阳 110034;2.辽宁中医药大学药学院,沈阳 110032)
目的:研究参麦注射液活性成分人参皂苷Rg1、人参皂苷Re在正常和心肌缺血Beagle犬体内的药动学。方法:取6只Beagle犬sc盐酸异丙肾上腺素(1.1 mg/kg)以复制心肌缺血模型(模型组),另取6只犬sc等体积生理盐水(2.2 ml/kg)作为对照组。两组犬分别于第1天上午8:00、下午13:00和第2天上午8:00给药。第2天给药后1 h,各组犬iv参麦注射液(1.6 ml/kg),在1 h左右滴注完成。各组犬于iv开始后0、0.25、0.5、0.75、1(iv结束)、1.5、2、3、4、6、8、12、24 h取血。采用液相色谱-质谱联用法测定人参皂苷Rg1、人参皂苷Re的血药浓度,WinNonlin 6.3软件计算药动学参数并进行比较。结果:人参皂苷Re在模型组犬体内的t1/2为(2.69±1.12)h,AUC0-24 h为(2 060.78±812.18)h·μg/L,Vz为(46.16±20.98)ml,CL为(9.02±4.45)ml/h;与正常组比较,AUC0-24 h显著升高,Vz、CL显著降低,差异均有统计学意义(P<0.05)。而两组犬人参皂苷Rg1的药动学参数无显著性差异(P>0.05)。结论:心肌缺血会影响Beagle犬体内人参皂苷Re的消除,对人参皂苷Rg1药动学过程无明显影响。
参麦注射液;心肌缺血模型;人参皂苷Rg1;人参皂苷Re;Beagle犬;药动学
参麦注射液的主要成分为红参、麦冬,具有益气固脱、养阴生津、生脉之功效,临床广泛用于气阴两虚型休克、冠心病、病毒性心肌炎、慢性肺心病、粒细胞减少症等疾病的治疗[1-3]。参麦注射液中红参为君药,主要成分为人参皂苷,其中人参皂苷Rg1、人参皂苷Re含量稳定,是参麦注射液的标志性成分之一。目前,多项研究报道了参麦制剂的药动学研究[4-6],但对不同模型下参麦注射液的药动学比较的研究尚未见文献报道。因此,在本研究中笔者探讨了参麦注射液活性成分人参皂苷Rg1、人参皂苷Re在正常和心肌缺血Beagle犬体内的药动学过程,旨在为其临床应用提供一定的实验依据。
1 材料
1.1 仪器
6410型三重四级杆串联液质联用(LC-MS/MS)仪,包括电喷雾离子源、Quantitative Analysis B.01.04数据处理系统(美国安捷伦公司);XW-80A微型旋涡混合仪(上海沪西分析仪器厂);XS105分析天平(瑞士梅特勒-托利多仪器有限公司);SIGMA3-18k低温高速离心机(德国Sigma公司);Milli-Q超纯水机(德国默克公司);DW-86L836超低温保存箱(青岛海尔公司);MTN-2800W氮吹浓缩装置(天津奥特赛恩斯仪器有限公司)。
1.2 试药
参麦注射液(正大青春宝药业有限公司,批号:1308261,规格:10 ml/支;1 ml参脉注射液中含人参皂苷Rg1184.86 μg、人参皂苷Re 105.59 μg);盐酸异丙肾上腺素(上海禾丰制药有限公司,批号:131001,规格:2 ml∶1 mg);肝素钠注射液(江苏万邦生化医药股份有限公司,批号:1209124,规格:1 ml/支)。人参皂苷Rg1对照品(批号:110703-201128)、人参皂苷Re对照品(批号:110754-201324)、内标地西泮对照品(批号:171225-200302)均购自中国食品药品检定研究院;乙腈、甲醇(色谱纯)均购自德国默克公司。
1.3 动物
普通级Beagle犬12只,♂♀各半,体质量(8~10)kg,由北京市沙河通利试验动物养殖场提供,许可证号:SCXY(京)2010-0004。
2 方法
2.1 色谱与质谱条件
色谱柱为ZORBAX SB-C18Synergi POLAR-RP柱(30 mm×2.16 mm,3.5 μm);流动相为水(A)-乙腈(B),梯度洗脱(0~5 min,15%B→30%B;5~18 min,30%B;18~23 min,30% B→100%B;23~25 min,100%B);流速为0.3 ml/min;柱温为40 ℃;进样量为10 μl。
质谱条件:ESI离子源;气体流量为9 L/min;气体温度为350 ℃;雾化压力为276 kPa;毛细管电压为4 000 V;扫描方式为选择多反应监测(MRM),正离子方式检测;用于定量的离子m/z分别为823.5→643.5(人参皂苷Rg1)、969.5→789.5(人参皂苷Re),碎裂电压分别为350、320 V,碰撞能量(CE)分别为40 V、45 V;内标m/z为285.0→193.0,碎裂电压为165 V,CE为30 V;扫描时间均为200 ms。
2.2 贮备液的制备
准确称取人参皂苷Rg1、人参皂苷Re和内标对照品各10 mg,分别置于10 ml量瓶中,加甲醇溶解并定容,即得1 mg/ml的贮备液,4 ℃保存,使用时用乙腈稀释至所需质量浓度即可。
2.3 分组、造模与给药
采用分层随机法,将12只Beagle犬分为心肌缺血模型组和正常组,每组6只,♂♀各半。心肌缺血模型组犬sc盐酸异丙肾上腺素(1.1 mg/kg,剂量选择依据文献[7-9]),正常组犬sc等体积生理盐水(2.2 ml/kg)作为对照。两组犬分别于第1天上午8:00、下午13:00和第2天上午8:00给药。第1次给药前16 h各组犬禁食不禁水,第2天给药后1 h,各组犬iv参麦注射液(1.6 ml/kg,剂量选择依据文献[10]),在1 h左右滴注完成。各组犬于iv开始后0、0.25、0.5、0.75、1(iv结束)、1.5、2、3、4、6、8、12、24 h静脉采血5 ml于肝素化离心试管中,以离心半径为8 cm、3 500 r/min离心10 min分离血浆,于-70 ℃冰箱保存,备用。
2.4 血浆样品处理
精密吸取血浆200 μl,置于2 ml空白离心管中,加入内标贮备液10 μl,涡旋混匀30 s;加入乙腈400 μl,涡旋混匀3 min;以离心半径为6 cm、14 000 r/min离心10 min。取上清液于2 ml空白离心管中,在40 ℃水浴下氮气吹干,再加入流动相100 μl复溶,涡旋2 min,以离心半径为6 cm、14 000 r/min离心10 min,取上清液10 μl进样分析。
2.5 人参皂苷Rg1和人参皂苷Re测定的方法学考察
按照相关方法考察人参皂苷Rg1、人参皂苷Re测定方法的回归方程与线性范围、回收率、基质效应、精密度、准确度和稳定性。
2.6 数据处理
采用WinNonlin 6.3药动学软件对犬体内的药-时曲线进行非房室模型拟合,采用SPSS 19.0统计软件对两组犬的药动学参数进行比较。
3 结果
3.1 方法学考察结果
3.1.1 专属性考察结果 检测方法为课题组前期研究的方法[5]。取“2.2”~“2.4”项下溶液按“2.1”项下方法进样测定,结果人参皂苷Rg1和人参皂苷Re在选定的色谱和质谱条件下专属性良好。色谱图见图1。

图1 LC-MS/MS色谱图Fig 1 LC-MS/MS chromatogram
3.1.2 线性范围、回收率、精密度及基质效应考察结果 人参皂苷Rg1、人参皂苷Re线性范围分别为0.64~509.00 μg/L(r= 0.996 7)、0.62~501.00 μg/L(r=0.997 8),定量限(信噪比为10)分别为0.64、0.62 μg/L;日间和日内精密度均小于15% (n=18);提取回收率均大于85%(RSD<15%,n=9);基质效应在90%~110%之间(RSD<15%,n=18),结果见表1。
3.1.3 稳定性考察结果 将含人参皂苷Rg1、人参皂苷Re的血浆样品分别进行室温(25 ℃)放置6 h、反复冻融、长期冷冻60 d考察。结果显示,人参皂苷Rg1、人参皂苷Re在上述条件下均能保持稳定,RSD均小于15%(n=18)。
3.2 药动学研究
两组犬分别于各时间点测定人参皂苷Rg1、人参皂苷Re血药浓度,平均药-时曲线见图2。采用WinNonlin 6.3软件,按非房室模型进行处理,计算药动学参数,见表2。
表1 精密度及回收率试验结果(±s)Tab 1 Results of precision and recovery tests(±s)

表1 精密度及回收率试验结果(±s)Tab 1 Results of precision and recovery tests(±s)
组分人参皂苷Rg1人参皂苷Re加入量,μg/L 1.28 50.90 407.20 1.24 50.10 400.80日内精密度测得量,μg/L 1.00±0.04 52.18±3.03 368.49±32.79 1.05±0.05 49.36±2.65 402.20±11.84 RSD,% 4.48 5.80 8.90 5.10 5.36 2.95日间精密度测得量,μg/L 1.03±0.07 51.99±2.50 401.59±36.49 1.00±0.07 51.98±3.36 398.91±21.55 RSD,% 6.85 4.80 9.09 6.79 6.46 5.40提取回收率,% 86.63±8.23 100.24±2.27 95.27±6.98 96.22±3.60 94.54±7.86 100.97±6.21基质效应,% 103.67±5.96 104.06±6.31 101.49±4.05 108.11±3.84 94.16±3.84 99.91±5.12
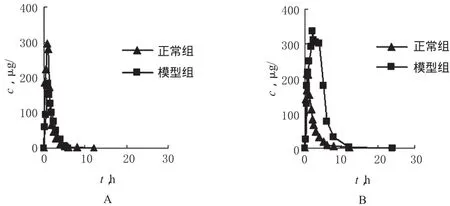
图2 两组犬人参皂苷Rg1、人参皂苷Re平均药-时曲线Fig 2 Mean drug concentration-time curves of ginsenoside Rg1and ginsenoside Re of dogs in 2groups
表2 两组犬人参皂苷Rg1、人参皂苷Re药动学参数比较(x± s,n=6)Tab 2 Comparison of the pharmacokinetic parameters of ginsenoside Rg1and ginsenoside Re of dogs between 2groups(±s,n=6)

表2 两组犬人参皂苷Rg1、人参皂苷Re药动学参数比较(x± s,n=6)Tab 2 Comparison of the pharmacokinetic parameters of ginsenoside Rg1and ginsenoside Re of dogs between 2groups(±s,n=6)
注:与正常组比较,*P<0.05Note:vs.the normal group,*P<0.05
模型组2.69±1.12 2.00±1.10 2 060.78±812.18*2 098.23±855.41*46.16±20.98*9.02±4.45*4.50±1.23 4.66±1.21参数t1/2,h tmax,h AUC0-24,h·μg/L AUC0-∞,h·μg/L Vz,ml CL,ml/h MRT0-24 h,h MRT0-∞,h人参皂苷Rg1正常组2.41±2.21 0.83±0.29 437.45±206.63 443.91±206.48 178.56±225.53 42.49±17.42 0.95±0.31 1.20±0.61模型组1.04±0.55 1.16±0.41 363.58±138.82 372.74±138.02 76.03±57.83 49.39±21.84 1.31±0.35 1.47±0.42人参皂苷Re正常组2.44±0.98 0.81±0.31 460.79±173.51 471.51±174.42 142.55±87.86 38.73±15.96 1.69±0.46 2.02±0.66
结果,正常组与模型组Beagle犬在iv参麦注射液后,人参皂苷Rg1的主要药动学参数两组间差异无统计学意义(P>0.05)。而模型组犬人参皂苷Re的t1/2为(2.69±1.12)h,AUC0-24 h为(2 060.78±812.18)h·μg/L,Vz为(46.16±20.98)ml,CL为(9.02±4.45)ml/h;与正常组比较,模型组犬人参皂苷Re的AUC0-24 h显著升高,Vz、CL显著降低(P<0.05)。
4 讨论
相关研究报道,大剂量注射异丙肾上腺素可致心肌收缩过快、收缩力过大、冠脉充盈不足、心肌耗氧量大大超过供氧量,导致心肌缺血[7-9]。笔者前期进行了预实验,筛选异丙肾上腺素制备心肌缺血模型的用量,最终确定sc盐酸异丙肾上腺素1.1 mg/kg复制心肌缺血模型。另外,根据参麦注射液临床用药的剂量,按单位体质量计算剂量[10],经换算后给予Beagle犬参麦注射液剂量确定为1.6 ml/kg。
本研究首次对参麦注射液在心肌缺血与正常Beagle犬中的药动学参数进行了比较。结果,人参皂苷Rg1在模型组犬体内药动学无显著变化。但相关研究报道,人参皂苷Rg1对心肌缺血有一定治疗作用[11-12],提示后续研究可结合药效研究、扩大样本量进一步探讨人参皂苷Rg1治疗心肌缺血的疗效与机制。
相关研究报道,人参皂苷Re可以抑制急性缺血再灌流诱导的心肌细胞凋亡[13-14]。本研究表明人参皂苷Re在模型组犬体内的Vz、CL显著低于正常组,使血药浓度、AUC0-24 h和AUC0-∞显著高于正常组,这可能是造模后Beagle犬的组织分布、代谢酶等发生了病理变化原因导致的,但也不排除是由于实验用Beagle犬数量少或是个体差异造成的。
综上所述,心肌缺血会影响Beagle犬体内人参皂苷Re的消除;对人参皂苷Rg1药动学过程无明显影响。后续研究应尽可能找出与之相关活性物质及其代谢产物,并结合药理、药效进行更全面的研究。
[1]余健,辛艳飞,宣尧仙.参麦注射液药理作用的物质基础研究进展[J].医药导报,2013,32(4):662.
[2]徐成恒.参麦注射液的临床应用进展[J].安徽医学,2011,32(6):839.
[3]曹旭东,丁志山,陈建真.参麦注射液药理及临床研究进展[J].中国中医药信息杂志,2010,17(3):104.
[4]李国信,唐思,夏素霞,等.生脉拆方系列注射液中人参皂苷Rg1和Re药代动力学研究[J].中华中医药学刊,2010,28(11):2 310.
[5]夏素霞,李国信,姜春梅,等.液相色谱-质谱联用法同时测定生脉注射液中人参皂苷Rg1、Re、Rb1和五味子醇甲在健康人血浆的浓度[J].中国临床药理学杂志,2011,27 (10):789.
[6]李国信,姜春梅,夏素霞,等.生脉注射液与参麦注射液在健康人体的药代动力学[J].中国临床药理学杂志,2011,27(6):432.
[7]孙波,高海成,黄秀英,等.冠脉结扎法与给药法制作大鼠心肌缺血模型的比较[J].实验动物科学,2010,27(5):16.
[8]杨勇,容蓉,陈明强,等.异丙肾上腺素诱导小鼠急性心肌缺血模型的方法比较[J].中药药理与临床,2010,26(5):153.
[9]李晶华,肖铁卉,马静,等.芪丹通脉片对犬慢性心肌缺血预防作用及其机制[J].安徽中医学院学报,2010,29 (4):52.
[10]黄继汉,黄晓晖,陈志扬,等.药理实验中动物间和动物与人体间的等效剂量换算[J].中国临床药理学与治疗学,2004,9(9):1 069.
[11]来方远,潘永明,艾秀锋,等.人参皂苷Rg1对急性心肌缺血豚鼠心电图的影响[J].中华中医药学刊,2011,29(17):2 529.
[12]来方远,潘永明,艾秀锋,等.人参皂苷Rg1对豚鼠急性心肌缺血的保护作用[J].中药新药与临床药理,2011,22 (4):390.
[13]高莹,杨积武,王艳春,等.人参皂苷Re对大鼠心肌缺血再灌注细胞凋亡及Caspase-3的影响[J].辽宁中医药大学学报,2011,13(2):124.
[14]石楸鸣.人参皂苷的药理作用研究进展[J].中国药房,2010,21(31):2 967.
Pharmacokinetics Study of the Active Ingredients of Shenmai Injection in Normal Beagle Dogs and Those with Myocardial Ischemia
TANG Si1,YANG Rui1,ZHANG Shiliang1,DONG Xiaoqian1,LI Guoxin1,XIA Suxia1,ZHU Wanling2(1.Laboratory of Clinical Pharmacology,Liaoning Academy of Traditional Chinese Medicine,Shenyang 110034,China;2.College of Pharmacy,Liaoning University of Traditional Chinese Medicine,Shenyang 110032,China)
OBJECTIVE:To study the pharmacokinetics of the active ingredients of Shenmai injection,including ginsenoside Rg1and ginsenoside Re,in normal Beagle dogs and those with myocardial ischemia.METHODS:6 Beagle dogs were given isoproterenol hydrochloride(1.1 mg/kg)sc to establish the model of myocardial ischemia(model group).Another 6 Beagle dogs were given isometric normal saline(2.2 ml/kg)sc as controls group.The two groups of dogs respectively received corresponding drugs sc at 8:00 am and 13:00 pm on day 1 and at 8:00 am on day 2.Each group of dogs were given Shenmai injection(1.6 ml/kg)iv 1 h after administration on day 2,and such intravenous drip lasted for about 1 h.Blood was collected from each group 0,0.25,0.5,0.75,1(the end of iv),1.5,2,3,4,6,8,12 and 24 h from the start of iv.Liquid chromatography-mass spectrometry was adopted to determine the concentrations of ginsenoside Rg1and ginsenoside Re in blood,and WinNonlin 6.3 was used to calculate pharmacokinetic parameters for comparison.RESULTS:For ginsenoside Re in the dogs of the model group,t1/2was(2.69±1.12)h,AUC0-24 hwas(2 060.78±812.18)h·μg/L,Vzwas(46.16±20.98)ml and CL was(9.02±4.45)ml/h;compared to the normal control group,AUC0-24 hwas much greater and Vzand CL were significantly lower,showing a statistically significant difference(P<0.05).No significant difference in the pharmacokinetic parameters of ginsenoside Rg1was shown between 2 groups(P>0.05).CONCLUSIONS:Myocardial ischemia may affect the removal of ginsenoside Re in Beagle dogs,but has no effect on the pharmacokinetic process of ginsenoside Rg1.
Shenmai injection;Myocardial ischemia model;Ginsenoside Rg1;Ginsenoside Re;Beagle dogs;Pharmacokinetics
R284.1;R917
A
1001-0408(2016)25-3475-03
10.6039/j.issn.1001-0408.2016.25.06
2015-11-04
2016-07-18)
(编辑:刘明伟)
国家科技重大专项课题(No.2012ZX09303017);临床重点专科建设项目资助(2013年);国家中医药管理局临床中药学重点学科(2009年);辽宁中医药大学杏林学者青蓝工程(2013年)
*副研究员,硕士。研究方向:临床药理学。电话:024-86803043。E-mail:tangsi81@163.com
主任医师,博士。研究方向:临床药理学。电话:024-86803043。E-mail:syyljdlgx024@126.com
