大鼠血浆中重组人钙调磷酸酶B亚基的ELISA双抗体夹心法测定及其药动学研究Δ
2016-10-26韩克胜谢学立田树红邢桂兰林春华邵继平海口奇力制药股份有限公司海口57016海南省药物临床前药理毒理学研究重点实验室海口571199
韩克胜,谢学立,田树红,邢桂兰,符 江,邢 俊,林春华,谭 鹏,邵继平#(1.海口奇力制药股份有限公司,海口 57016;.海南省药物临床前药理毒理学研究重点实验室,海口 571199)
大鼠血浆中重组人钙调磷酸酶B亚基的ELISA双抗体夹心法测定及其药动学研究Δ
韩克胜1*,谢学立2,田树红2,邢桂兰2,符 江2,邢 俊2,林春华2,谭 鹏2,邵继平2#(1.海口奇力制药股份有限公司,海口 570216;2.海南省药物临床前药理毒理学研究重点实验室,海口 571199)
目的:建立大鼠血浆中重组人钙调磷酸酶B亚基(rhCNB)的测定方法,并研究其药动学特征。方法:采用酶联免疫吸附(ELISA)双抗体夹心法,将1µg/ml的rhCNB单克隆抗体mAb包板,加入待测样品,再加入rhCNB多克隆抗体pAb(稀释比例为1∶5 000)和辣根过氧化酶(HRP)标记抗免疫球蛋白G(IgG)(稀释比例为1∶10 000),以四甲基联苯胺显色,用酶标仪在450 nm波长处测定吸光度(OD值)。测定6只大鼠iv 2.5 mg/kg rhCNB后2、15、30、60、120、240、480、720 min的血药浓度,以BAPP 3.0软件计算药动学参数。结果:rhCNB检测质量浓度的线性范围为0.195~12.5 ng/ml(r2=0.995 0),定量下限为0.195 ng/ml,准确度为97.300%~103.622%(RSD均小于7.5%,n=6);批内、批间和反复冻融3次的RSD均不大于8.5%(n=6、18、15)。该药在大鼠体内的药动学特征符合二室模型,AUC0-720 min为173.038 mg·min/L、t1/2为94.62 min。结论:建立的方法特异性强、灵敏度高、准确度及精密度好,可用于生物样品中rhCNB的定量检测和药动学研究。
rhCNB多肽;酶联免疫吸附双抗体夹心法;大鼠;定量检测;药动学
肝癌(Liver cancer)是我国最常见的恶性肿瘤之一,其发病率和病死率仅次于胃癌和食道癌,严重威胁了人民的健康和生命,其晚期患者往往无有效药物可用。目前临床上大多数抗肝癌药缺乏组织选择性,在发挥疗效的同时也产生严重的毒副作用,常见的有消化道反应、骨髓抑制、脱发等。因此,寻找高效低毒的新型抗肝癌药势在必行。
钙调磷酸酶(Calcineurin,CN)是目前唯一一种依赖钙(Ca)/钙调素(CaM)的蛋白磷酸酶,由A、B亚基以1∶1组成异二聚体,其中A亚基(CNA)是催化亚基,B亚基(CNB)是调节亚基。CNB作为该酶的调节亚基,能促进CNA的活性,且相对分子质量小、性质稳定。CN在免疫激活通路中发挥着重要作用,是T细胞活化的关键酶。重组人CNB(rhCNB)能刺激T细胞和自然杀伤(NK)细胞增殖、增强NK细胞的杀伤活性、增强巨噬细胞吞噬能力等,且对肝癌H22细胞有显著的抑制作用,是高效低毒的新型抗肿瘤生物药[1]。
酶联免疫吸附法(ELISA)是蛋白类生物技术药物常用的分析方法,具有操作简单、灵敏度高、特异性好、易于标准化等优点[2-4]。本文建立了测定大鼠血浆中rhCNB的ELISA双抗体夹心法,并对其药动学进行了研究,以期为评价rhCNB用于肝癌治疗的临床疗效提供检测方法。
1 材料
1.1 仪器
Tecan Sunrise酶标仪(奥地利Tecan有限公司);Centrifuge 5810高速离心机(德国Eppendorf公司)。
1.2 药品与试剂
rhCNB标准品(批号:20140807,纯度:>99%)和rhCNB单克隆抗体mAb(rhCNB mAb,批号:150310)均由海口奇力制药股份有限公司提供;抗rhCNB多克隆抗体pAb(rhCNB pAb,批号:BM1694)、辣根过氧化物酶(HRP)标记抗免疫球蛋白G (IgG)(批号:BA1058)、四甲基联苯胺(TMB)显色液(批号:P0209)均购自武汉博士德生物工程有限公司。
1.3 动物
SD大鼠6只,SPF级,♀♂各半,体质量为200~250 g,由湖南斯莱克景达实验动物有限公司提供,合格证号为SCXK(湘)2013-0004,饲养于海南医学院药物安全评价中心动物房。
2 方法与结果
2.1 血浆样品的处理
从大鼠眼眶静脉丛取血0.3 ml,置于1.5 ml肝素钠抗凝管内,静置1 h后,以3 000 r/min(离心半径为3 cm)离心20 min,分离后的血浆样品保存于-20 冰箱备用。
2.2 ELISA双抗体夹心法测定rhCNB浓度
将用pH9.6的0.05 mol/L碳酸盐缓冲液(CBS)稀释后的rhCNB mAb包板,4 过夜;次日弃孔内液,用PBST[含0.5 ml/L聚山梨酯20的0.02 mol/L磷酸盐缓冲液(PBS),pH 7.4]洗板3次,拍干;再用0.1%牛血清白蛋白(BSA)封闭,250µl/孔,37孵育2 h,洗板同上;然后向孔中分别加入待测样品,37 孵育1 h,洗板同上。待rhCNB mAb与抗体发生特异性结合后,再分别加入rhCNB pAb和HRP标记抗IgG,用TMB底物避光显色5~15 min,显色强度与rhCNB浓度成正比。终止反应后,通过酶标仪在450 nm波长处检测各孔吸光度(OD值)。℃℃℃℃
2.3 3种抗体最优加入量的筛选
采用棋盘滴定法将rhCNB mAb、rhCNB pAb和HRP标记抗IgG进行一系列稀释(rhCNB mAb质量浓度为10、1、0.1 µg/ml;rhCNB pAb稀释比例为1∶1 000、1∶2 000、1∶5 000;HRP标记抗IgG稀释比例为1∶2 000、1∶3 000、1∶10 000),以rhCNB标准品为待测样品,按“2.2”项下方法测定OD值,根据rhCNB标准品制备的标准曲线,用线性拟合方式计算各孔rhCNB的质量浓度[5-6]。结果,当rhCNB mAb为1µg/ml、rhCNB pAb稀释比例为1∶5 000、HRP标记抗IgG稀释比例为1∶10 000时,阳性对照(rhCNB标准品)平均OD值与阴性对照(不含rhCNB的样品稀释液)平均OD值之比(P/N值)最大,以此作为rhCNB mAb、rhCNB pAb和HRP标记抗IgG的最优加入量。
2.4 数据处理
用药动学软件BAPP 3.0进行线性拟合求回归方程,并绘制标准曲线。用Microsoft Excel 2007软件进行统计分析。
2.5 方法学评价
2.5.1 专属性考察 将1 mg/ml rhCNB标准品溶液进行倍比稀释,获得12.5、6.25、3.125、1.56、0.78、0.39、0.195 ng/ml的标准品溶液;再用大鼠空白血浆将1 mg/ml rhCNB标准品溶液稀释为12.5、6.25、3.125、1.56、0.78、0.39、0.195 ng/ml的含标准品血浆。取6个不同大鼠的空白血浆;再从6份大鼠空白血浆中取1 μl加入1.5 ml EP管中,加入999 μl样品稀释液(磷酸缓冲盐溶液,pH 7.4)配成1 ml空白血浆稀释液。按“2.2”项下方法,对rhCNB标准品溶液、含标准品血浆、空白血浆和空白血浆稀释液进行ELISA测定。结果,rhCNB标准品溶液与含标准品血浆的OD值接近,空白血浆与空白血浆稀释液的OD值接近,表明空白血浆和空白血浆稀释液均对rhCNB的测定无干扰,具体结果见表1。

表1 不同溶液的ELISA法检测结果(OD值)Tab 1 Detection results of different solutions by ELISA(OD value)
2.5.2 线性范围考察 按“2.5.1”项下方法,制备12.5、6.25、3.125、1.56、0.78、0.39、0.195 ng/ml的含标准品血浆,照“2.2”项下方法测定OD值。以rhCNB的质量浓度(x)为横坐标,以OD值(y)为纵坐标进行线性拟合,绘制标准曲线。得回归方程为y=8.88x+0.1(r2=0.995 0)。结果表明,rhCNB检测质量浓度的线性范围为0.195~12.5 ng/ml,符合试验要求。
2.5.3 定量下限考察 以空白血浆溶液重复测定16次,计算其均值和标准差,以与10倍标准差所对应的质量浓度为定量下限。结果显示,本方法的定量下限为0.195 ng/ml,符合验证要求。
2.5.4 准确度试验 按“2.5.1”项下方法,制备10、5、1 ng/ml的含标准品血浆,每个质量浓度制备6份,照“2.2”项下方法测定OD值,以测得值/加入量×100%计算准确度,结果见表2。
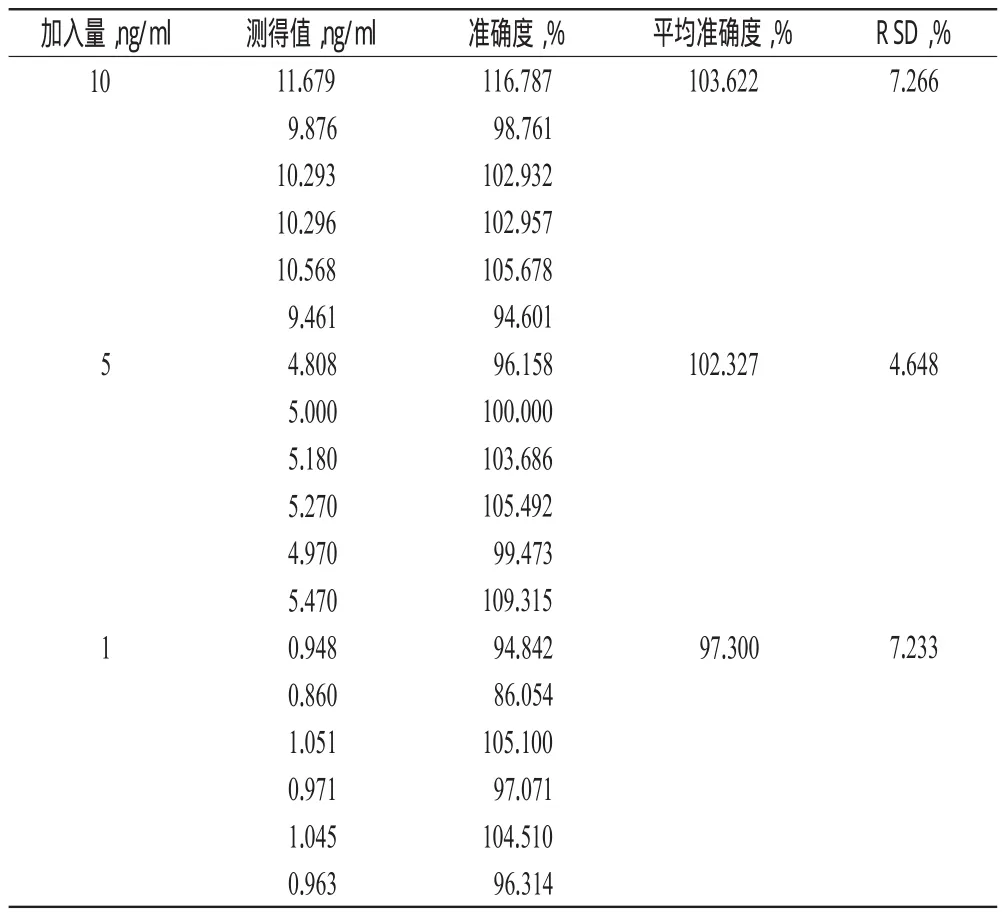
表2 准确度试验结果Tab 2 Results of accuracy test
2.5.5 精密度试验 按“2.5.1”项下方法,制备10、5、1 ng/ml的含标准品血浆,每个质量浓度制备6份,照“2.2”项下方法测定OD值,连续测定3 d,考察批内、批间精密度。结果显示,10、5、1 ng/ml的含标准品血浆的批内RSD分别为7.266%、4.629%、7.214%(n=6),批间RSD分别为5.7%、2.5%、4.6%(n=18)。
2.5.6 稳定性试验 按“2.5.1”项下方法,制备10、5、1 ng/ml的含标准品血浆,每个质量浓度制备5份,-20 下贮存,2~8 下缓慢融解,反复冻融3次后,照“2.2”项下方法测定OD值。结果显示,10、5、1 ng/ml的含标准品血浆OD值的RSD分别为2.9%、6.1%、8.5%(n=15),表明反复冻融3次不会影响rhCNB的稳定性。℃℃
2.6 药动学实验
取6只SD大鼠,iv 2.5 mg/kg rhCNB后分别于2、15、30、60、120、240、480、720 min尾静脉取0.1 ml全血,离心后分离血浆,4 保存,待测。按“2.1”项下方法处理后,照“2.2”项下方法测定OD值,代入回归方程计算血药浓度,绘制药-时曲线,℃结果见图1。

图1 大鼠体内rhCNB的药-时曲线Fig 1 The blood concentration-time curve of rhCNB in rats in vivo
结果表明,rhCNB在大鼠体内的药动学特征符合二室模型;以BAPP 3.0软件计算药动学参数,结果AUC0-720 min为173.038 mg·min/L、t1/2为94.62 min。
3 讨论
ELISA法是将酶催化的放大作用与特异性抗原抗体反应结合起来的一种微量分析技术,是高通量筛选和定量检测相结合的一种常用方法,适合于大批标本的检测,广泛应用于食品安全检测、医疗检测以及免疫实验分析等领域。其原理是利用抗原抗体特异性反应,检测灵敏度高达纳克甚至皮克级,具有特异性强、准确性高、操作简便、安全等优点[7-9]。但ELISA法也存在一定的局限性,如重复性较差、易受自身抗体或内源性酶等干扰。此外,影响因素多,尤其是温度和时间等,都会对检测结果带来一定的误差。因此,用ELISA法进行定量分析时对方法的灵敏度、线性范围、精密度与准确度、回收率等都有严格的行业标准。
本文建立了定量测定SD大鼠血浆中的rhCNB多肽的ELISA双抗体夹心法,以棋盘滴定法筛选出rhCNB mAb、rhCNB pAb和HRP标记抗IgG的最优加入量;以rhCNB mAb包被固相载体、抗原抗体特异性结合去除了杂蛋白的影响,提高了检测的特异性。rhCNB pAb能同时识别rhCNB的多个抗原表位,HRP酶标抗体又具有级联放大作用,因此提高了检测系统的灵敏度。本文结果表明,rhCNB mAb的最优质量浓度为1 µg/ml,rhCNB pAb和HRP标记抗IgG的最优稀释比例分别为1∶5 000、1∶10 000。方法学考察结果显示,本方法的特异性、准确度、精密度、线性范围、定量下限等均符合验证可接受标准,能够快速、灵敏、准确地对生物样品中的rhCNB进行定量检测。
[1]沈关心,周汝麟.现代免疫学实验技术[M].武汉:湖北科技出版社,2001:34-35.
[2]高锦,赵文军,王艳丽,等.注射用重组人钙调磷酸酶B亚基稳定性的初步研究[J].中国新药杂志,2008,17(8):675.
[3]杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008:142-167.
[4]中国生物制品标准化委员会.中国生物制品规程[M].2000年版.北京:化学工业出版社,2000:620-623.
[5] Savino E,Hu B,Sellers J,et al.Development of an inhouse,process-specific ELISA for detecting HCP in a therapeutic antibody:part 2[J].BioProcess International,2011,9(4):68.
[6]葛海良,张冬青.免疫学技术[M].北京:科学出版社,2009:66.
[7]Roda A,Guardigli M.Analytical chemiluminescence and bioluminescence:latest achievements and new horizons [J].Anal Bioanal Chem,2012,402(1):69.
[8]Dotsikas Y,Loukas YL.Improved performance of antigen-HRP conjugate-based immunoassays after the addition of anti-HRP antibody and application of a liposomal chemiluminescence marker[J].Anal Sci,2012,28(8):753.
[9]王春燕,纪松岗,陆世宁,等.酶放大免疫法与酶联免疫吸附法测定他克莫司血药浓度的对比研究[J].中国药房,2014,25(30):2 816.
Study on the ELISA Double-antibody Sandwich Method and Pharmacokinetics of Recombinant Human Calcineurin B Subunit in Rat Plasma
HAN Kesheng1,XIE Xueli2,TIAN Shuhong2,XING Guilan2,FU Jiang2,XING Jun2,LIN Chunhua2,TAN Peng2,SHAO Jiping2(1.Haikou Qili Pharmaceutical Co.,Ltd.,Haikou 570216,China;2.Key Laboratory of Preclinical Pharmacology and Toxicology of Hainan Province,Haikou 571199,China)
OBJECTIVE:To establish a method for determining recombinant human calmodulin B subunit(rhCNB)in rat plasma,and study its pharmacokinetics characteristics.METHODS:ELISA double-antibody sandwich method was adopted.1µg/ml rhCNB monoclonal antibody mAb was wrapped,added to the to-be-test sample,rhCNB polyclonal antibody pAb(dilution ratio of 1∶5 000)and HRP-labeled conjugate of anti-IgG(dilution ratio of 1∶10 000)were added.Using tetramethylbenzidine for developing,microplate reader was conducted in wavelength of 450 nm to determine the absorbance value(OD value)and plasma concentration of 6 rats after 2,15,30,60,120,240,480,720 min of iv 2.5 mg/kg rhCNB,and the pharmacokinetic parameters were calculated by BAPP 3.0 software.RESULTS:The linear range of rhCNB were 0.195-12.5 ng/ml(r2=0.995 0),lower limit of quantitation was 0.195 ng/ml,accuracy were 97.300%-103.622%(RSD<7.5%,n=6);RSDs of within-batch,inter-batch,freezing and thawing 3 times were no higher than 8.5%(n=6,18,15).rhCNB pharmacokinetics characteristics in rat fitted to two-compartment model,AUC0-720 minwas 173.038 mg·min/L and t1/2was 94.62 min.CONCLUSIONS:The established method has high specificity and sensitivity,good accuracy and precision,which can be used for rhCNB quantitative detection and pharmacokinetics study in biological samples.
rhCNB polypeptide;ELISA-antibody sandwich method;Rat;Quantitative detection;Pharmacokinetics
R927.2
A
1001-0408(2016)25-3468-03
10.6039/j.issn.1001-0408.2016.25.04
2016-01-11
2016-04-22)
(编辑:邹丽娟)
国家自然科学基金资助项目(No.81160408)
*工程师。研究方向:药物分析。电话:0898-66804181。E-mail:hanksh168@126.com
副教授,博士。研究方向:药物安全性评价。电话:0898-66961101。E-mail:jpshaosl@163.com
