铁掺杂二氧化钛空心球的制备及性能
2016-10-25李雅泊郑玉婴刘阳龙
李雅泊,郑玉婴,刘阳龙
铁掺杂二氧化钛空心球的制备及性能
李雅泊1,郑玉婴1,刘阳龙2
(1福州大学材料科学与工程学院,福建福州 350108;2福州大学石油化工学院,福建福州 350108)
以TiF4为钛源、九水合硝酸铁为掺杂前体,采用水热法制备铁掺杂的TiO2空心微球。采用SEM、TEM、XRD、BET、XPS等技术对样品的形貌、结构、晶型、比表面积、元素组成等进行表征,以亚甲基蓝(MB)的光催化降解为目标反应,评价其光催化活性。结果表明,160℃下水热反应生成的纳米TiO2空心微球晶型为锐钛矿,少量掺铁并不影响微球的形貌及晶体结构。光催化实验表明,160℃下水热反应12 h生成的TiO2空心微球样品均匀性好、光催化活性最佳;铁掺杂能显著提高TiO2空心微球的催化活性,当铁钛比为1.5:100时,所得样品粒径最小,比表面积最大,光催化活性最高。
氟化钛;二氧化钛;水热法;铁掺杂;光催化;空心微球
引 言
TiO2光催化剂因其具有催化活性高、化学稳定性好、无毒无害、价格低廉等优点,目前已广泛应用于能量储存器、传感器、环境污染治理等各种领域[1-4]。然而其带隙较宽(约为3.2 eV),光生电子与空穴复合率较高,光量子使用率较低,导致光催化效率不高,大大限制了其应用范围[5]。为了提高TiO2的光催化效率,学者们尝试了多种改性方法,如表面染料敏化、金属掺杂、非金属掺杂及半导体复合等[6-9]。
其中过渡金属掺杂是有效改性手段之一。过渡金属具有未填满的d电子壳层,在TiO2晶格中掺入少量过渡金属离子,可以引起晶格畸变产生缺陷,成为光生电子或空穴的浅势捕获陷阱,延长电子与空穴的复合时间,降低光生电子-空穴复合概率,可以有效地提高TiO2光催化效率[10-11]。Fe(Ⅲ)被认为是改善TiO2光催化性能的有效掺杂离子,如杨秋文等[12]以十八烷胺为模板,将钛酸丁酯水解后煅烧清除模板剂制备出Fe(Ⅲ)掺杂的TiO2介孔材料,其对甲基橙的降解速率明显高于未掺杂的TiO2;高远等[13]采用溶胶-凝胶法制备了铁掺杂纳米TiO2粉末,当掺杂量为3.0%时对的光催化降解效率最高;Li等[14]采用水热法合成了Fe(Ⅲ)掺杂的TiO2纳米线,并将此纳米线包覆于氧化石墨烯表面形成石墨烯/Fe-TiO2复合材料,其对亚甲基蓝的催化降解反应速率大大提高。
研究表明,TiO2的形貌对其光催化性能也有较大影响,其中提高TiO2的比表面积可以提供更多的光催化活性点,诸如TiO2纳米管、纳米棒、纳米空心球等各种形貌的TiO2应运而生[15-17]。其中空心结构材料具有低密度、高比表面积等优点,应用前景广阔。钟永辉等[18]采用溶剂热法合成了氟改性的TiO2空心微球,光催化效率得到很大提高;Xu等[19]以碳球为模板,通过水热处理制备了B掺杂的TiO2空心球,在可见光照射下降解活性红染料X-3B的催化性能比商用P25二氧化钛高出很多倍。
本文以TiF4为钛源、九水合硝酸铁为掺杂前体,采用水热法一步制备Fe-TiO2纳米空心球,与以往众多文献[20-22]不同的是,本文重点研究不同温度对TiO2晶型、形貌以及不同掺铁量对催化活性的影响。
1 实验材料和方法
1.1 材料
四氟化钛(TiF4);盐酸(HCl);氨水(NH3·H2O);九水合硝酸铁(Fe(NO3)3·9H2O);无水乙醇(CH3CH2OH),国药集团化学试剂有限公司,AR;去离子水。
1.2 实验过程
四氟化钛溶液不稳定,为了防止其水解,用1.5 mol·L-1的氨水(NH3·H2O)和1.5 mol·L-1的盐酸(HCl)配制200 ml pH2.1的溶液作为缓冲液。称取0.991g四氟化钛(TiF4)溶于上述溶液,形成0.04 mol·L-1的四氟化钛溶液,调节溶液pH至 1.8。此时溶液透明、稳定,可较长时间存放。
用去离子水将上述四氟化钛(TiF4)溶液稀释至0.002 mol·L-1后取70 ml于内衬聚四氟乙烯的高压反应釜中,在温度为100~200℃的鼓风干燥箱中恒温反应2~24 h,通过SEM图片分析,得出水热反应的最佳反应温度及反应时间。
在最佳反应条件下,用上述四氟化钛(TiF4)溶液及九水合硝酸铁(Fe(NO3)3·9H2O)溶液按照Fe:Ti原子比分别为0.5:100、1:100、1.5:100、2.5:100配制铁掺杂的四氟化钛(TiF4)溶液并分别记为Fe-0.5、Fe-1.0、Fe-1.5、Fe-2.5,将混合溶液转入内衬聚四氟乙烯的高压反应釜中并加去离子水至70 ml,在160℃下反应12 h,离心,用去离子水、无水乙醇分别冲洗3次,烘干。
1.3 样品表征
采用日产JEM-2100F型透射电子显微镜(TEM)和德国蔡司型场发射扫描电子显微镜(FE-SEM,Supra-55)观察微球的形貌和尺寸。X射线衍射源为铜靶,狭缝宽度为0.3 nm,工作管电压40 kV,工作管电流100 mA,量程为1000 cps,扫描范围2为10°~80°,扫描速率为5(°)·min-1。在ESCALAB-250型能谱仪上测试X射线光电子能谱(XPS)。在美国麦克仪器公司比表面积与孔径分析仪(ASAP2020)上测定样品的比表面积,测试前待测样品放置在300℃脱气3 h,样品的比表面积由BET法算得。在光催化反应仪上进行光催化降解亚甲基蓝实验,以500 W的紫外灯为光源,吸光度测试采用日本岛津UV-1800型紫外可见分光光 度计。
1.4 光催化实验
可见光催化实验通过降解甲基蓝(MB)来实现,反应在上海比朗BL-GHX-V型光催化反应仪中进行,光源为500 W氙灯。称取0.1 g自制样品分散于浓度为1.8×10-5mol·L-1的100 ml亚甲基蓝溶液中,置于光催化反应仪内,电磁搅拌0.5 h以达到吸附平衡后打开氙灯,每隔10 min取5 ml的亚甲基蓝溶液,离心分离取上层清液测定亚甲基蓝溶液的吸光度。在实验浓度范围内,亚甲基蓝溶液的吸光度与浓度呈正比,以吸光度代替浓度计算催化效率,即,式中,、、和分别表示降解后浓度、初始浓度、降解后的吸光度和初始吸光度。
2 实验结果与讨论
2.1 形貌分析
图1(a)~(d)分别是TiF4溶液在120、140、160、180℃下恒温水热反应12 h所得TiO2微球的SEM照片。由图可知,反应温度对晶体的形貌影响较大。当反应温度较低时,所得样品尚未完全定型;当温度升高至160℃时,样品逐渐转化为形貌完整、大小均一的小球,继续升高水热反应温度后得到的样品呈块状,由图可知样品团聚较为严重,粒径也比较大,不利于催化反应的进行[23]。从图2可以看出,催化活性顺序为160℃>180℃>140℃>120℃,因此160℃为实验研究条件下TiF4水热反应生成TiO2的最佳温度。

图1 不同水热反应温度制备的TiO2微球的SEM照片
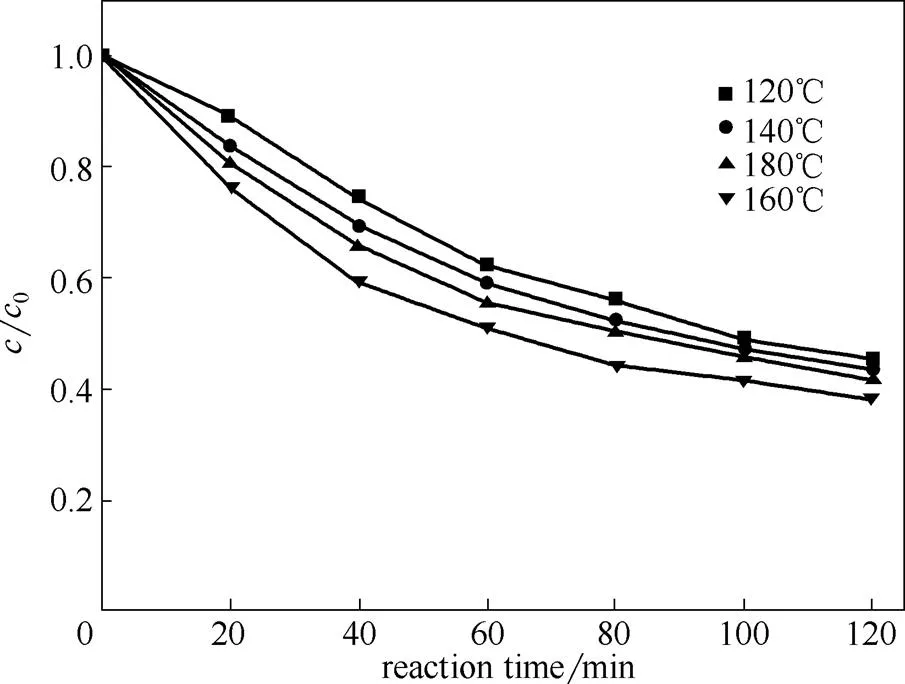
图2 不同水热反应温度制备的TiO2对亚甲基蓝的光催化降解曲线
图3(a)~(d)分别是TiF4在160℃下恒温水热反应2、6、12、18 h所得TiO2微球的SEM照片,由图可以看出,如果反应时间较短,TiF4在反应釜内反应不够充分,得到无规则性样品,随着反应时间的增加,TiO2逐渐转化为较规则的球形结构,符合奥斯特瓦尔德熟化机理[24-25],但反应时间太长会导致微球变大,不利于光催化反应的进行,因此12 h为TiF4水热反应生成TiO2纳米空心微球最佳反应时间。在水热反应条件下,由于氟盐前体的水解反应,许多小金属氧化物微晶成核并迅速集结成球形骨料以降低其表面能。由奥斯特瓦尔德熟化机理可知,晶粒的增长和再结晶过程中内部微晶由于高表面能而溶解并转移出来,形成的通道可以连接内部空间和外部空间来进行物质转移,因而形成空心球体结构。图3(e)是TiF4在160℃下恒温水热反应12 h所得TiO2微球的TEM照片,图3(f)是相同条件下制得的Fe-1.5样品的TEM照片,由图可知,所得微球是太阳花状的空心球,铁的掺入并不影响空心微球的形貌,微球直径约为500 nm。

图3 不同水热反应时间制备的Fe-TiO2微球的SEM和TEM照片
2.2 XRD分析
图4中为160℃下制得的Fe-0(不掺杂Fe)、Fe-0.5、Fe-1.0、Fe-1.5、Fe-2.5的TiO2微球的XRD衍射谱图。由图可知,在衍射角2为25.30o、37.80o、47.60o、54.10o、69.01o、75.50o附近出现了衍射峰,说明所制得的样品晶型均为锐钛矿型,同时说明少量掺杂Fe3+并不影响TiO2的晶型[26-28]。根据衍射峰的宽化程度,用Scherer公式计算所有样品粒径于表1中,比较发现,适量掺入Fe3+可以明显抑制空心微球的生长,这可能是由于Fe3+与Ti4+粒径相近,比较容易进入晶格取代Ti4+或进入晶格间隙,抑制了TiO2晶体的团聚,使得生成的TiO2空心微球粒径较小[29-31]。
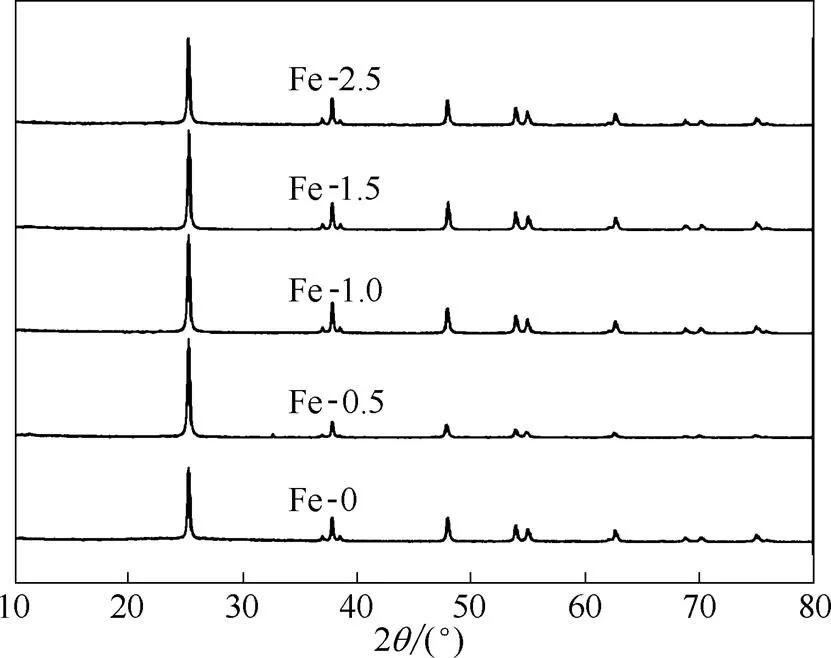
图4 不同铁钛比的Fe-TiO2微球的XRD谱图
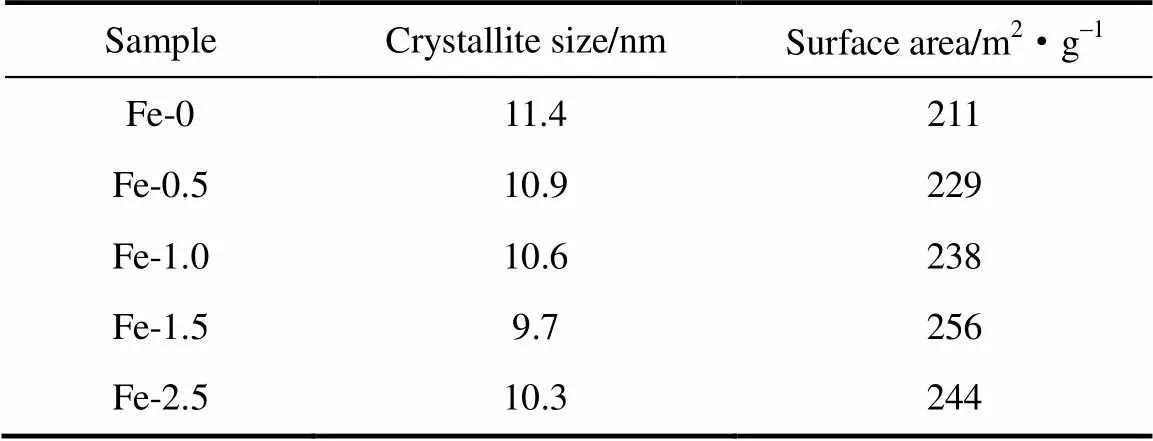
表1 样品的粒径和比表面积
2.3 XPS分析
图5为Fe-1.5的样品的XPS谱图。由图5(a)可见,除C、O、Ti、Fe等元素特征能谱峰外,无其他元素能谱峰,表明样品有较高的纯度,其中C元素主要来源于测试过程中XPS仪器本身的油污染或样品煅烧后残留的碳。图5(b)显示Ti 2p3/2和Ti 2p1/2峰分别出现在458.35和464.15 eV左右(略大于Ti的标准XPS谱图453.9和460.0),说明Ti元素主要以四价形态存在[32],铁的掺入改变了Ti4+周围的电子云密度导致钛的电子结合能增大。图5(d)为铁的2p轨道结合能,结合能为709.70 eV,略大于标准数据中的Fe 2p(706.7 eV)的电子结合能,说明Fe3+的微区环境发生了变化,可能是形成了TiOFe键,导致TiO2晶格变形[33]。同时根据XPS的定量分析结果可得,当Fe、Ti和O元素的原子个数比近似为1.5:100:200,说明样品的纯度较高,掺杂效果较好。
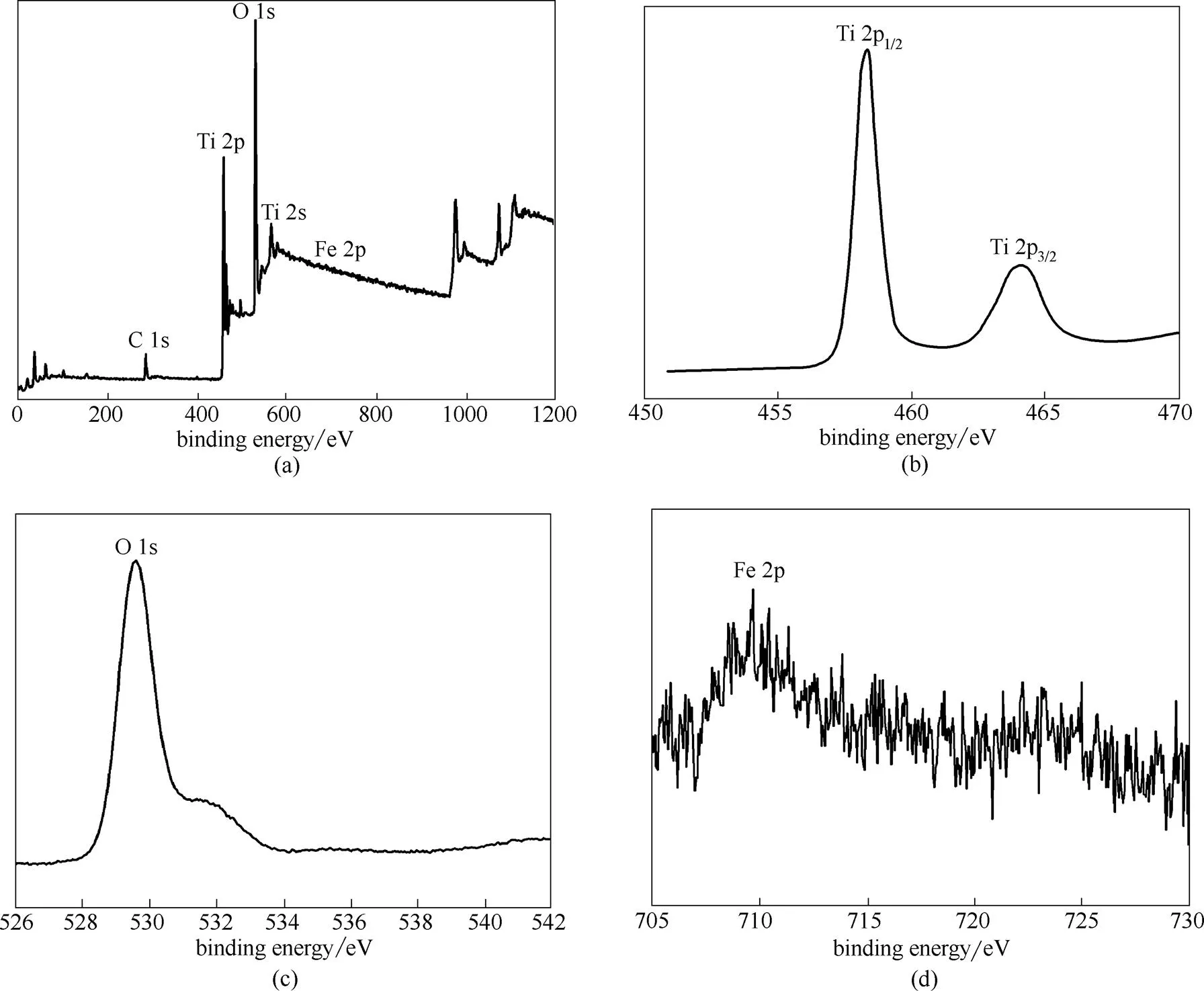
图5 铁钛比为1.5:100的Fe-TiO2微球的XPS能谱图
2.4 BET分析
图6是不同掺铁量的TiO2空心微球样品的N2吸附-脱附等温线。结果显示,这些样品的等温线形状相似,均属于Ⅳ型,曲线上有一个滞后环,是典型的介孔结构吸附-脱附等温线。吸附曲线的起始部分对应于在较低的相对压力下介孔表面的单层吸附,在相对压力较高时产生的突跃是由于介孔内的氮气冷凝造成的。这是由于毛细管凝聚作用使N2分子在低于常压下冷凝,产生了滞后效应,从而导致吸附曲线和脱附曲线不重合。计算各个样品的比表面积列于表1中,可知当Fe和Ti的掺杂比为1.5:100时,样品的比表面积最大。
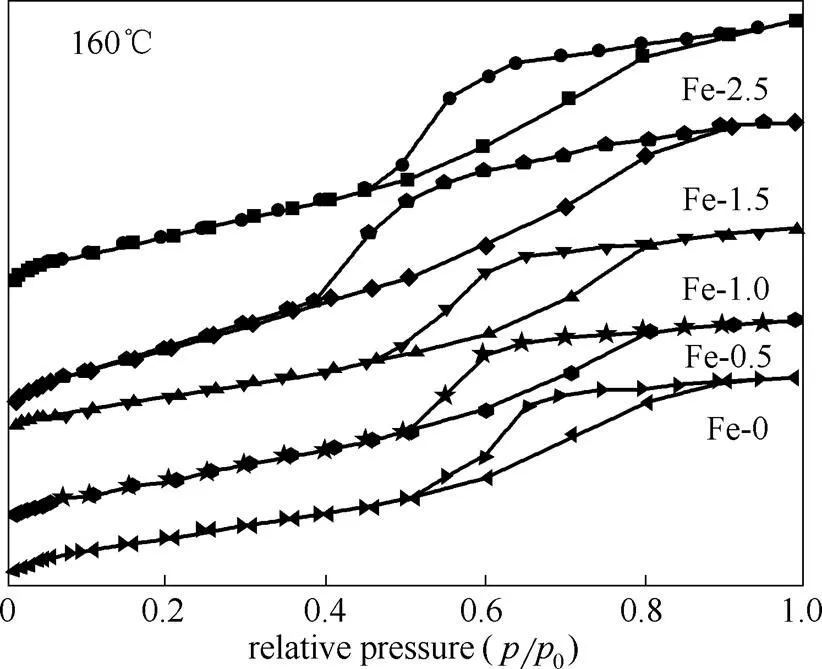
图6 不同铁钛比的Fe-TiO2微球的N2吸附-脱附等温线
2.5 光催化分析
图7是不同掺铁量的TiO2对亚甲基蓝的降解活性比较。从图7可以看出,催化活性顺序为Fe-1.5>Fe-1.0>Fe-2.5>Fe-0.5>Fe-0,说明掺杂适量的Fe3+,可以显著地提高材料的光催化活性。Fe3+与Ti4+的半径相当而且Fe3+/Fe2+的能级与TiO2的导带比较接近,因而在进行离子掺杂时铁离子比较容易进入到TiO2晶格中,同时Fe3+作为过渡原子而具有的未填满的d电子壳层也有利于半导体光生电子的浅度捕获。这种浅度捕获有利于光生电子-空穴对的快速移动并且有效分离.从而会提高光催化活性。当Fe和Ti的掺杂比为1.5:100时,TiO2的催化活性最高,进一步增加掺杂量,催化活性反而降低,可能是因为过多的掺杂会导致Fe3+成为简洁的光致电子和空穴的复合中心,反而使其催化活性降低[34]。
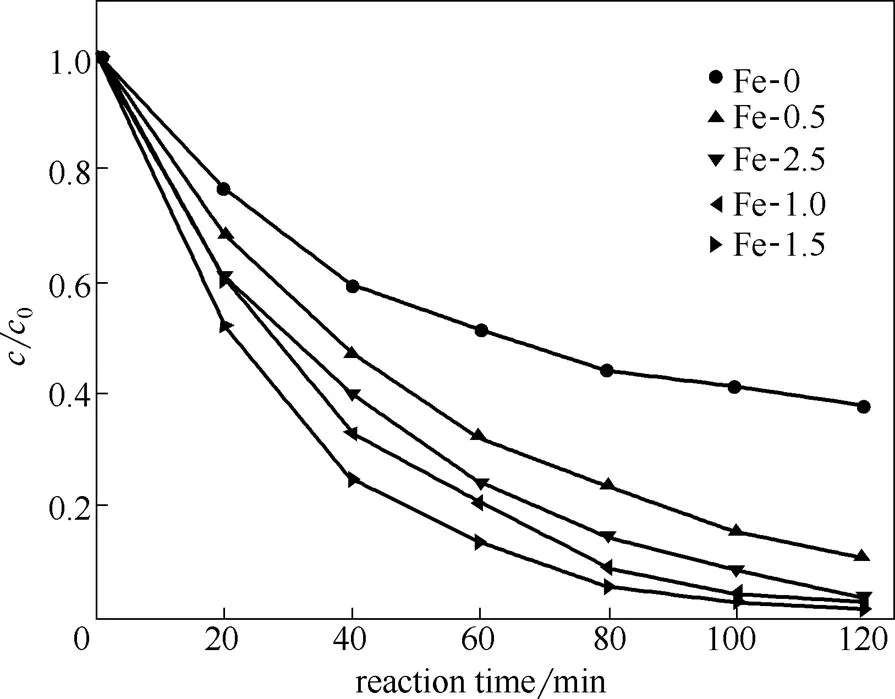
图7 不同铁钛比的Fe-TiO2微球对亚甲基蓝的光催化降解曲线
3 结 论
(1)以氟化钛为钛源,水为溶剂,在不同温度下通过水热法一步合成二氧化钛空心微球。结果表明,在160℃下恒温反应12 h时可得形貌完整、大小均一的小球,此时样品的光催化活性最高。
(2)通过水热法一步合成铁掺杂的空心二氧化钛微球,实验结果表明,所得样品的比表面积随铁含量的增加先增大后减小,样品粒径随掺铁量的增大先减小后增大。
(3)适量的铁掺杂能提高二氧化钛的催化活性,二氧化钛的光催化活性随铁掺杂量的增加先增大后减小,当Fe和Ti的掺杂比为1.5:100时,光催化效果最佳,这是因为Fe3+比较容易进入TiO2晶格中,从而有效地提高电子和空穴的分离效率,而且Fe3+的掺入可以形成TiOFe键导致TiO2晶格变形而更容易产生电子-空穴对,从而提高了光催化效率。
References
[1] ZHANG Q H, FAN W G, GAO L. Anatase TiO2nanoparticles immobilized on ZnO tetrapods as a highly efficient and easily recyclable photocatalyst [J]. Applied Catalysis B: Environmental, 2007, 76 (12): 168-173.
[2] 陈建新, 张娜, 李银辉, 等. 氮掺杂TiO2/壳聚糖复合膜吸附和光降解染料 [J]. 化工学报, 2015, 66 (9): 3746-3752. CHEN J X, ZHANG N, LI Y H,. Adsorption and photocatalytic degradation of dye by N-doped TiO2/chitosan composited films [J]. CIESC Journal, 2015, 66 (9): 3746-3752.
[3] ZHAO D L, SHENG G D, CHEN C L,. Enhanced photocatalytic degradation of methylene blue under visible irradiation on graphene@TiO2dyade structure [J]. Applied Catalysis B: Environmental, 2012, 111/112: 303-308.
[4] LIAO Y C, XIE C S, LIU Y,, Comparison on photocatalytic degradation of gaseous formaldehyde by TiO2, ZnO and their composite [J]. Ceramics International, 2012, 6 (38): 4437-4444.
[5] SUN B, VORONTSOV A V, SMIRNIOTIS P G. Role of platinum deposited on TiO2in phenol photocatalytic oxidation [J]. Langmuir, 2003, 19 (8): 3151-3156.
[6] MONA S, ABDEL M. Titanium dioxide nanomaterial doped with trivalent lanthanide ions of Tb, Eu and Sm: preparation, characterization and potential applications [J]. Inorganica Chimica Acta, 2007, 360 (9): 2863-2874.
[7] KARTHIK K, VICTOR J N. High pressure electrical resistivity studies on Ni-doped TiO2nanoparticles [J]. Journal of Alloys and Compounds, 2011, 509 (16): 5173-5176.
[8] AO Y H, XU J J, FU D G,. A simple method to prepare N-doped titania hollow spheres with high photocatalytic activity under visible light [J]. Journal of Hazardous Materials, 2009, 167: 413-417.
[9] WEI F Y, ZENG H L, SHI L,. Effect of sulphur and iron co-doping on photocatalytic activity of titanium dioxide [J]. Journal of the Chinese Ceramic Society, 2008, 36 (9): 1272-1276.
[10] RANJIT K T, WILLNER I, BOSSMANN S H,. Lanthanide oxide doped titanium dioxide photocatalysts: effective photocatalysts for the enhanced degradation of salicylic acid and t-cinnamic acid [J]. Journal of Catalysis, 2001, 204 (2): 305-310.
[11] BAE E, CHOI W. Highly enhanced photoreductive degradation of perchlorinated compounds on dye-sensitized metal/TiO2under visible light [J]. Environmental Science and Technology, 2003, 37 (1): 147-152.
[12] 杨秋文, 刘素琴, 黄可龙, 等. Fe(Ⅲ)掺杂介孔TiO2的溶剂热法合成与表征 [J]. 湘潭大学自然科学学报, 2009, 31 (1): 71-76. YANG Q W, LIU S Q, HUANG K L,. Solvothermal fabrication and characterization of iron doped mesoporous TiO2[J]. Natural Science Journal of Xiangtan University, 2009, 31 (1): 71-76.
[13] 高远, 徐安武, 刘汉钦. 掺铁TiO2用于光催化降解研究 [J]. 中山大学学报, 2000, 30 (5): 1-5. GAO Y, XU A W, LIU H Q. The photocatalysis of iron doped TiO2used in the degradation of[J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2000, 30 (5): 1-5.
[14] LI W Q, LIU X, LI H X. Hydrothermal synthesis of graphene/Fe3+-doped TiO2nanowire composites with highly enhanced photocatalytic activity under visible light irradiation [J]. Journal of Materials Chemistry A, 2015, 3:15214-15223.
[15] LI G C, ZHANG Z K. Preparation and characterization of hollow titania microspheres [J]. Journal of Functional Materials Contents, 2004, 35 (1): 2786-2791.
[16] SYOUFIAN A, NAKASHIMA K. Degradation of methylene blue in aqueous dispersion of hollow titania photocatalyst: optimization of reaction by peroxydisulfate electron scavenger [J]. Journal of Colloid and Interface Science, 2007, 313 (1): 213-218.
[17] LIANG Y C, WANG C C, KEI C C,. Photocatalysis of Ag-loaded TiO2nanotube arrays formed by atomic layer deposition [J]. The Journal of Physical Chemistry C, 2011, 115 (19): 9498-9502.
[18] 钟永辉, 周琪, 刘家琴, 等. 氟化改性TiO2空心微球的制备及光催化性能 [J].无机化学学报, 2013, 29 (10): 2133-2139. ZHONG Y H, ZHOU Q, LIU J Q,. Preparation of fluorizated TiO2hollow microspheres and their photocatalytic activity [J]. Chinese Journal of Inorganic Chemistry, 2013, 29 (10): 2133-2139.
[19] XU J J, Ao Y H, Chen M D. Preparation of B-doped titania hollow sphere and its photocatalytic activity under visible light [J]. Materials Letters, 2009, 28 (63): 2442-2444.
[20] JAE H J, DONG H K, SUN J K,. Synthesis and photocatalytic property of a mixture of anatase and rutile TiO2doped with Fe by mechanical alloying process [J]. Journal of Alloys and Compounds, 2008, 459: 386-389.
[21] LIN F, JIANG D M, LIN Y,. Magnetism of Fe-doped TiO2milled in different milling atmospheres [J]. Physica B, 2008, 403: 2193-2196.
[22] YANG P, LU C, HUA N P,. Titanium dioxide nanoparticles co-doped with Fe3+and Eu3+ions for photocatalysis [J]. Materials Letters, 2002, 57 (4): 794-801.
[23] TU Y F, HUANG S Y, SANG J P,. Preparation of Fe-doped TiO2nanotube arrays and their photocatalytic activities under visible light [J]. Materials Research Bulletin, 2010, 45: 224-229.
[24] LI J, ZENG C H. Hollowing Sn-doped TiO2nanospheresOstwald ripening [J]. American Chemical Society, 2007, 129 (51): 15839-15847.
[25] YANG H G, ZENG H C. Preparation of hollow anatase TiO2nanospheresOstwald ripening [J]. The Journal of Physical Chemistry B, 2004, 11 (108): 3492-3495.
[26] REGINLDO S S, GUILHERME A F, CARLOS G,. Iron insertion and hematite segregation on Fe-doped TiO2nanoparticles obtained from sol-gel and hydrothermal methods [J]. Applied Materials, 2012, 4: 5555-5561.
[27] DONG H K, HYUN S H, SUN J K,. Photocatalytic behaviors and structural characterization of nanocrystalline Fe-doped TiO2synthesized by mechanical alloying [J]. Journal of Alloys and Compounds, 2004, 375: 259-264.
[28] NASRALLA N, YEGANEH M, ASTUTI Y,. Structural and spectroscopic study of Fe-doped TiO2nanoparticles prepared by sol-gel method [J]. Scientia Iranica, 2013, 20: 1018-1022.
[29] MOHAMED S H, EIHAGARY M, ALTHOYAIB S. Growth of undoped and Fe doped TiO2nanostructures and their optical and photocatalytic properties [J]. Applied Physics A, 2013, 111: 1207-1212.
[30] KITIROTE W, LAKSANA L, PONGTANAWAT K,. Calcination temperature effect on solvothermal Fe-TiO2and its performance under visible light irradiation [J]. Journal of the Taiwan Institute of Chemical Engineers, 2010, 41: 612-616.
[31] VIJAYALASHMI K, JEREIL S D. Influence of Fe catalytic doping on the properties of TiO2nanoparticles synthesized by microwave method [J]. Materials in Electronics, 2014, 25: 5089-5094.
[32] WU Q P, ZHENG Q, Roel K. Creating oxygen vacancies as a novel strategy to form tetrahedrally coordinated Ti4+in Fe/TiO2nanoparticles [J]. The Journal of Physical Chemistry, 2012, 116: 7219-7226.
[33] Zoltan A, Nandor B, Tunde A. Synthesis, structure and photocatalytic properties of Fe(III)-doped TiO2prepared from TiCl3[J]. Applied Catalysis B: Environmental, 2008, 81: 27-37.
[34] ZHU J, REN J, HUO Y N,. Nanocrystalline Fe/TiO2visible photocatalyst with a mesoporous structure prepareda nonhydrolytic sol-gel route [J]. The Journal of Chemical Physics, 2007, 111: 18965-18969.
Preparation and properties of iron doped TiO2hollow microspheres
LI Yabo1, ZHENG Yuying1, LIU Yanglong2
(1College of Materials Science and Engineering, Fuzhou University, Fuzhou 350108, Fujian, China;2School of Chemical Engineering, Fuzhou University, Fuzhou 350108, Fujian, China)
Iron-doped titanium dioxide hollow microspheres were prepared hydrothermally using titanium tetrafluoride and ferric nitrate nonahydrate in aqueous solution as starting materials, and were characterized by scanning electron microscopy (SEM), transmission electron microscopy (TEM), X-ray diffraction (XRD),surface area (BET) and X-ray photoelectron spectroscopy (XPS). Photocatalytic activity of the microspheres was evaluated on photocatalytic degradation of aqueous methylene blue (MB). TiO2in hollow microspheres created at 160℃ were anatase crystal and doping a relatively small amount of iron did not alter morphology and crystal structure of TiO2. Iron doping could significantly improve the photocatalytic activity of TiO2hollow microspheres. The TiO2hollow microspheres obtained at a condition of 160℃ for 12 h had optimal dimensional uniformity and photocatalytic activity, which the best photocatalytic effect were observed on hollow microspheres with a 1.5% ratio of iron over titanium because of the smallest size and the highest surface area.
TiF4; TiO2; hydrothermal method; iron doping; photocatalytic; hollow microspheres
2016-04-07.
Prof. ZHENG Yuying, yyzheng@fzu.edu.cn
10.11949/j.issn.0438-1157.20160443
TQ 032
A
0438—1157(2016)10—4493—07
福建省科技厅引导性项目(2015H0016)。
2016-04-07收到初稿,2016-06-06收到修改稿。
联系人:郑玉婴。第一作者:李雅泊(1990—),男,硕士研究生。
supported by the Science and Technology Department of Fujian Province (2015H0016).
