环糊精聚氨酯磁性吸附剂制备、表征及对柯里拉京的吸附
2016-10-25赵珺闵书学林集端陈国王晓琴
赵珺,闵书学,林集端,陈国,王晓琴
环糊精聚氨酯磁性吸附剂制备、表征及对柯里拉京的吸附
赵珺1,2,闵书学1,林集端1,陈国1,王晓琴1,2
(1华侨大学化工学院,福建厦门 361021;2华侨大学油脂及天然产物研究所,福建厦门 361021)
以环糊精聚氨酯-CDPU包覆Fe3O4磁核及SiO2/Fe3O4复合粒子,制备出两种磁性吸附剂-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)。考察了吸附剂对多酚类天然产物柯里拉京的吸附,并结合磁分离技术,从珠子草粗提液中直接富集柯里拉京。采用FTIR、XRD、SEM及热重分析法对两种磁性吸附剂进行了结构表征,表明两种吸附剂中聚合物含量分别为41.5%和36.5%,-CDPU的包覆未改变Fe3O4的晶型。吸附机理研究表明,二者对柯里拉京的吸附均符合Langmuir型等温线,但Fe3O4磁核对柯里拉京具有特殊的相互作用,造成柯里拉京洗脱困难,总洗脱率和回收率仅17.0%和10.5%。而磁核经SiO2修饰后,可以阻碍Fe3O4对柯里拉京的接触,提高柯里拉京的洗脱率(41.0%)和回收率(22.8%),实现珠子草中柯里拉京的初步富集。
环糊精聚氨酯;磁性;吸附剂;柯里拉京;珠子草;吸附;分离
引 言
磁性吸附剂兼具吸附性能和磁响应性,是近年来发展起来的一类新型功能材料。磁性吸附剂内部含有磁核,可在外加磁场的作用下方便地被定位、导向和分离,且磁核经过表面衍生化修饰,偶联功能基团后,可以专一性地识别某种类型的分子[1]。在生化及天然产物的分离分析领域,磁性吸附剂操作过程简便,分离效率优于常规分离方法,因此得到重要的应用[2-4]。
在磁核表面连接或修饰环糊精(cyclodextrin,CD)或CD聚合物可以得到功能化的磁性吸附剂[5]。CD具有独特的疏水性空腔结构,能与多种客体分子通过氢键、疏水作用等次级键形成包结复合物[6-7]。CD的包结作用与磁核的磁响应特征相结合,可以实现对客体分子的快速分离或检测[8-9]。然而由于CD分子本身基团的单一性,与客体分子的识别位点有限,识别和包结能力相对较弱,故CD修饰的磁性吸附剂用于分离领域的报道较少。鉴于此,有必要在CD分子周围引入其他功能性基团以增强CD磁性吸附剂的吸附能力。
环糊精聚氨酯(cyclodextrin polyurethane,CDPU)负载的磁性吸附剂是一种重要的功能材料,它是在CD与二异氰酸酯交联的过程中加入磁性粒子共混分散而制得[10-11]。Wilson等[12]认为CDPU中的CD空腔和氨基甲酸酯是两种类型的吸附位点,即CDPU的结构中CD的疏水空腔可对芳香族化合物的芳环基团以疏水作用进行包结复合,而聚合物骨架中引入了氨基甲酸酯基团,其亚氨基¾N¾H能与含活泼氢的极性基团(尤其是酚羟基)之间形成氢键而定位在聚氨酯骨架附近[13]。这两种吸附位点在酚类化合物的吸附过程中均起作用,形成双位点吸附效应。因此CDPU对酚类化合物具有特殊的吸附能力,目前在含酚废水的处理方面得到较广泛的应用[14-15]。
CDPU的双位点吸附特性亦使其成为多酚类天然产物富集分离的备选吸附剂,然而这方面的研究报道较少。本课题组[15]曾以球形-CDPU树脂为吸附剂,填充在固定床中,对珠子草(L.)粗提液中的柯里拉京(corilagin)进行富集和初步纯化,其中20%(质量)乙醇洗脱液中柯里拉京含量达到64.8%,收率为49.4%,实现了柯里拉京的有效富集。柯里拉京是一种含没食子酸酯结构的多酚糖苷类化合物,主要来源于叶下珠、蜜柑草、老鹳草、余甘子、龙眼等植物,分子结构如图1所示[16]。柯里拉京具有抗肿瘤、抗氧化、抗炎以及保护心血管系统等作用,近年来受到国内外研究者的广泛关注[17]。尤其在治疗恶性肿瘤方面,柯里拉京已显示出对于肝脏肿瘤细胞增殖的强烈抑制作用[18],有望成为肝癌治疗药物。目前柯里拉京主要从植物中提取而得[19-21]。但由于植物中含量低,导致其分离路线长,过程烦琐耗时,且需消耗大量的有机溶剂。因此,寻找快速而高效的富集分离手段,对柯里拉京的制备及临床应用将产生极大的推动。球形-CDPU树脂在固定床中对柯里拉京进行富集,耗时长,效率较低。本文引入磁分离技术,将-CDPU包覆Fe3O4磁核及SiO2/Fe3O4复合粒子,制备磁性吸附剂,利用CD分子的包结效应和Fe3O4的磁响应特征,对柯里拉京的分离做新的尝试,以期简化柯里拉京的富集分离过程,并对柯里拉京在吸附剂上的吸附机理和洗脱特性进行探讨。
1 实验材料和方法
1.1 材料
珠子草(L.)采自厦门鼓浪屿华侨亚热带植物引种园,并经福建省亚热带植物研究所鉴定。全草洗净、风干,粉碎至0.25~0.60 mm,密封,置于4℃冰箱中冷藏待用。
-CD(DRAMAX®W7 Pharma,≥98%,广州泰龙生化有限公司);柯里拉京(≥98%,上海鼎杰生物技术有限公司);异氰酸丙基三乙氧基硅烷(IPTS,95%)、六水氯化铁(FeCl3·6H2O)、四水氯化亚铁(FeCl2·4H2O)(上海晶纯生化科技股份有限公司);1,6-六亚甲基二异氰酸酯(HDI)(成都格雷西亚化学技术有限公司);氨水、无水乙醇、丙酮、正硅酸四乙酯(TEOS)(汕头市西陇化工股份有限公司);二甲基亚砜(DMSO)、磷酸(国药集团上海化学试剂有限公司)。以上试剂均为分析纯。甲醇(色谱纯)、乙腈(色谱纯)(美国Tedia公司)。实验用水均为去离子水。
1.2 分析测试仪器及方法
傅里叶变换红外光谱(FTIR)表征:FTIR-8400S傅里叶变换红外光谱仪(日本Shimadzu公司),KBr压片法制样,扫描范围4000~400 cm-1,分辨率1 cm-1,采样10次后取平均值。
扫描电镜(SEM)表征:JSM-7001F热场发射扫描电子显微镜(日本电子株式会社),加速电压10 kV,电流0.05 mA,未进行镀金处理。表面能谱分析电压15 kV,脉冲2 kcps。
热重(TGA)和差热(DTA)分析:DTG-60H热重分析仪(日本Shimadzu公司),载气N2流量50 ml·min-1,升温范围30~600℃,升温速率10℃·min-1。
X射线粉末衍射(XRD)表征:RIGAKU Smartlab X射线粉末衍射仪(日本理学株式会社),发射源Cu-Ka(= 0.154 nm,40 kV,100 mA),石墨单色器。室温下测试。样品测试范围(2):5°~80°,扫描速率0.5(°)·s-1。
1.3 Fe3O4磁核的制备
采用共沉淀法制备Fe3O4磁核[22-23]。在500 ml三口烧瓶中加入5 g FeCl2·4H2O、10 g FeCl3·6H2O和300 ml去离子水,70℃剧烈搅拌下快速加入10 ml氨水,500 r·min-1继续快速搅拌1 h。反应结束后用磁铁吸引,回收分离,去离子水重新悬浮并反复洗涤3次,60℃真空干燥24 h,得到Fe3O4粒子。FTIR(KBr,cm-1)max:3413(Fe¾O¾H),587(Fe¾O)[24-25]。
1.4 磁性吸附剂-CDPU@Fe3O4和-CDPU@ (SiO2/Fe3O4)的制备
1.4.1-CDPU@Fe3O4在100 ml三口烧瓶中加入4 g-CD和50 ml DMSO,搅拌下缓慢滴加8 ml HDI,60℃反应2 h得到黏稠状预聚物-CDPU。加入4 g Fe3O4粒子,高速搅拌,室温下继续反应12 h。反应结束后用磁铁回收吸附剂,依次用丙酮、去离子水反复洗涤3次,真空干燥24 h,即得到-CDPU@Fe3O4吸附剂。FTIR(KBr,cm-1)max:3448(O¾H),2932,2858(C¾H),1695(CO),1617,1559(¾NH¾CO),1259(C¾CO),1033(C¾O¾C),582(Fe¾O)。
1.4.2 SiO2/Fe3O4复合粒子 称取0.5 g干燥的Fe3O4粒子于0.1 mol·L-1HCl中超声分散10 min,水洗3次后加入250 ml三口烧瓶中,再加入20 ml去离子水和80 ml无水乙醇,室温搅拌30 min。而后加入 10 ml 氨水,继续搅拌30 min,再加入1 ml TEOS,室温继续搅拌反应6 h。产物磁分离回收,无水乙醇、去离子水各洗涤3次,60℃真空干燥24 h,得到SiO2/Fe3O4复合粒子。FTIR(KBr,cm-1)max:3425(O¾H),1095,798,470(Si¾O)[26],580(Fe¾O)。
1.4.3-CDPU@(SiO2/Fe3O4) 取8 g-CD溶于50 ml DMSO,搅拌下缓慢滴加8 ml HDI,60℃反应2 h。而后加入上述制得的SiO2/Fe3O4复合粒子4 g,缓慢滴加5 ml IPTS,继续反应12 h。反应结束后磁分离,丙酮、去离子水各洗涤3次,60℃真空干燥24 h,得到-CDPU@(SiO2/Fe3O4)吸附剂。FTIR(KBr,cm-1)max:3348(O¾H),2936,2853(C¾H),1699(CO),1629,1570(¾NH¾CO),1254(C¾CO),1050(C¾O¾C),1085,450(Si¾O),584(Fe¾O)。
1.5 磁性吸附剂对柯里拉京的吸附等温线测定
柯里拉京0.03 g加去离子水溶解定容至100 ml,制成母液。取8个100 ml具塞三角摇瓶,分别加入母液 3.0、5.5、8.0、10.5、13、15.5、18、20.5 ml,加去离子水补足25 ml,各瓶分别加入0.4 g磁性吸附剂置于恒温水浴振荡器中,150 r·min-1、25℃振荡3 h后取出,磁铁分离除去吸附剂,上清液稀释后测定270 nm吸光度值。根据柯里拉京吸光度-浓度标准曲线方程计算其平衡浓度(*)及吸附量(),用Langmuir吸附等温线方程拟合
1.6 珠子草中柯里拉京的吸附和洗脱
采用乙醇浸提法提取珠子草中的柯里拉京,首先优化提取条件:称取若干份等量的干燥珠子草粉末,分别加入5倍质量的0、15%、30%、45%、60%、75%、90%、100%(质量)乙醇溶液,超声浸提30 min。抽滤,滤渣再加入100 ml同样浓度乙醇重复超声浸提3次,合并滤液,45℃以下蒸干,用50%甲醇超声振荡溶解并定容至10 ml,用HPLC法测定柯里拉京含量。
另取适量珠子草粉末,按前述方法以60%乙醇超声浸提,蒸发至无醇味后用去离子水溶解,配制成一定浓度的粗样溶液,滤膜过滤备用。取两个50 ml三角摇瓶,分别加入15 ml粗样溶液和5 g吸附剂,25℃振荡6 h。而后用磁铁分离,分别投入30 ml去离子水,37℃振荡脱附6 h。用同样方法分别以30 ml 20%乙醇、50%乙醇为第二、三次洗脱剂,分别用HPLC法测定柯里拉京含量。
HPLC检测:样品在45℃以下蒸干,用50% (质量)甲醇溶解定容至10 ml,0.22 µm滤膜过滤。色谱条件为:Waters XBridgeTMShield RP18(4.6 mm×250 mm,5 μm)反相柱,柱温30℃,DAD检测器,检测波长270 nm,流速1.0 ml·min-1,进样量20 µl,流动相为0.1%磷酸水溶液(A)和乙腈(B)。梯度洗脱程序为:0~10 min,A(85):B(15);10~15 min,A(80):B(20);15~25 min,A(75):B(25)(以上均为体积比)。采用外标法定量。柯里拉京保留时间为7.50 min。
2 实验结果与讨论
2.1 磁性吸附剂的表征
2.1.1 表面形貌 对SiO2/Fe3O4复合粒子和吸附剂-CDPU@Fe3O4、-CDPU@(SiO2/Fe3O4)的表面结构进行SEM表征,如图2所示。其中-CDPU/Fe3O4吸附剂[图2(a)]的粒径在30~50mm之间,其表面具有褶皱突起的纤维状及凹坑状结构。SiO2/Fe3O4复合粒子[图2(b)]粒径3~10mm,表面具有大量80~100 nm的颗粒状突起,这可能是由TEOS水解生成的微小SiO2晶核的沉积所致。对其进行表面能谱分析(图3)可知,复合粒子由Fe、Si、O 3种元素构成,其质量分数分别为47.4%、11.5%和41.1%(3次测定平均值),说明SiO2已与Fe3O4发生复合。而-CDPU包覆了SiO2/Fe3O4复合粒子之后,吸附剂粒径为20~50mm,颗粒呈疏松的网格笼状结构,表面的聚合物呈树枝状突起,形成复杂的褶皱和大量的孔隙[图2(c)],这种结构有助于增加吸附剂的比表面积。
2.1.2 磁性吸附剂的晶相分析 采用XRD分析法考察了-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)的晶相结构,结果如图4所示。图中Fe3O4(谱线a)的主要衍射峰(2)30.4°、35.2°、43.1°、54.0°、57.3°、63.0°依次对应反式尖晶石型Fe3O4的(220)、(311)、(400)、(422)、(511)、(440)晶面的衍射峰[27-28],由此可确定所制得的Fe3O4粒子晶型为反式尖晶石型。SiO2/Fe3O4复合粒子的谱线b与Fe3O4几乎完全一致,这是由于TEOS水解得到的为无定形SiO2,仅在22°附近有一很弱的宽峰[29],而SiO2与Fe3O4仅通过物理作用混合,并未生成新的晶型,且Fe3O4本身的晶型并未发生变化[30]。
-CDPU的晶相区在10°和21°附近有两个典型的宽峰[15,31]。但从图3看出,两种-CDPU磁性吸附剂的衍射谱线c、d在低于25°的区域内存在一个很宽的衍射带,却没有典型的峰形,这说明包覆在磁核上的-CDPU以非晶态为主。而谱线c、d中仍然含有Fe3O4磁核的特征谱峰,说明聚合物包覆过程对Fe3O4的晶型未产生明显影响。
2.1.3 磁性吸附剂的热稳定性表征 对磁性吸附剂的热稳定性进行了考察,分别测定了热失重情况(TGA)及对应的差热曲线(DTA),如图5所示。从Fe3O4的热重曲线可以看出,由于蒸发掉吸附在粒子表面的一些水分,在100℃以下出现了失重,之后曲线几乎没有显著变化,但DTA曲线在535℃附近出现了强放热峰,表明Fe3O4的晶型发生了变化。SiO2/Fe3O4复合粒子的热重曲线与Fe3O4相似,这是由于SiO2中Si—O键的键能很高,SiO2热稳定性好,600℃以下不分解。但DTA曲线的放热峰的位置移至544℃,表明与SiO2复合后,Fe3O4晶型转变温度升高。
-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)两种吸附剂的热重曲线均能观察到3段阶梯式失重。第1阶段为200℃以下,吸附在样品表面的水分及-CD水合物的分解,此时可以观察到DTA曲线上有一个明显的吸热峰。第2阶段为200~350℃范围内-CD结构和氨基甲酸酯基团的分解,其中280~320℃主要是-CD的热分解[32],而氨基甲酸酯在300℃以上则开始分解[33]。此时在DTA曲线上分别于310℃(-CDPU@Fe3O4)和331℃[-CDPU@(SiO2/Fe3O4)]附近观察到显著的吸热峰。第3阶段在350~480℃之间,为聚氨酯骨架及其他有机成分的热分解,两种吸附剂分别在346℃和382℃附近观察到放热峰。两种吸附剂的DTA曲线上Fe3O4晶型转变的放热峰分别移至558℃和593℃附近,且峰形变得平缓,这一现象说明Fe3O4被聚合物包覆后,晶型的热转变受到一定阻碍。
由热重曲线可以估算吸附剂中聚合物的含量。由图5可知,聚合物从200℃开始分解,至480℃基本结束。因此,从热重曲线上截取这一温度范围的失重百分比可视为聚合物的含量,由此计算得到吸附剂-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)中聚合物的含量分别为41.5%和36.5%。
2.2 吸附等温线和吸附机理分析
在25℃下测定了吸附剂-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)分别吸附水溶液中柯里拉京的吸附等温线,如图6所示。随着柯里拉京平衡浓度的增加,吸附量亦逐渐增加,且吸附量的增加趋势逐渐减缓。采用Langmuir方程[式(1)]进行非线性拟合,发现方程与实验数据吻合较好,说明这两种吸附剂对柯里拉京的吸附基本符合Langmuir型。通过拟合可得到-CDPU@Fe3O4的m= 69.96 mg·g-1,= 0.321 ml·mg-1,而-CDPU@(SiO2/Fe3O4)的m= 75.96 mg·g-1,= 0.268 ml·mg-1。拟合结果表明,两种吸附剂对柯里拉京的吸附能力差异较小。
文献报道-CDPU具有两种类型的吸附位点,即-CD空腔和聚氨酯骨架[12]。-CD空腔能与柯里拉京形成包结复合物(25℃时的包结平衡常数为1.69×103L·mol-1 [15]),在吸附过程中可能起重要作用;而聚氨酯骨架结构中的酰胺基团具有与酚羟基形成氢键的能力[13],可能亦参与了对柯里拉京的吸附。这两类吸附位点的数量是有限的,故在理论上存在最大吸附量,这也与Langmuir吸附模型相吻合。
实验发现,Fe3O4磁核对柯里拉京具有很强的吸附能力,不同浓度水溶液中柯里拉京吸附率高达95%以上,且几乎无法从磁核上洗脱,表明Fe3O4与柯里拉京之间可能存在特殊的相互作用。在前期研究中发现XRD晶相分析可以捕捉CD聚合物吸附机理的一些信息[15],故借鉴此法对Fe3O4吸附柯里拉京前后的晶相做一比较,如图7所示。图中显示,Fe3O4的反式尖晶石型特征谱线均无明显变化。然而有趣的是2值在6°~19°范围内各条谱线的谱峰位置变化情况。Fe3O4的宽峰极值在12°附近;Fe3O4与柯里拉京物理混合物的峰值移至15°附近,与柯里拉京主要谱峰分布范围(12°~20°)相一致,故这一范围的宽峰可认为是Fe3O4与柯里拉京的谱线相互叠加的结果;而Fe3O4从水溶液中吸附了柯里拉京之后,峰值却向低衍射角方向移动至8°附近,且柯里拉京的特征谱线消失。
Amstad等[34]报道,一些具有邻苯二酚结构的化合物与Fe3O4之间的亲和力强且不可逆。他们发现这些酚类物质与Fe3O4中的Fe3+发生p电子离域,增强了邻二酚羟基与Fe3+的结合强度,而酚被电负性基团修饰后与Fe3+的作用更加强烈;同时粒子表面的Fe3+催化邻苯二酚分解,依次生成半醌、醌,最终生成含羧基的产物[35]。李媛等[36]认为,Fe3O4粒子能和酚类发生配位是由于Fe3O4粒子中Fe2+、Fe3+的价电子不饱和度高,易于和含有孤对电子的原子(N、O、S等)配位而发生强特异性吸附。柯里拉京分子中亦含有邻位酚羟基(图1),据此可推测柯里拉京被Fe3O4吸附后,Fe3O4磁核表面Fe(Ⅲ)与酚羟基形成了配合物。而从XRD谱图来看,这种配合物微晶具有较小的晶面指数()值,致使谱带向低衍射角方向发生显著移动。
2.3 磁性吸附剂对珠子草中柯里拉京的吸附和洗脱
采用乙醇水溶液浸提法提取珠子草中的柯里拉京,对乙醇浓度进行了优化,发现60%(质量)乙醇提取液中柯里拉京的含量最高。因此确定了提取条件为60%乙醇在超声振荡下浸提3次,每次30 min。粗提液中柯里拉京的浓度可达1.34 mg·ml-1。
根据HPLC分析的数据计算得到的结果如表1所示。表1显示Fe3O4对柯里拉京具有很强的吸附能力,对粗提液中柯里拉京的吸附率高达98.1%,但总洗脱率和回收率极低,证实了Fe3O4与柯里拉京之间的特殊相互作用,且一般的有机溶剂不足以克服这种相互作用而洗脱柯里拉京。受Fe3O4磁核的影响,-CDPU@Fe3O4对粗提液中柯里拉京的吸附率虽然可达63.6%,但依次用水、20%和50%(质量)乙醇的分步洗脱率分别只有10.0%、3.9%、3.1%,总洗脱率也仅为17.0%,表明Fe3O4磁核可能参与了柯里拉京的吸附,而且这种吸附占据了主要地位,导致总脱附率和回收率不高。而将Fe3O4用SiO2修饰,再包覆-CDPU之后,对柯里拉京的吸附率没有显著影响,但由于SiO2部分阻隔了Fe3O4磁核,降低了磁核与柯里拉京直接接触的概率,故分步洗脱率均有显著提高,总洗脱率亦提高到41.0%,柯里拉京回收率也增加了1倍。
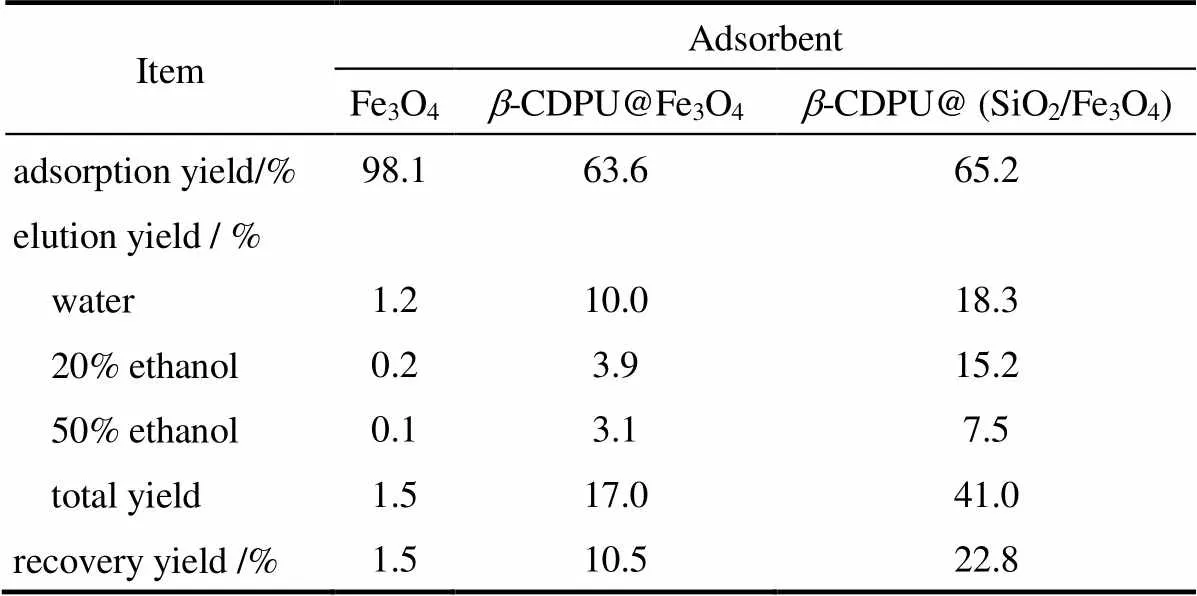
表1 磁性吸附剂对珠子草粗提物中柯里拉京的吸附率和洗脱率
传统的柯里拉京分离大多采用有机溶剂萃取法,过程烦琐,耗时长,有机溶剂消耗量大[16,19]。本课题组[15]前期将反相悬浮交联法制得的-CDPU球形吸附剂填充于固定床中用于柯里拉京的吸附分离,经上样、水洗、洗脱、再生等过程富集柯里拉京,在20%乙醇洗脱液中回收率为49.4%,纯度可达64.8%,纯化倍数6.5。此过程一次过柱处理量约7.5 ml·g-1吸附剂,但整个流程耗时长达30 h以上,耗用各种溶剂体积总计超过2 L。而本文采用-CDPU@(SiO2/Fe3O4)磁性吸附剂吸附珠子草粗提液中的柯里拉京,处理量3 ml·g-1吸附剂,耗时12 h,溶剂消耗量仅90 ml,回收率22.8%,纯度9.7%,纯化倍数3.1,虽然在分离指标上弱于固定床色谱法,仅能对柯里拉京进行初步富集,但操作简便快捷,并节约了大量有机溶剂。
然而,-CDPU@(SiO2/Fe3O4)磁性吸附剂也存在一定的不足,主要表现为洗脱效率仍然不高,这可能与极性SiO2对柯里拉京的强保留特性有关。此外,吸附剂的分辨率及选择性尚待提高。针对这一问题,可能需要引入分子印迹[37]等技术对吸附位点进行专门设计。可以预见,未来经过改进的环糊精聚氨酯磁性吸附剂将在柯里拉京乃至其他多酚类天然产物的富集分离方面有着广阔的应用前景。
3 结 论
以环糊精聚氨酯-CDPU包覆Fe3O4磁核及SiO2/Fe3O4复合粒子,制备出两种磁性吸附剂-CDPU@Fe3O4和-CDPU@(SiO2/Fe3O4)。通过分析得到以下结论。
(1)通过FTIR、XRD、SEM及热重分析可知,采用共混包埋法可以成功地将-CDPU包覆在Fe3O4及SiO2/Fe3O4磁核外层,且包覆之后吸附剂中Fe3O4的晶型仍保持反式尖晶石型。通过热重分析表明吸附剂在200℃以下稳定性好,通过曲线的失重程度可知吸附剂中聚合物所占的比例较高。
(2)两种吸附剂对柯里拉京的吸附均符合Langmuir型等温线,反映了吸附具有-CD和氨基甲酸酯结构单元的双位点效应。通过XRD分析发现Fe3O4磁核亦参与吸附过程,吸附机理可能与Fe(Ⅲ)和柯里拉京的酚羟基形成配合物有关。
(3)两种吸附剂对珠子草粗提物中柯里拉京的吸附率差异不大,但由于SiO2阻隔了Fe3O4磁核,减弱了磁核与柯里拉京的相互作用,使得-CDPU@(SiO2/Fe3O4)更有利于柯里拉京的洗脱,可实现珠子草粗提物中柯里拉京的初步富集。与其他分离富集方法相比,此法操作简便快捷,溶剂消耗量小,在柯里拉京以及其他多酚类天然产物提取分离方面有着潜在的应用前景。
符 号 说 明

C*——柯里拉京的平衡浓度,mg·ml-1 K——吸附平衡常数,ml·mg-1 Q——吸附平衡时的吸附量,mg·g-1 Qm——吸附剂对柯里拉京的饱和吸附量,mg·g-1
References
[1] 廖鹏飞, 夏金兰, 聂珍媛, 等. 磁性微球的制备及在生物分离应用中的研究进展 [J]. 生物磁学, 2005, 5 (4): 47-51. LIAO P F, XIA J L, NIE Z Y,. Progress in preparation and bio-separation application of magnetic microspheres [J]. Biomagnetism, 2005, 5 (4): 47-51.
[2] FRANZREB M, SIEMANN-HERZBERG M, HOBLEY T J,. Protein purification using magnetic adsorbent particles [J]. Applied Microbiology and Biotechnology, 2006, 70 (5): 505-516.
[3] ZHANG B, XING J M, LANG Y Q,. Synthesis of amino-silane modified magnetic silica adsorbents and application for adsorption of flavonoids fromFisch [J]. Science in China Series B: Chemistry, 2008, 51 (2): 145-151.
[4] 徐秋生, 李文松. 超顺磁性吸附剂1步高效提取和纯化丹参中丹参酮 [J]. 中草药, 2015, 46 (24): 3670-3674. XU Q S, LI W S. Superparamagnetic adsorbent for one-step efficient extraction and purification of tanshinones from[J]. Chinese Traditional and Herbal Drugs, 2015, 46 (24): 3670-3674.
[5] 李凯斌, 沈一丁, 费贵强, 等. 阴离子-环糊精/Fe3O4磁性微球对Cu2+的吸附 [J]. 化工学报, 2014, 65 (6): 2148-2155. LI K B, SHEN Y D, FEI G Q,. Adsorption of Cu2+by anionic-cyclodextrin/Fe3O4magnetic microspheres [J]. CIESC Journal, 2014, 65 (6): 2148-2155.
[6] CONNORS K A. The stability of cyclodextrin complexes in solution [J]. Chemical Reviews, 1997, 97 (5): 1325-1357.
[7] 刘甜甜, 赵珺. 亲水作用色谱研究及环糊精固定相的应用 [J]. 化学研究与应用, 2014, 26 (5): 615-622. LIU T T, ZHAO J. The application of hydrophilic interaction chromatography with cyclodextrin-stationary phase [J]. Chemical Research and Application, 2014, 26 (5): 615-622.
[8] 沈海民, 武宏科, 纪红兵, 等.-环糊精-Fe3O4超分子体系的构筑及其应用研究进展 [J]. 有机化学, 2014, 34 (4): 630-646. SHEN H M, WU H K, JI H B,. Progress in the construction of-cyclodextrin-Fe3O4supramolecular systems and their application [J]. Chinese Journal of Organic Chemistry, 2014, 34 (4): 630-646.
[9] WANG M, LIU P, WANG Y,. Core-shell superparamagnetic Fe3O4@-CD composites for host-guest adsorption of polychlorinated biphenyls (PCBs) [J]. Journal of Colloid and Interface Science, 2015, 447: 1-7.
[10] KIASAT A R, NAZARI S. Magnetic nanoparticles grafted with-cyclodextrin-polyurethane polymer as a novel nanomagnetic polymer brush catalyst for nucleophilic substitution reactions of benzyl halides in water [J]. Journal of Molecular Catalysis A: Chemical, 2012, 365: 80-86.
[11] 张欠欠, 彭延庆. 可磁回收的-环糊精聚氨酯纳米催化剂催化还原羰基化合物 [J]. 化学世界, 2015, (11): 649-652. ZHANG Q Q, PENG Y Q. Magnetically recoverable-cyclodextrin polyurethane nano-catalyst for the reduction of carbonyl compounds [J]. Chemical World, 2015, (11): 649-652.
[12] WILSON L D, MOHAMED M H,HEADLEY J V. Surface area and pore structure properties of urethane-based copolymers containing-cyclodextrin [J]. Journal of Colloid Interface Science, 2011, 357 (1): 215-222.
[13] YAMASAKI H, MAKIHATA Y, FUKUNAGA K. Preparation of crosslinked-cyclodextrin polymer beads and their application as a sorbent for removal of phenol from wastewater [J]. Journal of Chemical Technology and Biotechnology, 2008, 83 (7): 991-997.
[14] MOHAMED M H, WILSON L D, HEADLEY J V,. Investigation of the sorption properties of-cyclodextrin- based polyurethanes with phenolic dyes and naphthenates [J]. Journal of Colloid and Interface Science, 2011, 356: 217-226.
[15] ZHAO J, LIU T T, CHEN G. An effective-cyclodextrin polyurethane spherical adsorbent for the chromatographic enrichment of corilagin fromL. extract [J]. Reactive and Functional Polymers, 2016, 102: 119-129.
[16] 张树峰, 明艳林, 林毅, 等. 叶下珠属植物活性成分柯里拉京研究进展 [J]. 亚热带植物科学, 2010, 39 (4): 79-83. ZHANG S F, MING Y L, LIN Y,. Research progress on corilagin of Phyllanthus [J]. Subtropical Plant Science, 2010, 39 (4): 79-83.
[17] 陈一燕, 陈崇宏. 柯里拉京药理活性研究进展 [J]. 中国现代应用药学, 2010, 27 (5): 390-394. CHEN Y Y, CHEN C H. Advances in the pharmacological activity research on corilagin [J]. Chinese Journal of Modern Applied Pharmacy, 2010, 27 (5): 390-394.
[18] HAU D K P, ZHU G Y, LEUNG A K M,.anti-tumour activity of corilagin on Hep3B hepatocellular carcinoma [J]. Phytomedicine, 2010, 18 (1): 11-15.
[19] MARKOM M, HASAN M, DAUD W R W,. Extraction of hydrolysable tannins fromLinn.: effects of solvents and extraction methods [J]. Separation and Purification Technology, 2007, 52 (3): 487-496.
[20] PRASAD K N, YANG B, ZHAO M,. High pressure extraction of corilagin from longan (Lour.) fruit pericarp [J]. Separation and Purification Technology, 2009, 70 (1): 41-45.
[21] YANG Y C, LI J, ZU Y G,. Optimisation of microwave-assisted enzymatic extraction of corilagin and geraniin fromLinne and evaluation of antioxidant activity [J]. Food Chemistry, 2010, 122 (1): 373-380.
[22] 苏鹏飞, 陈国, 赵珺. 表面羧基化Fe3O4磁性纳米粒子的快捷制备及表征 [J]. 高等学校化学学报, 2011, 32 (7): 1472-1477. SU P F, CHEN G, ZHAO J. Convenient preparation and characterization of surface carboxyl-functioned Fe3O4magnetic nanoparticles [J]. Chemical Journal of Chinese Universities, 2011, 32 (7): 1472-1477.
[23] 陈佳璐, 陈国, 赵珺, 等. 羧基修饰的超顺磁纳米粒子直接固定化罗伊氏乳杆菌 [J]. 化工学报, 2012, 63 (4): 1175-1181. CHEN J L, CHEN G, ZHAO J,. Direct immobilization ofusing carboxyl- functional superparamagnetic nanoparticles [J]. CIESC Journal, 2012, 63 (4): 1175-1181.
[24] 黄丽珍, 李二冬, 李波, 等.-环糊精/Fe3O4水基磁流体的制备表征及其对中性红的吸附行为 [J]. 应用化学, 2014, 31 (5): 607-612. HUANG L Z, LI E D, LI B,. Preparation of water-based-cyclodextrin/Fe3O4magnetic fluid and its adsorption behavior for neutral red [J]. Chinese Journal of Applied Chemistry, 2014, 31 (5): 607-612.
[25] HU H, WANG Z, PAN L,. Ag-coated Fe3O4@SiO2three-ply composite microspheres: synthesis, characterization, and application in detecting melamine with their surface-enhanced Raman scattering [J]. Journal of Physical Chemistry C, 2010, 114 (17): 7738-7742.
[26] 杜雪岩, 马芬, 李芳, 等. Fe3O4@SiO2磁性纳米粒子的制备及表征 [J]. 兰州理工大学学报, 2011, 37 (2): 22-25. DU X Y, MA F, LI F,. Preparation and characterization of Fe3O4@SiO2magnetic nanoparticles [J]. Journal of Lanzhou University of Technology, 2011, 37 (2): 22-25.
[27] JIANG Y J, JIANG J H, GAO Q M,. A novel nanoscale catalyst system composed of nanosized Pd catalysts immobilized on Fe3O4@SiO2-PAMAM [J]. Nanotechnology, 2008, 19 (7): 369-381.
[28] 徐芳, 王军涛, 韩朝晖. 正癸酸修饰磁性纳米Fe3O4对溶菌酶的吸附研究 [J]. 化学研究与应用, 2013, 25 (9): 1251-1257. XU F, WANG J T, HAN Z H. Adsorption of lysozyme by Fe3O4magnetic nanoparticles modified by the capric acid [J]. Chemical Research and Application, 2013, 25 (9): 1251-1257.
[29] TANG B, CUI J, WANG Y,. Facile synthesis and performances of PEG/SiO2composite form-stable phase change materials [J]. Solar Energy, 2013, 97: 484-492.
[30] 张笛, 邓满凤, 赵赫, 等. 多巴胺包埋磁性SiO2固定化漆酶催化去除4-氯酚 [J]. 化工学报, 2015, 66 (9): 3705-3711. ZHANG D, DENG M F, ZHAO H,. Immobilization of laccase on magnetic SiO2through dopamine self-polymerization for 4-CP removal [J]. CIESC Journal, 2015, 66 (9): 3705-3711.
[31] MOHAMED M H, WILSON L D, HEADLEY J V. Tuning the physicochemical properties of-cyclodextrin based polyurethanescross-linking conditions [J]. Microporous and Mesoporous Materials, 2015, 214: 23-31.
[32] HEDGES A R, SHIEH W J, SIKORSKI C T. Use of cyclodextrins for encapsulation in the use of treatment of food products [J]. ACS Symposium Series, 1995, 590: 60-71.
[33] WEI Y, CHENG F, LI H,. Thermal properties and micromorphology of polyurethane resins based on liquefied benzylated wood [J]. Journal of Scientific and Industrial Research, 2005, 64: 435-439.
[34] AMSTAD E, GILLICH T, BILECKA I,. Ultrastable iron oxide nanoparticle colloidal suspensions using dispersants with catechol-derived anchor groups [J]. Nano Letters, 2009, 9 (12): 4042-4048.
[35] AMSTAD E, GEHRING A U, FISCHER H,. Influence of electronegative substituents on the binding affinity of catechol-derived anchors to Fe3O4nanoparticles [J]. Journal of Physical Chemistry C, 2011, 115 (3): 683-691.
[36] 李媛, 肖乐辉, 周乃元, 等. 在茶叶农药残留测定中用四氧化三铁纳米粒子去除样品中的色素 [J]. 分析化学, 2013, 41 (1): 63-68. LI Y, XIAO L H, ZHOU N Y,. Purification of pigments by iron oxide nanoparticles for analysis of pesticide residues in tea [J]. Chinese Journal of Analytical Chemistry, 2013, 41 (1): 63-68.
[37] 李凯, 孙蕊, 彭羽, 等. Fe3O4磁性分子印迹聚合物的研究进展 [J]. 化学研究与应用, 2015, 27 (12): 1790-1795. LI K, SUN R, PENG Y,. Research progress of Fe3O4magnetic molecularly imprinted polymers [J]. Chemical Research and Application, 2015, 27 (12): 1790-1795.
Synthesis and characterization of-cyclodextrin polyurethane magnetic adsorbents and their adsorption on corilagin
ZHAO Jun1,2, MIN Shuxue1, LIN Jiduan1, CHEN Guo1, WANG Xiaoqin1,2
(1College of Chemical Engineering, Huaqiao University, Xiamen 361021, Fujian, China;2Institute of Oil and Natural Products, Huaqiao University, Xiamen 361021, Fujian, China)
Two magnetic adsorbents-CDPU@Fe3O4and-CDPU@(SiO2/Fe3O4) were synthesized by encapsulating Fe3O4and SiO2/Fe3O4composite magnetic beads by-cyclodextrin polyurethane polymer (-CDPU), and adsorption and enrichment of polyphenolic natural product corilagin fromL. herb plants by magnetic separation were studied. Both adsorbents were characterized by FTIR, XRD, SEM and TG/DTA techniques. The appearance of several new peaks in FTIR spectra around 1695, 1617, 1559, 1259 and 1033 cm-1was attributed to urethane and-CD moiety. The adsorbent polymeric surface was rough with many protuberant lumps, folds and pores as observed by SEM. Both adsorbents were thermostable below 200℃, indicating suitability for separation usage at room temperature. Polymer content of the two adsorbents reached as high as 41.5% and 36.5%, respectively, based on the mass loss at high temperature in TG/DTA analysis. XRD showed that the crystal structure of Fe3O4in both adsorbents was nearly the same as that of Fe3O4and SiO2/Fe3O4composite beads. Hence,-CDPU encapsulation did not alter crystal structure of Fe3O4. Adsorption of corilagin by both adsorbents followed Langmuir adsorption isotherm, which was expected from double adsorption sites in-CDPU skeleton. But the special interaction between Fe3O4magnetic-core and corilagin, probably due to the complex formation of Fe(Ⅲ) and phenolic hydroxyl groups in corilagin molecule, made it difficult to elute corilagin and resulted in low elution and recovery yield of corilagin at 17.0% and 10.5%, respectively. SiO2modification on Fe3O4magnetic core was able to hinder such interaction and the adsorbent-CDPU@(SiO2/Fe3O4) exhibited more favorable performance for corilagin enrichment with the elution yield of 41.0% and recovery yield of 22.8%. The corilagin enrichment fromL. showed the adsorbent-CDPU@(SiO2/Fe3O4) would find commercial application for recovery and enrichment of specific natural products from plant materials.
cyclodextrin polyurethane; magnetic; adsorbent; corilagin;L.; adsorption; separation
2016-04-11.
ZHAO Jun, zhaojun@hqu.edu.cn
10.11949/j.issn.0438-1157.20160468
O 647.3;TB 33
A
0438—1157(2016)10—4246—09
国家自然科学基金项目(21576108);福建省自然科学基金项目(2013J05028);华侨大学引进人才科研启动项目(11BS408)。
2016-04-11收到初稿,2016-07-01收到修改稿。
联系人及第一作者:赵珺(1982—),男,博士,讲师。
supported by the National Natural Science Foundation of China (21576108), the Natural Science Foundation of Fujian Province (2013J05028) and the Scientific Research Starting Foundation of Huaqiao University (11BS408).
