原子荧光光谱法测定尿中微量砷元素
2016-10-25杨志羡
杨志羡
(内蒙古地方病防治研究中心,呼和浩特 100031)
原子荧光光谱法测定尿中微量砷元素
杨志羡
(内蒙古地方病防治研究中心,呼和浩特 100031)
建立了测定尿中微量砷元素含量的原子荧光光谱法。以硝酸-高氯酸(4∶1)混合液消解样品,加入5%的硫脲-抗坏血酸混合液还原样品消解液,将处理好的样品导入原子荧光仪进行测定,荧光强度If与砷元素质量浓度c线性相关,线性方程为If=178.351c+3.131,相关系数为0.999 8,砷的检出限为0.024 3 μg/L,测定结果的相对标准偏差为3.0%~4.1%(n=9),加标回收率为100%~104%。该法样品处理简便,适于大批量尿样中砷含量的检测。
原子荧光光谱;尿样;砷;样品前处理
砷在自然界中分布较广,在环境中的主要存在形态为有机态砷和无机态砷。砷的来源主要为工业“三废”排放和部分地区的土壤、水源。人类通过大气、饮水、食物、药品摄入砷元素,砷元素被人体吸收后主要经肾脏以尿液排出[1]。在一定时间内通过测定受试者尿中砷含量,可以对受测者的砷接触情况、砷摄入量、砷中毒情况提供参考依据。
尿中微量砷元素常见的测定方法有新银盐分光光度法[2]、氢化物原子吸收光谱法[3]、原子荧光光谱法[4]等。新银盐分光光度法样品前处理程序复杂,检测灵敏度低,不适合大批量样品的检测分析;氢化物原子吸收法的精密度和准确度较低;原子荧光光谱法近些年在尿中砷含量的测定方面应用较多,其优点是准确度和灵敏度高,可大批量测定样品。以上方法均需要对尿样进行前处理,样品前处理方法主要有湿法消解法[5]和微波消解法。微波消解法较易操作,但其试剂用量大,样品空白大,在做低浓度样品时准确度差[6];湿法消解是处理生物样品的经典方法,但不同的消解液其消解效果差异很大,因此要根据实际的实验条件和样品性质进行前处理方法的优化及选择。
笔者对硝酸-高氯酸(4∶1)、硝酸-硫酸(8∶1)、硝酸-双氧水(1∶2)3种消解液对尿样的消解效果进行了比较,优化了实验条件,建立了操作简便、测定结果准确的原子荧光光谱法。
1 实验部分
1.1 实验原理
尿中各种形态的砷在经过强氧化性、强酸性的混酸下消解,形成+5价无机态砷,经过硫脲和抗坏血酸还原后,+5价砷被还原为+3价态砷。在氢化物发生-原子荧光光谱法测定过程中,NaBH4和HCl反应生成初生态氢,+3价砷被初生态氢还原并结合形成AsH3,AsH3被载气(高纯氩气)导入原子化器中,分解为原子态砷,在砷空心阴极灯的照射下,原子态砷元素的最外层电子从基态跃迁至激发态,由于激发态不稳定,最外层电子会瞬间回落至基态或低能态,同时释放出原子荧光,在一定条件下,荧光强度与样品中的砷含量成正比,与标准工作曲线对比即可准确定量测定砷的含量[7]。
1.2 主要仪器与试剂
双道原子荧光仪:AFS-230E型,附硒元素特种空心阴极灯,北京科创海光仪器有限公司;
管式炉:5B-1C型,兰州连化环保科技有限技术公司;
盐酸、高氯酸、硝酸、硫酸、双氧水(30%)、硼氢化钠、氢氧化钠、硫脲、抗坏血酸:优级纯,北京化工厂;
硼氢化钠-氢氧化钠溶液:称取2.5 g氢氧化钠溶于少量纯水中,制得氢氧化钠溶液,再称取硼氢化钠7.5 g溶于其中,以纯水定容至500 mL;
硫脲-抗坏血酸混合溶液:称取5 g硫脲,溶于100 mL纯水中,可加热促使其溶解,待硫脲全部溶解后将溶液冷却至室温,向其中加入5 g抗坏血酸,搅拌促使其溶解;
高纯氩气:纯度为99.999 9%;
砷元素溶液标准物质:1 mg/mL,编号为GBW 08611,中国科学技术研究院;
砷标准使用溶液:0.1 μg/mL,准确吸取砷元素溶液标准物质1 mL于100 mL容量瓶中,以1%的硝酸定容至标线,再准确吸取该溶液10 mL于100 mL容量瓶中,以1%硝酸溶液定容。
1.3 仪器工作条件
灯电流:45 mA;负高压:260 V;载气:高纯氩气,流量为400 mL/min;屏蔽气:高纯氩气,流量为900 mL/min;读数方式:峰面积法;原子化器高度:9 mm。
1.4 样品前处理
准确吸取1.00 mL编号分别为A401,A402的尿样,移入两只硬质玻璃试管中,各加入3 mL硝酸-高氯酸混酸;同时再取3支试管,加入1.00 mL纯水和3 mL硝酸-高氯酸,作为样品空白装入管式炉中,静置12 h以上,升温赶酸;冷却后将其移至10 mL容量瓶中,同时加入3 mL硫脲-抗坏血酸混合溶液,以0.5 mL盐酸定容至标线,静置30 min后上机测定。
1.5 系列砷标准溶液的配制
分别准确吸取0.1 μg/mL的砷标准使用溶液0.00,1.00,2.00,4.00,8.00,10.00,15.00,20.00 mL于8只100 mL容量瓶中,每只容量瓶内加5.00 mL盐酸,20.00 mL硫脲-抗坏血酸混液,稀释至标线,配制 成 0.00,1.00,2.00,4.00,8.00,10.00,15.00,20.00 μg/L的系列砷标准溶液。
2 结果与讨论
2.1 样品前处理方法
分别采用硝酸-高氯酸(4∶1)、硝酸-硫酸(8∶1)、硝酸-双氧水(1∶2) 3种湿法消解前处理方法处理冻干尿样,在1.3仪器工作条件下测定尿样中总砷的含量,对测定结果的相对标准偏差、空白样品加标回收率进行比较,并对相关数据进行统计学的显著性分析,若3种处理方法测定结果精密度及准确度之间存在显著性差异,则综合考虑操作便利性、测定精密度和准确度,从中选择最理想的样品处理方式。
2.1.1 不同样品处理方法测定结果
取AN401,AN402两种样品,按照1.4步骤分别在酸-高氯酸(4∶1)、硝酸-硫酸(8∶1)、硝酸-双氧水(1∶2) 3种混酸中消解(混酸类型及赶酸方法见表1),两种样品各处理9份,定容后上机测量,计算其均值和相对标准偏差,所得数据列于表2。

表1 样品前处理混酸及赶酸方法
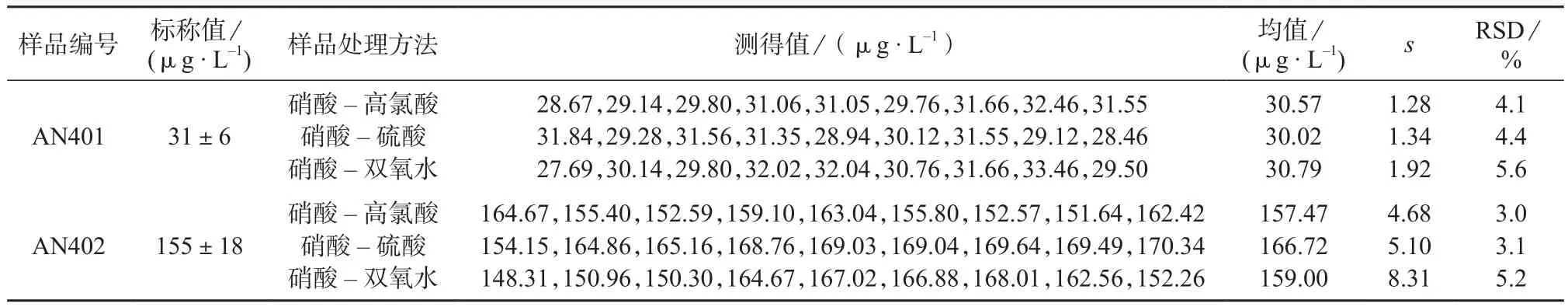
表2 不同处理方法的样品测定结果
由表2可知,经硝酸-高氯酸、硝酸-硫酸处理的样品测定结果的相对标准偏差优于WS/T 28-1996 《尿中砷的二乙基二硫代氨基甲酸银三乙醇胺分光光度测定方法》的精密度(1.8%~5.1%)[8];由硝酸-双氧水组合的消解液处理所得样品,测定结果的相对标准偏差均大于5.1%,可知该方法不如前两种方法处理效果理想。原因可能是个别样品在消解时存在碳化现象,为了消解彻底,在碳化样品中补加了一定量的双氧水,导致测量精密度不够理想。
取3种不同的尿样,分别在酸-高氯酸(4∶1)、硝酸-硫酸(8∶1)、硝酸-双氧水(1∶2) 3种混酸消解液中消解,并进行加标回收试验,测定结果列于表3。由表3可知,硝酸-高氯酸及硫酸-硝酸的前处理方法回收率均优于卫生标准WS/T 28-1996 《尿中砷的二乙基二硫代氨基甲酸银三乙醇胺分光光度测定方法》的91%~94%。而硝酸-双氧水的混酸处理方法所得的加标回收率低于卫生标准。

表3 不同处理方法的样品加标回收试验结果
2.1.2 3种处理方法样品测定结果显著性分析
鉴于硝酸-双氧水样品前处理方法测定结果的精密度、准确度[9]均低于卫生标准要求,因此仅对硝酸-高氯酸、硝酸-硫酸两种处理方法样品测定结果进行显著性分析[10]。
(1)F检验。将表2中前两种方法所得的标准偏差值代入公式F=s22/s12计算两种浓度样品的F值,得F1=1.10,F2=1.19;当置信度为95%、自由度为8时,查表得知F0.95,n-1=3.44,F1<F0.95,n-1,F2<F0.95,n-1,表明两种方法处理的样品测定结果的精密度无显著性差异,两组数据中无偶然误差。
(2) t检验。利用表2中两种浓度样品的平均值、标准偏差计算t值[10],与置信度95%自由度为8的t表临界值比对。样品AN401经两种方法处理后,测定结果经计算得t=0.89,查表得知t0.95,n-1=2.31,t<t0.95,n-1,表明该样品经两种方法处理后测量结果的均值无显著性差异,两组数据无系统误差。样品AN402经两种前处理方法处理所得测定结果经计算得t=4.01,t >t0.95,n-1,表明A402样品经两种方法处理后测定结果有显著差异,存在系统误差。结合回收率数据可知,在处理高浓度的样品时,硝酸-硫酸组合的混酸处理方法存在正误差。
以上分析结果表明:硝酸-高氯酸组合的混酸处理尿样是3种前处理方法最为理想的一种[11-12]。
在尿中砷含量检测过程中,遇到个别样品有机物含量高,使用硝酸-硫酸混酸和硝酸-双氧水处理样品时,在赶酸阶段会出现碳化现象,为了消解彻底,必须补加双氧水或硝酸;在同一批处理的样品中,样品空白的信号值是一定的,碳化现象越严重,需要加试剂越多,荧光强度也越高,抵减样品空白信号后,可能导致碳化样品测量结果偏高[13]。而使用硝酸-高氯酸混酸处理样品时就不存在此问题。但高氯酸在浓、热状态时氧化性极强,与有机物混合时会发生爆炸反应[14]。因此应先将样品在硝酸中加热消解,待溶液澄清且颜色变浅,取下样品冷却至室温再加入高氯酸,继续升温加热将硝酸赶尽,冷却至室温再用还原剂定容样品,保证实验安全。
2.2 仪器工作条件
2.2.1 灯电流
调整灯电流大小可以控制激发光源的强弱。灯电流越大,光源越强,灵敏度越高;但过大的灯电流会引起自吸效应,且会导致空心阴极灯的寿命减少[15]。分别调节灯电流为40,45,50,55,60 mA进行试验,结果表明选择灯电流为45 mA时荧光强度最大。
2.2.2 负高压
负高压增加时,仪器信号强度增大,灵敏度升高;但噪声增大,稳定性不够好[15]。分别调整负高压为240,250,260,270 V进行试验,结果表明选择260 V负高压荧光强度最大。
2.3 还原剂和碱的浓度
还原剂NaBH4是一种极易分解的物质,只有在碱性环境下稳定存在。因此要先配制一定浓度的稀碱溶液,再将称好的NaBH4溶于碱液中。但体系碱性过大会降低反应的酸度而降低灵敏度。试验表明,碱液质量分数宜控制在0.5%。还原剂NaBH4的浓度不易过大,否则会引起液相干扰;但浓度过低又使氢化物发生反应不完全,同样导致灵敏度下降。分别取质量分数为1.05%,1.50%,2.00%,2.50%的NaBH4溶液进行试验,结果表明NaBH4溶液的质量分数为1.5%时荧光强度最大。
2.4 载流液盐酸的浓度
载流槽中的盐酸与NaBH4产生初生态的氢,初生态的氢与砷元素生成氢化物而进入原子化器原子化。载流盐酸浓度的大小直接影响初生态氢与砷元素的有效结合[16]。分别取体积分数为2.0%,5.0%,10%,15%,20%的盐酸溶液作为载流液,试验结果表明,过高的酸度信号强度也高,但背景干扰严重,载流液盐酸的体积分数宜选择为5%。
2.5 线性方程及检出限
取1.5配制的系列砷标准溶液,按照1.3仪器工作条件上机测定,以荧光强度(If)为纵坐标、以溶液的质量浓度(c)为横坐标进行线性回归[17],线性方程为If=178.351c+3.131,相关系数r=0.999 8。
连续测定11次空白溶液的荧光强度,将11次测定结果的标准偏差s及标准曲线斜率k代入公式LD=3s/k,计算得检出限[18]为0.024 3 μg/L。
2.6 精密度与准确度
由表2、表3试验数据可知,在最佳条件下,本法测定结果的相对标准偏差为3.0%~4.1%(n=9),样品加标回收率为100%~104%。表明本法测量精密度和准确度均较好。
3 结论
采用硝酸-高氯酸(4∶1)消解尿样,再以5%的硫脲-抗坏血酸混液还原,利用原子荧光光谱法测定尿液中的砷含量,测定结果的准确度、精密度优于标准方法。本法样品前处理简便,可用于大批量尿中微量砷的测定。
[1] 吴坤,孙秀发.营养与食品卫生学[M].5版.北京:人民卫生出版社,2004: 383-384.
[2] 彭速标,蔡慧华.砷的光度分析法的进展[J].理化检验(化学分册),2006,42(2): 145-149.
[3] 范洪斌,侯春梅,徐丽芳.流动注射氢化物-原子吸收光谱法测定人发中砷[J].理化检验(化学分册),2003,39(12): 735-737.
[4] 李莎莎,陈卫东.原子荧光光谱法测定尿中痕量砷[J].理化检验(化学分册),2004,40(9): 549-551.
[5] 云奋,马彩超,曾德斌,等.原子荧光法测定尿砷时尿样前处理与分析条件探讨[J].中华地方病学杂志,2015,34(1): 66-69.
[6] 邬春华,吕元琦,袁倬斌.微波消解原子荧光光谱法测定生物样品中的砷汞[J].理化检验(化学分册),2006,42(1): 41-42.
[7] 刘明钟,汤志勇.原子荧光光谱分析[M].北京:化学工业出版社,2008: 35-38.
[8] 冯仁丰.再说说精密度[J].检验医学,2014,29(8): 787-793.
[9] 邓波.仪器定量分析中几个问题的探讨[J] .中国无机分析化学,2011,1(2): 1-5.
[10] 武汉大学.分析化学[M]. 5版.北京:高等教育出版社,2006.
[11] 任春华,方卫民,罗春明,等.测量方法确认技术及其指标评价[J].理化检验(化学分册),2006,42(8): 677-681.
[12] 于亚东.化学分析方法的确认[M]. 2版.北京:中国质检出版社,2013: 9-11.
[13] 胡刚,童成.原子荧光使用中影响空白值的因素分析[J].计测技术,2015,35(增刊): 250-252.
[14] 大连理工大学无机化学教研室.无机化学[M].5版.北京:高等教育出版社,2006: 81-88.
[15] 马志刚,郑永雯.原子荧光光谱仪改进意见[J].分析仪器,2014(5): 76-78.
[16] 崔彦杰,李文娟.不同酸基体砷锑混合溶液对原子荧光光度计性能测试结果的影响[J].测量与设备,2015(8): 12-15.
[17] 陈怀玉.环境监测分析中校准曲线可靠性和检验方法的探讨[J].理化检验(化学分册),2000,36(8): 363-365.
[18] 《理化检验》编辑部.灵敏度、检出限、测定限[J].理化检验:(化学分册),2007,43(4): 329-331.
Determination of Trace Arsenic in Urine by Atomic Fluorescence Spectrometry
Yang Zhixian
(Inner Moglia Center for Endemic Disease Control and Research, Hohhot 010031, China)
An atomic fluorescence spectrometry for determining arsenic content in urine was set up. Nitric acidperchloric acid (4∶1) was used to digest the urine sample, and the sample solution was reducted by adding 5% thioureaascorbic acid solution, the digested sample was determined by atomic fluorescence spectrometer. The fluorescence enhencity was linear with the concentration of arsenic, the linear equation was If=178.351c+3.131 with the corelatopn coefficient of 0.999 8. The detection limit of arsenic was 0.024 3 μg/L, the relative standard deviation of determination results were 3.0%-4.1%(n=9), and the recoveries were 100%-104%. This method has the advantage of simple pretreatment method for sample, and it was suitable for determining large batch of urine samples.
atomic fluorescence spectroscopy; urine samples; arsenic; sample pretreatment
O657.31
A
1008-6145(2016)05-0091-04
10.3969/j.issn.1008-6145.2016.05.024
联系人:杨志羡;E-mail: 5959120.ok@163.com
2016-06-23
