腹膜转移的结肠癌患者MDT诊治二例
2016-10-21王展怀孙立峰袁瑛丁克峰张苏展
王展怀 孙立峰 袁瑛 丁克峰 张苏展
•病例讨论•
腹膜转移的结肠癌患者MDT诊治二例
王展怀孙立峰袁瑛丁克峰张苏展
本文描述了2例异时性腹膜转移的结肠癌病例的多学科诊治过程。1例多发转移,1例单发转移。这两例患者经MDT讨论后都首先采用了肿瘤减灭术联合腹腔热灌注化疗的治疗模式(cytoreductive surgery,CRS/hyperthermic intraperitoneal peroperative chemotherapy,HIPEC),单发转移的患者目前获得了12个月的无病生存期(disease-free survival,DFS),而多发转移的患者也获得了12个多月的总生存期(overall survival,OS)。目前发现与结直肠癌腹膜转移患者OS相关的因素包括肿瘤减灭术(CRS)完全程度和肿瘤累及的范围(腹膜转移癌指数)等。因此,对于结直肠癌的腹膜转移患者,评估病变范围极其重要,对于较局限的腹膜转移,多学科的综合诊治和积极的治疗手段能改善这部分患者的生存时间和生存质量。
结直肠肿瘤;肿瘤转移;肿瘤减灭术;腹腔热灌注化疗
腹膜转移(peritoneal metastases,PM)同时发生在大约17%的结直肠癌(colorectal cancer,CRC),复发的CRC中腹膜转移达到25%~50%。腹膜转移的治疗效果差,是CRC的第2大死亡原因。本文描述了2例异时性腹膜转移的结肠癌病例的多学科诊治过程,现总结如下。
一、结肠癌术后多发腹膜转移的MDT诊治报道(病例1)
(一)初诊情况
患者郑某,女性,46岁。因“右半结肠癌术后14月余,发现CA199升高7月余”于2015年03月20日收治入浙江大学医学院附属第二医院肿瘤外科。追溯病史:患者于2014年01月07日行“腹腔镜辅助下右半结肠癌根治术”。术后病理报告:(右半结肠)高分化腺癌,部分为粘液腺癌,溃疡型,大小4×3.5 cm,浸润至浆膜外,脉管侵犯阳性,两侧切缘均阴性,淋巴结1/48阳性(pT3N1M0)。术后患者接受XELOX方案化疗4周期后,自行停止化疗,末次化疗时间为2014年04月16日。2014年10月15日(术后9个月)复查时发现CA199升高,但CT等影像学检查阴性。之后患者的CA199持续升高,并伴随CA242也逐渐升高;于2015年01月(术后12个月)再行全腹增强CT扫描,仍未发现肿瘤复发转移迹象,因经济原因未行PET-CT检查。此次因CA199和CA242继续升高,而且腹部MRI检查提示:右侧结肠旁沟占位,考虑结肠癌术后复发,患者再次入院。此次入院,神清,精神可,胃纳可,二便无殊,近3个月内体重减轻2.5 kg。否认高血压、糖尿病、肝炎等病史,否认家族中肿瘤病史。
入院评估:体重指数(Body Mass Index,BMI)20.5 kg/m2;营养风险评分:1分;日常生活能力评分(activity of daily living,ADL)评级:I级;美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分:0分。查体:血压110/75 mmHg,全身浅表淋巴结未触及明显肿大,心肺无殊,腹平软,右中腹似可触及一个质硬肿块,较固定,腹部无压痛反跳痛,肝脾下界未触及。肛门指检:直肠内进指6 cm未及明显肠内外肿块,退出指套无染血。
入院检查:血尿粪三大常规、肝肾功能、凝血谱、肿瘤标记物等检查发现以下异常:血CA199:193.7 ng/mL;CA242:129.8 IU/ml;胸部高分辨平扫CT:未见转移;结肠镜检查:未见明显异常;腹部MRI:右侧结肠旁沟占位,考虑结肠癌复发;PET/CT:腹腔肠管间可见5~6处大小不一的软组织影,最大2.9 cm,放射性摄取明显升高,SUV max=6.83,考虑结肠癌复发(图1)。
初步诊断:结肠癌术后腹膜转移
(二)诊疗经过
1. MDT讨论及治疗情况(2015年3月22日)
放射科医师:阅读了患者住院前后影像资料,特别是从腹部增强MRI和PET/CT所见,结合病史及肿瘤标记物的结果,患者基本上可以诊断为结肠癌术后腹盆腔复发转移;胸部高分辨平扫CT:两肺及纵隔未见明显转移征象,未见明显感染。
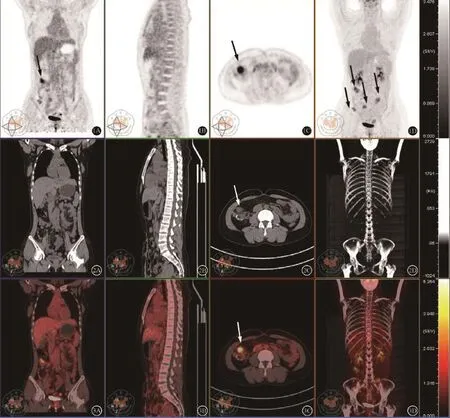
图1 结肠癌术后14个月(2015年3月)PET/CT:1A~3A和1D~3D是冠状位,1B~3B是矢状位,1C~3C是横断位。腹腔肠管间可见5-6处大小不一的软组织影(图中箭头处),最大2.9cm,放射性摄取明显升高,SUVmax=6.83,考虑结直癌复发
肿瘤外科医师:目前患者诊断为结肠癌术后腹膜多发转移,虽然从影像学上观察复发转移的病灶较局限,但是也有可能腹盆腔存在广泛细小的转移灶,对于这些细小腹膜转移灶的诊断目前还是比较困难的。对于这些病例的治疗建议,可以选择全身化疗也可以选择手术治疗,目前没有指南和规范推荐标准的治疗方案;但近几年国内外有些专家共识,推荐可以采用肿瘤减灭术(CRS)联合腹腔热灌注化疗(HIPEC)的治疗模式(CRS/HIPEC)治疗这类患者,我们中心也已添置腹腔热灌注治疗仪,对于这个患者可以考虑采用这类治疗模式。
肿瘤内科医师:目前患者转移的诊断基本明确,全身评估业已完善,建议首先检测原发灶全RAS基因的突变情况;另外患者原发灶病理是高分化腺癌,部分粘液腺癌,淋巴结有1颗转移,而术后的辅助化疗只做了4个周期,有欠缺,建议可先行几个周期全身化疗然后再考虑CRS/HIPEC;术前化疗的第一个目的是可以评估转移肿瘤对化疗的敏感性,第二个目的是可以控制其他微小转移灶,考虑到粘液腺癌的成分,且存在血浆-腹膜屏障,化疗的疗效可能较为有限,可结合RAS检测结果选择合适的靶向药物联合治疗。
总结:结合团队专家的意见,该患者术后转移的诊断是确立的,为结肠癌术后异时性多发腹膜转移,但从目前的影像资料来看转移灶较局限,有R0切除的机会。目前在全身化疗疗效不明确的情况下,可以考虑行剖腹探查术,根据探查情况行CRS/HIPEC,然后术后再行标准的全身化疗。根据目前资料对于这类患者如果能R0切除联合术中HIPEC, 5年的OS可以达到40%~50%。
2. 治疗情况
患者于2015年03月24日在全麻下行剖腹探查术,术中见:腹腔多发转移结节,分布腹盆腔7个区,最大约4.0 cm,最小0.5 cm,Sugarbaker 腹膜转移癌指数(Sugarbaker peritoneal carcinomatosis index,PCI)评分14分,术中决定行肿瘤减灭术,切除肉眼所有可见肿瘤及相邻的肠段,然后置引流管关腹行术中腹腔热灌注化疗(3 L生理盐水加入丝裂霉素C:30 mg,400 ml/分钟流量恒温43 ℃,腹腔循环灌注60 min;灌注过程中实时监测腹腔内温度,并密切监测患者体温)。术程顺利,术后恢复顺利。术后病理如图2,小肠切除标本:中分化腺癌;结肠肿块:中分化腺癌;盆腔结节:转移性中分化腺癌,明确为结肠癌腹腔多发转移。术后以mFOLFOX6方案化疗4个周期后,患者再次拒绝化疗,遂常规随访复查。二次术后8个多月后患者血CA199再次升高,并逐渐出现腹胀腹痛,肛门排气排便减少,考虑肠梗阻;又于2015年12月12日经MDT讨论后再次行剖腹探查发现盆腔及右髂窝多发种植肿瘤融合成团固定无法完整切除,遂行回肠造瘘术解除肠梗阻,并行肿瘤活检术再次明确结肠癌转移。目前患者仍然带瘤生存,从复发到现在获得了16个多月的OS。
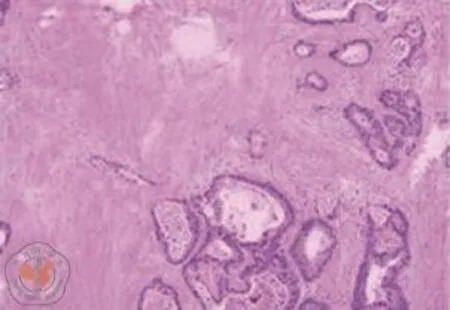
图2 肿瘤减灭术后病理
二、结肠癌术后单发腹膜转移的MDT诊治报道(病例2)
(一)初诊情况
患者,男性,53岁。“右半结肠癌术后10月余,发现腹腔结节10余天”于2015年03月04日收治入浙江大学医学院附属第二医院肿瘤外科。患者于2014年05月10日因当地医院诊断为升结肠癌,收治入浙江大学医学院附属第二医院,完善术前准备于2014年05月12日行“腹腔镜辅助下右半结肠癌根治术”,术后病理报告:(右半结肠)高分化腺癌,溃疡型,大小3×2.5 cm,侵至浆膜,两侧切缘均阴性。淋巴结0/35阳性(pT3N0M0)。术后未行辅助化疗,常规定期复查,于2015年03月01日(术后10月)开始发现CEA升高,遂行全腹增强CT扫描,结果提示:原手术疤痕右侧腹壁发现一2×2 cm结节,考虑肿瘤复发转移,遂收住入院。此次起病来,神清,精神可,胃纳可,二便无殊,体重无明显下降。否认高血压、糖尿病、肝炎等病史,否认家族中肿瘤病史。
入院评估:BMI:22.5 kg/m2;营养风险评分:1分;ADL评级:I级;ECOG评分:0分。查体:血压125/65 mmHg,全身浅表淋巴结未触及明显肿大,心肺无殊,腹平软,右中腹可触及一约2 cm质硬肿块,较固定,腹部无压痛反跳痛,肝脾下界未触及。肛门指检:进指7 cm未及明显肿块,退出指套无染血。
辅助检查:(2015年3月01日)血CEA:15.6 ng/mL;血细胞分析、肝肾功能等无明显异常,凝血谱未见明显异常。大便隐血阴性。胸部高分辨率CT:正常。结肠镜检查正常。CT:结果提示:原手术疤痕右侧腹壁发现一2×2 cm结节,考虑肿瘤复发转移。
初步诊断:(1)结肠癌术后腹膜转移;(2)结肠癌术后。
(二)诊疗经过
1. MDT讨论及治疗情况(2015年3月04日)
放射科医师:从增强CT所见,原手术疤痕右侧腹壁发现一2×2 cm结节,动脉期有明显增强,结合病史及肿瘤标记物的结果,可以诊断结肠癌术后腹壁转移。胸部高分辨率CT示,两肺及纵隔未见明显转移征象。必要时可考虑行PET/CT扫描,以排除其他部位的转移。
肿瘤外科医师:目前患者诊断为结肠癌术后腹膜单发转移,可考虑行PET/CT扫描,但对于细小腹膜转移灶的发现目前还是比较困难。对于腹膜转移的结直肠癌,全身化疗的有效率极其有限,而肿瘤减灭术联合腹腔热灌注化疗的治疗模式(CRS/HIPEC)是局限性腹膜转移的结直肠癌的最佳适应症,因此,对于这个患者可以考虑采用CRS/HIPEC。
肿瘤内科医师:目前患者诊断基本明确,同意行PET/CT扫描做全身评估。可以检测原发灶全RAS基因的突变情况;对于这个患者也可以先行几个周期全身化疗,然后再做CRS/HIPEC;化疗方案的选择可以选用标准两药化疗,也可以选择两药联合靶向药物。当然直接手术行CRS/HIPEC也是可行的。
总结:结合团队专家的意见,该患者可以先行PET/CT检查,如果仅是结肠癌术后单发转移,可以R0切除,目前在全身化疗疗效不明确的情况下,可以考虑行CRS/HIPEC,然后术后再行标准的全身化疗。这类患者有可能获得长期生存。
2.治疗情况
患者先完成PET/CT检查未发现其他病灶。于2015年3月06日全麻下行剖腹探查术,术中见:右侧腹壁单发结节,最大直径约2 cm,Sugarbaker 腹膜转移癌指数PCI评分2分,决定行肿瘤减灭术,切除肿瘤及相邻部分正常组织,然后关腹行术中腹腔热灌注化疗(3 L生理盐水加入丝裂霉素C:30 mg,400 ml/分钟恒温43 ℃循环灌注60 min)。术程顺利,术后恢复顺利。术后病理提示为结肠癌转移,粘液腺癌,断端切缘阴性。术后以XELOX方案化疗8个周期后,末次化疗时间2015年10月。后常规随访复查。目前无复发迹象。
三、讨论
结直肠癌发生腹膜转移后,往往被认为是终末期疾病,在TNM分期中归为M1b,姑息性的全身化疗是常规推荐的治疗手段。在多中心EVOCAPE研究中,5-FU 联合CF的化疗使结直肠癌腹膜转移的患者生存时间不超过7个月;而再联合奥沙利铂或伊立替康的化疗,也只能达到23.4个月的生存时间。然而从20世纪80年代以来,在腹膜转移的结直肠癌患者中引入了细胞减灭术(cytoreductive surgery,CRS)联合腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPEC)的治疗模式,给这部分患者带来了治愈的可能和明显的生存获益,总生存时间平均可达到46个月,5年生存时间(OS)可达51%[1-2]。
结直肠癌腹膜转移的临床症状多样并且无特异性。有些患者因为腹水和肠梗阻而表现出极度疲劳,腹部不适和腹痛等症状。而大约50%的腹膜转移患者的腹水的细胞学检查可以找到肿瘤细胞;另外,大约40%的患者可以通过CT,MRI,PET和超声等影像学检查而被诊断;还有约8%的患者是在开腹手术中被发现存在腹膜转移。因此早期诊断结直肠癌腹膜转移以及评估转移灶累及腹膜的范围,目前仍然比较困难[2-3]。
本次MDT病例是2例结肠癌伴异时性腹膜转移的患者,1例多发(术中探查发现腹盆腔转移病灶多于术前的影像学评估),1例单发。目前用于评估腹腔内肿瘤负荷及播散范围的可量化的评分系统主要是Sugarbaker 腹膜转移癌指数(PCI),研究发现PCI <6分,结直肠癌腹膜转移患者的 4年OS 为 44%,而PCI >19分,4年OS 仅为 7%。与结直肠癌腹膜转移患者OS相关的另外一个因素是肿瘤减灭术(CRS)完全程度。CRS的完全性以细胞减灭术完全性分级(completeness of cytoreduction,CC)进行评估。在众多的CC评分系统中,Jacquet 和Sugarbaker的CC分级系统应用最为广泛,只要残留肿瘤组织小于0.25 cm都认为是完全性肿瘤减灭术[1-2]。因为从理论上讲,0.25 cm以下的肿瘤组织可以被腹腔内热灌注化疗(HIPEC)杀灭。因此,对于结直肠癌的腹膜转移患者,评估病变范围极其重要,对于较局限的腹膜转移患者,多学科的综合诊治和积极的治疗手段能改善这部分患者的生存时间和生存质量。
[ 1 ] 孙立峰, 童舟, 丁克峰.外科肿瘤细胞减灭术联合腹腔内热灌注化疗-结直肠癌腹膜转移治疗的突破方向[J]? 中华结直肠疾病电子杂志, 2015, 4(3): 234-239.
[ 2 ] Arjona-Sánchez A, Medina-Fernández FJ, Muñoz-Casares FC, et al. Peritoneal metastases of colorectal origin treated by cytoreduction and HIPEC: An overview [J]. World J Gastrointest Oncol, 2014,6(10): 407-412.
[ 3 ] Anke M. J. Kuijpers, Boj Mirck, et al. Cytoreduction and HIPEC in The Netherlands: Nationwide Long-term Outcome Following the Dutch Protocol [J]. Ann Surg Oncol,2013, 20(13): 4224-4230.
Two case reports of colon cancer peritoneal metastases treated by multidisciplinary team
Wang Zhanhuai, Sun Lifeng, Yuan Ying, Ding Kefeng, Zhang Suzhan.
Department of Surgical Oncology, The Second Hospital Affiliated of Zhejiang University School of Medicine, Hangzhou 310009, China
Sun Lifeng, Email: sunlifeng@zju.edu.cn
This article describes that 2 cases of heterochronic colon cancer peritoneal metastases were treated by multidisciplinary team (MDT). One case was colon cancer with multiple metastases, and the other case was single metastasis. After MDT discussion both patients were underwent cytoreductive surgery combined with hyperthermic intraperitoneal chemotherapy (CRS/HIPEC), the patient with single metastasis obtained the DFS of 16 months, and multiple metastases patient achieved more than 16 months of OS. Currently some study revealed that the OS of colorectal cancer patients with peritoneal metastases was associated with completeness of cytoreduction (CC), the disease burden (peritoneal cancer index, PCI), etc. Therefore, for patients with peritoneal metastasis of colorectal cancer, assessmemt of the extent of metastases is extremely important, if peritoneal metastasis is relatively limited, multi-disciplinary comprehensive treatment, and radical treatment approach may improve these patient′s overall survival and quality of life.
Colorectal neoplasms;Neoplasm metastasis;Cytoreduction;Hyperthermic intraperitoneal chemotherapy
2016-07-02)
(本文编辑:杨明)
10.3877/cma.j.issn.2095-3224.2016.04.016
310009杭州,浙江大学医学院附属第二医院肿瘤外科
孙立峰,Email:sunlifeng@zju.edu.cn
王展怀, 孙立峰, 袁瑛, 等. 腹膜转移的结肠癌患者MDT诊治二例[J/CD]. 中华结直肠疾病电子杂志, 2016, 5(4): 351-354.
