胶原纤维在[Emim]Br离子液体中溶解机理的初步研究
2016-10-20韩雪梅
李 那,韩雪梅,邓 宇
(天津科技大学化工与材料学院,天津300457)
胶原纤维在[Emim]Br离子液体中溶解机理的初步研究
李那,韩雪梅,邓宇
(天津科技大学化工与材料学院,天津300457)
胶原纤维与[Emim]Br离子液体固液比一定时,考察溶解时间、溶解温度对胶原纤维在离子液体中的溶解的影响,得出在溶解温度140℃、溶解时间60min的溶解量最大为13.9%;并通过FT-IR、SEM分析初步探究胶原纤维在离子液体中的溶解机理。
胶原纤维;离子液体;溶解
我国传统制革工业的特征是原料的高投入、低产出、高消耗。大约每年有140万t的制革废弃物[1],这些废弃物中又有约80%的胶原蛋白被废弃浪费[2],未实现其利用价值。这一方面污染了环境,另一方面又浪费了资源。
胶原纤维具有很好的韧性和热稳定性,这是因为胶原分子的多肽链内和链间存在着氢键、离子键、范德华力键等,保持了胶原的螺旋稳定性结构。并且,胶原3股螺旋的旋转方向与构成它们的多肽链的旋转方向相反,不易解旋,所以很难溶于普通溶剂。有文献报道离子液体可以作为天然高分子物质的溶剂[3-10],且离子液体具有低挥发、不可燃和热稳定性好的特点。天然高分子的溶解机理属于EDA理论[11](electrondonor-electronacceptor),即氢键破坏理论。
本着将废弃皮革回收利用、降低原料成本及减少环境污染的研究目的,以胶原纤维作为原料,研究了溶解时间、溶解温度对胶原纤维在[Emim]Br离子液体中溶解效果的影响,并初步探究了其溶解机理。
1 实验部分
1.1仪器与试剂
1.1.1主要仪器
DK-98-1电热恒温水浴锅(天津市泰斯特仪器有限公司);SHB-III循环水式多用真空泵(郑州长城科工贸有限公司);JT302N电子天平(上海精密科学仪器有限公司);DH-101电热恒温鼓风干燥箱(天津市中环实验电炉有限公司);RE-52A旋转蒸发仪(上海亚荣生化仪器厂);WQF-510傅里叶变换红外光谱仪(北京第二光学仪器厂);JMS-6380LV扫描电子显微镜(日本电子公司)。
1.1.2主要试剂
溴化-3-甲基-1-乙基咪唑离子液体([Emim]Br)(实验室制备);
KBr(光谱醇,天津市大茂化学试剂厂);胶原纤维(天津科技大学材料科学与化学工程学院皮革研究室)。
1.2胶原纤维在离子液体中的溶解
称取1g胶原纤维置于盛有15g离子液体的50mL三口瓶中,在油浴中加热搅拌。在一定温度下溶解;一定时间后迅速进行真空抽滤,将滤渣洗净后干燥称重,计算胶原纤维在离子液体中的溶解量;滤液静置一定时间后再过滤,滤液用旋转蒸发仪旋蒸回收再利用。
1.3胶原纤维在离子液体中溶解机理的初步研究
1.3.1FT-IR分析
1.3.1.1胶原纤维的FT-IR分析
取100mg左右的KBr,将其与1mg胶原纤维和不同溶解时间后的残渣分别在玛瑙研钵中研成粉末,装到模具中,放在压片机上控制压力在6~8MPa、1min后减压,制得透明薄片,采集样品谱图,根据谱图中氢键变化初步探究胶原纤维在离子液体中的溶解机理。
1.3.1.2离子液体的FT-IR分析
取100mg左右的KBr,在玛瑙研钵中研成粉末装到模具中,放在压片机上控制压力在6~8 MPa、1min后减压,制得透明薄片,将离子液体均匀涂抹到KBr片上采集样品谱图。
1.3.2SEM分析
对溶解前后的胶原纤维进行喷金处理后,采用JMS-6380LV扫描电子显微镜分别于×500、×1000和×5000条件下观察样品形貌,进行SEM分析。
1.4离子液体的回收
将离子液体用旋转蒸发器蒸发回收,计算离子液体的回收率。

式中:W是离子液体的回收率(%);m是回收到的离子液体量(g);m0是加入的离子液体量(g)。
2 结果与讨论
2.1离子液体对胶原纤维溶解效果的影响
2.1.1溶解温度对胶原纤维在离子液体中溶解效果的影响
实验条件:固定胶原纤维和离子液体的固液比为1∶15,在一定的溶解温度下溶解一定时间。胶原纤维为1g,离子液体为15g,溶解时间为60 min,改变胶原纤维在离子液体中的溶解温度,探究不同溶解温度对胶原纤维在离子液体中溶解效果的影响,结果见图1。

图1 溶解温度对胶原纤维在离子液体中溶解效果的影响
如图1所示,胶原纤维在离子液体中的溶解效果是随着溶解温度的增加呈现先增加后降低的趋势。随着温度的升高,胶原纤维在离子液体中的溶解量也随之增大;当温度达到140℃时,胶原纤维的溶解量最大,为13.9%;温度高于140℃,胶原纤维的溶解量又降低。这是因为在低温时,离子液体的黏度大、流动性差,从而使传质传热速率较低,降低了胶原纤维的溶解;随着溶解温度的升高,离子液体中分子间运动速率加快,促进了胶原在离子液体中的溶解;温度继续升高时,胶原纤维分子出现降解,降低了它的溶解量。因此,选择140℃为胶原纤维在离子液体中溶解的最佳溶解温度。
2.1.2溶解时间对胶原纤维在离子液体中溶解效果的影响
实验条件:固定胶原纤维和离子液体的固液比为1∶15,在一定的溶解温度下溶解一定时间。胶原纤维为1g,离子液体为15g,溶解温度为140℃,改变胶原纤维在离子液体中的溶解时间,探究不同溶解时间对胶原纤维在离子液体中溶解效果的影响,结果见图2。

图2 溶解时间对胶原纤维在离子液体中溶解效果的影响
如图2所示,胶原纤维在离子液体中的溶解效果是随着溶解温度的增加呈现先增加后降低的趋势。随着溶解时间的延长,胶原纤维的溶解量逐渐增多,溶解时间为60min时,溶解量最大,为13.9%;之后溶解量又降低。这可能是因为胶原纤维在溶解过程中是有非结晶区到结晶区的溶胀过程,加之胶原纤维的结构不一性,它的溶胀程度和完整性就难以控制和实现。溶解时间较短时,胶原纤维仅发生溶胀,或少量的开始溶解,此时溶解量较低;随着时间的增加,胶原纤维充分溶胀,减弱了离子液体与胶原纤维分子间的相互作用力,同时增大了胶原纤维与离子液体的接触面积,有利于胶原纤维在离子液体中的溶解;但时间越长,胶原纤维也越容易发生降解,所以胶原纤维的溶解量又降低。因此,选择60min为较佳溶解时间。
2.2离子液体对胶原纤维溶解机理的初步研究
2.2.1FT-IR分析
实验条件:胶原纤维在140℃条件下溶解不同时间(a—胶原纤维;b—溶解30min;c—溶解45min;d—溶解60min),分析在不同溶解时间下胶原纤维中氢键的变化情况,结果见图3。
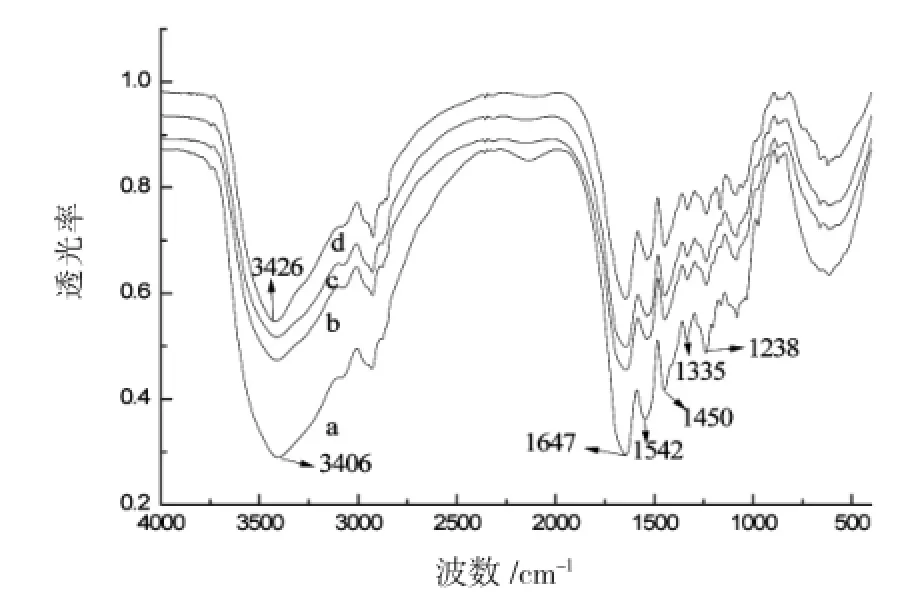
图3 胶原纤维的FT-IR谱图
如图3所示,图中3406cm-1处是N—H的伸缩振动峰,代表胶原纤维分子链间的氢键;1647 cm-1处对应酰胺Ⅰ带的C——O伸缩振动峰,1542 cm-1处对应酰胺Ⅱ带N—H的面内变形振动峰,1450cm-1、1335cm-1处对应酰胺Ⅲ带C—N伸缩和N—H变形振动峰,657cm-1对应酰胺Ⅳ带、Ⅴ带O——C—N变形振动峰;1450~1230cm-1附近的吸收峰,表示胶原纤维存在3股螺旋结构的存在性。
由图3可知,随着溶解时间的延长,代表胶原纤维分子链间氢键的吸收峰由3406cm-1处显著地移动到了3426cm-1处,N—H的伸缩振动峰向高频方向前移了20cm-1,吸收谱带变窄、吸收强度减弱,说明在溶解过程中胶原纤维的氢键逐渐发生了变化。原因为在加热和搅拌力的作用下,[Emim]Br离子液体破坏了胶原纤维分子链间-NH基团中的H原子和-COO基团中的O原子相互作用形成的氢键,导致N—H的伸缩振动峰频率发生改变,而这一点,恰好符合EDA理论。
根据EDA理论,在本实验中,[Emim]Br离子液体受热发生解离,形成游离态的[Emim]+阳离子和Br-阴离子,Br-充当EDA理论中的电子给予体,而[Emim]+充当电子接受体中心,搅拌时,游离的[Emim]+阳离子和Br-阴离子相应地和胶原纤维胶原分子链-NH基团中的H原子和-COO基团中的O原子相互作用,胶原分子链间氢键遭到破坏,分子链断裂分散,最终实现胶原纤维在[Emim]Br离子液体中的溶解,见图4。
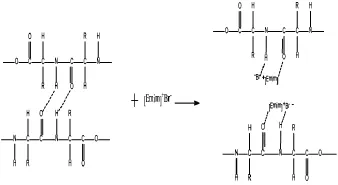
图4 胶原纤维在[Emim]Br离子液体中的溶解机理图
2.2.2SEM分析
通过SEM可以形象地观察与对比溶解前后胶原纤维形态的变化。图5为胶原纤维溶解前后放大倍数分别为×500(a、d)、×1000(b、e)和×5000(c、f)的SEM照片。

图5 胶原纤维在[Emim]Br离子液体中溶解前后的SEM图
由图5可以看出,胶原纤维经[Emim]Br离子液体溶解后,与溶解前具有明显差异。未经过[Emim]Br离子液体溶解的胶原纤维3股螺旋结构明显,胶原卷曲折叠、互相缠绕,形成坚实紧密的空间结构;而经过[Emim]Br离子液体溶解后的胶原纤维,其空间结构出现了不同程度的空洞,且排列松散,部分胶原遭到破坏后无明显的螺旋状纤维结构,并逐渐趋于碎片化、松散化、凌乱化。这可能是因为[Emim]Br离子液体破坏了胶原多肽链间对维持胶原螺旋结构稳定起重要作用的氢键,使胶原分子链断开,使胶原的强度和结构稳定性下降,纤维结构不再硬挺紧锁,而是趋向于空洞化、松散化。
2.3离子液体的回收
2.3.1离子液体的回收率
滤液用旋转蒸发器旋蒸回收,离子液体的回收率如表1。

表1 离子液体的回收率
2.3.2离子液体FT-IR表征
离子液体和第3次回收后的[Emim]Br离子液体的FT-IR图,见图6。

图6 [Emim]Br离子液体回收前后FT-IR图
由图6可以看出,第3次回收后的[Emim]Br离子液体与使用之前的[Emim]Br离子液体基团谱图基本一致,说明在使用了3次后[Emim]Br离子液体基团未发生变化。[Emim]Br离子液体至少可以循环使用3次,且回收率可稳定在94.89%,具有很好的重复利用性,可以很好地节约实验成本。
3 结论
(1)通过考察溶解时间、溶解温度对胶原纤维在离子液体中的溶解,得出在溶解温度为140℃、溶解时间为60min时的溶解量最大,为13.9%。
(2)初步判定胶原纤维在离子液体中的溶解机理符合EDA理论。
(3)离子液体作为溶剂可回收重复使用。
[1]AlvesDosRM,BelezaV.Utilizationofleatherwaste:animalfeedstuffchromeshavings[J].JSocLeatherTechnol Chem,1991,75(1):15-19.1991,75(2):45-47.
[2]TaylorMM,DiefendorfEJ,ThompsonCJ.Effectofprocessingvariablesonashcontentofgelableandhydrolyzedproteinproductsisolatedfromtreatmentof chromiumleatherwaste[J].JAmLeatherChemAssoe,1996,91(6):271-273.
[3]周雅文.胶原纤维在离子液体中的溶解特性研究[J].中国皮革,2010,39(7):22-27.
[4]付飞飞.胶原纤维在不同离子液体中溶解特性的研究与比较[J].中国皮革,2010,39(23):21-24.
[5]严国良,谢桂军,陈小军,等.丝素蛋白在离子液体中的溶解特性研究[J].合成技术与应用,2009,24(4):1-5.
[6]张慧慧,胡晨光,邵惠丽,等.丝素在离子液体中的溶解及再生丝素纤维的结构[J].高分子材料科学与工程,2011,27(7):66-68.
[7]XieHB,LiSH,ZhangSB.Ionicliquidsasnovelsolventsforthedissolutionandblendingofwoolkeratin fibers[J].GreenChemistry,2005,7(18):606-608.
[8]王明,汪青,王怀芳,等.用离子液体溶解羊毛纤维的研究[J].中原工学院学报,2010,21(6):52-54.
[9]赵玲,汤尧旭,赵瑞方,等.羽毛在离子液体中的溶解及再生研究[J].毛纺科技,2010(8):1-5.
[10]汤尧旭,赵玲,覃发正,等.猪皮胶原蛋白在1-丁基-3-甲基氯代咪唑中的溶解性能[J].皮革科学与工程,2010,20(1):5-12.
[11]RicoED,CynthiaC,AlR,eta1.Tetraa1kylphophonium-basedionicliquids[J].JOrganometallicChem,2005(690):2536.
10.13752/j.issn.1007-2217.2016.01.004
2015-09-07
