雪菊花黄酮分散片的处方工艺研究
2016-10-19龚飞戴青郁建平
龚飞 戴青 郁建平

摘要:对雪菊花黄酮分散片的处方工艺进行优化,以崩解时间、片剂表面形态或软材制备情况为考察指标,通过单因素以及正交试验,考察不同辅料的种类及用量对雪菊花黄酮分散片的影响,确定最佳处方。结果表明,最佳处方工艺为25%雪菊花提取物,64%微晶纤维素(MCC),5%交联聚乙烯吡咯烷酮(PVPP),5%低取代羟丙基纤维素(L-HPC)和1%硬脂酸镁,其崩解时间为(63±5)s。采用此工艺所制备的雪菊花黄酮分散片溶出度高,分散均匀性好,质量可控,满足速释的要求,具有一定的开发和利用价值。
关键词:雪菊花;黄酮;分散片;制备工艺
中图分类号:S567.21+9;R284 文献标识码:A 文章编号:0439-8114(2016)06-1526-04
DOI:10.14088/j.cnki.issn0439-8114.2016.06.041
雪菊又名血菊,学名为两色金鸡菊(Coreopsis tinctoria Nutt.),是菊科金鸡菊属的一年生草本植物,主要生长在中国新疆昆仑山脉[1]。雪菊花作为一种药食两用资源,长期冲泡饮用,具有清热解毒、活血化瘀健胃健脾的功能,可用于心慌、痢疾等病症,同时可降低血压和血脂[2-4]。雪菊花作为一种药用植物,具有抗炎[5]、抗癌[6,7]、抗病毒[8]以及抗糖尿病等作用[9,10]。雪菊花中黄酮类化合物是主要有效成分,总黄酮含量达到12%以上,远超过其他菊类[11]。分散片具有在水中迅速崩解,分散均匀,制备工艺简单,生物利用度高的特点[12,13]。分散片稳定性好,服用方便,携带简单,特别适合老幼及吞咽困难患者[14]。该研究旨在对雪菊花黄酮分散片进行初步研究,以期为雪菊花进一步开发和利用提供参考。
1 材料与方法
1.1 仪器
HZY-A200型电子天平(福州华志科学仪器有限公司),TDP-6A型单冲压片机(南通市华宇制药机械有限公司),CJY-300D型片剂脆碎度测定仪、LB-2D型崩解时限测定仪、RCZ-6B3型药物溶出度仪、YPD-300C智能片剂硬度测定仪。
1.2 试剂
雪菊花总黄酮(自制,经紫外分光光度计检测,含量>50%),芦丁(含量>99.9%,上海源叶生物科技有限公司),微晶纤维素(MCC)、预胶化淀粉、低取代羟丙基纤维素(L-HPC)、羧甲基淀粉钠(CMS-Na)(湖州展望化学药业有限公司),交联聚乙烯吡咯烷酮(PVPP,上海金穗生物科技有限公司),硫酸钙(AR,天津市科密欧化学试剂有限公司),糊精(辽宁东源药业有限公司),可溶性淀粉(安徽山河药用辅料股份有限公司),滑石粉(广西龙胜华美滑石开发有限公司),PEG-4000(湖南尔康制药股份有限公司),PEG-6000(辽陽奥克纳米材料有限公司),硬脂酸镁(北京化学试剂有限公司),无水乙醇、95%乙醇(AR,天津市富宇精细化工有限公司),试验用水均为双蒸水。
1.3 片剂的制备
将原、辅料分别过100目筛后充分干燥,按处方比例混匀后加50%乙醇溶液制软材,24目筛制粒,50 ℃干燥30 min,24目筛整粒,外加崩解剂及润滑剂,混合均匀后压片。
2 结果与分析
2.1 辅料的选择
2.1.1 填充剂的选择 按处方量加入25%主药、64%填充剂、10%崩解剂和1%的润滑剂,按“1.3”制备分散片,选用硫酸钙、糊精、预胶化淀粉、微晶纤维素作为填充剂,以片剂表面形态和崩解时间为考察指标,优选填充剂种类,试验结果见表1。选用预胶化淀粉和微晶纤维素作为组合对象,按比例1∶2、1∶1、2∶1进行试验,以片剂表面形态、崩解时间和硬度作为考察指标,优选填充剂合适的组合,试验结果见表2。由表1和表2的比较可知,选用微晶纤维素作为填充剂崩解时间和硬度都较为适中,综合考察,选用微晶纤维素作为填充剂较为合适。
2.1.2 崩解剂的选择 以微晶纤维素作为填充剂,按“1.3”制备分散片,分别选用PVPP、L-HPC、CMS-Na 3种崩解剂作为考察对象,采用L9(34)设计正交试验,以崩解时间作为考察指标,确定崩解剂的用量及种类,试验设计见表3,结果及分析见表4,方差分析见表5。由表5可知,以崩解时间作为评价指标,影响因素主次为A>B>C,且A因素对于崩解时间有显著影响(P<0.05)。由于C因素对于崩解时间的影响较小,根据正交试验以及实际结果,确定最优的处方为A3B3,即以1.0 g PVPP和1.0 g L-HPC为崩解剂的组合方式。
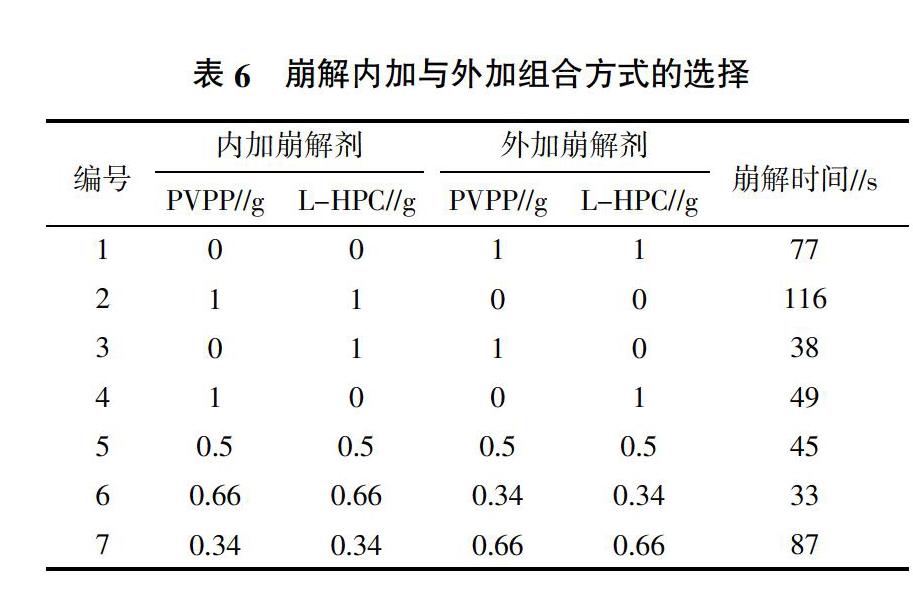
2.1.3 崩解剂加入方式的选择 按照“1.3”的制备方法,拟采用崩解剂内加、外加以及内外加的方式进行试验,组合方式见表6。由表6可知,组合6的加入方式崩解时间最短,为最优的组合方式,即采用崩解剂内加与外加相结合的方式,内加与外加的比例为2∶1,即内加0.66 g PVPP、0.66 g L-HPC和外加0.34 g PVPP、0.34 g L-HPC。
2.2 崩解时限及分散性测定
按照《中国药典》2010年版二部附录ⅩA崩解时限检查法,分别取3批样品各6片,置于(37±1) ℃水中测定崩解时限,测得崩解时间为(63±5)s,符合《中国药典》对于分散片的质量要求。按照《中国药典》2010年版二部附录ⅠA片剂方法检查,分别取3批样品各6片,置250 mL烧杯中,加15~25 ℃的水100 mL,振摇3 min,分散片在水中能全部崩解,且均能通过二号筛。
2.3 含量测定
2.3.1 标准曲线的制备 准确称取100 ℃烘干至恒重的芦丁标准品25.0 mg,置于50 mL容量瓶中,加适量70%乙醇使其完全溶解后,定容,即得到0.5 mg/mL芦丁标准品溶液。分别量取上述芦丁标准品溶液0.0、1.0、2.0、3.0、4.0、5.0、6.0、7.0 mL于25 mL容量瓶中,分别加入5%的亚硝酸钠溶液1 mL,摇匀,放置6 min,然后各加入10%的硝酸铝溶液1 mL,摇匀,放置6 min,最后各加入5%的氢氧化钠溶液5 mL,用70%的乙醇溶液进行定容,放置15 min。以第一管试剂溶液做空白,在505 nm波长处测定吸光度。以浓度C为横坐标,吸光度A为纵坐标,得到线性回归方程A=11.978C-0.002 3,R2=0.999 8,浓度在0.02~0.10 mg/mL范围内线性关系良好。
2.3.2 稳定性试验 取同一批次分散片粉末,称取240 mg,置于50 mL容量瓶中,加入适量60%乙醇,超声波溶解5 min,样品过0.45 μm微孔滤膜。取滤液0.5 mL于25 mL容量瓶中,按“2.3.1”操作,在505 nm处每隔10 min测定一次吸光度。结果表明,样品在30 min内稳定性良好,RSD为0.63%。
2.3.3 精密性试验 取“2.3.2”样品溶液,按“2.3.1”操作,在505 nm处连续测定吸光度6次,结果表明,仪器精密度良好,RSD为0.15%。
2.3.4 重现性试验 取同一批次分散片样品6份,按“2.3.2”制备供试品溶液。取滤液0.5 mL于25 mL容量瓶中,按“2.3.1”操作,在505 nm处测定吸光度,RSD为0.32%,表明该方法重现性良好。
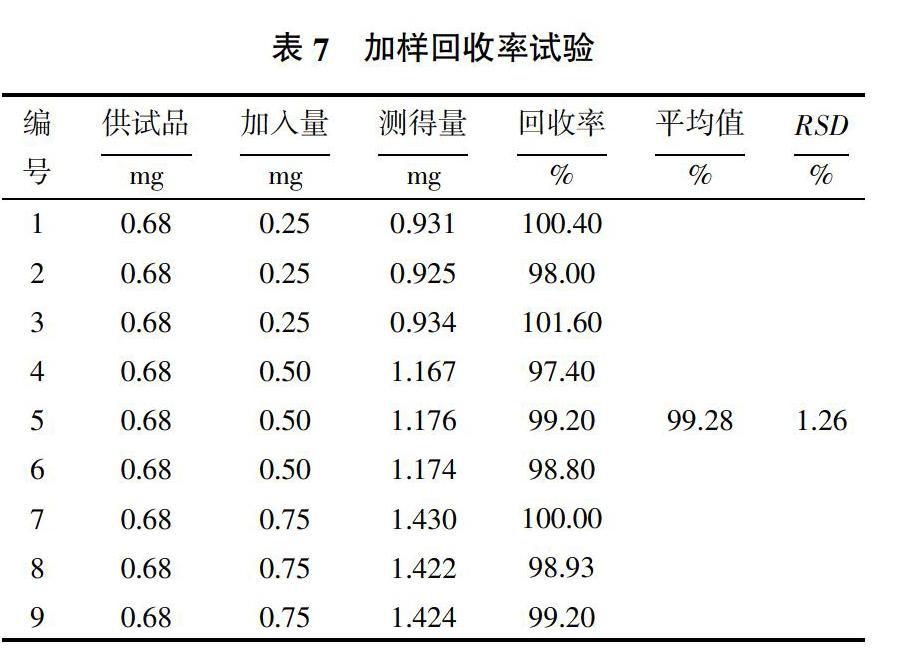
2.3.5 加样回收率试验 取同一批次已知含量分散片粉末9份,每份为420 mg,按“2.3.2”制备供试品溶液。精密量取0.5 mL供试品溶液于25 mL容量瓶中,再分别加入0.5 mg/mL芦丁标准品溶液0.5、1.0、1.5 mL,按“2.3.1”操作,在505 nm处测定吸光度,计算回收率,结果见表7。由表7可知,平均回收率为99.28%,RSD为1.26%,表明本方法的加样回收率试验符合要求,说明该方法作为含量测定方法是可行的。
2.3.6 样品含量测定 分别取雪菊花黄酮分散片三批,每批20片,研细。分别称取约240 mg置于50 mL容量瓶中,加入适量60%乙醇溶液,超声波溶解5 min,样品过0.45μm微孔滤膜。量取0.5 mL滤液于25 mL容量瓶中,按“2.3.1”操作,计算得总黄酮含量为68.10 mg/片。
2.4 溶出度测定
取雪菊花总黄酮分散片,按《中国药典》2010年版二部附录ⅩC溶出度测定法中第一法操作,以900 mL脱气蒸馏水、pH 1.0盐酸溶液、pH 4.0乙酸缓冲液、pH 6.8磷酸缓冲液作为溶出介质,温度(37±0.5) ℃,转速为50 r/min,并分别于1、5、10、15、30、45 min取样10 mL,并同时补充10 mL等温溶出介质,样品立即用0.45μm微孔滤膜过滤,移取5 mL溶液于25 mL容量瓶中,按“2.3.1”处理,测定吸光度,计算出各个时间点的累积溶出度(图1)。由图1可知,以pH 1.0盐酸缓冲液、pH 4.0乙酸缓冲液作为溶出介质,在30 min时,累积溶出度都小于85%,以pH 6.8磷酸缓冲液、蒸馏水作为溶出介质时,在5 min时溶出度均超过85%,能达到速释的要求。以pH 6.8磷酸缓冲液作为溶出介质,较蒸馏水只是释放速度稍快。综合考察,选用蒸馏水作为溶出介质,既满足要求又能够节省原料,符合要求。
3 讨论
雪菊花作为一种药食两用的植物资源,黄酮含量较高,提高其药用价值,具有良好的应用前景。研究对雪菊花黄酮分散片进行制备,优选的制备工艺明显降低了其崩解时间,分散均匀性也符合规定,选用的溶出介质显著的提高了黄酮的溶出度,达到速释的要求。
在研究中曾以单因素考察硬脂酸镁、滑石粉、PEG-4000以及PEG-6000作为润滑剂对分散片的影响。试验结果表明,硬脂酸镁作为润滑剂所制备的分散片更加光滑、平整、有光泽,且崩解时间、分散均匀性均符合要求。综合考虑选用硬脂酸镁作为润滑剂较为合适。
在黏合剂的选用预试验过程中,考察过5%淀粉浆、1%淀粉浆、蒸馏水、50%乙醇以及95%乙醇。试验结果表明,50%乙醇作为黏合剂,制得的软材适中,颗粒粉末比例均匀,休止角、压缩度以及崩解时间均较小。综合考察,选用50%乙醇作为黏合剂较为合适。
在研究中,制备分散片采用的是湿法制粒压片法, 其制备工艺的关键在于制得粉末的流动性要好。用优化处方制备的分散片崩解迅速,硬度合适,脆碎度较好,溶出度高,且其制备工艺简单、可行,适合工业化生产。
参考文献:
[1] 吴 瑛,王秀芳,袁守亮.响应面分析昆仑雪菊水溶性黄酮类化合物的提取工艺[J].食品科学,2013,36(6):129-133.
[2] LIU W X,DENG J H,XU H. Pharmacognostical studies on the flower of species Coreopsis sp.[J].Journal of Medicine and Pharmacy of Chinese Minorities,2009(1):24-25.
[3] 兰 卫,赵保胜,李玉清,等.昆仑雪菊中多种含量成分的测定[J].中国实验方剂学杂志,2012,18(10):101-103.
[4] 张彦丽,阿布都热合曼·合力力,阿依吐伦·斯马义.苯酚-硫酸法测定维吾尔药昆仑雪菊多糖含量的研究[J].药物分析杂志,2010,30(11):2205-2207.
[5] MOTOHIKO U,TOSHIHIRO A,KEN Y,et al.Constituents of compositae plants.2. Triterpene diols,triols,and their 3-O-fatty acid esters from edible chrysanthemum flower extract and their antiinflammatory effects[J]. Journal of Agricultural and Food Chemistry,2001,49(7): 3187-3197.
[6] KEN Y,TOSHIHIRO A,YOSHIMASA K,et al.Inhibitory effect of heliantriol C: A component of chrysanthemum,on tumor promotion by 12-O-tetradecanoylphorbol-13-acetate in two-stage carcinogenesis in mouse skin[J].Phytomedicine,1998(5):215.
[7] UKIYA M,AKIHISA T,TOKUDA H,et al.Constituents of compositae plants III. Anti-tumor promoting effects and cytotoxic activity against human cancer cell lines of triterpene diols and triols from edible chrysanthemum flowers[J]. Cancer Letters,2002,177(1):7-12.
[8] HU C Q,CHEN K,SHI Q,et al.Anti-AIDS agents,10. Acacetin-7-O-beta-D-galactopyranoside, an anti-HIV principle from Chrysanthemum morifolium and a structure-activity correlation with some related flavonoids[J].Journal of Natural Products,1994,57(1):42-51.
[9] 張淑鹏,李琳琳,木合布力·阿布力孜,等.昆仑雪菊对α葡萄糖苷酶的抑制作用[J].现代生物医学进展,2011,11(6):1055-1058.
[10] 张 燕,李琳琳,木合布力·阿布力孜,等.新疆昆仑雪菊5种提取物对α-葡萄糖苷酶活性的影响[J].中国实验方剂学杂志,2011,17(7):166-169.
[11] 买买提·艾买提,木合布力·阿布立孜,孟 磊.新疆昆仑雪菊水溶性总黄酮含量的测定[J].海峡药学,2010,22(10):56-58.
[12] 苏占辉,王书君,张滋明,等.金银花总黄酮分散片处方工艺优选[J].中国实验方剂学杂志,2013,19(6):8-11.
[13] 左安刚,周 英,李 俐,等.山楂叶总黄酮分散片的研制[J].中国实验方剂学杂志,2011,17(11):26-29.
[14] 张兆旺.中药药剂学专论[M].北京:人民卫生出版社,2009.
