高效液相色谱法同时测定金银花中的六种成分
2016-10-19梁恕坤
梁恕坤
摘要:建立同时测定金银花(Lonicera japonica Thunb.)中绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素含量的高效液相色谱法。采用Aglient phenyl柱(4.6 mm×250 mm,5 μm),流动相乙腈(A)-0.5%醋酸(B)为流动相梯度洗脱,在波长365 nm检测绿原酸、在波长327 nm检测咖啡酸,在波长358 nm检测芦丁、金丝桃苷、木犀草苷,在波长368 nm检测槲皮素,柱温40 ℃,进样量10 μL。结果表明,6种化合物分别在测定范围内呈现良好的线性关系,回收率为96.85%~103.61%。该方法准确、快速、简单地进行金银花中6种成分的测定。
关键词:金银花(Lonicera japonica Thunb.);绿原酸;咖啡酸;芦丁;金丝桃苷;木犀草苷;槲皮素;高效液相色谱
中图分类号:O657.72 文献标识码:A 文章编号:0439-8114(2016)08-2100-02
DOI:10.14088/j.cnki.issn0439-8114.2016.08.046
Abstract:To develop an HPLC method for the determination of chlorogenic acid,caffeic acid, rutin, hyperoside,luteoloside, quercetin in Lonicera japonica Thunb. The analysis was carried out on an Aglient phenyl column(4.6 mm×250 mm,5 μm) by a gradient elution using(A) acetonitrile-(B)water(0.5% HAc),the detection was set at UV 365 nm to detecte chlorogenic acid,UV 327 nm to detecte caffeic acid,UV 358 nm to detecte rutin,hyperoside,luteoloside,UV 368 nm to detecte quercetin. The column temperature was 40 ℃ and injection volume was 10 μL. The recovery of the method was in the range of 96.85%~103.61%,and the six compounds showed good linear relationship in a detected concentration range. The method was proved to be precision,repeatability, simple and accurate.It was successfully applied to the analysis of the 6 components in Lonicera japonica Thunb.
Key words: Lonicera japonica Thunb.; chlorogenic acid;caffeic acid; rutin; hyperoside; luteoloside; quercetin; HPLC
金银花(Lonicera japonica Thunb.)是忍冬科植物忍冬、红腺忍冬、山银花或毛花柱忍冬的干燥花蕾或带初开的花,主产区为山东平邑等地。药理研究表明,金银花具有抗菌、抗病毒、护肝、解热、止血、抗氧化、降血脂等多种功效[1,2],主要含有绿原酸、咖啡酸、奎宁酸、阿魏酸等有机酸,还含有芦丁、金丝桃苷、木犀草苷、槲皮素等黄酮成分,有机酸和黄酮是金银花抑菌抗病毒的主要活性成分[3,4]。2010年版中国药典将绿原酸和木犀草苷作为金银花药材的质量控制指标,采用C18柱和苯基柱分别测定,不利于快速鉴定金银花药材的成分。金银花的成分分析一般采用C18柱,而使用苯基柱且采用变换波长同时测定金银花中的6种成分,尚未见文献报道,该方法简单、快速、准确地分析金银花的质量。
1 仪器与试药
1.1 仪器
LC-10Atvp型高效液相色谱仪(日本岛津公司);SP-UV2000型紫外可见分光光度计(上海光谱仪器有限公司);电子天平(日本AN公司)。
1.2 试药
绿原酸、木犀草苷(中国药品生物制品检定所);芦丁、咖啡酸(北京希凯创新科技有限公司);槲皮素(天津马克生物技术有限公司);金丝桃苷(TREECHEM,编号Th110020);乙腈、乙醇为色谱纯,水为石英亚沸蒸馏水。
1.3 药材
本地金银花采自平邑魏庄、郑成九间棚;外地金银花购于各大超市、药店。
2 方法与结果
2.1 色谱条件
色谱柱为Aglient phenyl柱(250 mm×4.6 mm,5 μm),乙腈為流动相乙腈A,0.5%醋酸为流动相B,洗脱程序为0~22 min,A由10%→20%;0~11 min检测波长为365 nm,11~15 min检测波长为327 nm;22~25 min,A由20%→25%;25~28 min,A由25%→25%;25~28 min,A由25%→30%;28~32 min,A由30%→30%;15~28 min检测波长为358 nm,28~40 min检测波长为368 nm。
2.2 对照品溶液的制备
精密称取绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素,用70%的乙醇溶液溶解制成0.129、0.041、0.042、0.046、0.044、0.038 μg/mL的对照品混合溶液,2 ℃避光保存。
2.3 供试品溶液的制备
取金银花粉末(过80目篩)约2.0 g,精密称量50 mL 70%的乙醇溶液,在功率150 W、频率40 Hz下超声1 h,冷却至室温后称量,不足部分加70%的乙醇溶液补足后,静置待分层后取适量用22 μm滤头过滤,置于样品瓶中待测。
2.4 线性关系考察
取“2.2”条件下的混合对照品溶液2、4、6、8、10、12、14、16、18、20 μL分别注入高效液相色谱仪测定,以质量浓度为横坐标,以峰面积为纵坐标,进行线性回归处理,得到线性回归方程:绿原酸y=4.52×105x+24 058,r=0.999 9;咖啡酸y=5.66×106x-92 297,r=0.999 7;芦丁y=1.80×106x-27 990,r=0.999 3;金丝桃苷y=2.34×106x-40 139,r=0.999 7;木犀草苷y=2.10×106x+17 170,r=0.999 5;槲皮素y=2.49×106x-37 547,r=0.999 7;线性范围分别是0.012 9~10.32 μg、0.002 1~0.84 μg、0.002 1~0.84 μg、0.002 3~0.92 μg、0.002 2~0.88 μg、0.001 9~0.722 8 μg。
2.5 精密度试验
精密称量同一对照品溶液10 μL,连续进样5次,测定峰面积,计算得绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素峰面积的RSD分别为1.67%、1.46%、1.48%、1.37%、1.67%、2.29%,表明精密度良好。
2.6 稳定性试验
取同一供试品溶液,精密称量供试品溶液,间隔一定时间进样,测定峰面积。结果表明,8 h内6种成分峰面积的RSD分别为2.83%、2.26%、2.71%、2.35%、1.68%、2.59%。
2.7 重复性试验
取同一产地药材5份,按供试品溶液制备方法,分别测定绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素峰面积。结果表明,峰面积RSD为依次2.67%、2.94%、2.32%、2.72%、2.15%、2.83%。
2.8 加标回收率试验
精密称定6份金银花粉末1.0 g,分别精密加入适量绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素对照品,按“2.3”方法进行测定并计算回收率。结果表明,绿原酸的平均回收率为97.68%,RSD为2.48%(n=6);咖啡酸的平均回收率为101.23%,RSD为2.83%(n=6);芦丁的平均回收率为99.71%,RSD为2.47%(n=6),金丝桃苷的平均回收率为96.85%,RSD为2.25%(n=6);木犀草苷的平均回收率为100.52%,RSD为1.85%(n=6);槲皮素的平均回收率为103.61%,RSD为2.79%(n=6)。
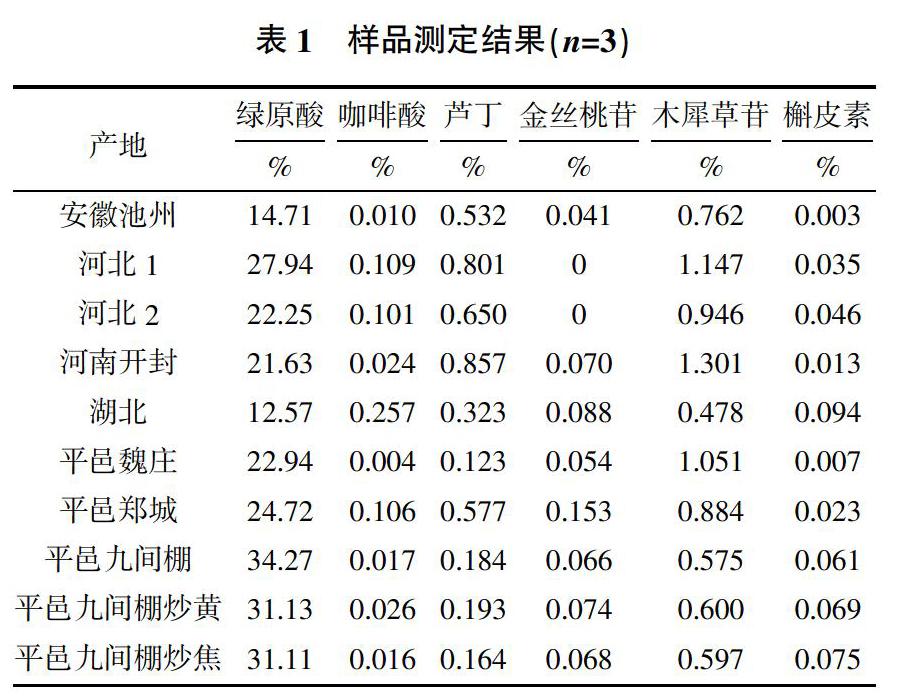
2.9 样品测定
取不同产地的金银花药材,按“2.3”方法制备供试品溶液,依次测定计算药材中绿原酸、咖啡酸、芦丁、金丝桃苷、木犀草苷、槲皮素的平均质量分数,结果见表1。
3 小结与讨论
本试验中的洗脱程序改进了2010版《中国药典》的洗脱方法,使得木犀草苷和前峰得到彻底分离,更能准确测定木犀草苷的含量。从样品测定的结果来看,产地不一样,各成分的含量存在差异;同一产地品种不一样,其含量也不一样;同一产地同一品种,处理工艺不一样,其成分含量也存在差别。采用变换波长的方法,能准确、快速测定金银花中的6种成分,可做为评判金银花质量好坏的依据。
参考文献:
[1] 马成俊,李桂生,任召言,等.金银花药材对照指纹图谱的建立及质量评价[J].时珍国医国药,2006,17(2):238-241.
[2] 梁生旺,崔永霞,王淑美,等.金银花的HPLC药效指纹图谱研究[J].中草药,2006,37(10):1489-1493.
[3] 孙国祥,杨宏涛,邓湘昱,等.金银花的毛细管电泳指纹图谱研究[J].色谱,2007,25(1):96-100.
[4] 国家药典委员会.中国药典[Z].一部.北京:中国医药科技出版社,2010.
