基于聚乙烯醇/金纳米棒复合凝胶膜的Hg2+传感器构建及应用
2016-10-16刘广力朱笑天汤克勇
刘广力, 李 霞, 朱笑天, 汤克勇, 刘 捷*
(郑州大学材料科学与工程学院,河南郑州 450001)
Hg2+是一种重要的重金属污染物,对环境生态系统有严重危害,极微量的Hg2+就会对人的大脑、心脏和胃等组织器官造成显著的损害[1]。研究高选择性、高灵敏度、高稳定性、简便易行且低成本的Hg2+测定方法,一直以来都是分析化学领域研究热点之一。经典的汞的分析方法有原子吸收光谱、原子发射光谱、原子荧光光谱、电感耦合等离子体质谱和电化学法等,但这些方法大多存在如制样复杂、设备要求高等缺点[2]。
金纳米棒(Gold Nanorods,GNRs)是一类呈棒状的贵金属纳米粒子,在可见光-近红外区具有独特的横向和纵向表面等离子共振(SPR)吸收峰。金纳米棒的尺寸、长径比、分散状态和形状改变都会诱导其分散液颜色和光谱特征发生变化[3]。Matthew在金纳米棒溶液中利用弱还原剂还原Hg2+,利用金纳米棒和单质汞能够形成金汞齐的原理,改变金纳米棒有效长径比和光学特性,发展出基于比色法的高度灵敏的Hg2+非聚集型传感器[4],Jin等[5]进一步发展和完善了这种方法。但是,金纳米棒的光学特性和胶体稳定性极易受环境介质的离子强度、折光指数、pH等多种因素影响,其保存时间、可检测环境和测量精度有很大的局限性。Warinya、Emily和Huang等将金纳米棒固定在玻璃片表面,以提高金纳米棒在存储和检测过程中的稳定性[6 - 8]。但由于金纳米棒仅能以单层分散状态被固定在玻璃片表面,导致构建的传感器信号较弱,不利于提高测量的精度,且金纳米棒在玻璃表面的固定过程较为复杂。
本文利用聚乙烯醇(PVA)水凝胶优异的化学稳定性和机械性能、高透明性和高传质性以及易于成型等优点[9],将金纳米棒固定在化学交联的PVA网络中,制备了PVA/GNRs复合水凝胶膜。在弱还原剂抗坏血酸辅助下,基于PVA/GNRs水凝胶膜构建了光学传感器,实现了对水样中Hg2+的检测。
1 实验部分
1.1 仪器与试剂
2550型双光束紫外-可见分光光度计(日本,岛津公司);Tecnai G220S-Twin型透射电子显微镜(美国,FEI公司)。
聚乙烯醇(PVA,聚合度1 750,醇解度88%,百灵威科技有限公司);NaBH4(上海思域化工科技有限公司);AgNO3(国药集团化学试剂有限公司);戊二醛(GTA,天津大茂化学试剂厂);HAuCl4、十六烷基三甲基溴化铵(CTAB)、抗坏血酸(AA)等均购自阿拉丁试剂有限公司。以上试剂均为分析纯。实验用水均为去离子水。
1.2 实验方法
1.2.1金纳米棒的合成以HAuCl4为金源,利用种子生长法合成金纳米棒[10]。首先制备金种子溶液:分别取5 mL 5.0×10-4mol/L HAuCl4溶液和5 mL 0.2 mol/L CTAB溶液于锥形瓶中,搅拌15 min。加入预先在冰水浴中新鲜配制的0.01 mol/L NaBH4溶液60 μL,溶液迅速变为棕黄色,继续搅拌1 min后,放入28 ℃水浴静置3 h,得金种子溶液。然后配制生长溶液:取50 mL 0.2 mol/L CTAB溶液和1.0 mL 0.004 mol/L AgNO3溶液,加入200 mL锥形瓶中,搅拌均匀,再加入50 mL 1.0×10-3mol/L HAuCl4溶液,继续搅拌15 min。加入0.7 mL 0.0788 mol/L抗坏血酸溶液,充分混合,黄色溶液立即变为无色。继续加入120 μL金种子溶液,剧烈搅拌2 min,于28 ℃水浴中静置24 h,即得金纳米棒溶液。将金纳米棒溶液在10 000 r/min下离心15 min,倒掉上清后,重新分散在去离子水中。离心3次以去除游离的CTAB和未反应的原料,将金纳米棒沉淀分散在少量去离子水中备用。
1.2.2PVA/GNRs凝胶膜的制备取3 g 8%(m/V)的聚乙烯醇水溶液与0.3 mL 5.0×10-4mol/L金纳米棒溶液混合,搅拌30 min后,加入100 μL 10%(m/V) GTA继续搅拌30 min。然后快速加入70 μL 0.1 mol/L HCl并搅拌30 s,倒入自制玻璃模具中定型,凝胶膜厚度为1.0~1.2 mm。待凝胶化完成后,用大量去离子水冲洗凝胶膜,凝胶膜储存于去离子水中备用。
1.2.3测试及表征裁取10×25 mm的PVA/GNRs凝胶膜和0.1 mL 0.1 mol/L抗坏血酸溶液预混合,然后加入10 mL不同浓度的HgCl2溶液,在60 ℃水浴中反应5 min,将凝胶膜取出并固定在自制的样品架上,插入分光光度计中,扫描凝胶膜在波长400~900 nm的可见光谱,根据光谱数据绘制标准曲线。用透射电镜分析金纳米棒的形貌和粒度,将金纳米棒溶液滴到镀碳铜网上,待室温自然干燥后进行测定,加速电压200 kV。
2 结果与讨论
2.1 金纳米棒的表征
图1和图2分别为种子生长法制备金纳米棒的透射电镜(TEM)和吸收光谱图。由图1可见,制备的金纳米颗粒呈短棒状,利用软件统计其长径比为2.6±0.4。图2金纳米棒分散液的吸收光谱,金纳米棒的吸收光谱在可见光区有两个表面等离子共振(SPR)吸收峰,分别对应位于654 nm的纵向等离子共振(LSPR)和514 nm的横向等离子共振(TSPR)吸收峰,且吸收强度差值较大,说明所制备的金纳米棒具有典型的各向异性结构[10,11]。

图1 金纳米棒的透射电镜(TEM)图Fig.1 TEM images of gold nanorods
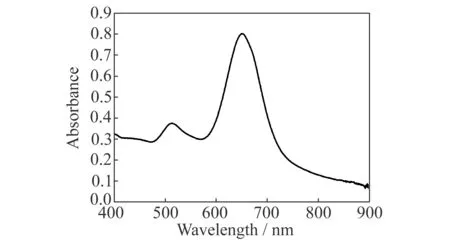
图2 金纳米棒的吸收光谱Fig.2 Absorption spectrum of gold nanorods
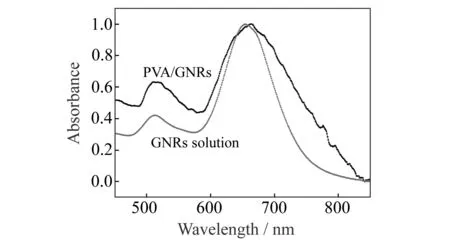
图3 PVA/GNRs复合凝胶膜和金纳米棒溶液的吸收光谱Fig.3 Absorption spectra of PVA/GNRs composite hydrogel film and GNRs solution
2.2 PVA/GNRs复合凝胶膜的光谱特征
为考察金纳米棒在不同介质中的光学特性,以构建基于PVA/GNRs复合凝胶膜的光学传感器,对比了金纳米棒在溶液和包埋在PVA水凝胶中的吸收光谱,结果如图3所示。当金纳米棒被包埋固定在聚乙烯醇凝胶网格中后,其LSPR吸收峰由654 nm红移至664 nm,且吸收峰明显变宽。这种变化是由于聚乙烯醇凝胶的折光指数略大于水的折光指数,引起金纳米棒表面等离子体振动改变导致LSPR最大吸收峰(λmax)向长波方向移动,这与文献报道[11]一致。
2.3 Hg2+传感器的构建及其响应特性
目前研究者在使用金纳米棒溶液检测水样中Hg2+含量时,常发生检测过程中测试溶液的吸收强度逐渐降低的现象(图4(A))。TEM分析表明,溶液中的金纳米棒在检测过程中容易发生团聚甚至沉降,会导致其吸收强度降低进而影响测量的准确性和可靠性。发生团聚的原因是金纳米棒表面CTAB的包裹并不均匀[10],由于布朗运动,在溶液中的金纳米棒发生碰撞时容易受到溶液中离子强度、pH等因素的影响发生聚集甚至沉降。图4(B)为PVA/GNRs复合凝胶膜在相同检测环境中的吸收光谱,其光谱强度随时间延长没有明显变化。稳定性的改善与纳米颗粒的分散环境有关,金纳米棒被固定在聚合物凝胶的三维网状结构中可以有效避免其在溶液中可能发生的聚集和沉降。采用这种新的固定和测量方式将为复杂水样中Hg2+的检测提供理想的平台,也是研究者们探索和发展金纳米棒固定方法的主要目的[6 - 8]。
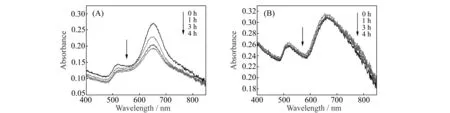
图4 金纳米棒溶液(A)和PVA/GNRs凝胶膜(B)的吸收光谱随时间的变化Fig.4 Change of absorption spectra of GNRs solution(A) and PVA/GNRs hydrogel film(B)
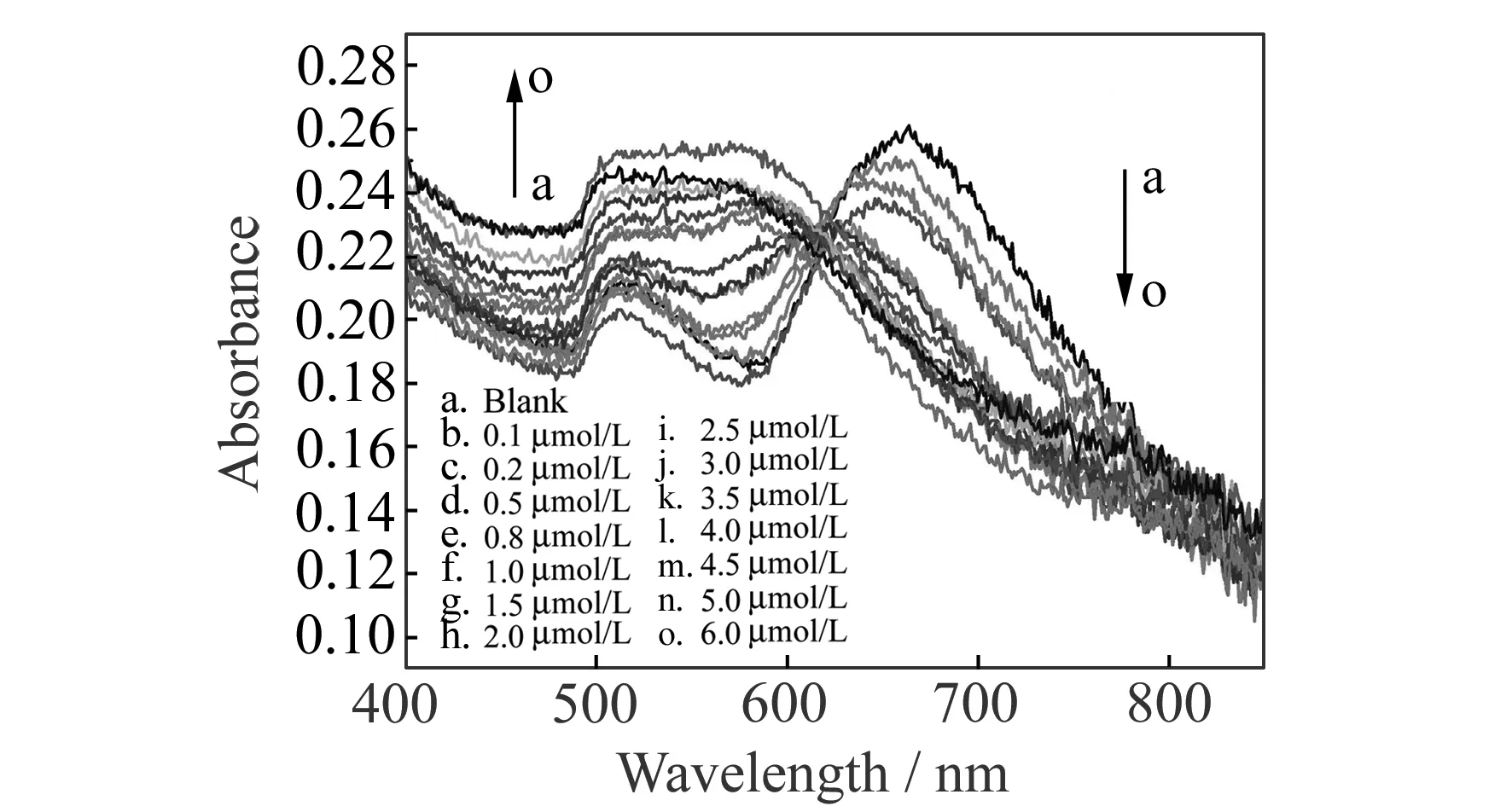
图5 PVA/GNRs复合凝胶膜响应Hg2+的吸收光谱Fig.5 Absorption spectra of PVA/GNRs composite hydrogel film in response to Hg2+concentration of Hg2+(from a to o):0.1-6.0 μmol/L.
图5为PVA/GNRs复合凝胶膜对不同浓度Hg2+溶液响应的吸收光谱图。可以看到,随着Hg2+浓度增加,凝胶膜的LSPR吸收峰逐渐蓝移,并最终消失,而TSPR吸收峰位置基本不变,只有强度改变。这表明金纳米棒被固定在高亲水性凝胶网格中仍然对Hg2+具有响应性,凝胶膜的颜色也由蓝变红,这与金纳米棒在溶液中对Hg2+的响应情况相似[4,5]。抗坏血酸加入Hg2+以后,迅速将凝胶网格中的Hg2+还原为单质汞(Hg0)。Hg0与固定在凝胶中的金纳米棒之间有两种可能的相互作用,其一是液体金属Hg0包覆在金纳米棒表面,其二为Hg0与金纳米棒之间的汞齐化作用[5,8]。如果Hg0大量包覆在金纳米棒表面或附近,会增大其环境介质的有效介电常数,应使金纳米棒的LSPR峰发生红移。但由图5可知,PVA/GNRs复合物的LSPR吸收峰随Hg2+浓度的增加发生蓝移。因此,PVA/GNRs响应机理应主要归因于汞齐化作用,可概括为:凝胶网格中的Hg2+被抗坏血酸还原为Hg0,Hg0在凝胶中扩散并与金纳米棒形成金汞齐合金,且优先与CTAB较少的纳米棒端部发生反应,使金纳米棒的表观长径比减小(图6)。随Hg2+浓度增大,与金纳米棒反应的Hg0的量也增加,金纳米棒的表观长径比进一步减小至平衡,LSPR吸收峰随之持续发生蓝移并达到平衡。
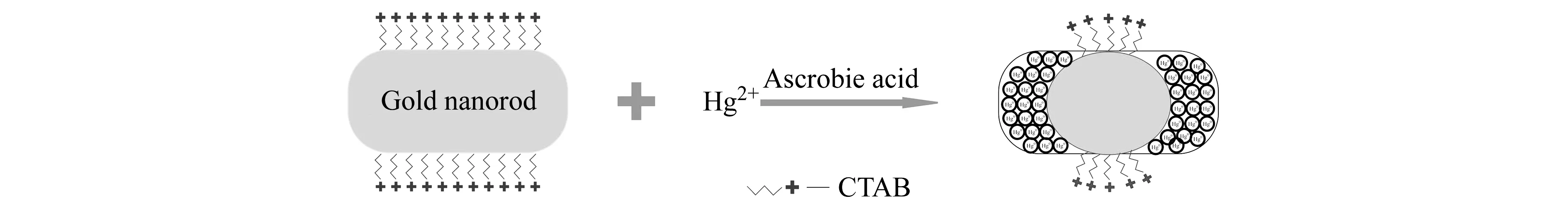
图6 基于PVA/GNRs复合凝胶膜Hg2+传感器的响应机理示意图Fig.6 Schematic diagram showing the response mechanism of Hg2+ sensor based on PVA/GNRs composite hydrogel film
Hg2+在0.1~3.0 μmol/L的浓度范围内,金纳米棒在664 nm波长处LSPR峰的吸光度(A664)逐渐减小,而514 nm处TSPR峰的吸光度(A514)逐渐增大(图5)。随着金纳米棒有效长径比的减小,反映其各向异性特征的LSPR吸收峰发生蓝移,原吸收峰664 nm处的吸收强度也随之降低。相应地,随着金纳米棒长径比的减小,具有各向同性特征的金纳米粒子比例提高,TSPR峰处的吸收强度持续增强。图7所示为514、664 nm波长处吸光度比值(A514/A664)与Hg2+浓度的关系曲线(标准曲线),在0.1~3.0 μmol/L浓度范围内,A514/A664对Hg2+浓度呈线性关系,拟合直线的相关系数R2达到0.997。与文献报道利用经化学修饰的玻璃片固定单层金纳米棒相比[6 - 8],本方法能够方便地调节复合凝胶中金纳米棒的体积分数,使该传感系统更容易获得较强的光学信号,这对改善传感器的灵敏度、检测限以及降低成本都具有积极的意义。
为验证该传感器的实用性,利用PVA/GNRs复合凝胶膜对实际水样进行了检测。水样取自郑州大学新校区眉湖湖水,经过0.45 μm水系滤头过滤后按照上述方法进行Hg2+含量测定,测定结果低于检测下限,可认为未检出。加标回收率实验测得该水样的加标回收率为92.5%~104.3%,说明由PVA/GNRs复合凝胶膜构建的传感器可用于实际水样中Hg2+的检测。
2.4 选择性评价
图8为PVA/GNRs复合凝胶膜对溶液中Ba2+、Al3+、Mg2+、Fe2+、Fe3+、Ca2+、Cr3+、Cu2+、Sn2+、Ag+、Hg2+的响应性(各离子浓度均为2 μmol/L)。从图8中数码照片可见,PVA/GNRs传感器仅对Hg2+有明显的响应,凝胶膜颜色也由蓝变红,而凝胶膜在其他离子溶液中则没有明显的颜色改变。可见光谱结果也证实了A514/A654对Hg2+的选择响应性。
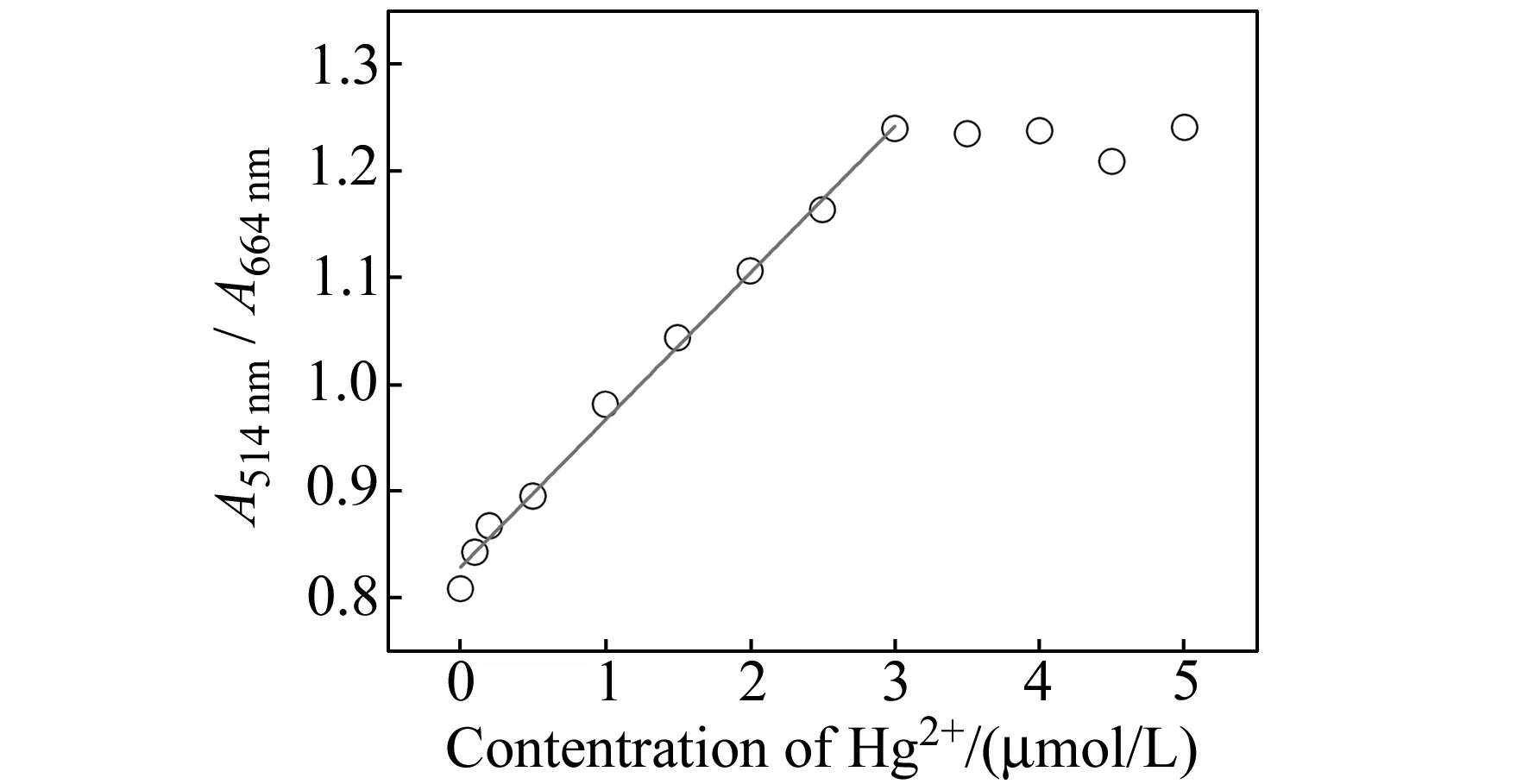
图7 PVA/GNRs凝胶膜的A514/A664 与Hg2+浓度关系图Fig.7 Plot showing the A514/A664 of PVA/GNRs hydrogel films versus the concentration of Hg2+

图8 PVA/GNRs复合凝胶膜对几种金属离子的选择性Fig.8 Selectivity of PVA/GNRs composite hydrogel films toward several metal ions
3 结论
以聚乙烯醇为载体固定金纳米棒制备了PVA/GNRs复合凝胶膜,并在此基础上构建了检测Hg2+的光学传感器。Hg2+在浓度0.1~3.0 μmol/L范围内,该传感器有良好的线性响应和选择性。PVA/GNRs复合凝胶膜的制备过程简单、使用方便、响应迅速,能够显著改善金纳米棒存储和测量中的稳定性问题,有望在基于金纳米棒的化学和生物传感器及其他相关分析领域得到更广泛的应用。
