冲激辐射天线实现皮秒脉冲电场在人体大脑模型中聚焦的研究
2016-10-14李成祥唐贤伦陈功贵姚陈果
郭 飞 李成祥 唐贤伦 陈功贵 姚陈果
(1.重庆邮电大学自动化学院 重庆 400065 2.输配电装备及系统安全与新技术国家重点实验室(重庆大学) 重庆 400030)
冲激辐射天线实现皮秒脉冲电场在人体大脑模型中聚焦的研究
郭飞1,2李成祥2唐贤伦1陈功贵1姚陈果2
(1.重庆邮电大学自动化学院重庆400065 2.输配电装备及系统安全与新技术国家重点实验室(重庆大学)重庆400030)
采用三维电磁场仿真软件CST Microwave Studio建立长椭球型天线模型和介质透镜模型,研究皮秒脉冲经冲激脉冲辐射天线发射后在人体大脑模型中的聚焦特性。结果表明,传播至大脑组织深度6 cm处的电场能够保持输入波形的时域特性;皮秒脉冲能够进入大脑组织深度8 cm处,且此时形成的焦斑尺寸最小;不包含介质透镜和包含非损耗介质透镜时,形成的焦斑尺寸为1 cm×2 cm×1 cm,而引入损耗介质透镜后,形成的焦斑尺寸小于1 cm×1 cm×1 cm。研究结果从理论上证明了联合损耗介质透镜和单个冲激脉冲辐射天线能够实现皮秒脉冲在深部脑组织中的有效聚焦。
皮秒脉冲冲激脉冲辐射天线大脑模型非损耗介质透镜损耗介质透镜
0 引言
近年来,电场脉冲对细胞结构和功能的作用逐渐成为生物电磁技术领域的一个研究热点[1-3],它不仅为电气工程师、细胞生物学家和临床医师等通过强大而简洁的电场方式(类似于“探针”)研究细胞内外膜跨膜电位变化并调控生物细胞响应开辟了一条全新途径,而且也为电场脉冲靶向作用于病变神经组织进而调控神经元动作电位提供了可能,并展示出良好的发展前景。文献[4-7]发现在场强为1 kV/cm、脉宽为100 μs的微秒电场脉冲作用下,细胞膜的脂质双分子层被暂时重新排列形成了一些被称为电穿孔效应(Electroporation)的亲水性通道。文献[8]首次采用微秒脉冲刺激丘脑下核(STN)和内侧苍白球(GPi),从而达到治疗帕金森的效果。文献[9,10]采用微秒脉冲电场治疗肌张力障碍。文献[11]将微秒脉冲用于癫痫症治疗,表现出较好的治疗效果。文献[12-14]发现不用化疗药物,采用场强约100 kV/cm、脉宽降低至10 ns级的纳秒电场脉冲可以改变细胞器膜(内膜)的跨膜电位,进而导致一系列称为内处理效应(Intracellular Electromanipulation)的细胞响应;单个脉宽1 ns、场强12 kV/cm的脉冲电场可有效刺激青蛙腓肠肌[15];单个脉宽12 ns、场强403 V/cm的脉冲电场可以激发大鼠皮肤伤害感受器动作电位[16]。
上述微/纳秒脉冲电场诱导的独特生物电效应已成功应用于临床试验。然而,如果将微/纳脉冲电场应用于癫痫等脑科疾病治疗,需借助有创/微创电极将电脉冲引入人体脑部癫痫病变区域,在一定程度上会对大脑正常组织和器官造成损伤,仍无法实现无创治疗。因此,能否找到一种既能无创进入人体深部脑组织,又能靶向调控癫痫病变区域神经元动作电位的电场脉冲成为解决上述问题的关键。
随着脉冲电场脉宽进一步降低至皮秒级,脉冲电场同样能诱导生物细胞结构和功能发生一定的改变,如文献[17]揭示脉宽800 ps、场强500 kV/cm级的脉冲电场可以增强细胞膜的通透性。文献[18]研究表明脉宽200 ps、场强20 kV/cm、重复频率10 kHz电场脉冲可以改变细胞膜跨膜电位。文献[16]的最新研究结果表明脉宽200 ps、重复频率为4 kHz、场强为3 kV/cm的脉冲电场可有效刺激大鼠皮肤伤害感受器的动作电位。此外,皮秒级脉冲电场由于脉宽极窄(~ps级),相应地其频域带宽非常丰富(DC~GHz),因而能够通过超宽带冲激脉冲辐射天线发射,并能实现电磁波在近场处的聚焦[19],此时将人体大脑组织置于近场处,并使脑部病变区域与电磁波聚集区域重合,通过调节皮秒脉冲参数则能实现对大脑病变区域细胞结构和功能的治疗作用,从而使皮秒脉冲无创聚焦治疗癫痫等脑科疾病成为可能。
目前,皮秒脉冲匹配冲激脉冲辐射天线(Impulse Radiating Antenna,IRA)能够在自由空间及均匀组织中实现良好聚焦[19,20],但皮秒脉冲匹配冲激脉冲辐射天线在人体大脑等复杂生物组织中的聚焦特性尚未有研究。
本文基于前期研究[21],引入数字化人体大脑模型Hugo和5层介质透镜模型,研究皮秒脉冲在人体大脑模型中的聚焦特性。
1 仿真设置
1.1冲激脉冲辐射天线
IRA的仿真模型如图1所示[19]。IRA由TEM锥形传输线实现馈源,反射镜由半个椭球构成,且短轴置于孔径平面。由焦点F1发出的球形TEM波经反射面传播后将汇聚于另一焦点F2,将生物组织置于F2即可实现脉冲在其中的聚焦。相较于一般天线,IRA具有线性极化辐射、超宽带辐射以及高功率发射等独特优势。
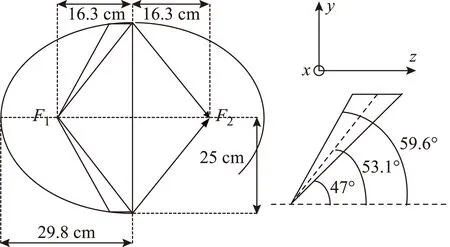
图1 冲激脉冲辐射天线仿真结构图Fig.1 Structural diagram of IRA
1.2Hugo人体大脑模型
如图2所示,选取CST公司的数字化人体大脑模型Hugo (1 mm×1 mm×1 mm),通过其侧视图和后视图都能明显地辨别出大脑组织各成分。受限于软件配置,仿真工作并未包含脑组织介电参数(介电常数、电导率)的频率色散效应。选取频率为1.8 GHz处的介电参数进行仿真,脑组织各结构组分的介电参数如表1所示。
1.3介质透镜仿真模型

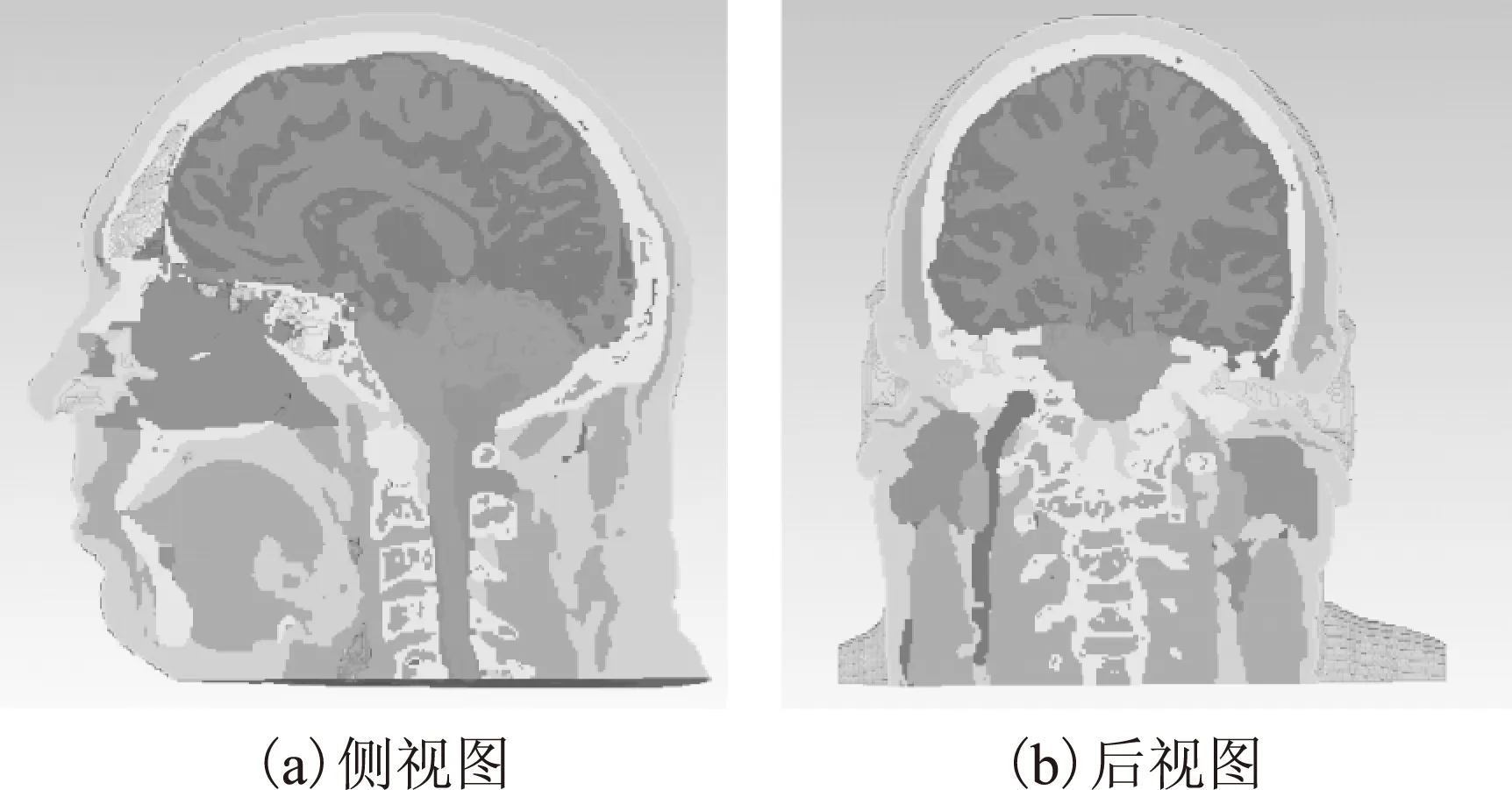
图2 数字化人体大脑模型Fig.2 Digitized human brain model表1 大脑模型介电参数Tab.1 Dielectric parameters of brain model

组织成分介电常数电导率/(S·m-1)白质37.010.9150灰质50.081.391头骨11.780.2752脂肪5.3500.07839视神经30.870.8428骨骼肌55.341.438


图3 介质透镜模型Fig.3 Dielectric lens model
1.4仿真聚焦模型
根据介质透镜是否包含损耗材料,将其分为非损耗介质透镜(图3)和损耗介质透镜。图4为IRA耦合损耗介质透镜实现皮秒脉冲在大脑组织中聚焦的仿真图,IRA焦点F2位于大脑深部6 cm处。该模型包含IRA、损耗介质透镜和大脑模型三部分,IRA和大脑的仿真模型如上述所示;损耗介质透镜与上述非损耗介质透镜(图3)仿真模型基本相同,唯一不同的是该仿真模型中损耗介质透镜最内两层45°范围内分别由电导率为5 S/m、4 S/m的损耗材料构成,电导率参数的选择是基于计算机优化的结果。本文分别研究了不包含任何介质透镜、包含非损耗介质透镜和包含损耗介质透镜三种情况下,皮秒脉冲电场经IRA发射后在大脑模型中的聚焦特性。仿真采用三维电磁场计算软件CST Microwave Studio (Framingham,MA),该软件基于有限积分法进行计算,并采用Transient Solver进行求解。

图4 皮秒脉冲在大脑模型中的聚焦模型Fig.4 Focusing model of psPEF in brain model
2 仿真结果
2.1不包含介质透镜时仿真结果
在IRA焦点F1处注入幅值1 V、脉宽200 ps的高斯脉冲,经大脑组织传播后,得到大脑组织内IRA几何焦点F2处的电场波形如图5所示。与Y轴方向电场相比,X轴和Z轴方向的电场基本忽略不计,且Y轴方向的电场保持了输入波形的时域特性。
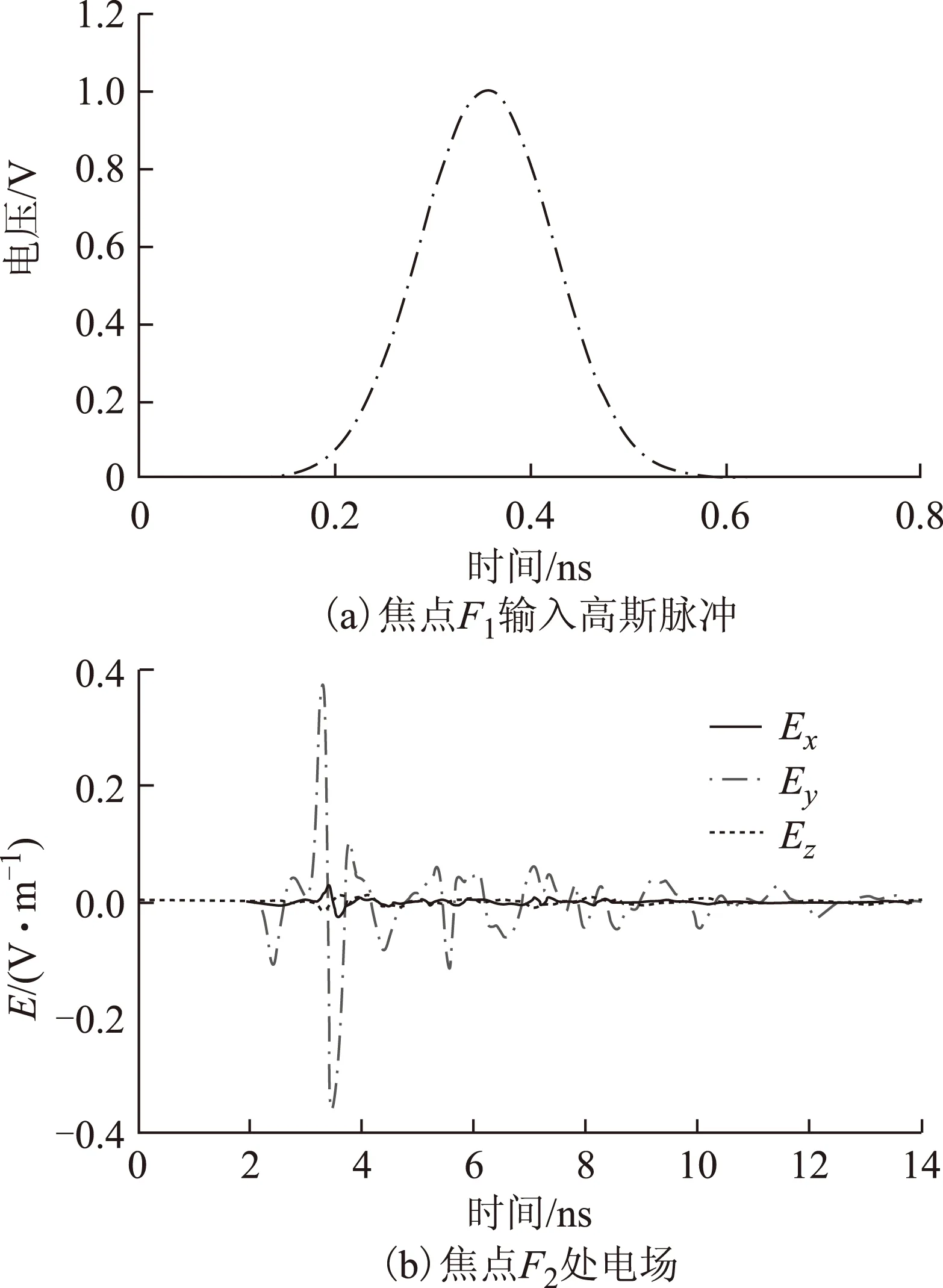
图5 电场波形Fig.5 Electric field waveforms
图6为皮秒脉冲在大脑内的传播过程。场强以线性等值线的方式显示,设定阈值范围为0.1~0.3 V/m,表明场强高于0.3 V/m将被认定为0.3 V/m。1.8 ns时前脉冲(Prepulse)已经进入大脑,同时前脉冲在面部和脑后部的传播速度大于在脑组织内的传播速度;3.1 ns时,冲激脉冲(Impulse)经由天线轴线直接传播至大脑组织,随着传播深度的增加,脉冲焦斑逐渐缩小,在3.7 ns时达到最小。图6中的侧视图(第一排)中,脉冲在3.1 ns包含两个明亮的焦斑,与双极性时域波形恰好吻合(图5);图6中的俯视图(第三排),从大脑深度8 cm处截取而来。在大脑内部放置一系列的探针,用于测量实际电场强度;探针以1 cm间距放置在以焦点F2为中心的各径向上。由于大脑不是规则的球形,因此各角度径向的长度不同。

图6 电场分布的等值线图Fig.6 The isoline plots of electric filed distribution
图7a为电场在不同路径角上的分布情况,最大的电场分布在Z轴,且电场基本沿Z轴对称分布;由于大脑包含损耗介质,使得电场随进入大脑深度的增加而不断衰减;然而在到达大脑深度7~8 cm时,电场出现极大值,稍高于焦点F2(大脑深度6 cm)处的场强,这也与图6的仿真结果吻合。
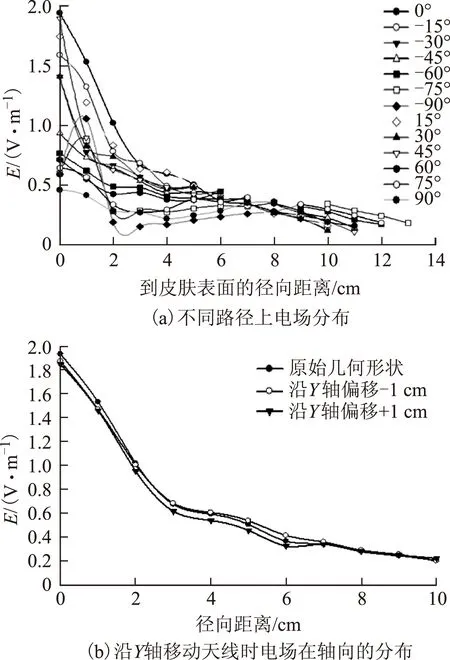
图7 电场在大脑内的分布Fig.7 Electric field distribution in the human brain

图8 电场分布的等值线图Fig.8 Isoline plots of electric field
为了得到3.7 ns时焦斑的尺寸,通过移动截面得到不同的切面图,如图8所示。观察X=-2~2 cm的侧视图,可以看出焦斑位于X=0~1 cm的范围;观察Y=-2~2 cm的后视图,很难直接得出焦斑的范围,但通过观察0.3 V/m电场的存在范围(中心小环区域),仍可得到焦斑位于Y=-1~1 cm;观察俯视图可看出焦斑位于7~8 cm处,即焦斑在Z轴方向范围仅为1 cm。这样可以大致估算焦斑在3.7 ns时的尺寸为1 cm×2 cm×1 cm,焦斑在X、Z轴的尺寸较小,而在Y轴尺寸相对较大。
皮秒脉冲传播至深部组织时,人体大脑和天线的相对位置改变将会影响电磁波焦点的位置。图7b为电场沿Z轴方向的分布,大脑位置不变,天线沿Y轴方向移动-1 cm、0 cm、1 cm时便可得到3个不同相对位置。由图7b可知,天线位置移动-1 cm和1 cm时,电场分布与Y=0 cm时基本重合。这也说明焦斑在Y轴方向分布范围较大,因此天线移动1 cm时焦斑改变不明显。焦斑在X、Z轴分布较窄,可以推测在X轴和Z轴方向焦斑对天线和大脑相对位置变化较为敏感。
2.2引入非损耗介质透镜后仿真结果
将非损耗介质透镜放置于大脑模型上,得到如图9所示的电场分布。场强以线性等值线的方式显示,设定阈值范围为0.1~0.5 V/m,比之前增加的原因是介质透镜会增强电磁波传播至大脑组织。3.7 ns时冲激脉冲形成的焦斑尺寸基本成型,并在3.9 ns时到达大脑组织深度8 cm处,随着电磁波透入深度的增加,电场强度逐渐减弱,到达9 cm时基本看不到焦斑。
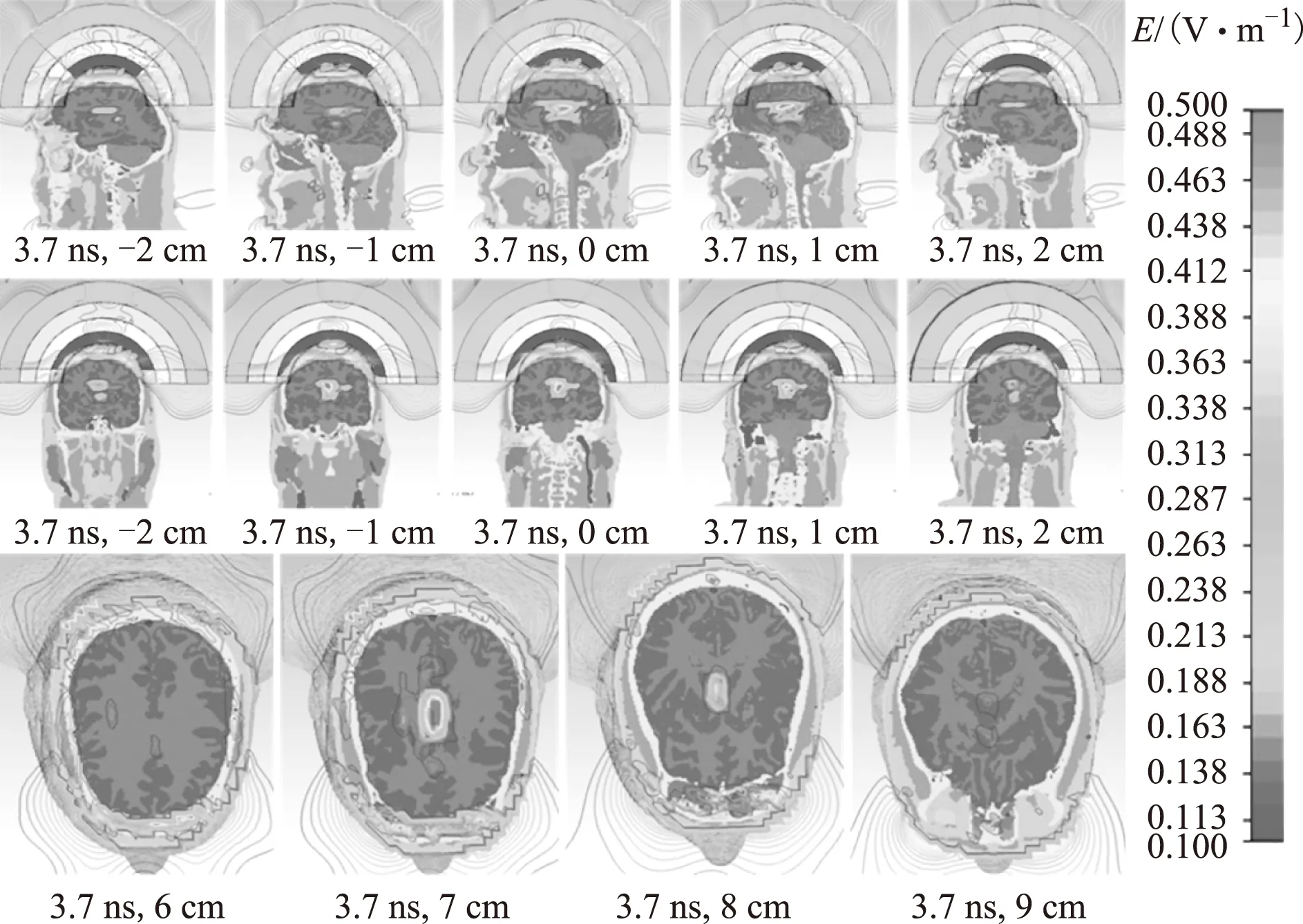
图9 电场分布的等值线图Fig.9 Isoline plots of electric field
电场沿径向的分布如图10a所示,不同路径角的电场分布与2.1节的仿真结果一致,然而介质透镜的引入,使得皮肤处电场强度大大增加。大脑组织深度8cm处的场强增为0.5 V/m,高于之前的0.2 V/m。总之,最大的电场分布在Z轴,而其两侧的电场较低,电场将随透入大脑组织深度的增加而不断衰减。
使用前面的方法研究非损耗介质透镜的引入是否改变焦斑的尺寸。如图9所示,包含最大场强(0.5 V/m,中心白色部分)的区域同样位于X=0~1 cm、Y=-1~1 cm和Z=7~8 cm的范围,即引入非损耗介质透镜后焦斑的尺寸未发生改变。
在Y轴方向整体移动天线和非损耗介质透镜,且保持大脑模型位置不变,研究二者相对位置改变对电场分布的影响,如图10b所示。大脑不是规则的球形,介质透镜将会和大脑模型存在重合部分,设置大脑模型优先级高于介质透镜,即大脑模型几何结构不变,而介质透镜变成与之适配的不规则形状。沿Y轴移动-1 cm和1 cm时的电场分布与Y=0 cm时基本一致,与焦斑在Y轴分布较宽相吻合。
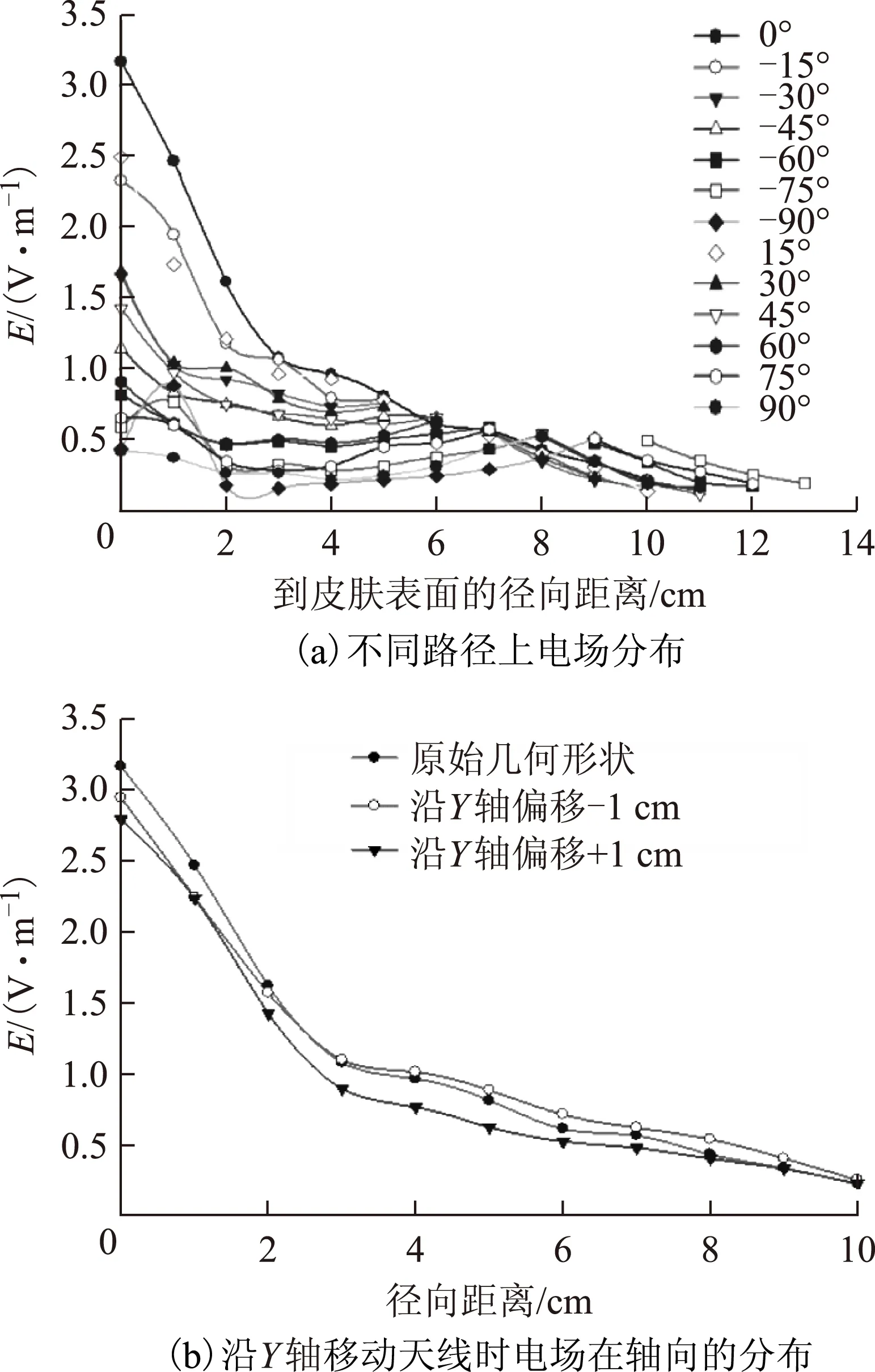
图10 电场在大脑内的分布Fig.10 Electric field distribution in the human brain
2.3引入损耗介质透镜后仿真结果
将非损耗介质透镜改造成第4层和第5层±45°范围分别填充电导率为4 S/m和5 S/m的损耗介质透镜,将之置于大脑模型上面进行仿真。如图11所示,3.7 ns时冲激脉冲分布与之前明显不同。损耗介质透镜使得Z轴方向的电场得到衰减,而径向远离Z轴方向的电场相对增强;3.9 ns时冲激脉冲汇聚于大脑组织深部8 cm 处。

图11 电场分布的等值线图Fig.11 Isoline plots of electric field
图12a为不同路径上电场的分布情况,Z轴方向(R vs 0)的电场变为最低,且在8 cm时有极大值,电场径向分布与图7a和图10a恰好相反,±45°方向的电场变为最高。损耗介质透镜的强烈衰减作用能够改变电场在大脑组织内的径向分布,同时使得汇聚处(8 cm)的场强减为0.2 V/m,远小于非损耗介质透镜的情况。

图12 电场在大脑内的分布Fig.12 Electric field in the human brain
和前面的研究方法一样,通过观察不同侧面的截面图可以估算焦斑的尺寸。如图11所示,焦斑的尺寸明显减小,侧视图和俯视图表明焦斑在X轴和Z轴的范围均小于1 cm,焦斑在Y轴方向的分布不明显,但可以看出有所减小。焦斑缩小表明其对天线和大脑模型相对位置变化更加敏感,这也可以通过图12b的仿真结果得到验证。天线沿Y轴移动-1 cm、1 cm时,电场分布明显与Y=0 cm不同,表明焦斑在Y轴方向对于天线和大脑模型相对位置变化变得敏感。损耗介质透镜的引入使得皮秒脉冲在大脑模型内形成的焦斑尺寸缩小,且汇聚处的场强将因损耗材料的衰减作用而出现降低。
3 讨论
P.Kumar等[22]同样采用CST Microwave Studio研究了冲激脉冲辐射天线在自由空间的分布,并将仿真结果和实验结果进行对比,二者能较好吻合,表明采用该软件研究皮秒脉冲经冲激脉冲辐射天线发射后在大脑组织中的聚焦特性是可行的。此外,研究人员在前期研究中也专门验证了采用CST Microwave Studio研究IRA聚焦特性的可行性,仿真结果与实验结果能较好吻合,证实了该仿真方法的正确性及可靠性[21]。
IRA作为一种新型的超宽带天线,能够实现超宽带电场信号在其近场处的良好聚焦。在焦点F1处注入皮秒级脉冲电场,经过反射面的传播,由于电磁波到达F2的光程相同,则达此处的电磁波相位相同,不同路径电磁波同相叠加则实现焦点F2汇聚的效果[19,20]。电磁波经过反射面传播时将被微分,因此焦点F1注入的单极性脉冲在焦点F2汇聚时将变为双极性脉冲电场信号,这也与图5的仿真结果一致。
为了实现皮秒脉冲靶向调控神经元结构和功能进而实现癫痫、帕金森等脑科疾病无创治疗的目的,本文研究了皮秒脉冲经单个IRA发射后,其在大脑深部组织中的聚焦特性。仿真结果表明:皮秒脉冲经IRA发射后,将会在大脑组织深度8 cm处形成汇聚,比IRA的几何焦点F2深度(大脑深度6 cm)大2 cm,在XYZ方向形成的焦斑尺寸为1 cm×2 cm×1 cm,且焦斑位于白质区域。白质的介电常数为37,在其中传播的电磁波空间宽度为1 cm,与输入200 ps高斯脉冲的仿真结果相吻合。因此,通过估算在相应介质中形成焦斑的空间宽度,就可推断出焦斑的尺寸。此时,皮秒脉冲虽然能够实现大脑深部组织中的聚焦,但聚焦区域的绝对场强太低且形成的焦斑尺寸较大,难以满足皮秒脉冲无创聚焦治疗的要求。
前期研究表明:引入介质透镜能够明显改善IRA在其中的聚焦特性,焦点处场强明显增加,同时焦斑尺寸明显降低[20]。因此,本文研究了引入介质透镜时IRA在深部脑组织中聚焦特性。引入非损耗介质透镜后,皮秒脉冲在大脑组织内形成的焦斑位置和尺寸未发生改变,但焦斑处的绝对场强由于非损耗介质透镜的引入而大大增强。这是由于大脑包含各种不同介电特性的组织,介质透镜的引入只能增强焦斑处的绝对场强而难以改变焦斑的尺寸。利用前期研究的思想,将介质透镜改造成内部小路径角填充损耗材料的损耗介质透镜,用于衰减无聚焦特性的小路径角电磁波,从而实现更好的聚焦效果[21]。仿真结果表明:引入损耗介质透镜后,脉冲仍然在大脑深度8 cm处形成聚焦,且焦斑尺寸大大缩小,同时电场在各个径向上的分布也发生改变,这也与前期研究能够较好吻合。本文的研究只是对介质透镜进行简单的改造,介质透镜结构在下一步研究中仍需要不断优化,可以考虑同一层介质由多种不同损耗材料构成,也可以考虑采用多变量优化算法,如遗传算法等进行介质透镜的结构优化。
基于Rodgers的线性等效方程[15],可以大致估算脉宽200 ps、重复频率为4 kHz、场强为0.5 kV/cm~5 kV/cm的脉冲电场,可有效刺激大鼠皮肤伤害感受器动作电位。由图7a、图10a、图12a可知,输入为1 V、200 ps的高斯脉冲经IRA发射后,皮秒脉冲可在大脑组织8 cm处形成明显的焦斑,且焦斑处的场强为0.2~0.5 V/m,需要输入电压幅值为250 kV~2.5 MV的皮秒脉冲才能达到电场刺激的最低阈值0.5 kV/cm。因此,高强度皮秒脉冲发生器(~MV)的研制将是无创聚焦成功实施的关键所在。
癫痫作为一种常见的神经性疾病,与大脑特定组织(如丘脑前核、丘脑中央内侧核、内侧苍白球、小脑、海马等)神经元的动作电位畸变密切相关。而本文的研究结果表明皮秒脉冲能够经由冲激脉冲辐射天线聚焦于上述特定大脑组织。因此,可通过匹配超宽带脉冲辐射天线将高强度皮秒脉冲电场无创聚焦于癫痫病变区域组织,通过调控靶区神经元动作电位,避免对周围正常组织的损伤及创伤后遗症等毒副作用的影响,实现无创治疗癫痫等神经性疾病的目的。本文的研究结果只是从理论给出了联合损耗介质透镜和单个IRA能够实现皮秒脉冲在深部脑组织中的聚焦,从而为皮秒脉冲无创聚焦治疗癫痫等脑科疾病提供了理论上的依据。然而欲实现上述方法的临床实际应用,尚需进行大量后续的研究工作。
4 结论
利用CST软件仿真计算了皮秒脉冲经IRA发射后在大脑模型中的聚焦特性,得出以下结论:
1)传播至大脑组织深度6 cm焦点F2处的电场能够保持输入波形的时域特性。
2)皮秒脉冲能够进入大脑组织深度8 cm处,此时形成的焦斑尺寸最小。
3)不包含介质透镜和包含非损耗介质透镜时,形成的焦斑尺寸为1 cm×2 cm×1 cm,而引入损耗介质透镜后,焦斑尺寸小于1 cm×1 cm×1 cm。
[1]Yao C,Guo F,Li C,et al.Gene transfer and drug delivery with electric pulse generators[J].Current Drug Metabolism,2013,14(3):319-323.
[2]Schoenbach K H,Peterkin F E,Alden III R W,et al.The effect of pulsed electric fields on biological cells:experiments and applications[J].IEEE Transactions on Plasma Science,1997,25(2):284-292.
[3]Schoenbach K H,Hargrave B,Joshi R P,et al.Bioelectric effects of intense nanosecond pulses[J].IEEE Transactions on Dielectrics and Electrical Insulation,2007,14(5):1088-1109.
[4]Neumann E,Rosenheck K.Permeability changes induced by electric impulses in vesicular membranes[J].The Journal of Membrane Biology,1972,10(1):279-290.
[5]Crowley J M.Electrical breakdown of biomolecular lipid membranes as an electromechanical instability[J].Biophysical Journal,1973,13(7):711-724.
[6]Zimmermann U,Friedrich U,Mussauer H,et al.Electromanipulation of mammalian cells:fundamentals and application[J].IEEE Transactions on Plasma Science,2000,28(1):72-82.
[7]Weaver J C.Electroporation of cells and tissues[J].IEEE Transactions on Plasma Science,2000,28(1):24-33.
[8]Obeso J A,Olanow C W,Rodriguez-Oroz M C.Deep-brain stimulation of the subthalamic nucleus or the pars interna of the globus pallidus in Parkinson’s disease[J].New England Journal of Medicine,2001,345(13):956-963.
[9]Coubes P,Roubertie A,Vayssiere N,et al.Treatment of DYT1-generalised dystonia by stimulation of the internal globus pallidus[J].Lancet,2000,355(9222):2220-2221.
[10]Yianni J,Bain P,Giladi N,et al.Globus pallidus internus deep brain stimulation for dystonic conditions:a prospective audit[J].Movement Disorders:Official Journal of the Movement Disorder Society,2003,18(4):436-442.
[11]Nuttin B J,Gabriёls L A,Cosyns P R,et al.Long-term electrical capsular stimulation in patients with obsessive-compulsive disorder[J].Neurosurgery,2003,52(6):1263-1274.
[12]Schoenbach K H,Katsuki S,Stark R H,et al.Bioelectrics-new applications for pulsed power technology[J].IEEE Transactions on Plasma Science,2002,30(1):293-300.
[13]Schoenbach K H,Joshi R P,Kolb J F,et al.Ultrashort electrical pulses open a new gateway into biological cells[J].International Power Modulator Symposium,2004,92(7):205-209.
[14]Schoenbach K H,Nuccitelli R,Beebe S J.ZAP:extreme voltage could be a surprisingly delicate tool in the fight against cancer[J].IEEE Spectrum,2006,43(8):20-26.
[15]Rogers W R,Merritt J H,Comeaux J J A,et al.Strength-duration curve for an electrically excitable tissue extended down to near 1 nanosecond[J].IEEE Transactions on Plasma Science,2004,32(4):1587-1599.
[16]Jiang N,Cooper B Y.Frequency-dependent interaction of ultrashort E-fields with nociceptor membranes and proteins[J].Bioelectromagnetics,2011,32(2):148-163.
[17]Schoenbach K H,Xiao S,Joshi R P,et al.The effect of intense subnanosecond electrical pulses on biological cells[J].IEEE Transactions on Plasma Science,2008,36(2):414-422.
[18]Xiao S,Guo S,Nesin V,et al.Subnanosecond electric pulses cause membrane permeabilization and cell death[J].IEEE Transactions on Biomedical Engineering,2011,58(5):1239-1245.
[19]Xiao S,Altunc S,Kumar P,et al.A reflector antenna for focusing subnanosecond pulses in the near field[J].IEEE Antennas Wireless Propagation Letters,2010,9(1):12-15.
[20]Altunc S,Baum C E,Buchenauer C J,et al.Design of a special dielectric lens for concentrating a subnanosecond electromagnetic pulse on a biological target[J].IEEE Transactions on Dielectrics and Electrical Insulation,2009,16(5):1364-1375.
[21]郭飞,姚陈果,刘泽辉,等.采用冲激脉冲辐射天线实现皮秒脉冲电场生物组织聚焦的仿真分析[J].高电压技术,2013,39(1):175-180.
Guo Fei,Yao Chenguo,Liu Zehui,et al.Simulation analysis of focusing picosecond pulsed electric fields into biological tissue with impulse radiating antenna[J].High Voltage Engineering,2013,39(1):175-180.
[22]Kumar P,Baum C E,Altunc S,et al.A hyperband antenna to launch and focus fast high-voltage pulses onto biological targets[J].IEEE Transactions on Microwave Theory and Techniques,2011,59(4):1090-1101.
Focusing of Picosecond Pulsed Electric Fields in Human Brain Model with Impulse Radiating Antenna
Guo Fei1,2Li Chengxiang2Tang Xianlun1Chen Gonggui1Yao Chenguo2
(1.College of Automation of Chongqing University of Posts and Telecommunications Chongqing400065China 2.State Key Laboratory of Power Transmission Equipment & System Security and New Technology Chongqing UniversityChongqing400030China)
A prolate-spheroidal reflector antenna model and a dielectric lens model are constructed with the 3D electromagnetic simulation software of CST Microwave Studio.The focusing properties of the picosecond pulsed electric field (psPEF) caused by the impulse radiating antenna (IRA) in the human brain model are then studied.The simulation results indicate that:The electric field at the second focusF2keeps the time-domain characteristics of the input pulse;The psPEF can penetrate into the brain at a depth of 8 cm where the smallest focal spot is created;The focal size is 1 cm×2 cm×1 cm with non-lossy dielectric lens or without dielectric lens,and the focal size is less than 1 cm×1 cm×1 cm with the help of lossy dielectric lens.The simulation results demonstrate that effective focusing of the psPEF in deep brain can be obtained with the combination of the lossy dielectric lens and a single IRA.
Picosecond pulsed electric field,impulse radiating antenna,hugo brain model,non-lossy dielectric lens,lossy dielectric lens
2015-01-29改稿日期2015-05-14
TM836;Q64
郭飞男,1988年生,讲师,博士,研究方向为生物电磁学。
E-mail:guofei@cqupt.edu.cn(通信作者)
李成祥男,1979年生,副教授,博士,研究方向为脉冲功率技术在生物医学中的应用。
E-mail:lichengxiang@cqu.edu.cn
国家自然科学基金(51507024、51307187)和重庆邮电大学自然科学基金(A2015-67)资助项目。
