铁锡复合氧化物催化合成ε-己内酯
2016-10-10章亚东马永丽马金玲赵岩岩贾金峰
章亚东,马永丽,马金玲,赵岩岩,贾金峰
(郑州大学 化工与能源学院,河南 郑州 450001)
铁锡复合氧化物催化合成ε-己内酯
章亚东,马永丽,马金玲,赵岩岩,贾金峰
(郑州大学 化工与能源学院,河南 郑州 450001)
在分子氧-苯甲醛体系,由共沉淀法制备的Fe-Sn-O复合氧化物作为催化剂,催化分子氧化环己酮合成ε-己内酯,通过单因素实验,得到适宜的合成条件:常温常压下,以环己酮用量为5 mmol计;n(苯甲醛) ∶n(环己酮) = 3∶1;1,2-二氯乙烷20 mL;氧气流速20 mL/min;反应时间4 h;反应温度55 °C.该条件下,ε-己内酯收率达到98.8 %,选择性达到99.0%;采用SEM、XRD等对催化剂的结构进行表征;催化剂重复使用5次仍保持较高活性.
Fe-Sn-O复合氧化物;环己酮;苯甲醛;ε-己内酯
0 引言
ε-己内酯是一种重要的化工中间体,常用于合成聚己内酯(PCL),PCL常用作生物降解塑料、医用高分子材料,此外低聚量的PCL还可用于合成革、胶黏剂、涂料等[1-2].ε-己内酯可由氧化环己酮进行缩合酯化重排反应[3]合成.传统氧化剂包括过氧酸类以及过氧有机醇类,其中过氧酸类对设备有较大的腐蚀性;过氧有机醇价格昂贵[4-6].双氧水与分子氧是比较环保的氧化剂,逐渐被科学研究者所关注,杨志旺等[2]采用双氧水作为氧化剂,用氧化环己酮制备ε-己内酯,在70 ℃反应8 h时,ε-己内酯收率达85.1%,但双氧水易分解,运输不方便.氧气作为氧化剂无污染,来源丰富[7-8],但氧化能力有限,需使用催化剂,常用的催化剂主要有均相催化剂与非均相催化剂,由于非均相催化剂易于从反应体系分离并重复使用,所以成为近年来研究的热点,如负载锡的分子筛、负载铁的黏土及负载锡的水滑石等非均相催化剂[ 9-11],Kawabata[12]采用负载铁的MCM-41作为催化剂,分子氧作为氧化剂,催化氧化环己酮合成ε-己内酯,可使目标产物收率达77 %,但上述催化剂存在制备复杂或活性低等缺点,所以探索出高活性高选择性以及易于回收利用的催化剂具有重大意义.
笔者选用Fe-Sn-O复合氧化物作为催化剂,制备简单,活性以及选择性均比较高,可重复使用,同时笔者还考察了各个因素对收率的影响,对催化剂进行了系列表征,并探讨了催化机理.
1 实验部分
1.1主要试剂与仪器
环己酮、九水硝酸铁、五水四氯化锡、苯甲醛,AR,国药集团化学试剂有限公司;GC9800型气相色谱仪,上海科创色谱仪器有限公司;D8型X射线衍射仪(德国布鲁克公司);扫描电子显微镜(JSM1500F).
1.2催化剂制备
在250 mL圆底三口瓶中加入2 mol/L的无水碳酸钠溶液,滴加一定摩尔比的SnCl4与Fe(NO3)3混合溶液,边滴边搅拌,使用2 mol/L的氢氧化钠溶液调节pH=10,继续搅拌2 h,然后333 K下静置40 h,抽滤,去离子水洗涤至中性,373 K干燥24 h,以7 K/min在马弗炉内上升至一定温度T1,煅烧一段时间t1.碾碎催化剂到一定颗粒度,超声作用2 h.同样方法制备不同底物的催化剂.所得催化剂以M-N-x-T1-t1表示(M、N为金属离子;x为M与N的摩尔比).
1.3ε -己内酯的合成过程
向带有冷凝管的50 mL的四口圆底烧瓶中加入20 mL 1,2-二氯乙烷,90 mg催化剂,5 mmol环己酮,20 mmol苯甲醛,加热搅拌,常温常压下以15 mL/min体积流量通氧气,反应温度T2= 50 °C,反应5 h,反应结束后离心分离出催化剂,过滤除去少量结晶出的苯甲酸.气相检测,检测结果见图1,保留时间及其对应物质见表1,由图1和表1可知,反应所得的ε-己内酯与平行产物苯甲酸沸点相近,并且高温下ε-己内酯易聚合,后续采用减压精馏分离ε-己内酯.
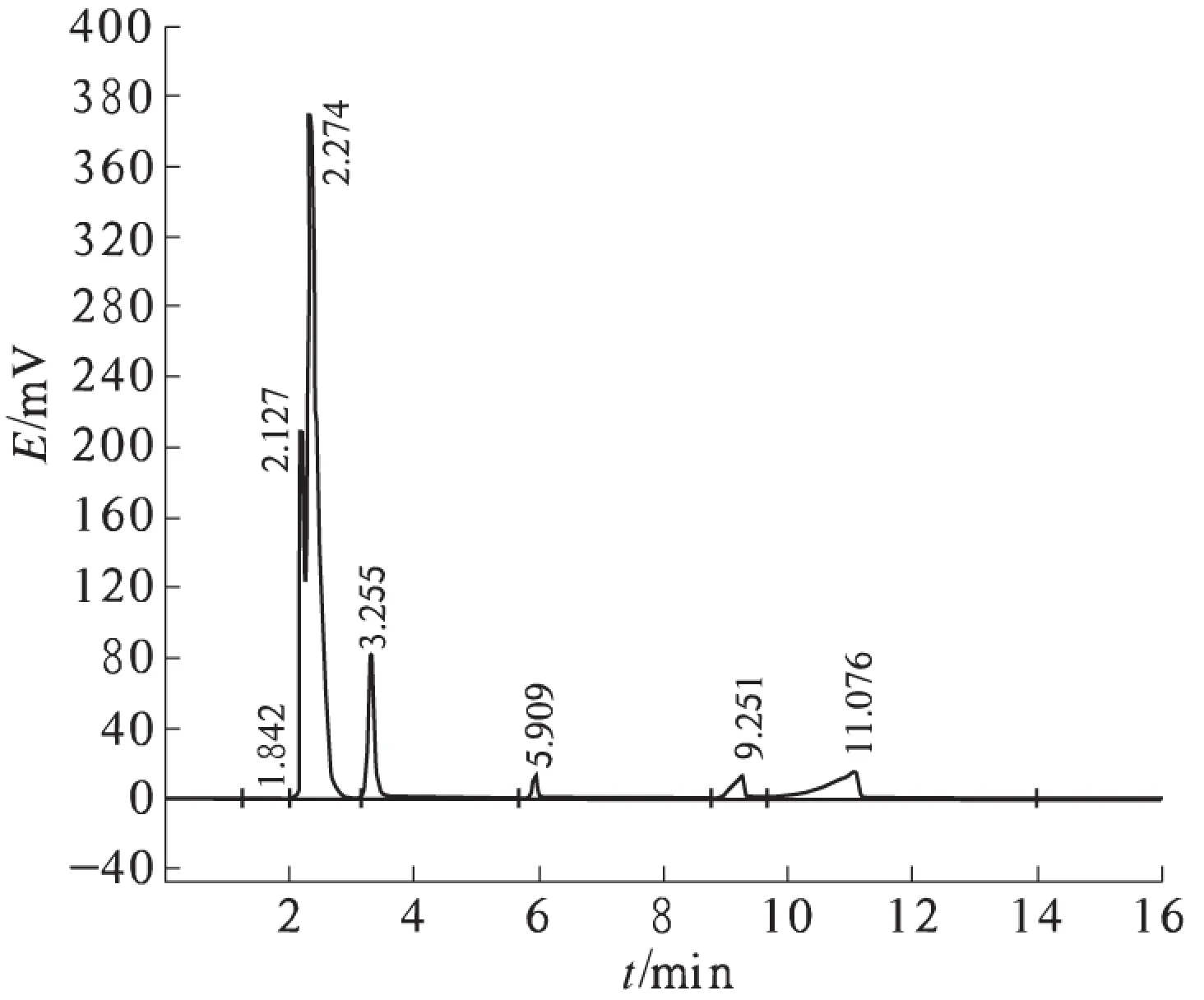
图1 反应液气相色谱图Fig.1 The gas chromatogram of reaction liquid

表1 保留时间与物质对应表Tab.1 Retention time and material table
2 结果与讨论
2.1催化剂的筛选
催化剂对反应收率有较大影响.实验考察了以5 mmol环己酮为反应底物,20 mmol苯甲醛为共氧剂,20 mL 1,2-二氯乙烷为溶剂,常温常压下以15 mL/min体积流量通氧气,50 °C下加热搅拌5 h,合成方程式如下:
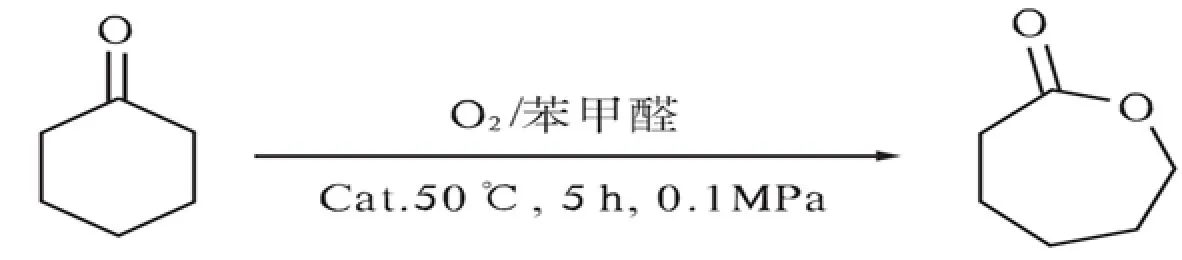
实验结果如表2所示.从表2可以看出,催化剂煅烧温度由450 °C逐渐增加时,反应收率先增加后减少,在850 °C反应收率达到最大(如实验3;实验7;实验11).煅烧温度引起煅烧产物物相的改变,实验结果表明850 °C所形成的催化剂所具备的物相活性最高.铁锡摩尔比在1∶1时催化剂活性最高,金属复合氧化物的催化活性与其含有的d轨道空穴数量有关,含较多d轨道空穴的铁原子与金属锡形成的复合氧化物时d轨道空穴数量相对减少,由实验结果可以推测铁锡摩尔比在1∶1时所具备的数量为较佳数量,催化性能较好.故合适的催化剂为Fe-Sn-1∶1-850-5.

表2 催化剂对收率的影响Tab.2 The impact on yield by catalysts
2.2醛还原剂的筛选
醛在合成过程中起还原剂作用,对反应收率影响较大.仅改变加入醛的种类,并使用2.1所筛选的催化剂,保持其他合成条件不变,考察醛的种类其对反应收率的影响,结果见表3.

表3 醛对收率的影响Tab.3 The impact on yield by aldehydes
表3表明,苯甲醛充当共氧剂收率最高,可达93.9 %,效果较好,这是因为反应过程中醛首先被氧气氧化为过氧酸,然后过氧酸的质子氢与环己酮分子结构中的羰基氧结合,同时过氧酸根与环己酮的羰基碳发生亲核作用,形成过渡中间体,而后过渡中间体发生分子内重排,苯甲酸根作为离去基团离去,同时得到目标产物.所以重排过程是反应过程中一个关键过程.而重排过程中,苯甲酸根结构由于存在羰基与苯环的共轭效应,因此,作为离去基团更加稳定,有利于产物的生成,故而苯甲醛是较好的还原剂.
2.3催化剂用量的选择
催化剂用量在催化合成中也至关重要.保持其他反应条件不变,同2.2节,仅改变加入催化剂的用量,考察其对收率的影响,结果见图2,加入催化剂,反应选择性大幅度提高,当催化剂量增加时,收率先增加后趋于平稳,催化剂可降低所需活化能使反应物分子易于活化,当催化剂达到与底物量相适应的量时,继续增加其用量不再使反应加速,反应趋于平衡,故合适催化剂用量为80 mg.
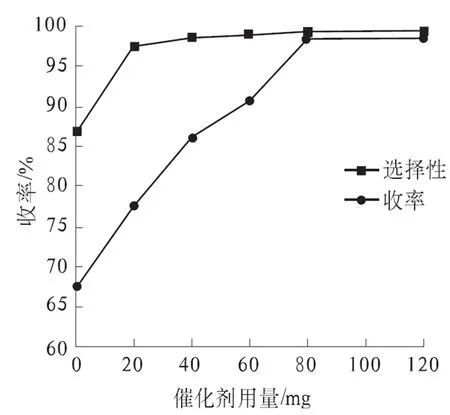
图2 催化剂用量对反应的影响Fig.2 The impact on yield by catalyst dosages
2.4醛酮摩尔比的影响
向5 mmol环己酮,20 mmol苯甲醛,20 mL 1,2-二氯乙烷的反应体系中,加入90 mg 所筛选出的催化剂,50 °C下加热搅拌5 h,改变加入苯甲醛的摩尔量,考察不同苯甲醛与环己酮的摩尔比对反应收率的影响,结果见图3.

图3 不同的苯甲醛与环己酮的摩尔比对反应的影响Fig.3 The impact on yield by molar ratio of benzaldehyde to cyclohexanone
图3表明,随苯甲醛用量的增加,反应收率增加,当苯甲醛与环己酮摩尔比为3∶1时,反应收率最高,继续增加苯甲醛的用量,收率有所下降,这是由于苯甲醛用量过大时,降低了环己酮的相对浓度,因此,适宜的苯甲醛环己酮的摩尔比为3∶1.
2.5反应温度与反应时间的影响
其他条件同2.4节,改变反应温度以及反应时间,考察其对收率的影响,结果见图4,反应温度由45 °C增加到55 °C,反应收率增加,反应温度继续增加时,收率降低.当反应温度过低时,反应物中活化分子数量太少,不利于反应进行;当反应温度过高时,氧气在反应液中的溶解度下降,也不利于反应进行.随着反应的进行,反应收率增加,反应进行4 h时,反应收率可达98.7 %,反应时间继续增长时,反应收率不再增加,所以较佳的反应温度与反应时间分别为55 °C与4 h.

图4 反应温度与反应时间对反应收率的影响Fig.4 The impact on yield by reaction Temperature and reaction time
2.6氧气流量影响
其他反应条件如2.5节,常温常压下,仅改变氧气流速,考察其对反应的影响,结果见图5,当氧气流速增大时,反应收率先增加后下降,而过大的氧气流速易将反应原料带出体系,使收率降低,所以较佳的氧气流速为20 mL/min.
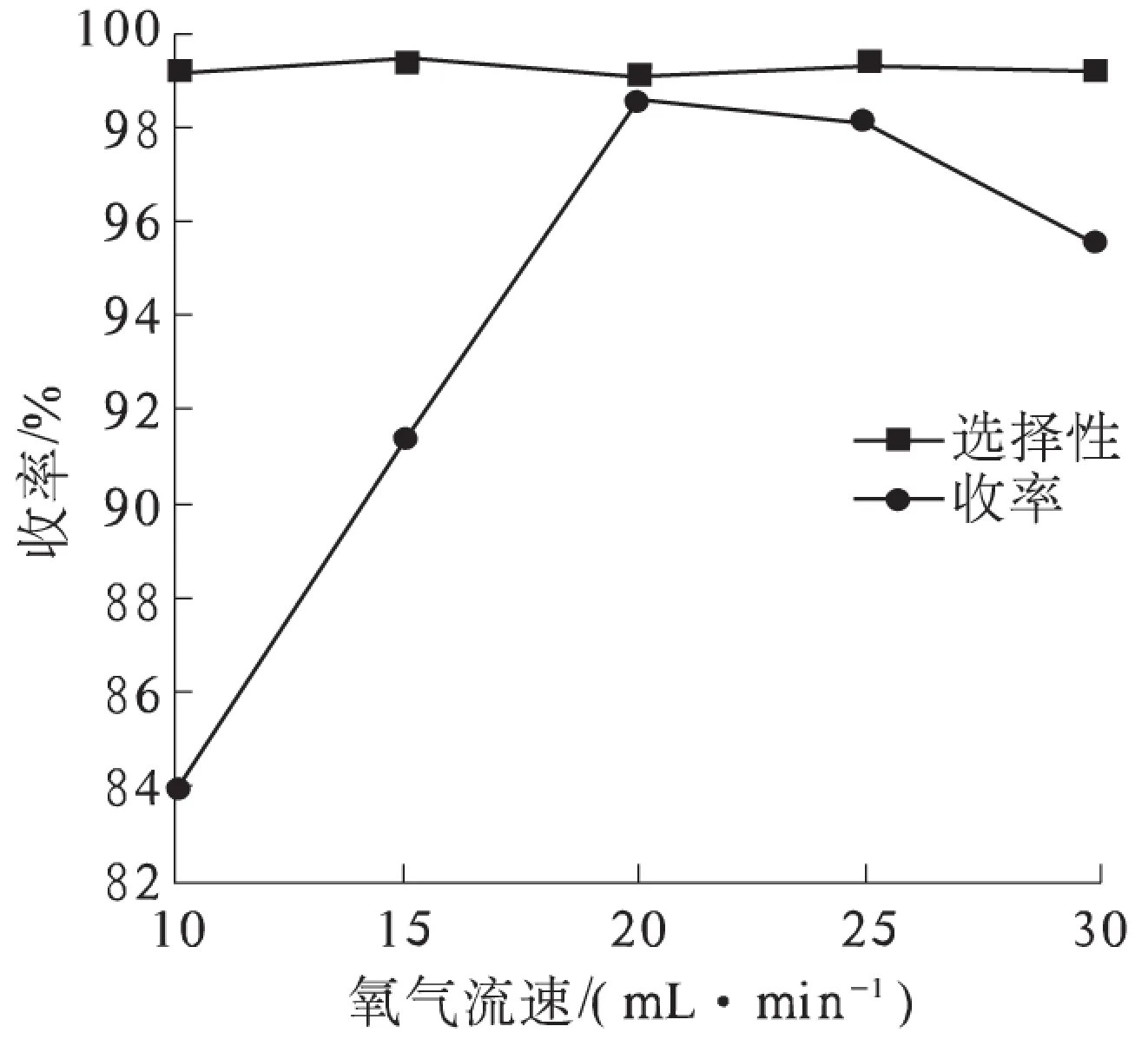
图5 氧气流速对反应收率的影响Fig.5 The impact on yield by oxygen flow rate
2.7催化剂重复性实验
在单因素所得反应条件下,对催化剂的重复性进行考察.结果表明,新制备的催化剂催化氧化环己酮制备ε-己内酯,可使环己酮转化率达99.9 %,ε-己内酯选择性达99.0 %,收率达98.8 %,对催化剂洗涤、干燥后,重复使用,反应5次后,活性与选择性仍然可以达到97.5 %以及96.3 %,此催化剂可多次重复使用,适于工业化生产.
2.8催化剂表征
通过扫描电子显微镜以及X射线衍射仪对催化剂进行表征.结果见图6~7.对比新制备的催化剂的XRD图谱(图6(a))、SEM图谱(图7(a))与重复使用5次后的催化剂的XRD图谱(图6(b))、SEM图谱(图7(b)),重复使用5次后催化剂的XRD峰型以及形貌基本无变化,表明催化剂在使用时结构没被破坏.图6(a)曲线中衍射峰26.584°、33.874°、37.949°在标准图库中分别对应SnO2(PDF NO.71-0652)的特征峰,其中衍射峰 26.584°、33.874°分别对应于正方晶形SnO2的110与101晶面,说明催化剂含有正方晶型结构;图6(a)曲线中衍射峰 24.200°、33.211°与标准图库中的α-Fe2O3(PDF NO.71-0652)的特征峰相对应,表明催化剂是由正方晶型的SnO2与α-Fe2O3两种氧化物组成.

图6 催化剂的XRD表征图谱Fig.6 XRD patterns of the catalyst

图7 催化剂的SEM图Fig.7 SEM images of catalyst
2.9催化机理探讨
催化反应过程如图8所示.Fe-Sn-O复合氧化物中铁为过渡金属,铁原子的d轨道中未占用的d电子或空穴较多,催化过程中 ,Fe-Sn-O复合氧化物的L酸中心与氧中的孤对电子配位结合,电子由氧气流入d轨道空穴,并同时将氧传递给苯甲醛形成过苯甲酸,活化的过苯甲酸上的H+将环己酮的羰基氧质子化,过氧酸根对羰基碳亲核进攻,进而与相邻的碳原子发生分子内重排,酸根离去,形成目标产物.
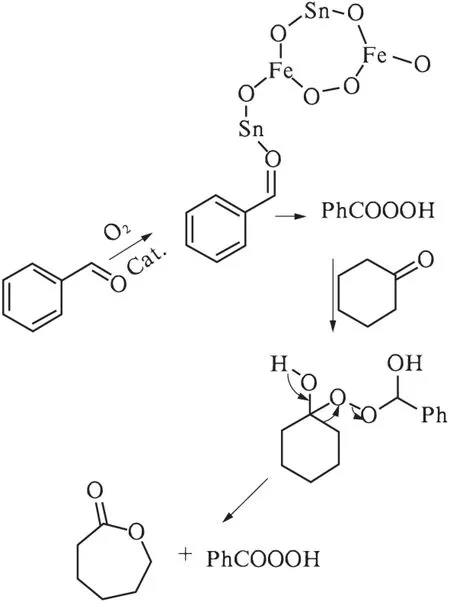
图8 可能的反应机理Fig.8 The possible catalytic mechanism
3 结论
实验所制备催化剂Fe-Sn-O复合氧化物制备简单,活性及选择性高,重复性好.通过单因素实验得到适宜的反应条件为:
常温常压下,以环己酮用量为5 mmol计,n(苯甲醛) ∶n(环己酮) = 3∶1;催化剂Fe-Sn-1∶1-850-5用量80 mg;1,2-二氯乙烷20 mL;氧气流速20 mL/min;反应温度55 °C持续反应4 h;环己酮转化率可达99.9 %;ε-己内酯选择性可达99.0 %;收率可达98.8 %;催化剂重复使用5次后依然保持较高活性,可使反应收率达96.3 %.
SEM、XRD表明催化剂中含有α-Fe2O3以及正方晶形SnO2,重复使用5次后形貌基本无变化.
[1]黎树根,李长存.ε-己内酯产业现状及其应用[J].合成纤维工业,2013,36 (1):46-49.
[2]杨志旺,马振宏, 牛棱渊,等.SBA-15负载硅钨酸催化环己酮 Baeyer-Villiger 氧化[J].催化学报,2011,32 (3):463-467.
[3]韩巧,卢会杰,王敏灿,等.γ-己内酯的合成研究[J].郑州大学学报(自然科学版),1999,31 (2):88-89.
[4]BAJ S,CHROBOK A,SLUPSKA R.The Baeyer-Villiger oxidation of ketones with bis(trimethylsilyl) peroxide in the presence of ionic liquids as the solvent and catalyst[J].Green Chem,2009, 11(2):279-282.
[5]MARIA E N,ROSSELLA M, ANDREA O, et al.Baeyer-villiger oxidation with potassium peroxomonosulfate supported on acidic silica gel. [J].J Org Chem,2005,70 (26):10879-10882.
[6]KOO D H, KIM M,CHANG S.WO3 nanoparticles on MCM-48 as a highly selective and versatile heter-ogeneous catalyst for the oxidation of olefins sulfides and cyclic ketones[J].Org Lett,2005,22(7):5015-5018.
[7]DUTTA B,JANAN S,BHUNIA S,et al.Heter-ogeneous Baeyer-Villiger oxidation of cyclic ketone using tert-BuOOH as oxidant[J].Appl Catal A,2010,382 (1):90-98.
[8]LI Yuefang,GUO Mingqi,YIN Shuangfeng,et al.Graphite as a highly efficient and stable catalyst for the production of lactones[J].Carbon,2013,55:269-275.
[9]YANG Z W,NIU L Y,MA Z H,et al.Fabrication of highly active Sn/W mixed transition-metal oxides as solid acid catalysts[J].Transition Met Chem,2011,36 (3):269-274.
[10]BELAROUI L S,SOROKIN A B,FIGUERAS F,et al.Comparative Baeyer-Villiger oxidation of cyclohexanone on Fe-pillared clays and iron tetrasuf-ophthalocyanine covalently supported on silica[J].Comptes Rendus Chimie,2010,13 (4):466-472.
[11]CORMA A,NAVARRO M T,RENZ M.Lewis acidic Sn(IV) centers grafted onto MCM-41 as catalytic sites for the Baeyer-Villiger oxidation with hydrogen peroxide[J].J Catal,2003,219:242-246.
[12]KAWABATA T,OHISHI Y,ITSUKI S,et al.Iron-containing MCM-41 catalysts for Baeyer-Villiger oxidation of ketones using molecular oxygen and be-nzaldehyde[J].J Mol Catal,2005,236:99-106.
Synthesis of ε-caprolactone with Fe-Sn Mixed Oxides as Catalysts
ZHANG Yadong,MA Yongli,MA Jinling,ZHAO Yanyan,JIA Jinfeng
(School of Chemical Engineering and Energy,Zhengzhou University,Zhengzhou 450001, China)
The ε-caprolactone was synthesized by cyclohexanone in the oxygen-benzaldehyde system, Fe-Sn-O mixed oxide prepared by coprecipitation being as catalyst. The proper conditions were obtained by single factor experiments. Based on 5 mmol cyclohexanone at ambient temperature and pressure, the proper conditions were as follows: the molar ratio of benzaldehyde to cyclohexanone being 3∶1, the oxygen flow ratio being 20 mL/min, the amount of 1,2-dichloroethane being 20 mL, reaction temperature being 55°C, reaction time being 4 h. The yield of 98.8 % and selectivity of 99.0 % of ε-caprolactone were obtained. The structure of the catalyst was characterized by the measures of SEM and XRD. And the catalyst can be reused for five times without significant loss in activity and selectivity.
Fe-Sn-O mixed oxide;cyclohexanone;benzaldehyde;ε-caprolactone
2015-10-27;
2015-12-22
河南省高校科技创新人才计划资助项目(2010HASTIT037)
章亚东(1965—),男,河南正阳人,郑州大学教授,博士,主要从事精细有机合成方面的研究,E-mail:zzuzhangyadong@126.com.
1671-6833(2016)04-0026-05
TQ426.94
A
10.13705/j.issn.1671-6833.2016.04.006
