典型咪唑类离子液体萃取水质组胺效率的研究
2016-09-26宋志军蔡美强
宋志军,蔡美强
1(浙江工商大学 食品与生物工程学院,浙江 杭州,310018) 2(浙江工商大学 环境科学与工程学院,浙江 杭州,310018)
典型咪唑类离子液体萃取水质组胺效率的研究
宋志军1*,蔡美强2
1(浙江工商大学 食品与生物工程学院,浙江 杭州,310018) 2(浙江工商大学 环境科学与工程学院,浙江 杭州,310018)
以离子液体([CnMIM]X:n=4、6、8、10;X=BF4-1、PF6-1、Br-1、Cl-1)为萃取剂,采用液-液分散微萃取技术及HPLC-UV检测方法研究了典型咪唑类离子液体萃取富集水质组胺的性能。结果表明:亲水性离子液体优于疏水性离子液体;随着取代基碳链的增长,BF4-1、PF6-1型离子液体萃取能力先增强后减弱,而Br-1、Cl-1型离子液体则呈现减弱趋势;阴离子对萃取效率的影响基本遵循BF4-1>PF6-1>Br-1>Cl-1的规律;常用超声、微波辅助萃取手段能有效提升组胺的萃取效率,且前者较适用于Br-1、Cl-1型离子液体,后者则较适用于BF4-1、PF6-1型离子液体。
咪唑类离子液体;组胺;萃取效率;分散液-液微萃取;HPLC-UV
组胺(histamine)是组胺酸在组氨酸脱羧酶的作用下脱去羧基后形成的一种胺类物质,是生物胺中对体健康影响最大的物质之一[1];水产品尤其是一些青皮红肉鱼类,在长时间贮存或腐败情况时易产生组胺,当食用后会发生过敏性食物中毒,严重时可危及生命[2-5]。目前,已建立了众多水产品中组胺的检测方法,如分光光度法[6]、薄层色谱法[7]、气相色谱法[8]、毛细管电泳法[9]和高效液相色谱法[10-11]等。因组胺在待测样品中的低浓度水平及样品自身基质的复杂性,检测前需对目标物进行萃取分离富集预处理。其常用的预处理方法有固相萃取法[12]、固相微萃取法[13-14]、液相微萃取法[15]及液-液微萃取法[16]等,在此过程中会使用大量的有毒、易爆、易燃、易挥发的有机溶剂,不仅价格昂贵、步骤繁琐,而且会带来二次环境污染问题。
离子液体(ILs)作为一种新型的绿色、多功能型溶剂,其自身具有低蒸汽压、宽液程、高溶解性(溶解大多数有机物)、热稳定好、无二次污染等特点,非常适合作为萃取富集(尤其是微萃取)溶剂;且与传统有机溶剂萃取剂相比,具有无毒、安全、简便、快速、富集能力强等优点;众多研究者[17-21]已将其应用于多种有机物、无机物的萃取分离,结果显示离子液体的萃取能力在一定程度上优于传统有机溶剂。本文基于国标《水质组胺等五种生物胺的测定—高效液相色谱法》(GB/T21970—2008)[22],以典型咪唑类离子液体([CnMIM]X:n=4、6、8、10;X=BF4-1、PF6-1、Br-1、Cl-1)为萃取溶剂、以水质组胺为目标物,利用分散液-液微萃取技术、HPLC-UV法,详细研究了咪唑类离子液体的水溶性、阳离子结构(碳链的长短)、阴离子种类(BF4-1、PF6-1、Br-1、Cl-1)及超声、微波辅助手段对离子液体萃取组胺性能的影响。
1 实验部分
1.1试剂材料
乙腈、甲醇、丙酮为色谱纯,德国Merck公司;氨水、乙酸铵、NaOH、NaH2PO4-H3BO3溶液为优级纯,上海国药集团公司,上述溶剂使用前经0.2μm滤膜过滤。丹磺酰氯(纯度≥ 99 %)和组胺二盐酸盐(纯度>99 %),购自Sigma公司;实验涉及的离子液体系列产品(纯度99 %),为本室自制;本实验用水均来自Milli-Q纯水系统。
组胺标准贮备溶液:准确称取组胺二盐酸盐标准品0.500 0g于50mL容量瓶中,用超纯水定容至刻度,配制成质量浓度为10.0mg/mL的组胺标准储备液,避光,4 ℃保存备用;使用时采用逐级稀释至所需浓度。
1.2仪器设备
Agilent1100液相色谱仪配紫外检测器,Agilent公司;涡旋混合器,美国Talboys公司; 高速离心机,日立;LegendRT型离心机,德国Heraeus公司;KQ-2200型超声波清洗器昆山市超声仪器有限公司;全玻璃溶剂过滤器,美国Waters公司;家用微波炉,广州美的生活电器公司;Milli-Q纯水系统,美国Millipore公司。
1.3色谱条件
色谱柱:AgilentXDBC18(250mm×4.6mm,5μm);流动相:A,乙腈;B,乙酸铵(0. 02mol/L);梯度洗脱条件见表1[22]。柱温: 35 ℃;流速:1mL/min;进样量:20μL;检测波长:254nm。
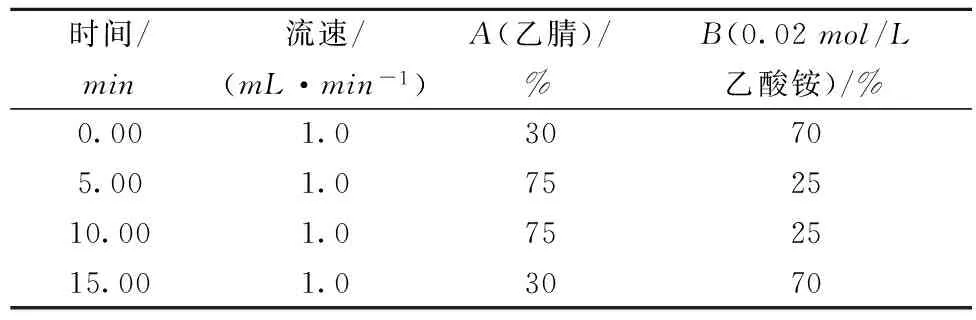
表1 梯度洗脱条件
1.4实验方法
实验在已优化的最佳参数条件下进行:取100μL组胺标准溶液(1.0μg/mL)于1.5mL离心管中,依次加入NaH2PO4-H3BO3溶液(pH8.0)200μL、丹磺酰氯溶液(10mg/mL)400μL,具塞室温避光衍生化反应40min,加体积分数为20%的氨水-乙腈溶液100μL,静置30min。将30μL的离子液体加入已衍生好的混合液中,超声或微波2~4min,使离子液体均匀分散到溶液中形成均一稳定的乳状液,将溶液放入离心机中5 000r/min下离心处理4min,待分层清晰后,吸出离子液体层,用高效液相色谱仪进行定量分析;重复测定6次取平均值。萃取效率(E)为离子液体相中组胺的量与组胺总量的比值,按公式(1)计算。
其中:cIL、c0为组胺在离子液体相及标准工作溶液中的浓度;VIL、V0为离子液体相及标准工作溶液的体积。
2 结果与讨论
2.1离子液体水溶性对萃取效率的影响
实验考察了两大类常用典型代表性离子液体(疏水性离子液体[C4MIM]PF6、[C6MIM] PF6、[C8MIM] PF6、[C10MIM] PF6和亲水性离子液体[C4MIM] BF4、[C6MIM] BF4、[C8MIM] BF4、[C10MIM] BF4)对水质组胺的萃取能力;其中,图1为典型空白样品及实际样品的色谱图,图2为具体实验结果。由图2可以看出,本实验条件下,亲水性离子液体对水质组胺的萃取能力整体略优于疏水性离子液体对水质组胺的萃取能力。
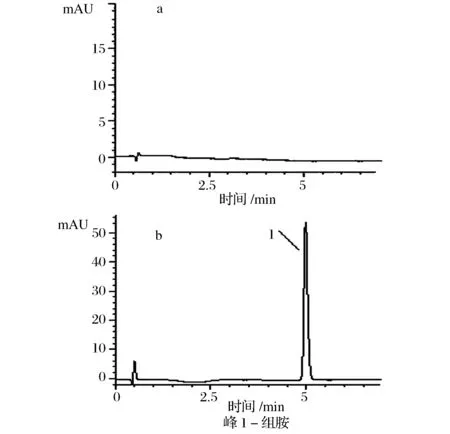
图1 组胺样品色谱图(a)空白样(b)典型阳性样品Fig.1 Typical chromatograms for the histamine samples, (a) blank sample (b) typical positive sample
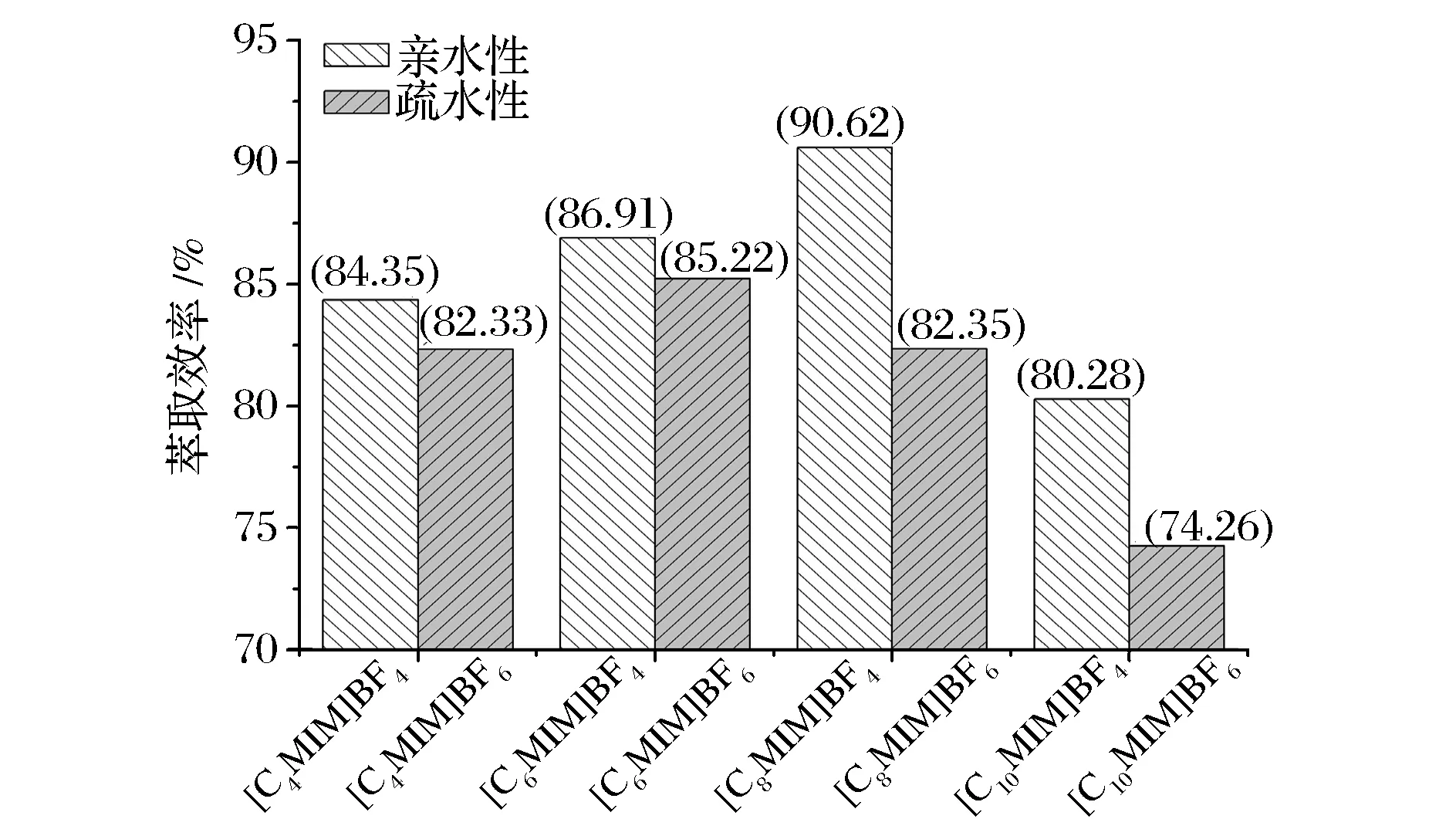
图2 离子液体水溶性对萃取效率的影响Fig.2 Effect of water solubility on the extraction efficiency of histamine
依据经典萃取理论来分析,在微波/超声辅助萃取过程中,亲水性离子液体更容易均匀分散到水质组胺中去,以形成更多的囊泡、增大了接触面积,尽而显现出更强萃取富集组胺的能力。
2.2离子液体阳离子结构对萃取效率的影响
咪唑作为五元杂环化合物,其1~5号位皆可被不同类别的取代基所取代而形成种类繁多的咪唑阳离子;其中,典型的咪唑类有机阳离子通常表现为1号位的H原子被烷基取代、3号位N原子的孤对电子与取代基形成大π键;对由此类有机阳离子与有机/无机阴离子组合形成的离子液体,在阴离子相同的情况下其取代基碳链的长短是影响离子液体熔点、密度、黏度等物理化学性质的主要因素之一[23- 24]。本实验研究了[CnMIM]X(n=4、6、8、10;X= BF4-1、PF6-1、Br-1、Cl-1)系列离子液体萃取富集组胺能力的变化规律,实验结果如图3所示。
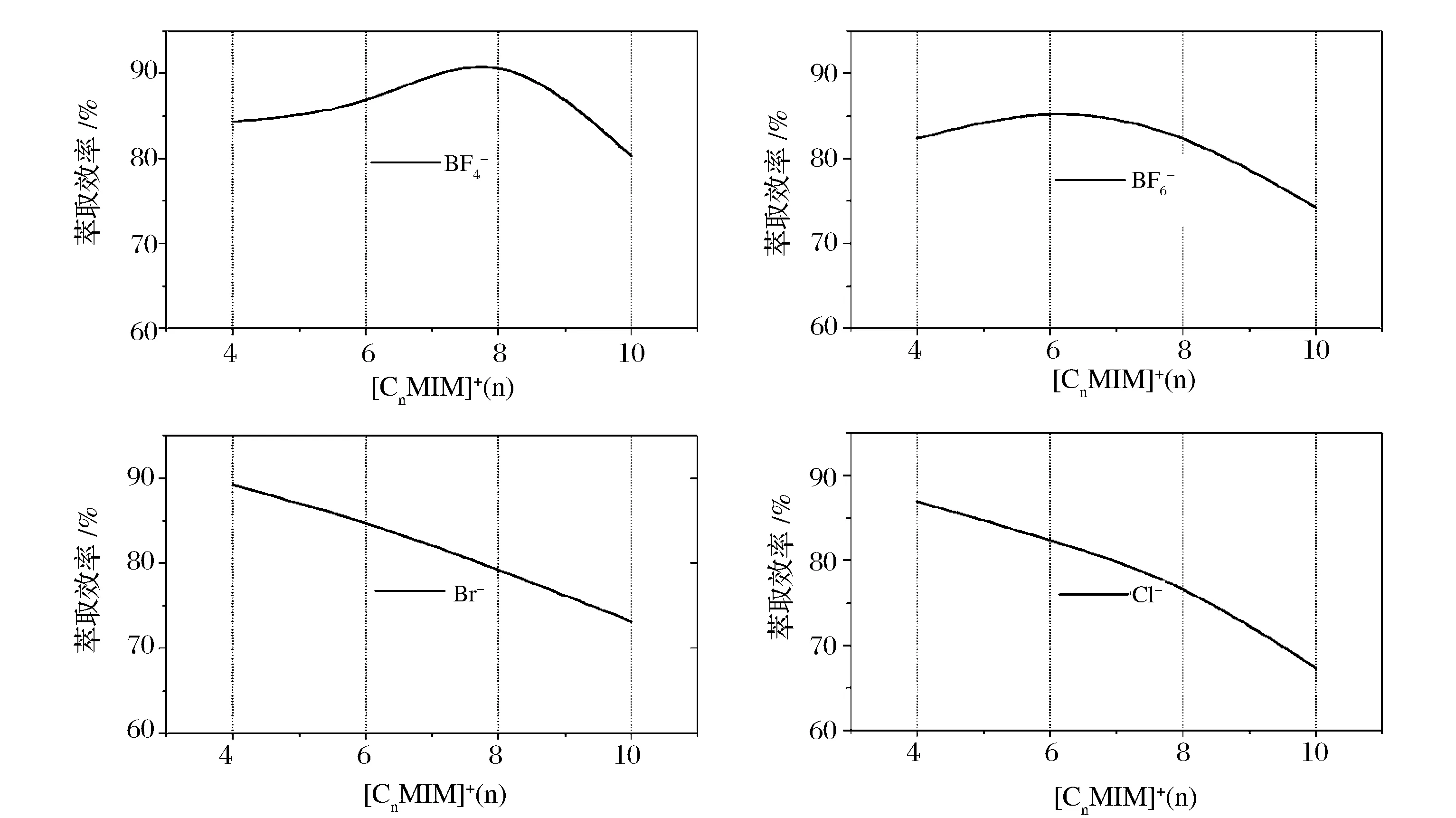
图3 离子液体阳离子结构对萃取效率的影响Fig.3 Effect of ionic liquid cation structure on the extraction efficiency of histamine
由图3可知,咪唑五元环1号位取代基碳链的长度会对离子液体萃取富集组胺的能力产生显著影响;随着取代基碳链增长,BF4-1、PF6-1型离子液体萃取能力先增强后减弱,而Br-1、Cl-1型离子液体则呈现减弱趋势。通常认为,离子液体的黏度随着取代基碳链增长而增加、亲水性减弱,其萃取组胺的能力相应下降,Br-1、Cl-1型离子液体严格遵循此规律;BF4-1、PF6-1型离子液体所呈现的实验结果,可能与BF4-1、PF6-1阴离子自身的体积较大、电荷分布复杂等特征有关。
2.3离子液体阴离子种类对萃取效率的影响
离子液体的物理化学性质,不仅受阳离子的影响,也同样受阴离子结构与性质的影响[25-27],如在阳离子相同的情况下,阴离子体积越大、熔点越高,阴离子亲水、离子液体亲水,阴离子对称性高、离子液体黏度大等。图4为BF4-1、PF6-1、Br-1、Cl-1系列阴离子液体对萃取组胺能力的影响。
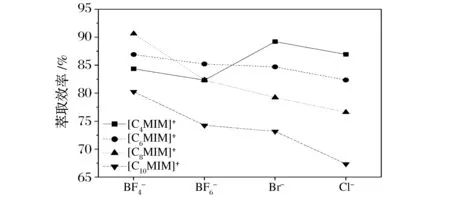
流体中不同阴离子种类图4 离子液体阴离子种类对萃取效率的影响Fig.4 Effect of ionic liquid anion species on the extraction efficiency of histamine
从图4中可以看出,对相同的[CnMIM]+(n=6、8、10)阳离子而言,阴离子对萃取能力的影响遵循BF4->PF6->Br->Cl-的规律;但对[C4MIM]+阳离子而言,却呈现Br-1>Cl-1>BF4-1>PF6-1规律,分析可能与其碳链较短、黏度相对较低有关。
2.4辅助萃取手段对萃取效率的影响
为了更好提升离子液体萃取富集目标物的实际效果,众多研究者曾尝试将各种辅助手段应用到萃取过程中去,其中较为常见的为超声[28-30]与微波[31-33]辅助;虽然二者基本原理不同(超声为机械波、微波为电磁波),但相关文献证明在实际应用中皆具有一定的效果。本研究在最佳实验条件下,以 [CnMIM]Br(n=4、6、8、10)、[C4MIM]X(X= BF4-1、PF6-1、Br-1、Cl-1)为对象,讨论对比了取得最大萃取效率的用时,如图5所示;以[C4MIM] BF4、[C4MIM] PF6、[C4MIM] Br、[C4MIM] Cl为对象,对2种辅助手段对萃取能力的提升影响情况进行对比分析,具体结果见表2。
由图5可知,对[CnMIM]Br系列离子液体而言,从时效角度考量,超声辅助萃取手段优于微波辅助手段;考虑其自身黏度变化的作用,离子液体侧链取代基碳链越短,则辅助手段的时效性越高。反观[C4MIM]X系列离子液体,2种辅助萃取手段所表现的时效性规律不够明显;对2种辅助手段而言,亲水型离子液体(BF4-1)较疏水型(PF6-1)离子液体的时效性高,Br-1离子液体时效性相对于Cl-1离子液体表现出较好的时效性;由于2种辅助萃取手段工作原理的差异,微波手段对对称性较好、体积较大的阴离子(BF4-1、PF6-1)型离子液体表现出较好的效果,而超声手段则比较适用于体积较小、结构简单阴离子(Br-1、Cl-1)型离子液体。同样,从表2可得出结论:阴离子(BF4-1、PF6-1)型离子液体宜选微波手段进行辅助萃取,超声则更适用于阴离子(Br-1、Cl-1)型
离子液体萃取组胺的辅助手段。

图5 辅助萃取手段对不同离子液体的时效性Fig.5 Effect of auxiliary extraction method on the time of extraction
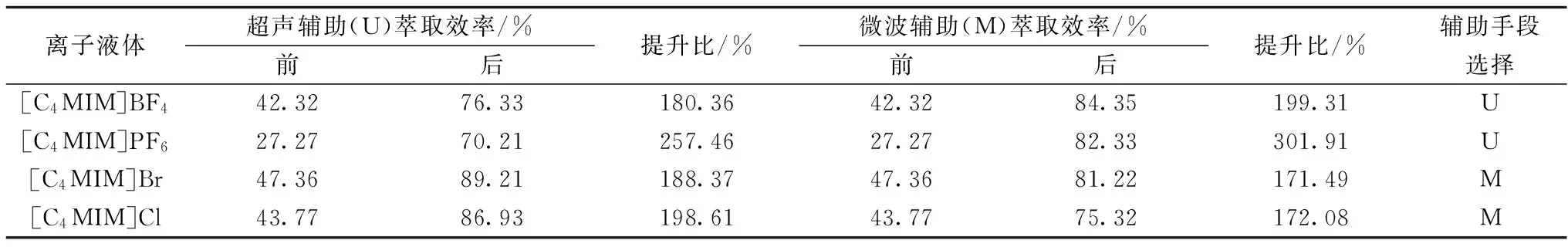
离子液体超声辅助(U)萃取效率/%前后提升比/%微波辅助(M)萃取效率/%前后提升比/%辅助手段选择[C4MIM]BF442.3276.33180.3642.3284.35199.31U[C4MIM]PF627.2770.21257.4627.2782.33301.91U[C4MIM]Br47.3689.21188.3747.3681.22171.49M[C4MIM]Cl43.7786.93198.6143.7775.32172.08M
注:U- ultrasonic assisted;M- microwave assisted。
3 结论
离子液体作为一种安全、环保的萃取溶剂,可被应用于水质组胺的萃取富集,且效果较好。本文以典型咪唑类离子液体([CnMIM]X:n=4、6、8、10;X= BF4-1、PF6-1、Br-1、Cl-1)为萃取剂,对其萃取富集水质组胺的性能进行了实验研究,得到如下结论:
(1)同等实验条件下,亲水性离子液体的组胺萃取效率优于疏水性离子液体。
(2)随着离子液体烷基取代基碳链的增长,BF4-1、PF6-1型离子液体萃取能力呈现先增强后减弱趋势,而Br-1、Cl-1型离子液体则呈现减弱趋势。
(3)阴离子对离子液体萃取组胺效率的影响基本遵循BF4-1>PF6-1>Br-1>Cl-1的规律([C4MIM]+阳离子型离子液体除外)。
(4)萃取过程中常用的超声、微波辅助萃取手段均能有效提升组胺的萃取效率,且前者适用于Br-1、Cl-1型离子液体、后者则较适用于BF4-1、PF6-1型离子液体。
[1]CHEN H C,Kung H F,CHEN W C,et at.Determination of histamine and histamine-forming bacteria in tuna dumpling implicated in a food-borne poisoning [J].Food Chem,2008,106(2):612-618.
[2]范青霞,孔亚明,马洪喜.一起因食用鲭鱼引起的组胺过敏慢性食物中毒[J].医学动物防制,2006,22(4):295-296.
[3]徐菊玲.一起鱼类引起的组胺中毒[J].中华预防医学杂志,2007,41(4):289.
[4]夏威,徐正龙,于颖慧.一起组胺中毒的调查报告[J].河南预防医学杂志, 2013,24(2):160-161.
[5]夏追平,程彬.杭州市下城区1997~2006年食物中毒情况分析[J].中国公共卫生,2008,24(8):1 013-1 015.
[6]张继红,马俊华,刘平.分光光度法测定鱼类产品中组胺[J].医学动物防制,2013(9):1 060-1 061.
[7]ROMANO A, KLEBANOWSKI H, LA GUERCHE S, et al. Determination of biogenic amines in wine by thin-layer chromatography/densitometry[J]. Food Chem, 2012,135(3):1 392-1 396.
[8]HWANG B S, WANG J T, CHOONG Y M. A rapid gas chromatographic method for the determination of histamine in fish and fish products[J]. Food Chem, 2003,82(2):329-334.
[9]NUMANOGLU E, BOYACI I H, TOPCU A. Simple determination of histamine in cheese by capillary electrophoresis with diode Array detection[J]. J Food drug Anal, 2008,16(6):74-80.
[10]WANG Z P, WU J L, WU S H, et al. High-performance liquid chromatographic determination of histamine in biological samples: The cerebrospinal fluid challenge - A review[J]. Anal Chim Acta. 2013,774:1-10.
[11]BUENO-SOLANO C, LOPEZ-CERVANTES J, SANCHEZ-MACHADO DI, et al. HPLC determination of histamine, tyramine and amino acids in shrimp by-products[J]. J Brazil Chem Soc, 2012,23(1):96-102.
[12]SELF R L, WU W H. Determination of eight biogenic amines in selected seafood products by MSPD extraction followed by UHPLC-Orbitrap MS[J]. Journal of Food Composition and Analysis, 2012,27(2):169-173.
[13]GONZALEZ-ALVAREZ J, BLANCO-GOMIS D, ARIAS-ABRODO P, et al. Analysis of beer volatiles by polymeric imidazolium-solid phase microextraction coatings: Synthesis and characterization of polymeric imidazolium ionic liquids[J]. Journal of Chromatography A, 2013,1 305:35-40.
[14]AUGER J, BOULAY R, JAILLAIS B, et al. Analysis of biogenic amines by solid-phase microextraction and high-performance liquid chromatography with electrochemical detection[J]. Journal of Chromatography A,2000,870(1/2):395-403.
[15]SAAID M, SAAD B, ALI ASM, et al. In situ derivatization hollow fibre liquid-phase microextraction for the determination of biogenic amines in food samples[J]. Journal of Chromatography A,2009,1 216(27):5 165-5 170.
[16]RAMOS R M, VALENTE I M, RODRIGUES J A. Analysis of biogenic amines in wines by salting-out assisted liquid-liquid extraction and high-performance liquid chromatography with fluorimetric detection[J]. Talanta, 2014,124(13):146-1451.
[17]ARCE A, EARLE M J, KATDARE S P, et al. Application of mutually immiscible ionic liquids to the separation of aromatic and aliphatic hydrocarbons by liquid extraction: a preliminary approach[J]. Phys Chem Chem Phys, 2008,10(18):2 538-2 542.
[18]ZHU H B, FAN Y C, Qian YL, et al. Determination of spices in food samples by ionic liquid aqueous solution extraction and ion chromatography[J]. Chinese Chem Lett,2014,25(3):465-468.
[19]KUBOTA F, SHIMOBORI Y, BABA Y, et al. Application of ionic liquids to extraction separation of rare earth metals with an effective diglycol amic acid extractant[J]. J Chem Eng Jpn, 2011,44(5):307-312.
[20]HOU D K, GUAN Y, DI X W. Temperature-induced ionic liquids dispersive liquid-liquid microextraction of tetracycline antibiotics in environmental water samples assisted by complexation[J]. Chromatographia,2011,73(11/12):1 057-1 064.
[21]VAEZZADEH M, SHEMIRANI F, MAJIDI B. Microextraction technique based on ionic liquid for preconcentration and determination of palladium in food additive, sea water, tea and biological samples[J]. Food Chem Toxicol, 2010,48(6):1 455-1 460.
[22]GB/T 21970—2008.水质组胺等五种生物胺的测定高效液相色谱法[S].
[23]APARICIO S, ATILHAN M, KARADAS F. Thermophysical properties of pure ionic liquids: Review of present situation[J]. Ind Eng Chem Res, 2010,49(20):9 580-9 595.
[24]邓友全.离子液体-性质、制备与应用[M].北京:中国石化出版社,2006:48-86.
[25]WAGNER Z, JACQUEMIN J, BENDOVA M. Database on ionic liquids solubilities in molecular solvents: Progress and prospects[J]. Abstr Pap Am Chem S, 2014,248(8):109.
[26]HAJIPOUR A R, RAFIEE F. Basic Ionic Liquids. A Short Review[J]. J Iran Chem Soc,2009,6(4):647-678.
[27]HAWKINS C A, GARVEY S L, DIETZ M L. Structural variations in room-temperature ionic liquids: Influence on metal ion partitioning modes and extraction selectivity[J]. Sep Purif Technol, 2012,89(2):31-38.
[28]JALBANI N, SOYLAK M. Ligandless ultrasonic-assisted and ionic liquid-based dispersive liquid-liquid microextraction of copper, nickel and lead in different food samples[J]. Food Chem, 2015,167:433-437.
[29]ZEEB M, MIRZA B, ZARE-DORABEI R, et al. Ionic liquid-based ultrasound-assisted in situ solvent formation microextraction combined with electrothermal atomic absorption spectrometry as a practical method for preconcentration and trace determination of vanadium in water and food samples[J]. Food Anal Method, 2014,7(9):1 783-1 790.
[30]ZHU S, MA C Y, FU Q Y, et al. Application of ionic liquids in an online ultrasonic assisted extraction and solid-phase trapping of rhodiosin and rhodionin from rhodiola rosea for UPLC[J]. Chromatographia, 2013,76(3/4):195-200.
[31]ZHANG R Z,SU P, YANG L,et al. Microwave-assisted preparation of poly(ionic liquids)-modified magnetic nanoparticles for pesticide extraction[J]. J Sep Sci, 2014,37(12):1 503-1 510.
[32]WEI Z F, ZU Y G, FU Y J, et al. Ionic liquids-based microwave-assisted extraction of active components from pigeon pea leaves for quantitative analysis[J]. Sep Purif Technol, 2013,102(1):75-81.
[33]JIAO J, GAI Q Y, F u Y J, et al. Microwave-assisted ionic liquids pretreatment followed by hydro-distillation for the efficient extraction of essential oil from Dryopteris fragrans and evaluation of its antioxidant efficacy in sunflower oil storage[J]. J Food Eng, 2013,117(4):477-485.
Study on the efficency of typical imidaxolium-based ionic liquid to extract water quality histamine
SONG Zhi-jun1*, CAI Mei-qiang2
1(School of Food Science and Biotechnology , Zhejiang Gongshang University, Hangzhou 310018, China) 2(School of Environmental Science and Engineering, Zhejiang Gongshang University, Hangzhou 310018, China)
The performance of the typical imidaxolium-based ionic liquid([CnMIM] X:n=4,6,8,10;X= BF4-1,PF6-1,Br-1,Cl-1)extraction and enrichment of the water quality histamine was studied by liquid - liquid micro-extraction and HPLC-UV detection. The results showed that the hydrophilic ionic liquid was better than the hydrophobic ionic liquids; with the increase of the carbon chain, the extraction ability of the PF6-1,BF4-1type ionic liquid was first increased and then decreased, while the Br-1,Cl-1type ionic liquid was weakened; The influence of anion on the extraction efficiency was followed the order of BF4-1>PF6-1> Br-1> Cl-1and the ultrasound and microwave assisted extraction can effectively improve the extraction efficiency of histamine. The former was suitable for Cl-1,Br-1type ionic liquid, the latter was more suitable for BF4-1,PF6-1type ionic liquid.
imidaxolium-based IL;extraction efficiency;histamine;dispersive liquid-liquid micro extraction; HPLC-UV
10.13995/j.cnki.11-1802/ts.201601042
博士研究生,讲师(本文通讯作者,E-mail:zhijunsong@zjgsu.edu.cn)。
浙江省科技计划项目(2014C37034)
2015-07-18,改回日期:2015-10-19
