大鼠肺间质纤维化造模的2种方法比较研究
2016-09-22谢艳华王四旺崔嘉辉吴让鑫
闫 莉,谢艳华,杨 倩,王四旺*,崔嘉辉,吴让鑫
(1.第四军医大学药学院天然药物学教研室,西安 710032;2.第四军医大学学员旅,西安 710032)
大鼠肺间质纤维化造模的2种方法比较研究
闫莉1,谢艳华1,杨倩1,王四旺1*,崔嘉辉2,吴让鑫2
(1.第四军医大学药学院天然药物学教研室,西安710032;2.第四军医大学学员旅,西安710032)
目的探讨气管和腹腔注射2种给药方式复制特发性肺纤维化(idiopathicpulmonaryfibrosis,IPF)大鼠模型的差异。方法240~260g雄性SD大鼠24只,按照随机数字表法分为气管对照组(QC组)、气管给药组(Q组)、腹腔对照组(FC组)和腹腔给药组(F组),每组 6 只。分别经气管一次性注射生理盐水0.2mL或博莱霉素(BLM)5mg·kg-1·d-1;腹腔注射生理盐水0.2mL或博莱霉素15mg·kg-1·d-1,连续10d。28d后处死。观察每组小鼠生存率、体质量、肺脏外观、病理改变及肺组织羟脯氨酸含量。结果Q组生存率为66.7%;F组生存率为83.3%,二者比较差异有统计学意义(P<0.05)。2种方法给药组大鼠体质量均减轻,F组动物体质量在1~7d内下降,第8天起开始恢复;Q组动物体质量在前15d内持续下降,第16d起开始恢复。2种方法给药组的肺脏外观基本相同,没有显著差别。病理检查证实,Q组的胶原纤维沉积主要分布在气管周围,而F组的胶原沉积则分布在胸膜和肺间质。2种方法复制的模型组肺组织羟脯氨酸含量均显著高于对照组,差异有统计学意义(P<0.05);模型组间差异无统计学意义。结论气管给药与腹腔给药对于复制大鼠IPF无明显差别,但气管给药法更方便、经济和可靠。
博莱霉素;肺间质纤维化;造模
肺纤维化是指在不同因素刺激下引起肺部炎症反应,肺泡持续损伤,细胞外基质被反复破坏、修复、重建并过度沉积,最终导致正常肺组织结构改变、功能丧失的一类疾病,是所有间质性肺病的终末结局。特发性肺间质纤维化 (Idiopathicpulmonaryfibrosis,IPF)中的特发性指发病原因不明,占所有间质性肺病的65%左右,严重威胁人类健康,但其确切的发病机制至今尚未明了,临床上仍缺乏有效的治疗手段,病死率高[1-8]。因此,建立肺纤维化大鼠模型,对进一步探索该疾病的发病机制、评价治疗新药具有重要意义。
截至目前,利用博莱霉素(bleomycin,BLM)可致肺纤维化的毒性不良反应,复制啮齿动物肺纤维化,用来研究IPF,是最普遍和最经典的动物模型[9-14]。常用的给药方法有:支气管给药,腹腔注射和尾静脉注射。因给药方法不同,复制IPF的成模率、成本及其病理变化特点尚缺乏统一标准;然而,良好的动物模型是疾病研究和新药研发的基础,故本文依据简便操作和经济的原则,重点比较研究了腹腔和气管给予博莱霉素建立肺间质纤维化模型的差异,为进一步探索IPF发病机制和筛查有效治疗药物提供方便、经济和可靠的动物模型。
1 仪器与材料
1.1仪器电子天平(丹佛仪器公司);高压蒸汽灭菌锅(上海启前电子科技有限公司);离心沉淀机、小型高速冷冻离心机(赛特湘仪离心机仪器有限公司);半自动生化仪(西化仪北京科技有限公司);照相用显微镜(日本Oylmpus公司)。
1.2试药注射用盐酸博莱霉素(15mg·支-1,日本化药株式会社,生产批号:730342);水合氯醛(上海山浦化工有限公司);多聚甲醛(优级纯,北京化工厂);生理盐水(山东康宁药业有限公司);羟脯氨酸(Hyp)测定试剂盒(酸水解法,南京建成生物工程有限公司);无水乙醇(分析纯,北京化工厂);水为实验室双蒸水。
1.3动物健康SD大鼠,雄性,SPF级,体质量240~260g,购自第四军医大学动物实验中心,合格证号:SCXK(陕)2014-002。
2 方法
2.1动物分组24只雄性SD大鼠,购回后寄养于第四军医大学药物研究所药理实验室SPF级动物房,适应性饲养3d[2]后,分成4组,每组6只,均于第28天处死。分别为气管对照组(QC组):第0天气管内注射生理盐水0.2mL;气管给药组(Q组):第0天气管内注射博莱霉素5mg·kg-1·d-1,0.2mL;腹腔对照组(FC组):第0天起腹腔注射生理盐水0.2mL,连续10d;腹腔给药组(F组):第0天起腹腔注射博莱霉素15mg·kg-1·d-1,0.2mL,连续给药10d。2.2动物模型的制备气管给药具体操作方法:①以体积分数10%的水合氯醛按照0.3mL·100g-1腹腔内注射麻醉动物。剃除动物前部颈毛。②将动物固定于操作台中的鼠板上消毒颈前皮肤后在距胸骨约1cm处纵行切开颈正中皮肤,钝性分离浅筋膜及肌肉,至能清楚看见气管环。③将已抽取含博莱霉素5mg·kg-1·d-1,0.2mL或相应体积生理盐水的1mL注射器(前带7号针头)经两气管软骨环间隙朝向心端刺入气管,将大鼠直立,继续进针约1cm,回抽无阻力,抽回空气,注药,在不影响剂量准确的前提下允许注射器中存有约0.5mL的空气以确保药物完全进入气道。④迅速将动物绕身体长轴左右旋转30s,使药物分布均匀。⑤缝合颈部皮肤。局部酒精消毒后放回笼中正常饲养。
腹腔给药操作方法:常规腹腔注射操作。
2.3观察指标每天观察动物的外貌特征,每天晚上测量大鼠体质量,记录体质量变化情况。28d后腹主动脉放血处死,观察肺脏外观,左肺浸泡在体积分数为10%的福尔马林溶液中固定后,用常规石蜡包埋切片,分别进行HE、Masson染色;取大鼠右肺装入冻存管用铝箔纸包好,在液氮中冻存30~60min后,转至-70 ℃冰箱中储存,以备制作肺组织匀浆测定羟脯氨酸(HYP)含量。
2.4统计学处理采用SPSS13.0统计软件进行分析,计数资料采用χ2检验,计量资料采用ANOVA检验。P<0.05为差异有统计学意义。
3 结果
3.1动物一般状况两对照组动物均进食正常,毛色光亮,活动自如;两模型组动物则食欲不振,毛色晦暗,变黄变糙,活动减少,状态变差,显示出明显的病态。3.2动物生存率比较两对照组动物均无死亡,生存率为100%;Q组有2只死亡,生存率为66.7%;F组有1只死亡,生存率为83.3%,P<0.05。
3.3动物体质量变化给予BLM造模后两对照组体质量平稳增长,F组动物体质量在1~7d内下降,第8天起开始恢复;Q组动物体质量在前15d内持续下降,第16天起开始恢复。多次腹腔注射给药组与一次气管给药组相比,大鼠体质量减少的个体间差异小,恢复快。见图1。
图12种给药方式小鼠体质量变化
Fig.1Thechangeofrat′sweightinducedbydifferentmedicineadministrationway
3.4肺脏外观情况2种给药方法的对照组大鼠双肺表面光滑,颜色粉嫩,质地均匀,弹性好;模型组情况基本相同,没有显著差别,均可见到肺脏萎缩,表面凹凸不平,有大小不等的囊气腔突出,切开后可见小如针尖、大如米粒的囊腔。组织弹性差,部分区域呈苍白色,可见散在的出血点及黄白色灶。3.5病理切片检查2种给药方法对照组大鼠的肺泡结构清晰,肺泡间隔无炎性细胞,肺泡和间隔内均未见到胶原成分;模型组动物中央气道和大血管周围有炎性细胞浸润,其中以中性粒细胞为主,还可见到成纤维细胞增生,胶原基质增多,肺泡间隔明显增厚并伴随细胞浸润,且纤维组织增生及成纤维细胞灶较多,肺泡腔塌陷,肺组织结构破坏,出现典型的肺纤维化改变。不同的是气管给药组胶原纤维分布在气管周围,而腹腔给药组胶原沉积则主要分布在胸膜和肺间质。见图2。
3.6组织匀浆HYP含量气管给药组含量1±0.09μg·mL-1和腹腔给药组含量1.05±0.05μg·mL-1均显著高于气管对照组0.75±0.04μg·mL-1和腹腔对照组0.80±0.04μg·mL-1,差异有统计学意义(P<0.05);两模型组含量相近,差异无统计学意义(P>0.05)。
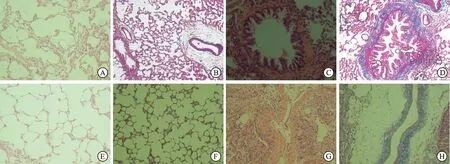
图2肺组织病理学变化(×200)
A.HE气管对照组:肺泡结构正常;B.Masson气管对照组:肺泡结构正常;C.HE气管给药组:肺组织结构破坏,大量炎性细胞渗出;D.Masson气管给药组:蓝色胶原分布在气管周围;E.HE腹腔对照组:肺泡结构正常;F.Masson腹腔对照组:肺泡结构正常;G.HE腹腔给药组:肺泡腔塌陷,大量炎性细胞渗出;H.Masson腹腔给药组:蓝色胶原主要分布在肺间质
Fig.2Pathologicalchangesinlungtissue(×200)
A.HEintratrachealcontrolgroup:normalalveolarstructurewasshown;B.Massonintratrachealcontrolgroup:normalalveolarstructurewasshown;C.HEintratrachealadministrationgroup:thepulmonaryarchitecturewasdestroyed,andthemassiveinfiltrationofinflammatorycellwasshown;D.Massonintratrachealadministrationgroup:collagenwaslocatednearthebronehia;E.HEintraperitonealcontrolgroup:normalalveolarstructurewasshown;F.Massonintraperitonealcontrolgroup:normalalveolarstructurewasshown;G.HEintraperitoneallyadministeredgroup:thepulmonaryarchitecturewasdestroyed,andthemassiveinfiltrationofinflammatorycellwasshown;H.Massonintraperitoneallyadministeredgroup:collagenwasevenlydistributedinpulmonaryinterstialspace
4 讨论
BLM是用于治疗多种肿瘤细胞毒性的药物,使用早期会出现全身炎症反应及类似肺炎症状,后期可产生呈进行性发展的严重肺间质纤维化[15]。由于其导致的动物肺间质纤维化与人类肺间质纤维化病理过程相似,故用BLM复制肺纤维化动物模型被认为最接近于人的(IPF)病理特征[13,16]。本实验选用日本化药株式会社生产的BLM。国产的博莱霉素A5 (BLM-A5)又名平阳霉素,是从我国浙江省平阳县土壤中的放线菌培养液中分离得到的抗肿瘤抗生素。经研究与国外的BLM成分相近。二者比较,BLM是多组分的复合药,主要成分为A2;平阳霉素则为单一的A5[17]。BLM与BLM-A5都是治疗多种肿瘤的细胞毒药物,具有导致肺间质纤维化的不良反应,并常用于复制肺纤维化动物模型。但张晓晔等[18]研究表明:BLM可在肺间质形成广泛的纤维化;但BLM-A5仅引起轻微的肺组织损伤,无法形成明显的间质纤维化。
经气管给药复制IPF模型的优点是方便、经济、可靠。此方法虽然要经过气管滴注,但仅需1次给药,与连续10d腹腔注射的造模方法相比操作方便。因造模药物昂贵,经气管给药所需药量仅为经腹腔给药所需药量的1/30,故经气管给药是非常经济的。此方法的缺点是对实验动物有一定的损伤,操作技术要求高。肺脏的结构特点决定了药物在肺部很难分布均匀。实验中虽采用了给药后直立旋转动物的方法,但BLM在左右两侧的数个肺叶中仍无法分布均匀。由于BLM致肺纤维化具有剂量依赖性[19],若进入各肺叶的BLM剂量不同,则各肺叶的纤维化程度也会有较大差异。预实验中曾发现经气管给药的个别大鼠在给药后仍活泼好动、状态良好,说明BLM只进入了部分肺叶,尚有一些肺叶未发生纤维化,故动物的呼吸功能并未受到明显影响,这也是影响该方法造模成功的主要原因。但只要操作标准,确保BLM完全进入气管,给药后对动物进行充分旋转使药物在两肺分布均匀,就可最大限度避免缺陷、保证造模成功。另外,气管内注射BLM,需麻醉大鼠后手术剖开颈部皮肤,钝性分离肌肉组织使气管暴露,存在感染及术中损伤造成大鼠死亡的危险,故操作中应尽量缩短操作时间、避免组织损伤,以期提高造模成功率。
采用腹腔注射BLM复制大鼠IPF模型操作简单、个体间差异小,给药剂量容易掌握,可减轻因手术操作差异造成的纤维化程度的差异。操作中应注意使大鼠处于头低脚高位,以避免误伤腹腔脏器。
2种给药方法复制IPF相比较,腹腔注射BLM后,BLM经循环系统进入肺脏,故病变主要分布于肺组织及胸膜下;气管内注射的BLM经支气管上皮吸收后,可在支气管周围形成局部的BLM高浓度区域;因此,可在支气管周围而非周边肺组织形成明显的纤维化改变。腹腔注射法与临床IPF病理分布更为接近,但二者所引起肺间质的病理改变并无明显差别。气管注射BLM以其操作简便、成模周期短和节省造模用药的明显优势,成为世界公认的大鼠IPF模型的制备方法。
[1]KaunistoJ,KelloniemiK,SutinenE,etal.Re-evaluationofdiagnosticparametersiscrucialforobtainingaccuratedataonidiopathicpulmonaryfibrosis[J].BMCPulmMed,2015,15:92.
[2]WellsAU,CostabelU,PolettiV,etal.ChallengesinIPFdiagnosis,currentmanagementandfutureperspectives[J].SarcoidosisVascDiffuseLungDis,2015,32(Suppl1):28-35.
[3]BendstrupE,MaherTM,ManaliED,etal.ChallengesintheclassificationoffibroticILD[J].SarcoidosisVascDiffuseLungDis,2015,32(Suppl1):4-9.
[4]JacobJ,HansellDM.HRCToffibrosinglungdisease[J].Respirology,2015,20(6):859-872.
[5]BehrJ,KreuterM,HoeperMM,etal.Managementofpatientswithidiopathicpulmonaryfibrosisinclinicalpractice:theINSIGHTS-IPFregistry[J].EurRespirJ,2015,46(1):186-196.
[6]PezzutoG,ClaroniG,PuxedduE,etal.StructuredmultidisciplinarydiscussionofHRCTscansforIPF/UIPdiagnosismayresultinindefiniteoutcomes[J].SarcoidosisVascDiffuseLungDis,2015,32(1):32-36.
[7]胡平.胺碘酮肺毒性的机理与临床[J].西北药学杂志,1992, 7(3):46-48.
[8]夏虎平,张子泰.硬膜外注射曲马朵止痛法在前列腺术后的应用[J].西北药学杂志,2001,16(4):189.
[9]MoellerA,AskK,WarburtonD,etal.Thebleomycinanimalmodel:ausefultooltoinvestigatetreatmentoptionsforidiopathicpulmonaryfibrosis?[J].IntJBiochemCellBiol,2008,40(3): 362-382.
[10]RobbeA,TassinA,CarpentierJ,etal.Intratrachealbleomycinaerosolization:thebestrouteofadministrationforascalableandhomogeneouspulmonaryfibrosisratmodel?[J].BiomedResInt,2015:198418.
[11]徐叔云,卞如濂,陈修.药理实验方法学[M].3版.北京:人民卫生出版社,2006:234-236.
[12]Gharaee-KermaniM,UllenbruchM,PhanSH.Animalmodelsofpulmonaryfibrosis[J].MethodsMolMed,2005,117: 251-259.
[13]ChuaF,GauldieJ,LaurentGJ.Pulmonaryfibrosis:searchingformodelanswers[J].AmJRespirCellMolBiol,2005,33(1): 9-13.
[14]ShiK,JiangJ,MaT,etal.Pathogenesispathwaysofidiopathicpulmonaryfibrosisinbleomycin-inducedlunginjurymodelinmice[J].RespirPhysiolNeurobiol,2014,190:113-117.
[15]WangQ,WangY,HydeDM,etal.Effectofantibodyagainstintegrinalpha4onbleomycin-inducedpulmonaryfibrosisinmice[J].BiochemPharmacol,2000,60(12):1949-1958.
[16]OrganL,BacciB,KoumoundourosE,etal.Structuralandfunctionalcorrelationsinalargeanimalmodelofbleomycin-inducedpulmonaryfibrosis[J].BMCPulmMed,2015,15:81.
[17]陈新谦.新编药物学[M]. 15版.北京:人民卫生出版社,2004:677-678.
[18]张晓晔,刘卫青,朱敏,等.博莱霉素与博莱霉素A5诱导小鼠肺组织损伤的差异[J].中国实验动物学报,2007,15(5):326-329.
[19]ZhaoY,ShahDU.Expressionoftransforminggrowthfactor-betatypeⅠandtypeⅡreceptorsisalteredinratlungsundergoingbleomycin-inducedpulmonaryfibrosis[J].ExpMolPathol,2000,69(2): 67-78.
Comparative study of 2 kinds of methods to induce pulmonary fibrosis model in rats
YAN Li1,XIE Yanhua1,YANG Qian1,WANG Siwang1*,CUI Jiahui2,WU Rangxin2
(1.Department of Natural Medicine,School of Pharmacy,the Fourth Military Medical University,Xi′an 710032,China;2.The Fourth Militory Medical University,Xi′an 710032,China)
ObjectiveToexplorethesimilaritiesanddifferencesbetweentheintratrachealandintraperitonealinjectiontoprepareidiopathicpulmonaryfibrosis(IPF)ratmodel.Methods24maleSDrats240-260g,wererandomlydividedintointratrachealcontrolgroup(QCgroup),intratrachealadministrationgroup(Qgroup),intraperitonealcontrolgroup(FCgroup)andintraperitoneallyadministeredgroup(Fgroup),n=6.Theyweretreatedwithasingleintratrachealinjectionofsaline0.2mLorbleomycin(BLM) 5mg·kg-1·d-1;intraperitonealinjectionofsaline0.2mLorBLM15mg·kg-1·d-1,for10daysconsecutively.Allratswerekilledat28days.Thesurvivalrate,weight,lungappearance,pathologicalchangesandlungtissuehydroxyprolinecontentofeachgroupwereobserved.ResultsQgroupsurvivalratewas66.7%;Fgroupsurvivalratewas83.3%.Therewasasignificantdifference(P<0.05)betweenthe2groups.TheweightoftheratsgivenBLMwaslostafterinjection,theweightofFgroupwaslessonedinthefirst7daysandstartedtorecoveronthe8thday;theweightofQgroupcontinuouslydeclinedinthefirst15daysandbegantorecoversincethe16thday.TherewasnosignificantdifferencebetweenQgroupandPgroupinlungappearance.Fibrosiswaswidelyandstablyformed,mainlyaroundthetracheainthegroupQ,however,thesamechangesweremainlyseenunderthepleuraandpulmonaryinterstialspaceintheratofgroupP.Lungtissuehydroxyprolineofthe2modelswassignificantlyhigherthancontrolgroups,thedifferencewasstatisticallysignificant(P<0.05);buttherewasnodifferencebetweenthe2models.ConclusionIntratrachealadministrationandintraperitonealadministrationshowednosignificantdifferenceforpulmonaryfibrosisinrats.
bleomycin;pulmonaryfibrosis;model
闫莉,女,硕士
王四旺,男,教授,博士生导师
10.3969/j.issn.1004-2407.2016.05.014
R965
A
1004-2407(2016)05-0485-05
2015-11-16)
