3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的合成与表征
2016-09-18谷应丽
叶 辉,谷应丽
(黄冈师范学院 化工学院,湖北 黄州 438000)
3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的合成与表征
叶辉,谷应丽
(黄冈师范学院 化工学院,湖北 黄州 438000)
以3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-β-D-吡喃葡萄糖为原料,通过pummerer重排反应、氟化反应,得到目标化合物3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖。采用核磁共振谱(1H、13C、DEPT135、19FNMR)对目标化合物进行了结构表征,确证了结构,为后续合成更复杂的糖类氟化物提供了基础。
葡萄糖;pummerer重排;合成;表征
近年来,含氟有机化合物的研究取得了巨大的成功。基于氟的特殊效应,在有机化合物分子设计过程中,氟的引入已成为重要的考虑因素。在含氟糖化合物中,由于氟对糖的分子结构的影响,从而改变了整个化合物的性质,表现在对酶的作用、对抗体的结合能力的不同。含氟糖化合物的化学生物学特性已使它们成为抗肿瘤、抗病毒的重要药物[1-2]。随着对含氟糖化合物的深入研究,针对糖化合物进行温和、高效的氟化反应就显得非常有必要。本文设计合成了一种新型的含氟化合物——3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖,并对其结构进行了表征,具体的合成路线[3-8]见图1。
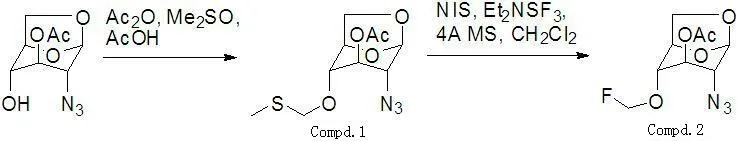
图1 3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的合成路线
1 实验部分
1.1试剂与仪器
仪器:Bruker 400 MHz型核磁共振仪;SHZ-Ⅲ型循环水式真空泵(上海荣生化学仪器厂;恒温加热磁力搅拌器;AL-206型电子天平(上海,梅特勒-拖利多公司)、DZF-602 型真空干燥箱(上海精宏实验设备有限公司)、磁力搅拌器、旋转蒸发仪、氮气保护装置。
试剂:所有试剂均为市售,试剂纯度均为分析纯。二氯甲烷经4A分子筛干燥备用。
1.2化合物1的合成
将化合物3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-β-D-吡喃葡萄糖(200 mg, 0.87 mmol)溶于二甲亚砜(5 mL),加入乙酸酐(2.5 mL)和冰醋酸(5 mL),室温下搅拌4天。TLC监测原料反应完全后,冰水浴下逐滴加入加入NaOH溶液(5 M, 12 mL),加入乙酸乙酯(20 mL),用饱和碳酸氢钠溶液(3×20 mL)洗涤,无水硫酸钠干燥。减压浓缩后,所得粗品用硅胶柱层析纯化(石油醚∶乙酸乙酯=10∶1→5∶1)得到淡黄色固体1(130 mg, 52.0%)。
1.3化合物2的合成
将化合物1(130 mg, 0.45 mmol)溶于无水二氯甲烷(2 mL),加入4A分子筛(200 mg)和N-碘代丁二酰亚胺(152 mg, 0.67 mmol),氮气保护,冷却至0℃,加入二乙氨基三氟化硫(89 μL, 0.67 mmol),继续在0℃下搅拌1 h。TLC监测原料反应完全后,加入饱和碳酸氢钠溶液(5 mL),剧烈搅拌5 min。加入二氯甲烷(20 mL),用饱和碳酸氢钠溶液洗涤(20 mL),有机相用无水硫酸钠干燥。减压浓缩后,所得粗品用硅胶柱层析纯化(石油醚∶乙酸乙酯=10∶1→5∶1)得到淡黄色固体2(80 mg, 68.0%),即目标产物。
2 结果与讨论
2.11HNMR谱图
图2为目标产物(化合物2)在CDCl3中的1HNMR图谱。氟甲基上氢原子的化学位移为5.52,这是由于氟原子和氧原子的吸电子诱导效应共同作用导致的;糖环上1位氢的化学位移为5.38,3位氢的化学位移为4.96,5位氢的化学位移为4.71,6位氢的化学位移分别为4.03、3.82,4位氢的化学位移为3.65,2位氢的化学位移为3.26;乙酰基(Ac)中氢原子的化学位移为2.13。每种氢对应的积分面积与结构相符,化合物1和化合物2具体1HNMR数据及核磁信号归属情况见表1。

图2 3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的1HNMR图谱

compd.1HNMR(400MHz,CDCl3),δcompd.15.50(s,1H,H-1),4.92(s,1H,H-3),4.87(d,1H,J=12.0Hz,-SCH2-),4.82(d,1H,J=12.0Hz,-SCH2-),4.61(d,1H,J=5.6Hz,H-5),4.05(d,1H,J=7.6Hz,H-6a),3.81(d,1H,J1=6.0Hz,J2=7.2Hz,H-6b),3.70(s,1H,H-4),3.24(s,1H,H-2),2.19(s,3H,-SCH3),2.12(s,3H,Ac)compd.25.54~5.51(m,2H,FCH2-),5.38(s,1H,J1=2.8Hz,J2=6.0Hz,H-1),4.96(t,1H,J=1.2Hz,H-3),4.71(d,1H,J=5.6Hz,H-5),4.03(d,1H,J=8.0Hz,H-6a),3.82(d,1H,J1=6.0Hz,J2=7.6Hz,H-6b),3.65(s,1H,H-4),3.26(s,1H,H-2),2.13(s,3H,Ac)
2.213CNMR图谱、DEPT135谱图和19FNMR图谱
图3为目标产物在CDCl3中的13CNMR图谱和DEPT135谱图。从DEPT135图谱[9]可知,103.6、101.5和65.1等三处共振信号的出峰方向与其它位移刚好相反,表明这三个共振信号代表结构式中亚甲基的共振信号,分别表示氟甲基和糖环6位碳的化学位移。从13CNMR图谱可知,乙酰基上两个碳原子的化学位移分别在169.6和21.1处出现共振信号;糖环1位碳原子的化学位移在100.2处出现共振信号,其它碳原子化学位移在75.5~59.1之间出现共振信号,分别对应于糖环上除1位碳以外的5个碳原子。
图4为目标产物在CDCl3中的19FNMR图谱。结构式中氟原子的化学位移为-150.9,与氟乙烷的化学位移-213相比,目标化合物的化学位移移向高场,这是由于氟甲基另一端的氧原子相对甲基具有更强的吸电子作用使F的电子云密度减小导致的。
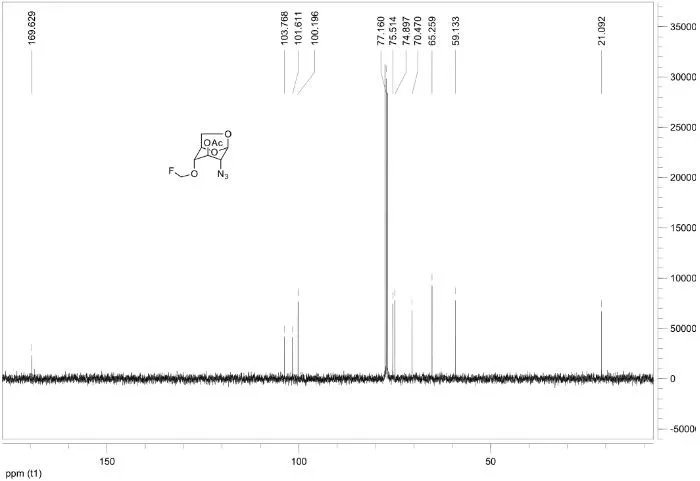

图4 3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的19FNMR图谱
通过核磁共振谱(1H、13C、DEPT135、19FNMR)对3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖的结构进行了表征,结果表明,能够确证该化合物的结构与结构式相符。
本文以简单易得的3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-β-D-吡喃葡萄糖为原料,通过pummerer重排反应、氟化反应,合成了目标化合物3-O-乙酰基-1,6-脱水-2-叠氮基-2-脱氧-4-O-氟甲基-β-D-吡喃葡萄糖。采用核磁共振谱(1H、13C、DEPT135、19FNMR)对目标化合物进行了结构表征,确证了结构,为后续合成更复杂的糖类氟化物奠定了基础。
[1]卢丽丽, 肖敏, 赵晗, 等. 1-氟代糖在化学-酶法合成糖类中的应用[J]. 有机化学, 2006, 26(12): 1631-1639.
[2]卢丽丽, 肖敏, 赵晗, 等. 氟代糖在糖苷酶研究中的应用[J]. 生物工程学报, 2006, 22(3): 351-360.
[3]Anjali R S, Coward J K. α∶β Selectivity in the synthesis of 3-substituted, 4-methyl umbelliferone glycosides of N-acetyl glucosamine and chitobiose[J]. Tetrahedron: Asymmetry, 2005, 16: 411-424.
[4]Izumi M, Tsuruta O, Harayama S,etal. Synthesis of 5-Thio-l-fucose-Containing Disaccharides, as Sequence-Specific Inhibitors, and 2'-Fucosyllactose, as a Substrate of α-l-Fucosidases[J]. J Org Chem, 1997, 62: 992-998.
[5]Coodée J D, Stubba B, Schiattarella M,etal. A modular strategy toward the synthesis of heparin-like oligosaccharides using monomeric building blocks in a sequential glycosylation strategy[J]. J Am Chem Soc, 2005, 127: 3767-3773.
[6]Kirsch P(原著);朱士正,吴永明(译). 当代有机氟化学——合成、反应、应用、实验[M]. 上海:华东理工大学出版社,2006: 61.
[7]Munro T A, Duncan K K, Xu W,etal. Standard protecting groups create potent and selective κ opioids: Salvinorin B alkoxymethyl ethers[J]. Bioorganic & Medicinal Chemistry, 2008, 16: 1279-1286.
[8]Iimura S, Uoto K, Ohsuki S,etal. Orally active docetaxel analogue: synthesis of 10-deoxy-10-C-morpholinoethyl docetaxel analogues[J]. Bioorganic & Medicinal Chemistry Letters, 2001, 11: 407-410.
[9]宁永成.有机化合物结构鉴定与有机波谱学[M]. 北京:科学出版社,2000: 187-190, 171-174.
责任编辑王菊平
Synthesis and characterization of 3-O-acetyl-1,6-anhydro-2-azido-2-deoxy-4-O-fluoridemethyl-β-D-glucopyranose
YE Hui, GU Ying-li
(College of Chemical Engineering, Huanggang Normal University, Huangzhou 438000, Hubei, China)
With 3-O-acetyl-1, 6-anhydro-2-azido-2-deoxy-β-D-glucopyranose as a raw material and through pummerer rearrangement and fluoridation reaction, the title compound 3-O-acetyl-1, 6-anhydro-2-azido-2-deoxy-4-O-fluoridemethyl-β-D-glucopyranose was synthesized. The structure of the title compound was characterized and confirmed by NMR (1H,13C, DEPT135 and19FNMR). It provided a foundation for the follow-up synthesis of more complex carbohydrate fluoride.
glucopyranose; pummerer rearrangement; synthesis; characterization
O629.1
A
1003-8078(2016)03-0034-04
2016-05-12
10.3969/j.issn.1003-8078.2016.03.09
叶辉,男,湖北黄冈人,讲师,博士,主要研究方向为糖药物化学。
黄冈师范学院青年科研基金(2015019103)。
