一种检测动物组织中呋喃西林代谢物快速检测检测卡的研制
2016-09-15邓传玉罗雪粤贵州勤邦食品安全科学技术有限公司
□ 扶 胜 杨 梅 邓传玉 罗雪粤 贵州勤邦食品安全科学技术有限公司
一种检测动物组织中呋喃西林代谢物快速检测检测卡的研制
□ 扶胜杨梅邓传玉罗雪粤贵州勤邦食品安全科学技术有限公司
利用胶体金免疫层析技术研制一种快速检测动物组织中呋喃西林代谢物的胶体金试纸卡,检测卡包含了胶体金标记物的制备,样品垫和反应膜的制备,检测卡的组装等研究步骤,所研制出的呋喃西林代谢物胶体金快速检测卡,对动物组织的检出限达到0.5 μg/kg,检测时间为10 min,假阳性率小于5%,假阴性率为0%,该试纸卡能够准确、可靠。简便地检测动物组织中呋喃西林代谢物,适合大量样品的现场检测。
呋喃西林代谢物;快速检测;胶体金检测卡;动物组织
呋喃西林(Nitrofurazone)是硝基呋喃类药物的一种,是一种人工合成的具有5-硝基呋喃结构的广谱抗菌药,呋喃西林以及其代谢物均具有很强的毒性和致癌作用,已引起世界各国的高度重视[1]。我国农业部发布的第193号公告中规定呋喃唑酮和呋喃它酮禁止所有用途,在所有食品动物中禁用[2],目前欧盟对硝基呋喃类代谢物的检测方法灵敏度规定为1 μg/kg[3]。目前呋喃西林及其代谢物的检测方法主要有免疫检测法和理化检测法[4,5],如液相色谱-质谱法[6,7]、紫外分光光度法[8,9]、液质联用技术[10,11]等,仪器方法前处理复杂、繁琐、成本高和操作技术要求高,胶体金免疫层析技术(GICA)的快速诊断试纸条具有灵敏度高、检出限低、特异性强和稳定性好,并且简便快速、无需检测仪器,且成本低、无污染的优点,适用于现场大规模地对动物源食品中呋喃西林代谢物残留的筛检,也适用于食品生产加工企业进行自检。
呋喃西林在动物体内代谢速度较快,代谢物与蛋白结合成为结合态,在弱酸条件下可以从蛋白质中释放出来,因此当含有呋喃西林抗生素残留的产品被人食用后,SEM可以在胃酸作用下从蛋白质中释放而严重危害人体健康。但由于该药物价格低廉和治疗效果好[12],仍然被部分国家使用,中国进口的禽肉和水产品中陆续检测出呋喃类药物残留,从2003—2006年,欧盟共发布200次有关硝基呋喃类药物残留警报,其中约47%为呋喃西林代谢物残留[13],本实验研究制备一种快速检测卡,拟建立快速、简便、准确和灵敏度高的方法检测水产养殖中残留的呋喃西林代谢物。
1 材料与方法
1.1材料与仪器
鱼肉、虾肉、猪肉和鸡肉当地市场购买;呋喃西林代谢物、牛血清白蛋白(BSA)、2-硝基苯甲醛,美国Sigma公司;柠檬酸三钠、氯金酸,美国Sigma公司;硝酸纤维素膜、样品吸收垫、吸水垫和PVC背板,江苏恩莫阿赛生物技术有限公司;乙酸乙酯、甲醇、正己烷、三水合磷酸氢二钾、碳酸钾、氢氧化钠和三氯乙酸,国药集团化学试剂有限公司,分析纯;呋喃西林代谢物单克隆抗体、抗原,自制;8010S匀浆机,上海斯伯明仪器设备有限公司;HGC-12D氮吹仪,天津市恒奥科技发展有限公司;XH-B漩涡混合器,上海皓庄仪器有限公司;Isoflow划 膜 仪,Imagene Technology INC;微量移液器(单道20~200 μL、100~1000 μL),美国Thermo公司,2000SBL电子天平,美国Setra公司;UV7502PC紫外可见分光光度计,上海精科实业有限公司;DHP-600生化培养箱,台湾全信电子仪器有限公司;10 L/H实验室超纯水机,沃尔奇环保股份有限公司;08-2T电热套搅拌器,上海梅颖浦仪器仪表制造有限公司;CT300数控切条机,上海金标生物科技有限公司;Z32HK-台式高速离心机,德国贺默公司。
1.2实验方法
1.2.1胶体金制备与质量鉴定
制备胶体金采用柠檬酸三钠还原法。量取297 mL的四蒸水装入500 mL的锥形烧瓶,置于磁力加热搅拌器上搅拌煮沸,加入1%氯金酸溶液3 mL,待溶液再次沸腾后迅速一次性加入6.0 mL柠檬酸三钠溶液,氯金酸溶液由灰色逐渐变为酒红色,颜色稳定后继续加热10 min,待溶液冷却后,4℃保存[14]。制备好的胶体金无沉淀和漂浮物,并且外观纯净、透亮。通过分光光度计扫描,获得胶体金可见光吸收光谱,测定最大吸收波长(λmax),并在透射电镜下观察胶体金颗粒的均一程度,测量金颗粒粒径[15]。
1.2.2胶体金标记抗体制备
取5 mL制备好的胶体金,加入150 μL 0.02 mol/L K2CO3,涡动混匀,再加入10 μL呋喃西林代谢物单克隆抗体,涡动混匀,放置20 min,加入10% BSA 150 μL,放置10 min。13 000 r/min、2 ℃离心30 min,弃去上清液,用金复溶液0.5 mL溶解金,得到的呋喃西林代谢物单克隆抗体-胶体金标记物溶液。
1.2.3样品垫的处理
配置好含牛血清白蛋白浓度为0.4%、pH为7.5、0.1 mol/L磷酸盐缓冲液,将样品吸收垫放置于配好的液体3 s,拿出后放置2 h,然后再放置在37 ℃烘2 h。
1.2.4C、T的包被
按19∶1的体积比用含2%乙醇的0.02 mol/L pH7.2的PBS稀释呋喃西林代谢物至16 μg/mL,按79∶1的体积比用含2%乙醇的0.02 mol/L pH7.2的PBS稀释羊抗鼠IgG抗体到50 μg/mL,用Isoflow划膜仪将其包被于硝酸纤维素膜上的T线和C线上,包被量为1.0 μL/cm。包被好C、T线后将板放置于37 ℃条件下干燥2 h。
1.2.5检测卡组装
将制备好的样品垫、金标垫、反应膜、吸水垫依次按图1所示粘贴在所述PVC板上(见图1),再将组装好的试纸固定在卡壳上。
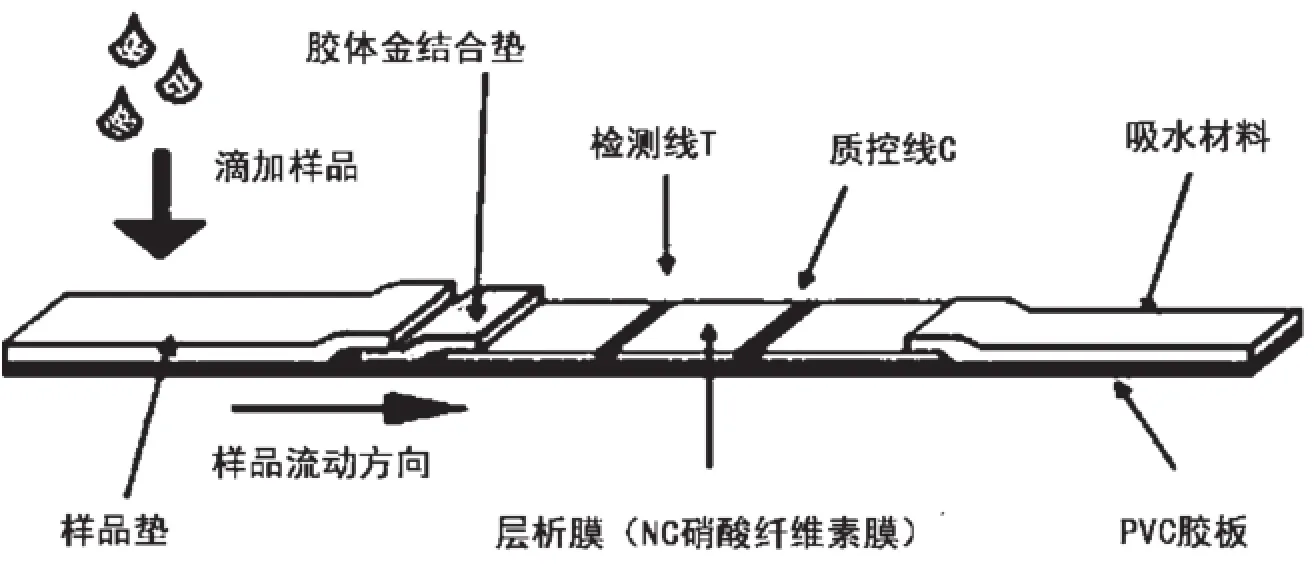
图1 胶体金检测卡结构图
1.2.6样本前处理方法
称取2.0(±0.05) g均质样本至15 mL聚苯乙烯离心管中,加入5 mL水,再加入100 μL衍生化试剂,上下振摇至样本混匀;将离心管放置于80 ℃水浴锅中30 min;取出离心管,加入0.6 mL 1 mol/L HCl、0.5 mL 1 mol/L NaOH,盖上离心管盖,将样本摇匀,加入5 mL乙酸乙酯,盖上离心管盖,上下翻转离心管20~25 次(切勿涡旋震荡);3 000 rpm以上,室温离心 5 min;取上层3 mL至10 mL玻璃试管或15 mL聚苯乙烯离心管中,于50~60 ℃水浴氮气流下吹干(或空气流下吹干);加入0.8 mL正已烷,用涡旋仪涡动1 min,再加入0.5 mL样本复溶液,涡动5~6 s充分混匀。取下层用于分析。
1.2.7检测卡检测方法
检测卡平放,取待检样品70 μL加入检测卡加样孔中,液体流动开始计时,5~10 min观察结果。T线显色强于C线显色或与C线显色无明显差异,表示组织样本中不含有呋喃西林代谢物,T线显色明显弱于C线显色或T线不显色,表示组织样本中呋喃西林代谢物浓度等于或高于检出限,未出现C线,表明不正确的操作过程或检测卡已失效。
1.2.8动物组织中呋喃西林代谢物的测定
通过确定试纸卡的稳定性、对相似物质交叉反应、检测卡的检出限、检测时的假阳性及假阴性最终实现产品对呋喃西林代谢物的检测。
1.2.8.1检测卡检出限的测定
在各种样本中添加不同浓度呋喃西林代谢物,将处理好的样品液分别滴加到组装好的检测卡的加样孔中。5~10 min后目测判断结果。检出限定义为能与阴性对照的检测卡的检测线有明显颜色差别的呋喃西林代谢物的最小浓度。
1.2.8.2检测卡的假阳性率、假阴性率测定
通过测试各种阴性样本至少30份,用至少3个批次的检测卡进行检测,和在各种样本中添加0.5 μg/kg高标,用至少3个批次的检测卡进行检测,根据最终检测结果计算出假阳性比例与假阳性比例。
1.2.8.3特异性实验
用检测卡分别将不同浓度(1、100、500 ppb)的硝基呋喃类代谢物CPAMOZ、CPAOZ、CPAHD滴加到试纸卡加样孔中,判断有无交叉反应。实验结果均为阴性,表明胶体金层析试纸具有较高的特异性。
1.2.8.4保存实验
将制备好的试纸卡在不同温度(一般是4、25、37 ℃)中保存,通过不同时间测试阴性样本和阳性样本,根据检测结果的稳定性及检测卡颜色情况判定检测卡的稳定性及稳定时间。
2 结果与分析
2.1胶体金质量鉴定
将制备好的胶体金溶液在400~600 nm进行紫外扫描,扫描后得出最大吸收峰波长,通过最大吸收峰的峰宽和峰形,可知在523.0 nm处有最大吸收,用透射电镜观察,胶体金颗粒分布均匀,金颗粒的粒径为20 nm左右(如图2所示)。胶体金电镜扫描图,如图3所示。
2.2检出限分析
按着1.2.6前处理方法做空白样本添加呋喃西林代谢物浓度为0、0.25、0.5 μg/kg和1 μg/kg;按照1.2.7检测步骤进行检测,对添加的浓度分别测试3次,确定检出限。T线显色比C线显色深或显色一致判定为阴性,检测线明显弱于质控线判定为阳性,检测结果如图4所示,试验结果见表1。
通过上表测试得出,该检测卡对各种组织样本中呋喃西林代谢物的检出限为0.5 μg/kg。
2.3特异分析
用复溶液配置浓度为100 μg/kg的呋喃唑酮代谢物、呋喃妥因代谢物、呋喃它酮代谢物,滴2~3滴于加样孔,5~10 min观察结果发现C、T线颜色一致都为阴性,说明该检测卡特异性较好。
2.4假阳性率、假阴性率分析
检测卡假阳性率为0%;所检阳性鱼肉、虾肉、猪肉、鸡肉各30份样品的检测结果都是阳性,该检测卡的假阴性率为0%,测试30份虾肉样品中有1份为阳性,其余都为阴性,说明检测卡假阳性小于5%(见表2)。
2.5稳定性试验
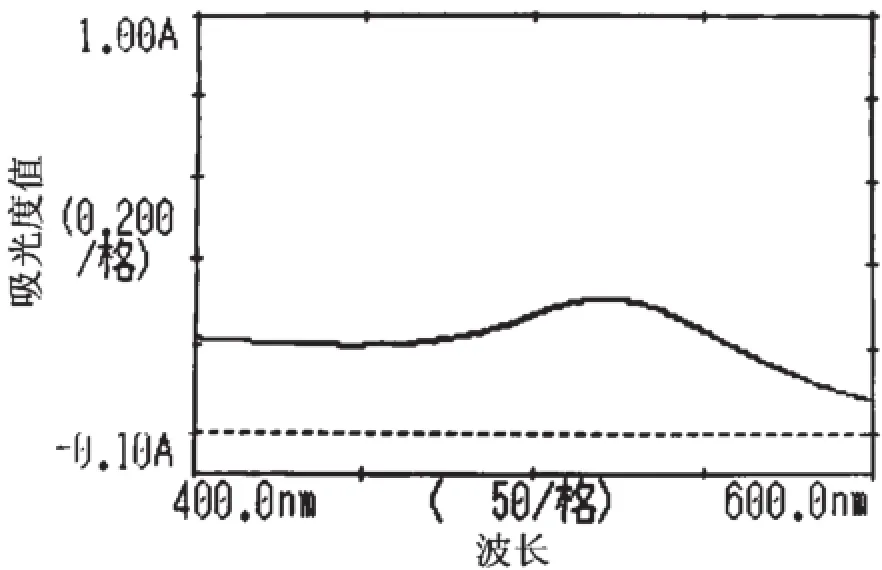
图2 胶体金紫外可见光分光光度计扫描图

图3 胶体金电镜扫描图(×100 000)

图4 检测卡检出限试验结果(虾肉样本)

表1 检测卡检测测结果
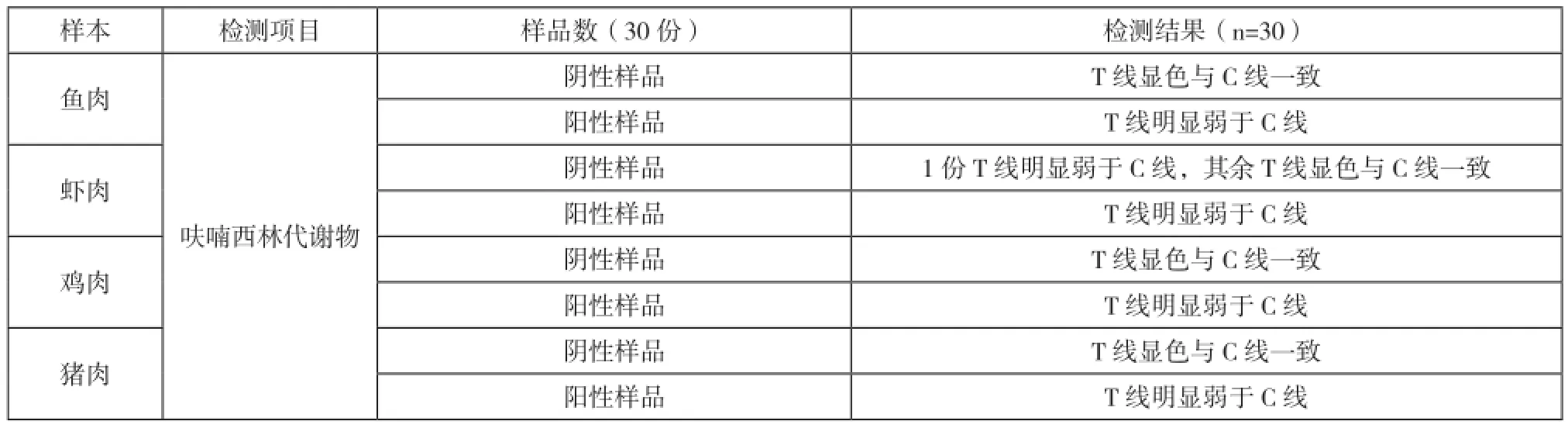
表2 检测卡假阳性率、假阴性率测定结果
检测卡在4、25、37 ℃环境下放置12个月,每个月进行1次实验验证,阴性阳性都较正常,超过12个月后,C线颜色有变浅现象,阳性样本有梯度但不明显,最后确定检测卡在常温下保存12个月正常,产品有效期为12个月。
3 结论
胶体金通过柠檬酸三钠还原法制备后,用紫外扫描和透射电镜观察金颗粒大小及均一性,测定直径为23 nm。用制备的胶体金标记呋喃西林代谢物单克隆抗体,通过优化稳定性、检出限、特异性、假阳性、假阴性最终确定胶体金免疫层析法。通过实验最终确定呋喃西林代谢物检测鱼肉、虾肉、猪肉、鸡肉样本中的检出限为0.5 μg/kg,与其他药物没有交叉反应,假阳性小于5%,达到要求,试纸卡通过目测即可判定结果。方法准确可靠,可用于现场快速筛查。在今后的兽药残留检测领域将会起着越来越重要的作用,并会作为工商质检、食品加工企业、出入境单位快速筛选的工具。
[1]沈建忠,万宇平,何方洋.检测呋喃西林代谢物的酶联免疫试剂盒及其应用:中国,200710063871.8[P].2007-02-13.
[2]中华人民共和国农业部.食品动物禁用的兽药及其他化合物清单[Z].2002.
[3]EU.2003/181/EC as regards the setting of minimum required performance limits (MRPLs) for certin residues in food of animal origin[S].2003.
[4]何方洋,沈建忠,万宇平,等.NFZ及其代谢物残留检测研究进展[J].中国兽药杂志,2009,43(4):51-54.
[5]王习达,陈辉,左健忠,等.水产品中硝基呋喃类药物残留的检测与控制[J].现代农业科技,2007(18):152-155.
[6]葛宋坤,王云风,常春艳,等.测定鸡肉、水产品中四种硝基呋喃类药物残留量的固相萃取一液相色谱法[J].分析测试学报,2003,22(5):91-93.
[7]林黎明,林回春,刘心同,等.固相萃取高效液相色谱-质谱法测定动物组织中硝基呋喃类代谢产物[J].分析化学,2005,33(5):707-710.
[8]欧翠华,陈江飞,胡毅坚,等.紫外分光光度法测定呋喃西林氧化锌搽剂中主药的含量[J].中国药房,2007,18(31):2461-2462.
[9]张龙麟,李枝端.紫外分光光度法测定硼砂酚醛器械消毒液中呋喃西林含量[J].海峡药学,2001,13(3):53-54.
[10]丁涛,徐锦忠,沈崇钰,等.高效液相色谱-串联质谱联用测定蜂王浆中的四种硝基呋喃类药物的代谢物[J].色谱,2006,24(5):432-435.
[11]彭涛,储晓刚,杨强,等.高效液相色谱/串联质谱法测定奶粉中的硝基呋喃代谢物[J].分析化学,2005,33(8):1073-1076.
[12]宋琍琍,张晓辉,张海琪,等.酶联免疫法快速测定水产品中呋喃西林、呋喃西林代谢物[J].浙江农业学报,2008,20(4):296-299.
[13]浙江省质量技术监督局.水产品中硝基呋喃类代谢物残留量的测定:液相色谱.串联质谱法(DB33/T 599-2006)[S].2006-01-05.
[14]杨挺,王姝婷,郭逸蓉,等.动物源食品中氯霉素残留速测金标试纸条的研制[J].食品科学,2007,23(11):156-161.
[15]孙秀兰,赵晓联,汤坚.单分散性胶体金的制备工艺优化[J].免疫学杂志,2004,20(2):151-154.
“十二五”国家科技支撑计划项目(编号:2012BAD29B06);2014贵阳技术创新项目(编号:[2014]20号)。
扶胜(1983-),男,贵州兴义人,硕士,高级工程师。研究方向:食品安全检测。
