丹参毛状根和丹参药材HPLC指纹图谱的比较研究
2016-09-15黄志成任加惠沈丽红金雯芳金江淼倪春红杨东风梁宗锁
黄志成,任加惠,沈丽红,金雯芳,金江淼,倪春红,杨东风,梁宗锁,b
(浙江理工大学,a.生命科学学院; b.浙江省植物次生代谢调控重点实验室,杭州 310018)
丹参毛状根和丹参药材HPLC指纹图谱的比较研究
黄志成a,任加惠a,沈丽红a,金雯芳a,金江淼a,倪春红a,杨东风a,梁宗锁a,b
(浙江理工大学,a.生命科学学院; b.浙江省植物次生代谢调控重点实验室,杭州 310018)
为了分析丹参毛状根和丹参原药材之间有效成分的差异,探讨丹参毛状根作为丹参药材使用的可行性,利用不同诱导处理后的丹参毛状根的HPLC指纹图谱进行研究。结果表明:ABA处理后的丹参毛状根有效成分提高了1.3倍,但与药材指纹图谱相似性较差,相似性系数仅为0.30,仅可以作为单一有效成分的提取原料;与原药材相比,MJ处理的丹参毛状根有效成分将近提高了15倍,指纹图谱相似性也较高,相似性系数达到0.96。因此,MJ处理的毛状根具有作为丹参药材使用的可行性。
丹参毛状根;诱导子;HPLC指纹图谱;相似性
0 引 言
丹参(SalviamiltiorrhizaBunge)作为一种传统的大宗药材,是唇形科鼠尾草属的多年生草本植物。丹参的主要次生代谢物包含两大类:即水溶性化合物(迷迭香酸、丹酚酸B和丹参素等)和脂溶性化合物(丹参酮ⅡA、隐丹参酮和二氢丹参酮等)[1-2]。在临床应用上,丹参对于心肌梗塞和脑血管疾病等具有一定的治疗功效[3]。
目前,对于丹参有效成分的药理作用研究及其开发的不断深入,丹参作为制备各种药物产品的需求日益增加。由于丹参原药材含有效成分低,生长周期长,再加上丹参品种的严重退化、产量降低、占用大量耕种资源等问题,从而导致丹参不能作为一种大规模使用的药用植物,而通过基因工程的方法是提高丹参有效成分生产的一种可靠有效的途径[4]。毛状根是由发根农杆菌侵染植物后,诱导产生的细小的、多分支的毛状物,具有生长速度快、稳定性好、培养方便等优点[5]。近年来,许多研究者对多种药用植物的毛状根培养进行了研究,付春祥等[6]对新疆雪莲根段外植体毛状根系的研究中发现,黄酮的含量是寻常的8.6倍;龚玉莲等[7]以少花龙葵(Solanmumphoteinocarpum)无菌叶片诱导毛状根,检测发现其中粗总糖苷生物碱含量为对照(少花龙葵无菌苗的根)的31倍,其中皂苷含量甚至达到了对照的107倍。因此,将毛状根培养技术运用于丹参药材培养,很大程度上解决了丹参生长周期长的问题,并且通过不同诱导子的诱导还可以进一步有效地提高有效成分的积累。陶如等[8]利用毛状根培养白花丹参,并采用真菌进行诱导,结果发现丹酚酸B和丹参素的产量得到有效提高。张顺仓等[9]研究显示,茉莉酸甲酯(methyl jasmonate, MJ)能够抑制丹参毛状根的生长,而总体上对于酚酸类以及丹参酮类成分含量的积累均表现出较强的促进效果;酵母提取物(yeast extract, YE)作为一种重要的生长物质使毛状根的干重显著提高,证明其可以有效地促进丹参毛状根的生长,并且有研究显示对于丹参酮积累的效果较为显著[10-11]。Cheng等[12]利用银离子(Ag+)等诱导丹参毛状根,发现丹参酮的积累得到明显的提升;同样,Ag+对于酚酸类成分积累也具有促进作用,用不同浓度的Ag+诱导毛状根,结果显示低浓度的Ag+能够有效提高总酚酸量[13]。此外,还有研究发现,当植物处于逆境胁迫时,脱落酸(abscisic acid, ABA)不仅可以诱导植物的防卫基因表达,还能够促进相关活性成分的生物合成,例如吲哚生物碱,羟基肉桂酸等活性成分[14-15]。外源性茉莉酸类化合物同样能够有效促进植物有效成分的快速积累,刺激次生代谢产物的生物合成[16]。然而丹参毛状根是否可以替代传统的丹参原药材、其品质如何,目前尚未清楚,而中药指纹图谱是评价中药材品质一致性的有效手段,但有关毛状根与药材指纹图谱的相似性尚未有报道。因此,本文分别通过添加ABA、MJ、YE和Ag+处理丹参毛状根,比较经诱导处理后丹参毛状根与丹参药材指纹图谱的相似性,探讨丹参毛状根作为丹参药材使用的可行性。
1 材料和方法
1.1实验材料
本实验选用的材料为该实验室培养的丹参毛状根。
1.2毛状根培养
本实验选用含有30 g/L蔗糖的6,7-V培养基培养作为基础培基,pH为5.8,使用前利用高压灭菌锅,121 ℃,灭菌30 min。在超净台中,称取0.2 g生长旺盛的丹参毛状根,然后将毛状根接种到装有50 mL液体6,7-V培养基的锥形瓶中,再放入恒温摇床中,110 r/min,25 ℃黑暗条件下培养18 d。
1.3诱导子的配制和处理
称取适量YE溶于双蒸水,加入适量无水乙醇至终浓度达到80%,室温下静置,弃去上清液,将获得的沉淀重新用双蒸水溶解,加入适量无水乙醇至终浓度达到60%。静置,弃上清,用200 mL双蒸水溶解所得的粘性沉淀物,溶液利用高压灭菌锅,121 ℃,灭菌30 min,即得到酵母提取物母液;ABA、MJ分别溶于蒸馏水和乙醇中,过0.22 μm滤膜,制成母液备用。AgNO3和Na2S2O3以摩尔比1∶4的比例混合,溶于蒸馏水中,过0.22 μm 滤膜,制成银离子母液备用。
分别向培养18 d的毛状根中加入不同诱导子(YE 100 μM,Ag+30 μM,MJ 100 μM,ABA 50 μM),继续培养,6 d后收集丹参毛状根,利用蒸馏水清洗3遍,滤纸吸干,50 ℃干燥至恒重。
YE购自上海生工生物工程股份有限公司,ABA和MJ购自美国Sigma-Aldrich公司,硝酸银购自上海三爱思试剂有限公司,硫代硫酸钠购自杭州萧山化学试剂厂。
1.4丹参有效次生代谢成分的提取
利用研钵分别将烘干的丹参毛状根和丹参药材磨碎,过0.45 mm的筛子,然后准确的称取0.10 g样品粉末后溶于2 mL 70%甲醇提取液中,反复均匀摇晃,提取液经超声提取45 min,将提取液取出后,静止冷却,再通过离心机,12 000 r/min离心10 min,小心吸取上清溶液过0.45 μm微孔滤膜,4 ℃冰箱储存。
1.5丹参有效成分测定与HPLC指纹图谱
丹酚酸B和丹参酮IIA标准样品全部来源中国食品药品鉴定所,准确的称取适量的标准品溶于过0.45 μm微孔滤膜的甲醇溶液中。利用甲醇溶液,分别将配置好的丹酚酸B和丹参酮IIA标准品储备液,进一步稀释成一系列浓度不同的标准溶液。通过高效液相色谱对溶液进行检测,进样量为10 μL,测定并获得峰面积积分值,绘制标准曲线,以标准品溶液浓度为横坐标,以有效成分的峰面积为纵坐标。通过标准曲线得到的回归方程分别为:丹酚酸B:y=5×10-8x+0.0042,R2=0.9997;丹参酮IIA:y=10-8x-0.0002,R2=1。
实验采用的二元高效液相色谱仪为Waters 1525,检测器为Waters 2996,检测中所用的色谱柱为Waters SunFire C18。丹参有效成分检测中采用的流动相是乙腈和水,通过流动相梯度洗脱。仪器参数设置:波长为270 nm,色谱柱温度为30 ℃,流速为1 mL/min,样品上样量为10 μL。实验检测程序:0~5 min,40 %乙腈,60%水;5~20 min,60 %乙腈,40%水;20~23 min,60 %乙腈,40%水;23~25 min,80 %乙腈,20%水;25 min,100 %乙腈[17]。
2 结 果
2.1诱导子对丹参毛状根生长变化的影响
分别通过四种不同诱导子处理后,丹参毛状根生长情况如图1所示。实验结果表明,四种不同的诱导子对丹参毛状根的生长均有不同程度的促进作用,其中ABA处理后毛状根干重增加了63.6%,而鲜重的变化并不显著;加入YE诱导后的丹参毛状根,毛状根的鲜重与干重都有明显的提高,分别增加了69.1%、45.4%;Ag+处理的效果与YE相似,鲜重与干重均有显著的增长,分别提高了52.7%、44.4%;然而,MJ诱导处理对丹参毛状根生长变化的作用不明显。
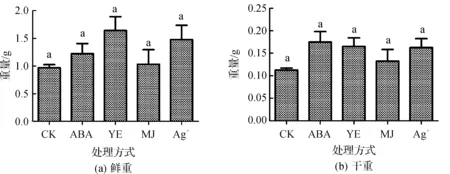
图1 四种不同诱导子对丹参毛状根生长变化的影响
2.2丹酚酸B与丹参酮ⅡA的含量比较
经过4种不同诱导子处理后,丹参毛状根以及原药材中丹酚酸B以及丹参酮IIA的含量,如图2所示。与对照组相比,ABA诱导后,丹参毛状根中丹酚酸B含量增加了1.3倍;YE处理后,丹酚酸B的含量与对照相比只提升了28 %;MJ处理后丹酚酸B含量变化最为显著,增加了15.0倍;Ag+处理后的丹酚酸含量却降低了。然而四种诱导子对于丹参酮IIA含量积累的效果均不明显。与丹参药材(YC)相比,丹参毛状根中丹酚酸B与丹参酮IIA的含量远远低于丹参药材中的含量,丹酚酸B的差距尤为显著,除MJ诱导处理(丹酚酸B含量约为丹参药材中含量的1/5)外,其余各组含量约为丹参药材中含量的1/50。
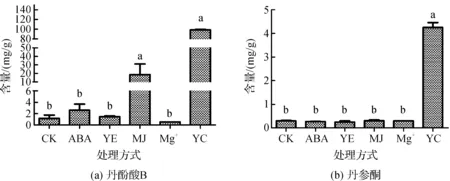
图2 丹参药材与毛状根中两种丹参成分的含量
2.3HPLC指纹图谱分析
2.3.1共有峰的选择
用高效液相色谱仪测定MJ诱导丹参毛状根后的色谱图及三维光谱图,由于峰具有一定的时间漂移特性,因此对于不同诱导子处理的丹参毛状根以及丹参药材的色谱图和三维光谱图,通过比较色谱图中指纹峰保留时间以及光谱图中的波长和强度,确定了13个共有指纹峰,如图3所示,图4为丹参药材HPLC指纹图谱。其中,保留时间33.47 min为丹酚酸B的指纹峰;保留时间85.62 min为丹参酮IIA的指纹峰,其所有对应的保留时间以及共有峰相对峰面积如表1所示。

图3 丹参毛状根HPLC指纹图谱

图4 丹参药材HPLC指纹图谱
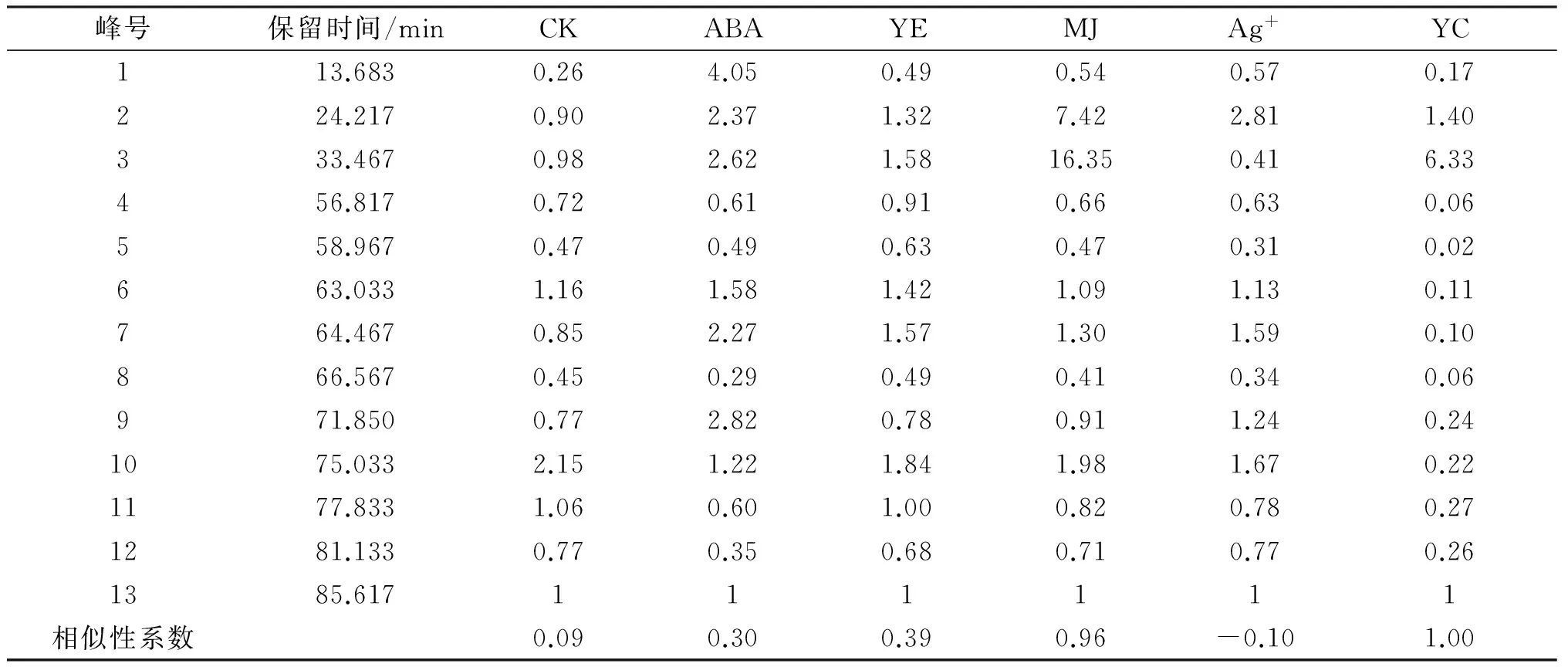
峰号保留时间/minCKABAYEMJAg+YC113.6830.264.050.490.540.570.17224.2170.902.371.327.422.811.40333.4670.982.621.5816.350.416.33456.8170.720.610.910.660.630.06558.9670.470.490.630.470.310.02663.0331.161.581.421.091.130.11764.4670.852.271.571.301.590.10866.5670.450.290.490.410.340.06971.8500.772.820.780.911.240.241075.0332.151.221.841.981.670.221177.8331.060.601.000.820.780.271281.1330.770.350.680.710.770.261385.617111111相似性系数0.090.300.390.96-0.101.00
2.3.2相似性系数的分析
不同诱导子处理的丹参毛状根及丹参药材的相似性比较如表1所示。本实验选择丹参酮IIA的指纹峰为参照峰(即保留时间为85.62 min的峰),计算相似性系数。由表1可以看出,不添加任何诱导子的丹参毛状根与丹参药材的相似性非常低,仅为0.09;添加Ag+后的丹参毛状根,与药材的相似性系数为负值,表明两者相似度非常低,尽管ABA和YE处理均能够提高毛状根与药材指纹图谱的相似性,但相似性系数均低于0.9,不能作为丹参药材使用。茉莉酸甲酯处理后,毛状根与药材指纹图谱相似性最高,达到0.96,高于《中药注射剂指纹图谱研究技术指南》中0.9的要求,具有作为丹参药材使用的可行性。
3 讨 论
自1907年首次发现毛状根可以由发根农杆菌诱导产生,毛状根的研究就被广泛的关注,相比较植物传统的组织培养技术,毛状根培养具有诸多优势,如有生长周期短、遗传稳定性好等,具有非常大的应用前景和发展空间。毛状根作为一种有效的培养方式,可以长期保持物种的优良性状,已经被越来越多的研究所采用,并且可以用来获取植物的次生代谢产物。目前已有超过百种的药用植物诱导出毛状根,主要是双子叶植物,其中对于数十种药材毛状根的培养条件、诱导机理以及有效成分积累都进行了有系统的研究[18-20]。
为了能够有效地解决丹参资源缺乏的状况,研究者成功从胚细胞中诱导出毛状根,并且从丹参毛状根中获得丹参酮类和酚酸类两类有效成分。然而由于丹参毛状根中有效成分含量较低,因此,近年来有关毛状根及其诱导方面的研究遍成为了国内外的研究热点。据文献报道,ABA作为植物一种信号分子,在植物生长过程中,能够有效的促进酚酸类及丹参酮类物质含量的积累[20-22],帮助植株应对逆境胁迫。此外,微生物对于毛状根有效成分同样有促进作用,Ming等[23]研究发现,内生真菌可以促进丹参毛状根的生长和丹参酮含量的积累。
然而,毛状根培养研究的时间还较短,仍处于发展阶段,还有许多问题需要进一步解决,尤其是品质等问题。中药指纹图谱技术是现今在国际中被公认的控制中药质量的质控模式,是一种比较综合并可量化的鉴定手段,它主要是以中药化学成分系统研究为基础的,一般多用于中药材以及中药生物制品质量可靠性、优劣性和稳定性的评价[24]。虽然毛状根是一种快速、有效的培养方式,然而,毛状根中有效成分的品质如何,与原药材中有效成分的比较如何,毛状根是否可以作为模型研究药材,甚至是否可以代替原药材用于研究或生产,这些都还尚不清楚。此外,目前有关毛状根与中药材指纹图谱的相似性的研究尚未有报道。
本实验利用四种不同诱导子处理丹参毛状根,通过指纹图谱分析诱导后毛状根与丹参药材的相似性,探讨丹参毛状根替代丹参药材使用的可能性。实验结果显示,MJ处理后的毛状根虽然干重和鲜重没有明显的增加,但其丹酚酸B的含量有较大幅度的提高,且变化最为显著,增加了15.0倍;ABA处理后干重明显增加,丹酚酸B的含量相较于MJ增加幅度小,增加了1.3倍。经HPLC指纹图谱数据分析处理后发现,不添加任何诱导子的丹参毛状根与丹参药材的相似性非常低,添加YE、ABA诱导子后,与丹参药材比较相似性分别为0.39、0.30,低于0.9,不能作为丹参药材使用。而MJ处理后,丹参毛状根与药材的指纹图谱相似性达到了0.96,已经高于《中药注射剂指纹图谱研究技术指南》中0.9的规定,已经具有了作为丹参药材使用的可行性。
本文首次对丹参毛状根中次生代谢产物的品质进行研究,通过指纹图谱比较毛状根与药材的相似性,为探究丹参毛状根作为研究模型以及生产原料提供基础,同时对于缓解丹参资源匮乏,提升次生代谢产物生产的工业化发展,以及促进丹参产业发展等都具有非常重要的意义。
[1] ZHOU L, BONDY S C, JIAN L, et al. Tanshinone IIA attenuates the cerebral ischemic injury-induced increase in levels of GFAP and of caspases-3 and -8 [J]. Neuroscience, 2015, 288: 105-11.
[2] ZHOU G J, WANG W, XIE X M, et al. Post-harvest induced production of salvianolic acids and significant promotion of antioxidant properties in roots ofSalviamiltiorrhiza(Danshen) [J]. Molecules, 2014, 19(6): 7207-7222.
[3] BI H C, ZUO Z, CHEN X, et al. Preclinical factors affecting the pharmacokinetic behaviour of tanshinone IIA, an investigational new drug isolated fromSalviamiltiorrhizafor the treatment of ischaemic heart diseases [J]. Xenobiotica, 2008, 38(2): 185-222.
[4] 谈荣慧, 张金家, 赵淑娟. 丹参毛状根的诱导及培养条件的优化 [J]. 中国中药杂志, 2014, 39(16): 3048-3053.
[5] XIAO Y, GAO S, DI P, et al. Methyl jasmonate dramatically enhances the accumulation of phenolic acids inSalviamiltiorrhizahairy root cultures [J]. Physiol Plant, 2009, 137(1): 1-9.
[6] 付春祥, 金治平, 杨睿, 等. 新疆雪莲毛状根的诱导及其植株再生体系的建立 [J]. 生物工程学报, 2004, 20(3): 366-371.
[7] 龚玉莲, 施和平, 李玲, 等. 少花龙葵毛状根的诱导和次生代谢物的产生 [J]. 热带亚热带植物学报, 2002, 10(1): 58-62.
[8] 陶如, 冯蕾, 赵法兴, 等. 白花丹参毛状根诱导体系的建立与其内生真菌提高毛状根中丹酚酸含量的研究 [J]. 时珍国医国药, 2015, 26(6): 1469-1473.
[9] 张顺仓, 刘岩, 沈双, 等. 诱导子对丹参毛状根酚酸类和丹参酮类成分积累的影响 [J]. 中国中药杂志, 2011, 36(10): 1269-1274.
[10] 晏琼, 胡宗定, 吴建勇. 生物和非生物诱导子对丹参毛状根培养生产丹参酮的影响 [J]. 中草药, 2006, 37(2): 262-265.
[11] SHI M, LUO X, JU G, et al. Increased accumulation of the cardio-cerebrovascular disease treatment drug tanshinone inSalviamiltiorrhizahairy roots by the enzymes 3-hydroxy-3-methylglutaryl CoA reductase and 1-deoxy-D-xylulose 5-phosphate reductoisomerase [J]. Functional & Integrative Genomics, 2014, 14(3): 603-615.
[12] CHENG Q, HE Y, LI G, et al. Effects of combined elicitors on tanshinone metabolic profiling and smCPS expression inSalviamiltiorrhizahairy root cultures [J]. Molecules, 2013, 18(7): 7473-7485.
[13] XING B C, YANG D F, Guo W L, et al. Ag+as a more effective elicitor for production of tanshinones than phenolic acids inSalviamiltiorrhizahairy roots [J]. Molecules, 2015, 20(1): 309-324.
[14] ZHAO J, DAVIS L C, Verpoorte R. Elicitor signal transduction leading to production of plant secondary metabolites [J]. Biotechnol Adv, 2005, 23(4): 283-333.
[15] HAO G P, JI H W, LI Y L, et al. Exogenous ABA and polyamines enhanced salvianolic acids contents in hairy root cultures ofSalviamiltiorrhizaBge. f.alba [J]. Plant Omics, 2012, 5(5): 446-452.
[16] HAO X L, SHI M, CUI L J, et al. Effects of methyl jasmonate and salicylic acid on tanshinone production and biosynthetic gene expression in transgenicSalviamiltiorrhizahairy roots [J]. Biotechnology and Applied Biochemistry, 2015, 62(1): 24-31.
[17] 杨东风. 丹参酮生物合成调控机理及丹参与绒毛鼠尾草cDNA-AFLP分析研究 [D].杨凌:西北农林科技大学, 2012.
[18] 余晓晖, 陈红刚, 赵磊, 等. 当归毛状根的诱导及其遗传稳定性研究 [J]. 时珍国医国药, 2015, 26(7): 1757-1759.
[19] 刘连旺, 张永清, 李先恩. 药用植物毛状根研究进展 [J]. 山东中医药大学学报, 2015, 27(3): 288-291.
[20] 李文龙, 王媛媛, 张芳芳, 等. 药用植物毛状根技术的研究 [J]. 安徽农业科学, 2015, 43(3): 44-46.
[21] 崔北米, 梁宗锁, 刘岩, 等. ABA及其生物合成抑制剂对丹参毛状根酚酸类成分和关键酶的影响 [J]. 中国中药杂志, 2012, 36(6): 754-759.
[22] LIANG Z, MA Y, XU T, et al. Effects of abscisic acid, gibberellin, ethylene and their interactions on production of phenolic acids inSalviamiltiorrhizabunge hairy roots [J]. Plos One, 2013, 8(9): e72806.
[23] MING Q L, SU C Y, ZHENG C J, et al. Elicitors from the endophytic fungus Trichoderma atroviride promoteSalviamiltiorrhizahairy root growth and tanshinone biosynthesis [J]. J Exp Bot, 2013, 64(18): 5687-5694.
[24] 陈林伟, 秦昆明, 徐雪松, 等. 中药指纹图谱数据库的研究现状及展望 [J]. 中草药, 2014, 45(21): 3041-3047.
(责任编辑: 许惠儿)
Comparative Study on HPLC Fingerprints ofSalviaMiltiorrhizaHairy Roots andSalviaMiltiorrhiza
HUANGZhichenga,RENJiahuia,SHENLihonga,JINWenfanga,JINJiangmiaoa,NIChunhonga,YANGDongfenga,LIANGZongsuoa,b
(a.College of Life Science; b.Key Laboratory of Plant Secondary Metabolism Regulation of Zhejiang Province, Zhejiang Sci-Tech University, Hangzhou 310018, China)
To analyze effective component differences ofS.miltiorrhizahairy roots andS.miltiorrhizaand explore the feasibility ofS.miltiorrhizahairy roots asS.miltiorrhiza, HPLC Fingerprints ofS.miltiorrhizahairy roots with different induction treatments were investigated. The results indicated that the effective components ofS.miltiorrhizahairy roots with ABA treatment were increased by 1.3 folds. However, the fingerprinting similarity between hairy foots andS.miltiorrhizaraw material was poor and the similarity coefficient was only 0.30, so it could only be used as an extractive raw material of a single effective component. Under MJ treatment, the effective component of hairy roots was almost increased by 15 folds when compared with the raw material. The fingerprinting similarity was high and similarity coefficient reached to 0.96. Therefore, hairy roots treated by MJ has the feasibility to be used asS.miltiorrhizamaterial.
Salviamiltiorrhizahairy root; elicitors; HPLC fingerprints; similarity
10.3969/j.issn.1673-3851.2016.05.021
2015-09-21
国家自然科学基金项目(81373908,81403033),浙江省科技厅公益性技术应用研究计划项目(2014C32108)
黄志成(1990-),男,浙江东阳人,硕士研究生,主要从事药用植物和中药资源开发研究。
梁宗锁,E-mail:liangzs@ms.iswc.ac.cn
R282.5
A
1673- 3851 (2016) 03- 0444- 06 引用页码: 050703
