TiO2-HNbMoO6复合材料的结构特征及其光催化性能
2016-09-13胡丽芳何杰刘媛赵芸蕾陈凯
胡丽芳 何杰 刘媛 赵芸蕾 陈凯
(1安徽理工大学化学工程学院,安徽淮南232001;2安徽理工大学地球与环境学院,安徽淮南232001)
TiO2-HNbMoO6复合材料的结构特征及其光催化性能
胡丽芳1,2何杰1,*刘媛1赵芸蕾1陈凯1
(1安徽理工大学化学工程学院,安徽淮南232001;2安徽理工大学地球与环境学院,安徽淮南232001)
通过插层-柱撑的方法制备了新型的复合材料TiO2-HNbMoO6。采用粉末X射线衍射(XRD)、高分辨透射电子显微镜(HRTEM)、激光拉曼光谱(LRS)、X射线光电子能谱(XPS)、紫外-可见漫反射光谱(UV-Vis DRS)及H2程序升温还原(H2-TPR)等技术对样品的相结构和它的微结构、骨架特征及光谱响应特性以及分散相粒子与片层间的相互作用进行表征,利用N2吸附-脱附法对样品的比表面积进行了表征,并通过模拟太阳光降解有机染料亚甲基蓝(MB)溶液考察复合材料的光催化活性。结果表明,HNbMoO6与TiO2复合后样品层间距增大,但无TiO2晶相生成,主体材料中的Nb―O键和客体材料中的Ti―O键复合前后发生明显变化等,证明了TiO2在HNbMoO6层间高度分散,并呈现明显的相互作用。复合后样品比表面积是本体材料的4倍有余,禁带宽度变窄,它在吸附和模拟太阳光照射下催化降解MB中的优越的活性都是主客体间明显的协同效应的结果。
HNbMoO6;TiO2;复合物结构;光催化;协同效应
1 引言
科技的快速发展使得社会对材料的要求越来越高,单一组分的材料远远满足不了人们的需要。复合材料由于在设计上综合了各组元的优点,并弥补了各自的不足,具有单一组分无法比拟的优异综合性能,成为当今材料科学的研究热点之一。
作为构建复合材料的基元之一,层状过渡金属复合氧化物因组成、结构等的多样性为构建复合光催化材料提供了巨大的潜在应用,在光催化性能上呈现许多突出的优点。特别是层状铌基复合氧化物,如层状钛铌酸盐、层状铌钨酸盐和层状铌钼酸盐等1,2,因其层间具有大量的活性位可以通过形成聚氧多酸盐、插层/嵌入以及剥离组装等方式实现改性或重组,从而形成丰富多彩的催化材料。在这些层状材料中,层状铌钼酸盐(图1)不仅层间具有大量的活性位且有较窄的禁带宽度,其在可见光区域就表现出良好的光谱响应特征3。
众所周知,固体层状化合物的光催化活性强烈地依赖于主体层板和客体离子之间的相互结合。我们前期的研究也表明,层间客体材料直接影响着光催化剂对反应物的吸附特性与光催化效果3。因此,人们开始在层状材料层间引入了不同价态和电子结构,且对反应物有较好吸附性能的过渡金属氧化物如TiO2、ZnO和Cu2O等以增强材料的光催化性能。华侨大学吴季怀教授课题组4-7制备了一系列0D-3D型的层状复合材料如TiO2-、Fe2O3-、NiO-、Cr2O3-、MnO-、CuO-HMWO6(M= Nb,Ta)等,并应用于光催化分解水和降解有机污染物反应中,获得了很好的光催化效果。人们不断提出层状复合光催化剂中各成分间的电荷分离与传递功能、几何效应能大大提高光催化量子效率,但复合材料主客体间的结构特征与相互作用特征、功能与性能协同效应等问题鲜有报道。
本研究采用固相反应法合成LiNbMoO6,经质子化得到HNbMoO6,以此作为主体材料,与客体TiO2进行复合,构建新型的复合材料,采用XRD、Raman、HRTEM、XPS、UV-Vis DRS、H2-TPR等手段对复合材料进行表征,考察复合材料的结构特征以及主客体之间的相互作用,并以亚甲基蓝的降解反应考察复合材料的光催化性能,以探讨主客体间的协同效应。

图1 LiNbMoO6的结构示意图Fig.1 Schematic of LiNbMoO6structure
2 实验部分
2.1原料与试剂
碳酸锂(Li2CO3,98%,AR)、五氧化二铌(Nb2O5,99.5%,AR)、钛酸四正丁酯(C16H36O4Ti,98.0%,AR)、无水乙醇(CH3CH2OH,99.7%,AR)和硝酸(HNO3,65%-68%,AR)均购置于国药集团化学试剂有限公司;正丁胺(C4H9NH2,98.0%,AR)购置于天津市光复精细化工研究院;正庚烷(C7H16,98.5%,AR)购置于天津市福晨化学试剂厂;三氧化钼(MoO3,99.5%,AR)购置于上海华谊集团华辰化工有限公司胶体化工厂。以上所有试剂在使用之前均未做进一步提纯。
2.2材料的制备
LiNbMoO6:将MoO3、Nb2O5和Li2CO3按化学计量比混合,研磨均匀,置于马弗炉中580°C焙烧24h,中间研磨一次,产物经蒸馏水洗涤、干燥后得前驱物固体粉末。
HNbMoO6:取10g上述方法制备的LiNbMoO6粉末与500m L浓度为2mol∙L-1的HNO3溶液混合,60°C下搅拌96h,每隔24h换一次酸液,过滤、分离,将固体洗涤至中性后于70°C干燥,得到HNbMoO6粉末。
TiO2溶胶:取25m L蒸馏水、1.5m L浓HNO3及30m L无水乙醇混合形成溶液A;8m L钛酸四正丁酯(C16H36O4Ti),25m L无水乙醇及0.7m L浓HNO3混合形成溶液B。在搅拌条件下将溶液A缓慢滴加至溶液B中,水浴加热至40°C,待滴加完后连续搅拌5h,再用硝酸调节pH=1.2-2.0,静置水解3 d,得到淡蓝色透明TiO2溶胶。取一部分洗涤干燥且经300°C煅烧3 h后作为参比的晶体TiO2。
TiO2-HNbMoO6:取4g HNbMoO6加入200m L体积分数为20%的正丁胺的正庚烷溶液中,50°C反应3 d,分别用乙醇和水进行洗涤,70°C干燥得到预柱撑产物C4H9NH2-HNbMoO6。将相同摩尔数的TiO2溶胶与C4H9NH2-HNbMoO6反应得到Ti(OH)4-HNbMoO6,经300°C煅烧3 h后得到TiO2-HNb-MoO6固体复合材料。
2.3表征方法
样品物相在XD-3型(北京普析通用仪器有限责任公司)X射线衍射仪上进行分析。Cu靶,Kα射线,λ=0.15406nm,Ni滤波片,管电压为36kV,管电流为30mA。样品的形貌表征在JEM-2010型透射电子显微镜(日本电子株式会社)上进行,能量散射谱(EDS)在操作电压200kV上进行。样品的骨架振动特征在inVia型拉曼光谱仪(Renishaw公司)上进行分析。样品中各元素所处的环境和化学态通过岛津/Kratos公司AXISULTRA DLD型光电子能谱仪测量,Al Kα射线,管电压为14kV,管电流为8mA。光响应特征在TU-1901双光束紫外-可见分光光度计(北京普析通用仪器有限公司)上进行,BaSO4作为参比样品。样品的H2还原特征采用TP-5080全自动多用吸附仪装置(天津市先权工贸发展有限公司)检测。催化剂用量:50mg,升温速率:10°C∙m in-1,预处理温度:180°C,还原温度范围:60-900°C,载气:N2,载气流速:30m L∙m in-1。
2.4光催化活性评价
本研究选用典型有机染料亚甲基蓝(MB)的光降解反应来评价催化剂光催化活性。将20mg催化剂与100m L,20mg∙L-1的MB溶液充分搅拌至分散均匀,避光暗处理90m in,使催化剂表面对亚甲基蓝吸附平衡。打开光源(500W氙灯)进行光催化反应,每隔15m in取样一次,离心分离后,取上清液进行紫外-可见光谱分析。根据样品在664nm处的吸光值及MB标准曲线来确定降解过程中MB浓度的变化。
3 结果与讨论
3.1TiO2-HNbMoO6复合材料的物相与光谱特征
HNbMoO6与复合样品TiO2-HNbMoO6的XRD和HRTEM表征结果分别如图2和图3所示。
图2(a,b)显示,样品LiNbMoO6和HNbMoO6的XRD图谱分别与JCPDS 50-0884和50-0886高度一致,说明所制备的样品即为四方相LiNbMoO6和HNbMoO6。同时,质子化后样品XRD中并未出现JCPDS 50-0886以外的峰,并且主晶面峰向小角度移动,结果说明LiNbMoO6中的Li+完全被H+取代。图2b于2θ=6.45°,12.93°出现衍射峰,它们分别对应于HNbMoO6晶格中的(002)和(004)面,说明HNbMoO6样品具有层状结构,图3a的HRTEM表征结果证实了HNbMoO6的这种层状结构。
图2c显示,在复合样品TiO2-HNbMoO6的XRD中也显示了主体材料HNbMoO6的(002)和(004)面的特征峰,结合该样品的HRTEM表征(图3b),说明复合材料保存着主体材料的层状结构,但主晶面(002)面层间距增大。另外,该复合后样品的XRD图中并未观察到TiO2的特征衍射峰,说明复合物中TiO2未形成晶相结构,TiO2物种可能以高度分散的状态均匀分散在HNbMoO6层间和表面,图3d中也能观察到这一点。
HNbMoO6和TiO2-HNbMoO6的EDS图谱如图4所示。结果显示,在TiO2-HNbMoO6的EDS图中除了主体材料HNbMoO6中的所有元素外,增加了Ti元素,证明TiO2成功与HNbMoO6复合。同时,钛钼比与投料比相近。

图2 样品的XRD图谱Fig.2 XRD pattern of theas-p repared sam ples (a)LiNbMoO6;(b)HNbMoO6;(c)TiO2-HNbMoO6;(d)TiO2
样品的N2吸附-脱附曲线如图5所示。由图5可知,复合前后样品的吸附等温线类型(II型)和回滞环类型(H4)均一致,说明在复合过程中样品的层状结构没有发生改变。复合后样品的BET比表面积增加至92.85m2∙g-1,是前驱物HNbMoO6比表面积(21.34m2∙g-1)的4倍有余。
激光拉曼光谱对于分析样品结构,特别是对价键连接以及骨架振动类型的判断具有非常重要的作用。样品在1000-100cm-1区域内的拉曼光谱如图6所示,相应的振动峰归属列入表18-19。

图3 HNbMoO6(a,c)和TiO2-HNbMoO6(b,d)的HRTEM图Fig.3 HRTEMimagesof HNbMoO6(a,c)and TiO2-HNbMoO6(b,d)
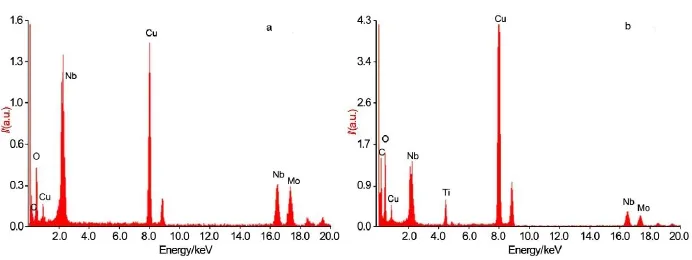
图4 HNbMoO6(a)和TiO2-HNbMoO6(b)的EDS图谱Fig.4Energy dispersive spectrum(EDS)of HNbMoO6(a)and TiO2-HNbMoO6(b)
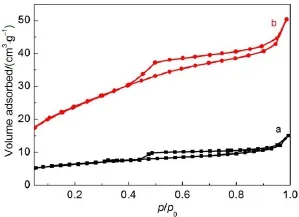
图5 样品的N2吸附脱附等温线Fig.5N2adsorption-desorption isotherm s of as-prepared samp les (a)HNbMoO6;(b)TiO2-HNbMoO6
图6(a)显示的是主体材料HNbMoO6的拉曼光谱,位于970.9和904.5cm-1Raman峰分别被归属为八面体单元中金属端氧键Mo=O和Nb=O键的伸缩振动峰。在800-400和400-100cm-1区域中的拉曼峰可以被归属为金属桥氧键M―O(M= Mo,Nb)的伸缩和弯曲振动峰。当HNbMoO6与TiO2复合后,主体材料的主要特征峰均存在,说明层板结构未遭到破环。然而,HNbMoO6样品的拉曼图谱中位于605.8和147.9 cm-1的峰(分别归属为Nb―O键的伸缩和弯曲振动峰)发生较小位移,说明Nb―O受到了复合的影响。与此同时,TiO2-HNbMoO6的拉曼光谱中出现了Ti―O的特征峰,且与TiO2中Ti―O键的峰相比,位置发生了明显的变化,进一步证明了TiO2成功与HNbMoO6复合且复合过程对Ti―O键产生了影响,这可能是分散在表面的TiO2与HNbMoO6片层间相互作用的结果。
通过程序升温还原技术(TPR)研究催化剂在H2作用下的还原行为对研究TiO2在HNbMoO6表面的分散状态以及相互作用有重要的意义。本研究中的催化剂样品H2-TPR图如图7所示。
Paiva等20指出,Nb5+具有很高的稳定性,在800°C才开始被氢气还原,在1300°C左右可以还原成Nb4+。因此,图7a所示的三个还原峰602、661和720°C均为HNbMoO6中钼氧化物的氢还原峰,他们分别为由Mo6+还原成中间体Mo4O1121、Mo4O11还原成Mo4+以及Mo4+还原成Mo0的还原峰22。图7c显示,纯的TiO2在900°C之内没有明显的还原峰,这与许波连23和范丰奇24等报道的一致。HNbMoO6与TiO2复合后,复合物中钼氧化物的三个还原峰向高温方向移动,这是因为在相互作用体系(Mo-O1-Nb-O2-Ti)中,Ti4+的Sanderson电负性(1.50)比Nb5+的(1.42)稍大25,使得对Nb5+的吸电子能力增强,进而使得对Nb5+的吸电子能力减弱,最终对Mo6+的吸电子能力增强,导致了Mo6+的还原温度增高。这也就说明了TiO2客体确与HNbMoO6发生了相互作用。
样品中各元素所处的环境和化学态可以通过XPS分析,结果如图8与表2所示。
如图8A所示,与前驱体HNbMoO6相比,复合后样品的XPS中多出了Ti2p的峰,证明了TiO2成功与HNbMoO6复合。另外,在Nb 3d、Mo 3d和O 1s的XPS图谱中,只有Nb 3d和O 1s的结合能在复合前后有变化,分别变化0.13、0.11和0.16eV,表明复合对Nb―O的影响较大,与Raman光谱分析结果一致。复合后,O 1s图谱中在533.35eV处(H2O中O 1s的特征峰26)少了一个峰,这是复合后样品300°C煅烧的结果。
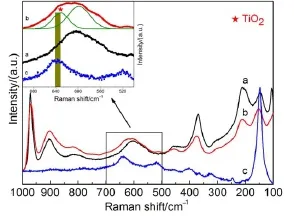
图6 样品的激光拉曼图谱Fig.6LRSof theas-p repared samp les(a)HNbMoO6;(b)TiO2-HNbMoO6;(c)TiO2

图7 样品的H2程序升温还原曲线Fig.7 H2-TPR curvesof theas-prepared sam ples (a)HNbMoO6;(b)TiO2-HNbMoO6;(c)TiO2
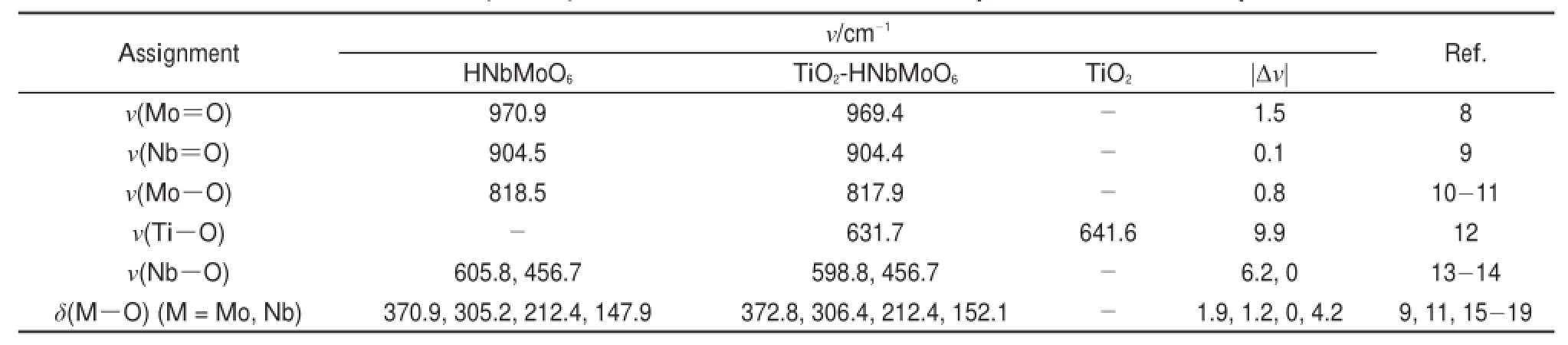
表1 拉曼光谱中振动峰的位置(v/cm-1)和归属Tab le 1 Position(v/cm-1)and attribution of the vibration peaksof the Ram an spectra
图9为HNbMoO6、TiO2-HNbMoO6及TiO2的UV-Vis DRS谱图,其中F(R)为Kubelka-Munk函数F(R)=(1-R)2/2R27,禁带宽度Eg通过经验公式Eg=1240/λ(λ为上升边波长)求得。
图9显示,HNbMoO6、TiO2-HNbMoO6和TiO2的上升边波长分别为438、445和396nm,其对应的带隙分别为2.83,2.78和3.13 eV。与主体材料HNbMoO6相比,复合材料的吸收波长发生微弱红移,其带隙宽度减小至2.78 eV,这归因于主体与客体之间的协同作用。
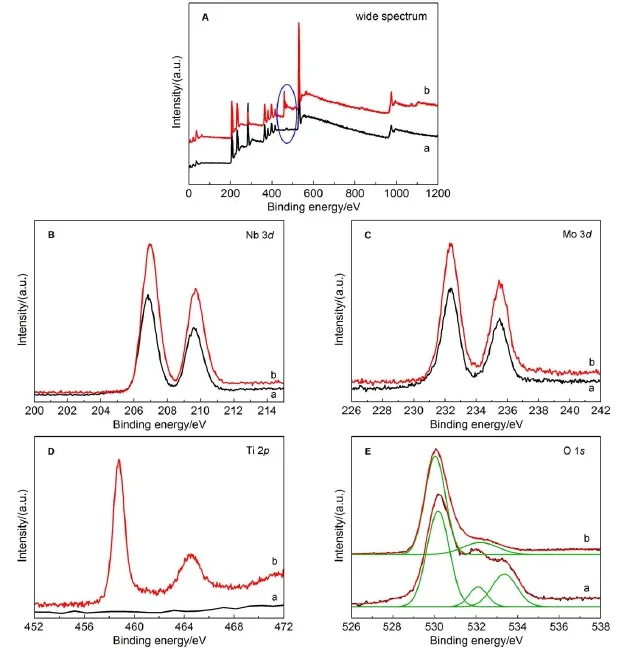
图8 HNbMoO6(a)和TiO2-HNbMoO6(b)的XPS图谱Fig.8 XPSspectra of HNbMoO6(a)and TiO2-HNbMoO6(b)
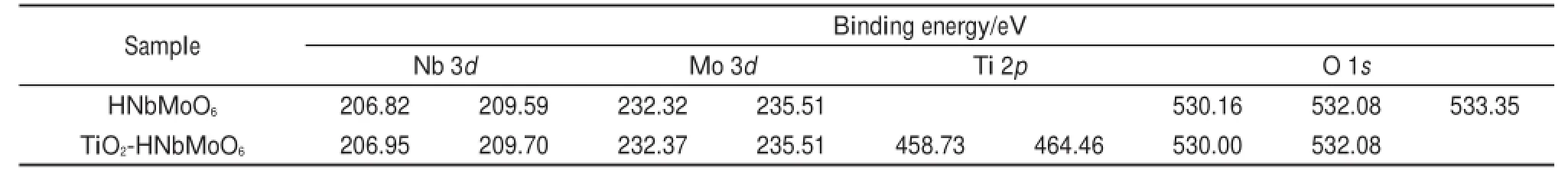
表2 XPS图谱(图8)中显示的各元素的结合能Tab le2 Binding energiesobtained from XPSspectra(Fig.8)
3.2样品的光催化活性
图10为不同催化剂吸附和光催化降解MB的曲线图,前90m in为暗处理过程,后120m in为光降解过程。由图可知,在暗处理45m in后各样品对MB的吸附基本达到平衡。通过比较所制备的各催化剂对MB的吸附和光降解效果可知,以TiO2-HNbMoO6为催化剂时,反应210m in后,MB的去除率达81.74%。而在相同条件下,以HNbMoO6和TiO2为催化剂时,MB的去除率分别为18.68%和16.75%。然而,不加催化剂,同等条件处理后,MB的自降解率几乎为0(图10d),故可以忽略不计。由图10可知,各样品的吸附和光催化活性依次为TiO2-HNbMoO6>>HNbMoO6>TiO2,TiO2-HNbMoO6对MB的降解效果分别是HNbMoO6和TiO2的近4.4和4.9倍。由此说明,在降解过程中,复合材料中的TiO2和HNbMoO6具有协同效应,是复合材料中主客体组分相互作用的结果。

图9 样品的紫外-可见漫反射光谱Fig.9 UV-VisDRSof theas-prepared samp les (a)HNbMoO6;(b)TiO2-HNbMoO6;(c)TiO2
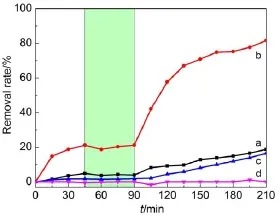
图10 样品光催化降解MB的曲线Fig.10Photocatalytic degradation curvesofMB over theas-prepared sam ples (a)HNbMoO6;(b)TiO2-HNbMoO6;(c)TiO2;(d)blank
3.3TiO2与HNbMoO6复合结构分析
结合各种表征手段,综上分析表明,柱撑材料中单分子层主体和锐钛矿纳米粒子客体紧密接触并相互作用,由此形成的电子耦合有利于增强材料的光催化活性。这种耦合作用能有效地将光生载流子对分离,减慢空穴和光生电子的复合。氧化物间接半导体的价带主要由O的2p轨道组成,导带由金属原子的d轨道组成3。由UV-Vis DRS可知,HNbMoO6的带隙能为2.83 eV,而实验测得所用TiO2锐钛矿的带隙为3.13 eV。Xu和 Schoonen28提出了的导带与带隙经验关系式ECB(V vs NHE)≈X-0.5Eg-4.5,式中Χ为化合物的绝对电负性,由此式可以得出HNbMoO6和TiO2的导带分别为0.585和-0.26eV,价带分别为3.415和2.88 eV,其光生载流子迁移模型如图11所示。在模拟太阳光照射下主体HNbMoO6片层和TiO2纳米粒子都有可能被激发产生光生电子和光致空穴,HNbMoO6片层和TiO2纳米粒子产生的光生电子经过异质结界面转移到HNbMoO6片层表面并被表面吸附的氧分子吸收。而半导体HNbMoO6片层和TiO2产生的空穴同样通过异质结聚集到TiO2纳米粒子的价带,空穴再迁移到粒子表面并被羟基和水分子捕获转化为自由基,这些自由基对有机物有较强的氧化能力。光生电子-空穴对通过这种空间转移可以很好地降低复合率,从而延长光生载流子的寿命,最终提高材料的光催化效率。

图11 TiO2-HNbMoO6中光生载流子迁移模型Fig.11 Transportmodelof the photoexcited carriers in TiO2-HNbMoO6
4 结论
通过TiO2纳米粒子与HNbMoO6的复合有效地构建了TiO2-HNbMoO6复合材料。复合材料的XRD,HRTEM,Raman,XPS,UV-Vis DRS和H2-TPR等表征均反映TiO2纳米粒子在HNbMoO6片层表面分散很均匀且两者之间存在着明显的相互作用。这种作用一方面改变材料的形貌特征与表面积,促进了主体材料的稳定性,同时也极大地改变了材料对光谱的响应特征,这些特点有助于提高复合材料对污染物的吸附性能和光催化性能。在模拟太阳光照射下TiO2-HNbMoO6对MB呈现出比HNbMoO6和TiO2更良好的光催化降解效果,这正是HNbMoO6与TiO2之间协同作用的结果。
References
(1)Hou,W.H.;Yan,Q.J.;Peng,B.C.;Fu,X.C.Acta Phys.-Chim.Sin.1994,10,289.[侯文华,颜其洁,彭秉成,傅献彩.物理化学学报,1994,10,289.]doi:10.3866/PKU. WHXB19940401
(2)He,J.;Li,Q.J.;Tang,Y.;Yang,P.;Li,A.;Li,R.;Li,H.Z. Appl.Catal.A-Gen.2012,443-444,145.doi:10.1016/j. apcata.2012.07.036
(3)He,J.;Hu,L.F.;Tang,Y.;Li,H.Z.;Yang,P.;Li,Z.RSC Adv. 2014,4,22334.doi:10.1039/c4ra01482k
(4)Wu,J.H.;Uchida,S.;Fujishiro,Y.;Yin,S.;Sato,T.J. Photochem.Photobiol.A 1999,128,129.doi:10.1016/S1010-6030(99)00157-4
(5)Wu,J.H.;Uchida,S.;Fujishiro,Y.;Yin,S.;Sato,T.Int.J. Inorg.Mater.1999,1,253.doi:10.1016/S1466-6049(99) 00038-0
(6)Wu,J.H.;Yin,S.;Lin,Y.;Lin,J.M.;Huang,M.L.;Sato,T.J. Mater.Sci.2001,36,3055.
(7)Wang,L.L.;Wu,J.H.;Li,T.H.;Cheng,Y.G.;Huang,M.L.; Lin.J.M.J.PorousMat.2005,12,23.doi:10.1007/s10934-005-5229-9
(8)Botella,P.;Solsona,B.;Nieto,J.M.L.;Concepción,P.;Jordá, J.L.;Doménech-Carbó,M.T.Catal.Today 2010,158,162. doi:10.1016/j.cattod.2010.05.024
(9)Murayama,T.;Chen,J.;Hirata,J.;Matsumoto,K.;Ueda,W. Catal.Sci.Technol.2014,4,4250.doi:10.1039/C4CY 00713A
(10)Zhang,H.;Liu,X.J.;Wang,R.L.;Mi,R.;Li,S.M.;Cui,Y. H.;Deng,Y.F.;Mei,J.;Liu,H.J.Power Sources 2015,274, 1063.doi:10.1016/j.jpowsour.2014.10.136
(11)Alemán-Vázquez,L.O.;Hernández-Pérez,F.;Cano-Domínguez,J.L.;Rodríguez-Hernández,A.;García-Gutiérrez, J.L.Fuel2014,117,463.doi:10.1016/j.fuel.2013.08.085
(12)Tian,H.;Wang,H.X.;Shi,W.M.;Xu,Y.Acta Phys.-Chim. Sin.2014,30,1543.[田红,王会香,史卫梅,徐耀.物理化学学报,2014,30,1543.]doi:10.3866/PKU. WXHB201406161
(13)Kioka,K.;Honma,T.;Komatsu,T.Opt.Mater.2011,33,1203. doi:10.1016/j.optmat.2011.02.011
(14)Hsu,S.M.;Wu,J.J.;Yung,S.W.;Chin,T.S.;Zhang,T.;Lee, Y.M.;Chu,C.M.;Ding,J.Y.J.Non-Cryst.Solids2012,358, 14.doi:10.1016/j.jnoncrysol.2011.08.006
(15)Idrees,F.;Cao,C.;Butt,F.K.;Tahir,M.;Shakir,I.;Rizwan, M.;Aslam,I.;Tanveer,M.;Ali,Z.Int.J.Hydrog.Energy 2014,39,13174.doi:10.1016/j.ijhydene.2014.06.142
(16)Li,W.;Meitzner,G.D.;Borry,R.W.;Iglesia,E.J.Catal. 2000,191,373.doi:10.1006/jcat.1999.2795
(17)Huang,H.;Wang,C.;Huang,J.;Wang,X.M.;Du,Y.K.;Yang, P.Nanoscale 2014,6,7274.doi:10.1039/c4nr00505h
(18)Usha,N.;Sivakumar,R.;Sanjeeviraja,C.Mat.Sci.Semicon. Proc.2015,30,31.doi:10.1016/j.mssp.2014.09.043
(19)Ou,J.Z.;Campbell,J.L.;Yao,D.;W lodarski,W.;Kalantarzadeh,K.J.Phys.Chem.C 2011,115,10757.doi:10.1021/ jp202123a
(20)de Paiva,J.B.,Jr.;Monteiro,W.R.;Zacharias,M.A.; Rodrigues,J.A.J.;Cortez,G.G.Braz.J.Chem.Eng.2006,4, 517.
(21)Botto,I.L.;Cabello,C.I.;Thomas,H.J.Mater.Chem.Phys. 1997,47,37.doi:10.1016/S0254-0584(97)80025-9
(22)Guan,J.Q.;Xu,C.;Wang,Z.Q.;Yang,Y.;Liu,Bo.Catal. Lett.2008,124,428.doi:10.1007/s10562-008-9496-3
(23)Xu,B.L.;Fan,Y.N.;Liu,L.;Lin,M.;Chen,Y.Science in China(Series B)2002,32,235.[许波连,范以宁,刘浏,林明,陈懿.中国科学(B辑),2002,32,235.]
(24)Fan,F.Q.;Meng,M.;Tian,Y.;Zheng,L.R.;Zhang,J.;Hu,T. D.Acta Phys.-Chim.Sin.2015,31,1761.[范丰奇,孟明,田野,郑黎荣,张静,胡天斗.物理化学学报,2015,31,1761.] doi:10.3866/PKU.WHXB201507291
(25)Sanderson,R.T.J.Chem.Educ.1988,65,112.doi:10.1021/ ed065p112
(26)Beccaria,A.M.;Poggi,G.;Castello,G.Brit.Corros.J.1995, 30,283.doi:10.1179/000705995798113709
(27)Wang,Q.Q.;Lin,B.Z.;Xu,B.H.;Li,X.L.;Chen,Z.J.;Pian, X.T.MicroporousMesoporousMat.2010,130,344.doi: 10.1016/j.micromeso.2009.11.033
(28)Xu,Y.;Schoonen,M.A.A.Am.Mineral.2000,85,543.doi: 10.2138/am-2000-0416
Structural Features and Photocatalytic Performance of TiO2-HNbMoO6Composite
HU Li-Fang1,2HE Jie1,*LIU Yuan1ZHAO Yun-Lei1CHEN Kai1
(1SchoolofChemical Engineering,AnhuiUniversity ofScience and Technology,Huainan 232001,AnhuiProvince P.R.China;2SchoolofEarth and Environment,AnhuiUniversity ofScience and Technology,Huainan 232001,AnhuiProvince P.R.China)
AnovelcompositematerialTiO2-HNbMoO6was prepared by an intercalation-pillar route.The phase and itsm icrostructure,skeleton feature,spectral-response characteristics,and the interaction between interlayer species and nanosheetswere characterized using powder X-ray diffraction(XRD),high resolution transm ission e lec tron m icroscopy(HRTEM),laser Ram an spec troscopy(LRS),X-ray photoelectron spectroscopy(XPS), UV-Vis diffuse reflectance spectroscopy(UV-Vis DRS),and H2tem perature-programmed reduction(H2-TPR). The specific surface areas of the samplesweremeasured by N2adsorption-desorption isotherms.The synergistic effectbetw een the hostand the guesto f the com posites was evalua ted by the degradation ofme thylene blue (MB)dye under simu lated sunlight.The results,such as the increase of the d-spacing,the absence of TiO2crystalline phase,and the change of the Nb―O bond in themain body and the Ti―O bond in TiO2before and a fter composition,demonstrate that TiO2is uniform ly dispersed in the interlayer of HNbMoO6,indicating the interaction between the host lam inates and the guest titanium oxide species.The specific surface area of the com posite was four times thatof its hostmate rial,the narrow ing band gap,the better adsorption ability,and the superior photocata lytic activity of TiO2-HNbMoO6were because of the synergistic effectbetween the hostand the guest.
November9,2015;Revised:December 14,2015;Published on Web:December 18,2015.
HNbMoO6;TiO2;Com posite structu re;Pho tocata lysis;Syne rgistic e ffec t
O649
10.3866/PKU.WHXB201512184
*Corresponding author.Email:jhe@aust.edu.cn;Tel:+86-554-6668520.
Theprojectwas supported by the NationalNaturalScience Foundation ofChina(21271008)and National Training Programsof Innovation and Entrepreneurship for Undergraduates,China(AH201410361062).
国家自然科学基金(21271008)和国家级大学生创新创业训练计划项目(AH201410361062)资助©Editorialofficeof Acta Physico-Chimica Sinica
