导电聚合物在正极材料LiFePO4上的应用及进展
2016-09-12侯春平董祥芝张秋禹
侯春平, 马 勇,董祥芝,张秋禹
(1. 西北工业大学 理学院应用化学系, 西安 710129; 2. 宁夏博尔特科技有限公司, 银川 750002)
导电聚合物在正极材料LiFePO4上的应用及进展
侯春平1,2, 马勇1,董祥芝1,张秋禹1
(1. 西北工业大学 理学院应用化学系, 西安 710129; 2. 宁夏博尔特科技有限公司, 银川 750002)
主要介绍了国内外在导电聚合物材料包覆改性LiFePO4方面的研究进展,包括聚苯胺、聚吡咯、聚噻吩等导电聚合物对LiFePO4改性及作用机理。同时,还分析了导电聚合物包覆改性存在的问题,并对将来的发展做了展望。
导电聚合物;锂离子电池;正极材料;LiFePO4;包覆掺杂
0 引 言
自1997年Padhi等[1]首次报道了具有橄榄石结构的LiFePO4以来,作为最有希望得到广泛应用的锂离子电池正极材料之一,LiFePO4得到广泛的关注,成为研究热点。这是因为LiFePO4具有安全无毒、热稳定性好、容量高以及成本低等优点。LiFePO4的理论比容量为170 mAh/g,具有3.4 V(vs.Li+/Li)的放电电压平台。相比其它正极材料而言,LiFePO4在过充或短路情况下更稳定,能够承受高温而不分解。
1 LiFePO4的结构和性能特点
磷酸铁锂的结构具有橄榄石结构,属于正交晶系,空间群为Pmnb。图1为LiFePO4结构示意图。在 LiFePO4中强的P—O 共价键形成离域的三维立体化学键,使得LiFePO4具有很强的热力学和动力学稳定性;且由于O原子与P 原子形成较强的共价键,削弱了O与Fe的共价键(即诱导效应),降低了Fe3+/Fe2+的氧化还原的Fermi能级,使Fe3+/Fe2+电位变为3.42 V(vs.Li+/Li)。此电压较为理想,因为电压过高会导致电解质分解,而电压过低又会牺牲能量密度。

图1 LiFePO4的结构示意图
Fig 1 Schematic illustration of crystal structure of LiFePO4
LiFePO4电池的氧化还原反应放热温度大于400 ℃,而LiMn2O4电池的氧化还原反应放热温度大250 ℃,LiCoO2电池的氧化还原反应放热温度大约为150 ℃。这主要归因于LiFePO4聚阴离子的稳定作用[2]。
然而,LiFePO4存在电子电导率低和离子扩散率小的缺点,未经过包覆改性的LiFePO4的电导率约为10-9~10-10S/cm,近乎绝缘体,其粒子扩散系数也很低,DLi+<10-14cm2/s[3]。这些缺点影响了材料的倍率性能和低温放电性能,LiFePO4在-20 ℃的放电容量不到20 ℃容量的50%,限制了其在高功率动力领域的大规模应用[3-5]。
2 LiFePO4的改性研究
2.1目前常用改性方法
为了克服LiFePO4材料本身的缺点,研究人员开展了大量的研究,通常采取碳包覆[6-8]、金属离子掺杂[9-10]、减小粒子尺寸和控制形貌[11]等方法来改善LiFePO4正极材料的导电性能和锂离子扩散性能。经过改性的LiFePO4导电性得到显著提高,可以达到10-1~10-2S/cm。除了上述方法,Park等[12]还采用银对LiFePO4进行表面金属包覆。
2.2导电聚合物对LiFePO4的包覆改性
导电聚合物改性基于碳包覆,是近年来研究逐渐增多的一种包覆改性方法,与通常有机前驱体碳源包覆不同,其一般要经过单体的氧化聚合,形成网状或三维结构,以此来提高电子传输和锂离子的扩散系数,使材料的放电容量、倍率性能和循环性能得到显著提高。导电聚合物,比如聚乙炔、聚苯胺(PANI)、聚吡咯(PPy)、聚噻吩(PTh)等,由于具有电化学活性,允许电解液进入聚合物本体,是潜在的锂离子二次电池的正极材料。这些聚合物能通过包含锂离子或电解液的平衡阴离子的氧化还原反应实现充电和放电。
2.2.1PANI特性及其改性LiFePO4
PANI是高分子化合物的一种,具有特殊的电学、光学性质,经掺杂后可具有导电性,在电子工业、信息工程、国防工程等的开发和发展方面都具有多种用途。PANI的电化活性源于分子链中的P电子共轭结构:随分子链中P电子体系的扩大,P成键态和P*反键态分别形成价带和导带,这种非定域的P电子共轭结构经掺杂可形成P型和N型导电态。不同于其它导电高分子在氧化剂作用下产生阳离子空位的掺杂机制,PANI的掺杂过程中电子数目不发生改变,而是由掺杂的质子酸分解产生H+和对阴离子(如Cl-、硫酸根、磷酸根等)进入主链,与胺和亚胺基团中N原子结合形成极子和双极子离域到整个分子链的P键中,从而使PANI呈现较高的导电性。这种独特的掺杂机制使得PANI的掺杂和脱掺杂完全可逆,掺杂度受pH值和电位等因素的影响,并表现为外观颜色的相应变化,PANI也因此具有电化学活性和电致变色特性。
PANI是最重要的导电聚合物之一,具有良好的导电性、热稳定性、化学稳定性、易加工性、制备容易和成本低这些特点,被研究应用在动力和储能电池领域。
Qin等[8]通过水热反应和电聚合PANI工艺制备了纳米C/LiFePO4/MWCNTs三维网状材料,大大提高了电子传输和锂离子的扩散系数,材料的放电容量、倍率性能和循环性能得到显著提高,0.1 C倍率放电容量高达169.9 mAh/g,20 C倍率的容量为143.4 mAh/g,200 cycles循环的容量保持率>95%,而且其振实密度高达1.78 g/cm3,图2为其合成路线示意图。

图2 C/LiFePO4/MWCNTs纳米粒子合成过程示意图[8]
Jiang等[13]采用FePO4/PANI作为铁源制备了LiFePO4/C核/壳结构纳米复合材料,考察了碳含量对其电化学性能的影响,发现在碳壳厚度小时,粒子表层存在结构无序和缺陷,致使纳米复合材料的电化学性能差;随着碳壳层厚度的增加,粒子表面的结构无序和缺陷减少;在碳壳层厚度较大时,材料的电化学性能得到显著改善。然而,碳壳层厚度的进一步增加会导致LiFePO4/C核/壳纳米复合材料充/放电容量的降低,但材料具有很好的循环稳定性。这是因为过多的碳包覆阻止电解液向碳层渗透以及Li+通过碳层向内/向外扩散,从而致使材料的充放电容量降低,见图3和4。
采用原位聚合法制备PANI/LiFePO4,是一种研究较多的PANI包覆改性LiFePO4的方法,制备复合材料的电荷转移阻抗显著降低,而且具备较高的放电容量和较好的循环性能、倍率性能[14-16]。

图3碳含量为0.9%,5.5%,8.6%,14.6%和26.6%(质量分数)的LiFePO4/C核/壳结构纳米复合材料的循环性能(充放电电压为2.5~4.2 V vs. Li+/Li,倍率为1.0 C,电解液1 mol/L LiPF6/EMC-DEC,25 ℃)[13]
Fig 3 Cycling performance of the LiFePO4/C core/shell nanocomposites with the carbon contents of 0.9%, 5.5%, 8.6%, 14.6% and 26.6wt%, respectively. The data are collected under the charge and discharge rate of 1.0 C at the cutoff voltage of 2.5-4.2 V vs. Li/Li+in 1 mol/L LiPF6/EMC-DEC (1∶1 in v/v) at 25 ℃[13]

图4(a)碳含量为0.9%,5.5%,8.6%,14.6%和26.6%(质量分数)的LiFePO4/C核/壳结构纳米复合材料在200 kHz~10 MHz频率范围的EIS图;(b)ZRe和ω-1/2在低频的关系,(a)的插图是等效电路[13]
Fig 4 (a) EIS spectra of the LiFePO4/C core/shell nanocomposites with the carbon contents of 0.9%, 5.5%, 8.6%, 14.6% and 26.6wt% in the frequency range between 200 kHz and 10 MHz; (b) The relationship betweenZReandω-1/2at low frequency. The inset of (a) shows an equivalent circuit[13]
Sehrawat等[17]采用聚合物凝胶燃烧的方法制备了LiFePO4/C复合材料,分别用0.5和1.0 mL苯胺单体形成不同量的凝胶,结果发现苯胺用量为1.0 mL时制备的LiFePO4样品比苯胺用量为0.5 mL制备的LiFePO4样品的在5和10 C倍率下的放电容量要高,倍率性能的改善归根于粒子尺寸和电荷转移阻抗的减小以及Li+扩散系数的提高。Shen等[18]采用化学还原氧化石墨烯和PANI相结合的方法改善LiFePO4材料的电化学性能。
苏畅等[19]通过溶液共混法制备了一种新型的聚三苯胺(PTPAn)修饰包覆的C-LiFePO4复合锂离子电池正极材料(C-LiFePO4/PTPAn)。结果表明,通过溶液共混法PTPAn能够致密地包覆在C-LiFePO4表面, 形成一个有效的电子/离子传输通道从而有效提高C-LiFePO4基复合材料的电化学活性。
Chen等[20]采用无机酸做掺杂剂制备了自组装LiFePO4/PANI 复合正极材料。使用HCl、H3PO4掺杂的C-LFP/PANI复合材料的容量和倍率性能得到提高,但H2SO4掺杂的效果却不尽人意。
2.2.2PPy及其复合物改性LiFePO4
在导电聚合物中,PPy是最有可能用作正极材料的材料之一,其具有2.0~4.5 V(vs. Li+/Li)的开路电压和80~390 Wh/kg的比容量(72 mAh/g的理论容量),电导率介于10-3~100 S/cm之间,具有较好的热稳定性和高的导电性。因此,PPy添加剂既可用作导电剂,又可用作正极材料。但是,PPy的实际比容量一般都很低,而且充放电曲线斜率较大,较差的机械性能,如加工性能差和脆性,这些都限制了PPy作为正极材料的大规模应用。在导电聚合物改性LiFePO4的研究中,采用PPy方法引起了众多关注。
Chen等[21]通过LiFePO4/PPy热解制得LiFePO4/C复合材料,这里LiFePO4/PPy是通过吡咯单体和水热合成LiFePO4的原位化学聚合制得。结果发现,在2 mol/L LiNO3水性电解液中,800 ℃烧结的LiFePO4/C含碳量为2.8%(质量分数),0.1 C放电容量为49.6 mAh/g,而纯相LiFePO4仅有11.6 mAh/g的放电容量,材料电化学性能的改善归功于PPy碳化生成了芳香族化合物。
Wang等[22]和Sehrawat等[23]采用在LiFePO4粒子表面聚合吡咯单体的方法制备了PPy-LiFePO4复合材料。
Park等[24]的研究通过化学或/和物理方法给聚合物主链引入氧化还原电对,这个电对通常是过渡金属的3dn/3dn+1,以此来使充放电曲线变平坦和增加聚合物的容量。通过在不锈钢筛网上进行电沉积制备了厚度不均匀的PPy/二茂铁聚合物膜(见图5)。该PPy/二茂铁膜具有65 mAh/g的比容量和接近3.5 V(vs. Li+/Li)的电压平台。相比之下,用同样方法制备的纯PPy正极膜仅有约20 mAh/g,而且充放电曲线倾斜度大。同时研究了PPy/ LiFePO4以及常规n(LiFePO4)/n(C)/n(PTFE)=75∶20∶5,PPy/ LiFePO4材料显示了较高的容量和较好的倍率性能,也降低了高放电倍率下的超电势。
Oriňáková等[25-32]的研究基于PPy基导电聚合物对LiFePO4的电化学效率的影响,评估了PPy中PEG添加剂的影响和复合材料纳米化的影响,将材料电化学性能的改善归因于粒子间接触阻抗和电极材料的电荷转移阻抗的降低、电子导电性的提高、电解液离子溶解性的增加、溶解Li+迁移率提高。PPy或PPy/PEG导电聚合物层引入改善了材料的机械和结构性能,增加了结构柔性。从低交联和减少结构缺陷就能反应出PEG在PPy中的稳定化效果,从而提高了PPy/PEG-LiFePO4的比容量。并采用飞行时间二次离子质谱仪(TOF-SIMS)分析确认了在PPy中PEG的支撑作用是改善了混合聚合物的机械稳定性(在充电过程尤其重要),通过使用SIMS测量不同二次离子的强度监控混合聚合物膜中PPy、PEG和Li+碎片的分布。

图5在不锈钢筛网上沉积的PPy/二茂铁聚合物膜的SEM照片(比例尺分别为102和20.1 μm)[24]
Fig 5 Scanning electron microscopy images of the polymer film (PPy/ferrocene polymer cathode) deposited on a stainless-steel mesh (scale bars: 102 and 20.1 μm, respectively)[24]
在C-LiFePO4/PPy复合材料的制备方法探索上,研究者们尝试了连续电压电沉积制备方法[33]、吡咯作高效还原剂水热制备方法[34]、类纸独立PPy和PPy-LiFePO4复合材料膜用于柔性弯曲充电电池[35],采用Fe(Ⅲ)甲苯磺酸盐制备方法[36],丰富和拓宽了C-LiFePO4/PPy复合材料的制备方法,对改善材料性能,满足应用要求具有积极意义。Yang[36]采用Fe(Ⅲ)甲苯磺酸盐制备LiFePO4/C-PPy复合材料表现出非常优异的倍率性能,20 C仍有115 mAh/g的放电容量,而且循环性能也非常好。
这要强调的是,提高LiFePO4/PPy实际效果的过程中,掌握作用机理更具指导意义。Gong等[37]采用化学气相沉积的方法制备了LiFePO4/C-PPy复合材料,结果显示,复合材料在20 ℃的倍率性能和55 ℃的循环性能非常优异,PPy包覆能够有效降低Fe在LiPF6电解液中的溶解,抑制了Fe离子在负极上的还原。
Xia等[38]研究工作对实际生产帮助很大,批次稳定性是LiFePO4生产的一个难点,容易出现材料的部分氧化,导致材料浪费和成本高。通过对空气氧化LiFePO4的再生和定性研究,发现LiFePO4暴露在热空气中会生成α-Fe2O3导致容量衰减,其在与PPy混合烧结后电化学性能可得到恢复,条件是PPy存在下于400 ℃Ar气保护气氛中烧结。
2.2.3PTh及其复合物改性LiFePO4
PTh是一种常见的导电聚合物,能隙较小,但氧化掺杂电位较高,故其氧化态在空气中很不稳定,迅速被还原为本征态。同时聚噻吩可以被还原掺杂。聚噻吩很容易在3位引入侧链,根据侧链的不同,聚噻吩的溶解性以及电化学性质有较大的区别。
Lepage等[39]提出用3,4-亚乙二氧基噻吩(EDOT)制备导电聚合物(PEDOT)/ LiFePO4复合材料的软化学制备方法,优点有:(1) 依靠Li(1-x)FePO4固有氧化性而不是使用外加氧化剂作为氧化聚合的动力,避免了从聚合物渗出的残留氧化剂或氧化剂副产品进入电解液影响负极; (2) 聚合增长要求Li再插入部分脱Li得LiFePO4,同时Li+和电子从沉积聚合物包覆层传输通过,因此聚合增长反应本质上提升了产品的功能,而且与常用碳包覆技术相比,这种方法不用高温加工,没有VOCs、CO、CO2生成;(3) 使用H2O2生成Li(1-x)FePO4是环境友好的方法,最终制备的导电聚合物/LiFePO4复合材料可以用作“非碳添加”正极。材料的电化学性能非常优异,0.1和10 C倍率放电容量分别高达163和123 mAh/g。
通过PTh以及PTh与其它物质的共聚物复合,也是导电聚合物改性LiFePO4的研究内容之一[40-42],此方法一般要经过噻吩单体及其它待复合单体在LiFePO4粒子表面聚合或者共聚,以此改善复合材料的电化学性能。Daniel Cíntora-Juárez等[43-44]和Nuria Vicente等[45]采用PEDOT以及PEDOT与PSS(聚磺苯乙烯)复合材料改性LiFePO4,显著提升了材料的导电性和倍率放电能力。
2.2.4C-N复合包覆改性LiFePO4
Avci等[46]采用氯化聚苯胺聚合热解法制备CN包覆的 LiFePO4/CN复合材料,最优LiFePO4/CN复合材料是采用10%(质量分数) PANI-Cl在700 ℃合成制得。相比碳包覆的磷酸铁锂,该LiFePO4/CN复合材料的容量、循环和倍率性能得到显著提高,0.1 C倍率下的放电比容量高达164 mAh/g,甚至在10 C倍率下仍有100 mAh/g的放电容量。另外,此复合材料的循环稳定性也非常出色,1 000次循环的容量损失仅为10%。LiFePO4/CN复合材料的粒度约150 nm,含1.6% N和15.8%(质量分数)C,LiFePO4粒子被纳米尺寸的C-N层包覆从而形成核-壳结构。
2.2.5导电聚合物在锂离子电池中的其它应用
(1) 用作电极导电粘结剂
传统的锂电池电极制备是由电极活性材料、导电碳黑、起粘结粒子作用的非导电粘结剂。Patel等[47]提出了一种新型导电粘结剂,研究了电化学氧化电子和粒子导电纳米结构嵌段共聚物锂电池电极,分析了在锂电池充/放电循环情况下双三氟甲烷磺酰亚胺锂(LiTFSI)氧化聚3-己基噻吩-聚氧化乙烯(P3HT-PEO)共聚物的电荷传输。采用固态三电极电池体系同时进行导电性测试和控制P3HT的电化学掺杂。在低氧化态(电极中转移电子摩尔数与3-己基噻吩之比),电子电导率从10-7S/cm提升至10-4S/cm,而在高氧化态,电子电导率则增至10-2S/cm。当将P3HT-PEO作为导电粘合剂在LiFePO4正极材料中使用时,P3HT在充放电电压范围内是具有电化学活性的材料,在大部分电压窗口范围P3HT-PEO粘结剂的电子电导率在10-4S/cm到10-2S/cm范围内变化。但是,在放电过程末端,材料的电导率陡降为10-7S/cm,意味着“导电”粘结剂变成了电绝缘的。导电粘结剂在正极导电态和绝缘态的转换能力为可充电电池的自动过放保护提供了一种新思路。
(2) 用作LiFePO4电池隔膜改性剂
电池的安全性一直是困扰大型锂离子电池(LIBs)在电动车和混合电动车上应用的主要难题。过充引起的电压失控是LIBs不良行为的主要原因。

图6隔膜的SEM照片和EDS图谱,(a)和(b)的插图是隔膜的横截面照片[彩图出处www.wileyonlinelibrary.com.][48]
Fig 6 SEM images and EDS patterns of the separators. The insets in (a) and (b) display the cross-section images of the separators.[Color figure can be viewed in the online issue, which is available at wileyonlinelibrary.com.][48]
Zhang等[48]研究了氧化还原聚噻吩改性隔膜,提高锂离子电池安全性。通过将氧化还原性聚3-丁基噻吩(P3BT)嵌入到商品化的多孔聚烯烃膜的微孔中制得对电压敏感的隔膜,以测试对LiFePO4/Li4Ti5O12锂离子电池的过充保护。随着正极电压从过充态到正常工作态的变化,嵌在隔膜中的氧化还原P3BT聚合物进行可逆掺杂-脱掺杂,这种隔膜能在电绝缘态和导电态转换以保持LiFePO4/Li4Ti5O12电池充电电压处于小于等于2.4 V的安全值,避免电池电压失控。由于这类隔膜能够可逆工作且对电池性能没有负面影响,可以用作商品化锂离子电池和其它可充电电池的内部和自我保护机能。研究者测试对比了改性隔膜和常规隔膜,改性隔膜的电导率下降了20%,这是由于改性隔膜部分封闭的孔结构造成。对比二者的充放电曲线,使用常规聚烯烃隔膜电池在充电至4 V时曲线陡升,而用P3BT改性隔膜电池在约3.85 V时会出现一个平台,能够对充电电压进行有效控制,见图6和7。
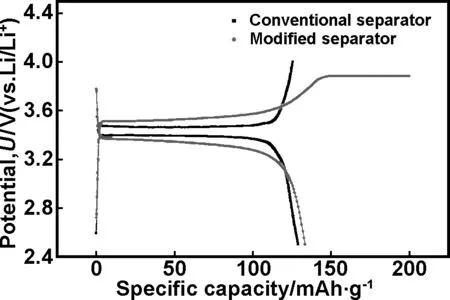
图7在0.382 mA/cm2恒电流下使用P3BT改性隔膜和常规多孔聚烯烃隔膜Li/LiFePO4电池的充放电曲线[彩图出处www.wileyonlinelibrary.com.][48]
Fig 7 Charge-discharge curves of theLi/LiFePO4cell using both P3BT-modified separator and conventional porous polyolefin membrane at a constant current of 0.382 mA/cm2. [Color figure can be viewed in the online issue, which is available at wileyonlinelibrary.com.][48]
Li等[49]研究了聚3-癸基噻吩(P3DT)改性隔膜,用于LiFePO4电池的过充保护,具有与上述P3BT改性隔膜相似的效果。
(3) 用作Li(Mn1/3Ni1/3Fe1/3)O2材料改性剂
Karthikeyan等[50]制备Li(Mn1/3Ni1/3Fe1/3)O2-PANI混合物做正极材料,其具有超快的充/放电能力,在5,30和40 C倍率下的可逆容量分别为127,114和110 mAh/g。通过与PANI纳米纤维复合制得网状Li(Mn1/3Ni1/3Fe1/3)O2-PANI复合材料的结构示意图见图8。
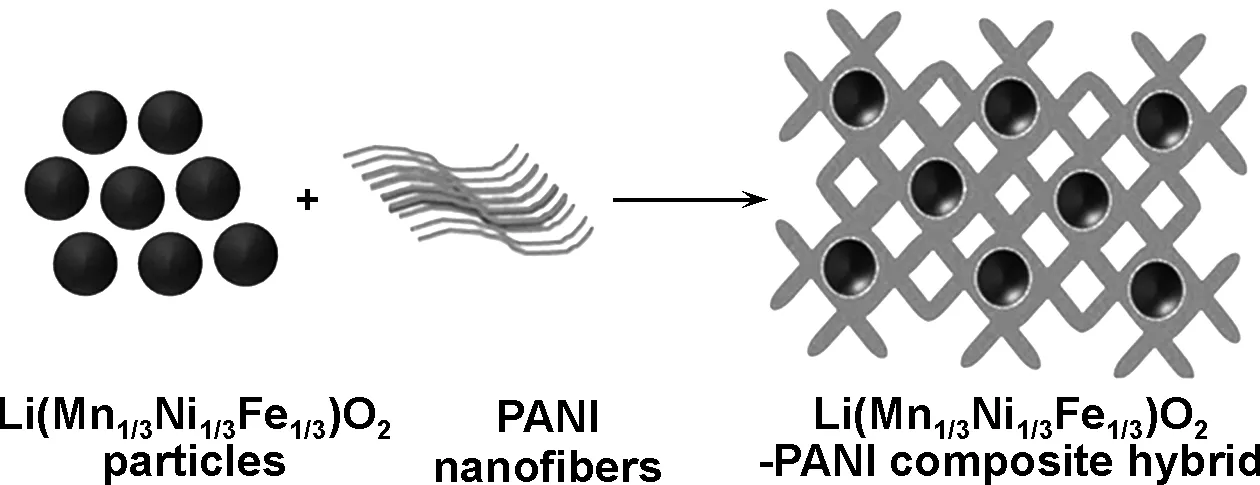
图8Li(Mn1/3Ni1/3Fe1/3)O2-PANI复合材料形成过程示意图[50]
Fig 8 Schematic illustration of the synthesis procedure of Li(Mn1/3Ni1/3Fe1/3)O2-PANI composite materials[50]
3 结 语
提高LiFePO4的电导率和离子扩散系数进而提高其大倍率充放电性能和循环性能,是LiFePO4能否成功地用作锂离子动力电池正极材料的关键。相对于纯LiFePO4正极材料,通过碳包覆尤其是导电聚合物包覆复合、金属离子掺杂、减小LiFePO4粒子尺寸等方法,其性能得到显著提高。
但是,目前通过导电聚合物复合LiFePO4制备材料的性能与动力电池正极材料的要求还有一定差距,而且鲜有导电聚合物复合LiFePO4材料产业化应用的报道。导电聚合物掺杂改性LiFePO4亟待解决的问题有:(1) 导电聚合物改性材料的低温性能还需不断探讨研究;(2) 虽然采用PANI包覆FePO4经烧结碳化制得LiFePO4/C纳米粒子材料有很高的放电容量,但这种方法会产生残留水和杂相,很难保证在Li和FePO4之间准确的化学计量比,因Li量变化生成的杂相会影响电化学性能[51];(3) 导电聚合物改性纳米LiFePO4是一个重要方向,制备纳米C/LiFePO4/MWCNTs三维网状材料具有振实密度高、容量高、倍率性能好、循环性能好等优点,其作用机理研究还有待于进一步加深,因为它能减少碳掺杂对材料能量密度的影响;(4) 导电聚合物复合掺杂改性或共聚掺杂改性的协同效应及其机理研究;(5) LiFePO4电池的放电电压平台平缓,电池过充/过放的电压监控难度大;(6) 导电聚合物包覆掺杂改性的产业化工艺优化验证,降低成本,减少环境污染,提高批次一致性。
因此,要保持LiFePO4能量密度提升,减少使用非储锂碳包覆,未来LiFePO4的导电聚合物改性有可能在以下方面取得突破:(1) C、N等多导电聚合物掺杂的协同效应研究及对LiFePO4低温性能的提升;(2) 采用其它非碳可储锂改性剂,提高容量,减小碳包覆对振实密度和压实密度的影响;(3) 作为一种成本低,来源广泛的导电聚合物,导电聚乙炔改性锂离子电池材料相关研究很少;(4) 导电聚合物通过网状结构均匀分散固定石墨烯/LiFePO4纳米粒子,以提升倍率性能和低温性能;(5) 鉴于LiFePO4电池的放电电压平台平缓,采用PTh等导电聚合物改性隔膜提高LiFePO4电池过充/过放保护的意义重大。
相信随着对LiFePO4改性机理研究的深入、改性合成方法的创新和检测评估手段日益丰富,LiFePO4的导电性、锂离子扩散性、低温性能、稳定性、安全性、可靠性等问题会得到逐步解决,定会使LiFePO4在动力/储能锂离子电池的应用前景更加广阔!
致谢:感谢宁夏回族自治区科技创新领军人才项目的大力支持!
[1]Padhi A K, Nanjundaswamy K S, Goodenough J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144 (4): 1182-1194.
[2]Tarascon J M, Armand M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414: 359-367.
[3]Hung S Y, Bloking J T, Chiang Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nature Materials, 2002, 1:123-128.
[4]Liao Lixia, Zuo Pengjian, Ma Yulin, et al. Effects of temperature on charge/discharge behaviors of LiFePO4cathode for Li-ion batteries[J]. Electrochimica Acta, 2012, 60: 269- 273.
[5]Rui X H, Jin Y, Feng X Y, et al. A comparative study on the low-temperature performance of LiFePO4/C and Li3V2(PO4)3/C cathodes for lithium-ion batteries[J]. J Power Sources, 2011, 196: 2109-2114.
[6]Dominko R, Gaberscek M, Bele M, et al. Carbon nanocoatings on active materials for Li-ion batteries[J]. Journal of the European Ceramic Society, 2007, 27: 909-913.
[7]Kang B, Ceder G. Battery materials for ultrafast charging and discharging[J]. Nature Letters, 2009, 458:190-193.
[8]Qin Guohui, Ma Qianqian, Wang Chengyang. A new route for synthesizing C/LiFePO4/multi-walled carbon nanotube secondary particles for lithium ion batteries[J]. Solid State Ionics, 2014, 257:60-66.
[9]Fan Changling, Zhang Kehe, Han Shaochang. Comprehensive methods to enhance the electrochemical performances of LiFe0.94Mg0.03Cu0.03PO4/C cathode for lithium ion batteries[J]. Materials Research Bulletin, 2013, 48: 2497-2503.
[10]Wang G X, Needham S, Yao J, et al. A study on LiFePO4and its doped derivatives as cathode materials for lithium-ion batteries[J]. J Power Sources, 2006, 159:282-286.
[11]Li Lingfang, Han Shaochang, Fan Changlin, et al. Synthesis and modification of nanocrystalline LiFePO4as acathode material for lithium-ion batteries[J]. Materials Letters, 2013, 108:156-159.
[12]Park K S, Son J T, Chung H T, et al. Surface modification by silver coating for improving electrochemical properties of LiFePO4[J]. Solid State Communications, 2004, 129: 311-314.
[13]Jiang Zhongqing, Jiang Zhongjie. Effects of carbon content on the electrochemical performance of LiFePO4/C core/shell nanocomposites fabricated using FePO4/polyaniline as an iron source[J]. J Alloys Compd, 2012, 537: 308-317.
[14]Lei Gangtie, Yi Xiaohua, Wang Lei, et al. An investigation of the electrochemical performance of polyaniline coated LiFePO4materials[J]. Polym Adv Technol, 2009, 20: 576-580.
[15]Chen W M, Qie L, Yuan L X, et al. Insight into the improvement of rate capability and cyclability in LiFePO4/polyaniline composite cathode[J]. Electrochimica Acta, 2011, 56: 2689-2695.
[16]Gu Ningyu, He Xinghua, Li Yang. LiFePO4@C cathode materials synthesized from FePO4@PAn composites[J]. Materials Letters, 2012, 81: 115-118.
[17]Sehrawat R, Sil A. Polymer gel combustion synthesis of LiFePO4/C composite as cathode material for Li-ion battery[J]. Ionics, 2015, 21: 673-685.
[18]Shen Wenzhuo, Wang Yanmei, Yan Jiao, et al. Enhanced electrochemical performance of lithium iron(Ⅱ) phosphate modified cooperatively via chemically reduced graphene oxide and polyaniline[J]. Electrochimica Acta, 2015, 173: 310-315.
[19]Su Chang, Huang Qifei, Xu Lihuan, et al. Preparation and performances of C-LiFePO4/polytriphenylamine composite as cathode material for lithium-ion batteries[J]. Acta Phys Chim Sin, 2014, 30 (1): 88-94.
苏畅, 黄启飞, 徐立环, 等. C-LiFePO4/聚三苯胺复合锂离子电池正极材料的制备与性能[J]. 物理化学学报, 2014, 30(1): 88-94.
[20]Chen Weimin, Huang Yunhui, Yuan Lixia. Self-assembly LiFePO4/polyaniline composite cathode materials with inorganic acids as dopants for lithium-ion batteries[J]. Journal of Electroanalytical Chemistry, 2011, 660: 108-113.
[21]Chen Shengyao, Gao Bo, Su Linghao, et al. Electrochemical properties of LiFePO4/C synthesized using polypyrrole as carbon source[J]. J Solid State Electrochem, 2009, 13: 1361-1366.
[22]Wang G X, Yang L, Chen Y, et al. An investigation of polypyrrole-LiFePO4composite cathode materials for lithium-ion batteries[J]. Electrochimica Acta, 2005, 50: 4649-4654.
[23]Sehrawat R, Sil A. Effect of solvents on electrochemical performance of polypyrrole coated LiFePO4/C cathode materials for Li-ion battery[J]. J Mater Sci: Mater Electron, 2015, 26: 5175-5185.
[24]Park K S, Schougaard S B, Goodenough J B. Conducting-polymer/Iron-redox-couple composite cathodes for lithium secondary batteries[J]. Adv Mater, 2007, 19: 848-851.
[25]Oriňáková R, Fedorková A, Oriňák A. Effect of PPy/PEG conducting polymer film on electrochemical performance of LiFePO4cathode material for Li-ion batteries[J]. Chemical Papers, 2013, 67 (8): 860-875.
[26]Fedorková A, Oriňáková R, Oriňák A, et al. Electrochemical and TOF-SIMS investigations of PPy/PEG-modified LiFePO4composite electrodes for Li-ion batteries[J]. Solid State Sciences, 2011, 13: 824-830.
[27]Fedorková A, Oriňáková R, Oriňák A, et al. Electrochemical and XPS study of LiFePO4cathode nanocomposite with PPy/PEG conductive network[J]. Solid State Sciences, 2012, 14: 1238-1243.
[28]Fedorková A, Wiemhföer H D, Oriňáková R, et al. Improved lithium exchange at LiFePO4cathode particles by coating with composite polypyrrole-polyethylene glycol layers[J]. J Solid State Electrochem, 2009, 13: 1867-1872.
[29]Fedorková A, Oriňáková R, Oriňák A, et al. PPy doped PEG conducting polymer films synthesized on LiFePO4particles[J]. J Power Sources, 2010, 195: 3907-3912.
[30]Fedorková A, Alejos A, Romero P, et al. Structural and electrochemical studies of PPy/PEG-LiFePO4cathode material for Li-ion batteries[J]. Electrochimica Acta, 2010, 55: 943-947.
[31]Fedorková A, Wiemhföer H D, Oriňáková R,et al. Surface modification of FePO4particles with conductive layer of polypyrrole[J]. Solid State Sciences, 2010, 12: 924-928
[32]Fedorková A, Oriňáková R, Oriňák A, et al. Surface treatment of LiFePO4cathode material with PPy/PEG conductive layer[J]. J Solid State Electrochem, 2010, 14: 2173-2178.
[33]Boyano I, Blazquez J A, Meatza I, et al. Preparation of C-LiFePO4/polypyrrole lithium rechargeable cathode by consecutive potential steps electrodeposition[J]. J. Power Sources, 2010, 195: 5351-5359.
[34]Liang Yiping, Li Chia-Chen, Chen Wenjing, et al. Hydrothermal synthesis of lithium iron phosphate using pyrrole as an efficient reducing agent[J]. Electrochimica Acta, 2013, 87: 763-769.
[35]Wang Jiazhao, Chou Shulei, Chen Jun, et al. Paper-like free-standing polypyrrole and polypyrrole-LiFePO4composite films for flexible and bendable rechargeable battery[J]. Electrochem Commun, 2008, 10: 1781-1784.
[36]Yang Yang, Liao Xiaozhen, Ma Zifeng, et al. Superior high-rate cycling performance of LiFePO4/C-PPy composite at 55 ℃[J]. Electrochem Commun, 2009, 11: 1277-1280.
[37]Gong Qiang, He Yushi, Yang Yang,et al. Synthesis and electrochemical characterization of LiFePO4/C-polypyrrole composite prepared by a simple chemical vapor deposition method[J]. J Solid State Electrochem, 2012, 16: 1383-1388.
[38]Xia Xin, Wang Zhaoxiang, Chen Liquan. Regeneration and characterization of air-oxidized LiFePO4[J]. Electrochem Commun, 2008, 10: 1442-1444.
[39]Lepage David, Michot Christophe, Liang Guoxian, et al. A soft chemistry approach to coating of LiFePO4with a conducting polymer[J]. Angew Chem Int Ed, 2011, 50: 6884-6887.
[40]Bai Yongmei, Qiu Peng, Wen Zhongliu, et al. Improvement of electrochemical performances of LiFePO4cathode materials by coating of polythiophene[J]. J Alloys Compd, 2010, 508: 1-4.
[41]Liu Jing, Yang Guiling, Zhang Xianfa, et al. Synthesis of the LiFePO4/C core-shell nanocomposite using a nano-FePO4/polythiophene as an iron source[J]. J Power Sources, 2012, 197: 253-259.
[42]Chang C C, Her L J, Hong J L. Copolymer from electropolymerization of thiophene and 3,4-ethylenedioxythiophene and its use as cathode for lithium ion battery[J]. Electrochimica Acta, 2005, 50: 4461-4468.
[43]Daniel Cíntora-Juárez, Carlos Pérez-Vicente, Shahzada Ahmad, et al. Electrochemical in battery polymerization of poly(alkylenedioxythiophene) over lithium iron phosphate for high-performance cathodes[J]. Phys Chem Chem Phys, 2014, 16: 20724-20730.
[44]Daniel C J, Carlos P V, Samrana K, et al. Judicious design of lithium iron phosphate electrodes using poly(3,4-ethylenedioxythiophene) for high performance batteries[J]. J Mater Chem A, 2015, 3: 14254-14262.
[45]Nuria V, Marta H, Daniel C J, et al. LiFePO4particle conductive composite strategies for improving cathode rate capability[J]. Electrochimica Acta, 2015, 163: 323-329.
[46]Avci E, Mazman M, Uzun D, et al. High performance LiFePO4/CN cathode material promoted by polyaniline as carbonenitrogen precursor[J]. J Power Sources, 2013, 240: 328-337.
[47]Patel S N, Javier A E, Balsara N P. Electrochemically oxidized electronic and ionic conducting nanostructured block copolymers for lithium battery electrodes[J]. ACS Nano, 2013, 7 (7): 6056-6068.
[48]Zhang Haiyan, Cao Yuliang, Yang Hanxi, et al. A redox-active polythiophene-modified separator for safety control of lithium-ion batteries[J]. Journal of Polymer Science, Part B:Polymer Physics, 2013, 51: 1487-1493.
[49]Li S L, Xia L, Zhang H Y, et al. A poly(3-decyl thiophene)-modified separator with self-actuating overcharge protection mechanism for LiFePO4-based lithium ion battery[J]. J Power Sources, 2011, 196: 7021-7024.
[50]Karthikeyan K, Amaresh S, Aravindan V, et al. Li(Mn1/3Ni1/3Fe1/3)O2-polyaniline hybrids as cathode active material with ultra-fast charge-discharge capability for lithium batteries[J]. J Power Sources, 2013, 232: 240-245.
[51]Nam Seunghoon, Wi Sungun, Nahm Changwoo, et al. Challenges in synthesizing carbon-coated LiFePO4nanoparticles from hydrous FePO4and their electrochemical properties[J]. Materials Research Bulletin, 2012, 47: 3495-3498.
The application and progress of the conducting polymers in LiFePO4cathode material
HOU Chunping1,2, MA Yong1, DONG Xiangzhi1, ZHANG Qiuyu1
(1. Department of Applied Chemistry, School of Science, Northwestern Polytechnical University,Xi’an 710129, China;2. Ningxia BOLT Technologies, Co., Ltd., Yinchuan 750002, China)
In this paper, the recent research progress of coating and doping modification of LiFePO4with conducting polymers was reviewed, including modification and mechanism of polyaniline(PANI), polypyrrole(PPy), polythiophene(PTh), and so on. Furthermore, some problems of modification and coating with conducting polymers were summarized, and the development prospect for modification of LiFePO4/conducting polymers were proposed.
conducting polymers;lithium ion battery;cathode material;LiFePO4;coating and doping
1001-9731(2016)08-08050-08
宁夏回族自治区自然科学基金资助项目(NZ13261)
2015-05-28
2016-03-22 通讯作者:张秋禹,E-mail: qyzhang@nwpu.edu.cn
侯春平(1976-),男,宁夏盐池人,在读博士,师承张秋禹教授,从事新能源材料研究。
TM912
A
10.3969/j.issn.1001-9731.2016.08.008
