4,6-二苯甲酰基-1,3-苯二胺的合成研究*
2016-09-01周园园吴弘辰武亚明朱红军
周园园,吴弘辰,武亚明,陈 昀,章 勤,朱红军
(1 南京科技职业学院,江苏 南京 210048;2 南京工业大学,江苏 南京 211816)
4,6-二苯甲酰基-1,3-苯二胺的合成研究*
周园园1,吴弘辰1,武亚明1,陈昀1,章勤2,朱红军2
(1 南京科技职业学院,江苏南京210048;2 南京工业大学,江苏南京211816)
以均苯四甲酸二酐为原料合成得到4,6-二苯甲酰基-1,3-苯二胺。通过傅-克酰基化反应得到4,6-二苯甲酰基-1,3-苯二甲酸,再通过氯代反应得到假-4,6-二苯甲酰基-1,3-苯二甲酰氯,继续通过酰胺化反应得到4,6-二苯甲酰基-1,3-苯二甲酰胺,最后通过Hofmann降解反应得到目标化合物。通过熔点、1H NMR对目标化合物结构进行了确认。得到假-4,6-二苯甲酰基-1,3-苯二甲酰氯的1H NMR。
傅-克酰基化;氯化;酰胺化;Hofmann降解;芳胺
二苯甲酰基类芳胺化合物是有机合成原料[1-3]和有机导电材料的重要中间体[4-6],通过缩合反应可以形成大分子共轭体系,在有机光电材料领域具有广泛的潜在用途。
在研究蒽啉小分子化合物的过程中,本课题小组用到了二苯甲酰基类芳胺化合物4,6-二苯甲酰基-1,3-苯二胺,本文主要讨论4,6-二苯甲酰基-1,3-苯二胺的合成工艺。
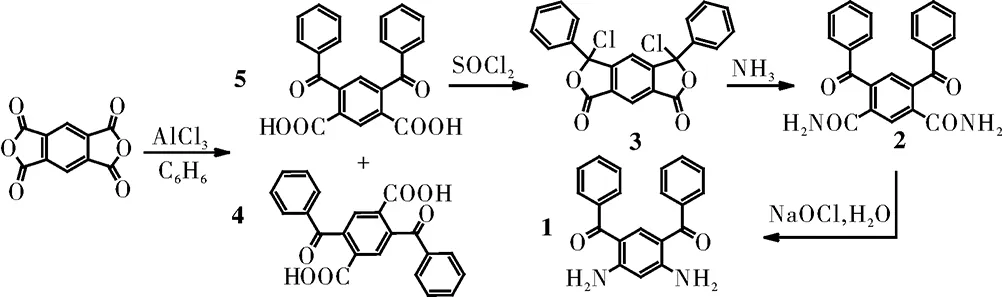
图1 化合物(1)的合成路线Fig.1 The synthetic route of compound (1)
1975年,Imai等[7]报道了,以均苯四甲酸二酐为原料,经过傅-克酰基化提纯得到4,6-二苯甲酰基-1,3-苯二酸,再进一步经过酰氯化、酰胺化制得4,6-二苯甲酰基-1,3-苯二酰胺,最后Hofmann降解共四步反应得到4,6-二苯甲酰基-1,3-苯二胺。合成路线如图1所示。这种方法的缺点是第一步的产物性质相近,比较难提纯,产率较低,本课题组在此方法的基础上,改进第一步提纯方法提高了产率。
1 实 验
1.1主要试剂和仪器
均苯四酸二酐、无水三氯化铝、苯、N-甲基-2-吡咯烷酮、N,N-二甲基甲酰胺(分析纯),国药集团化学试剂有限公司;次氯酸钠、KOH(分析纯),上海凌峰化学试剂有限公司。
X-4型数字显示显微熔点测定仪,Taike公司;AV-500核磁共振仪,Brucker公司。
1.2实验步骤
(1)2,5-二苯甲酰基-1,4-对苯二甲酸(4)和4,6-二苯甲酰基-1,3-苯二甲酸(5)的合成
将均苯四酸二酐粉末10.9 g(50.0 mmol)、无水三氯化铝粉末28.0 g(211.0 mmol)和苯250 mL,三者依次加入到500 mL的四口烧瓶中,在65~70 ℃下加热搅拌,反应4 h,溶液颜色逐渐由淡黄色到红棕色。反应结束后,将混合物倒入含有12.5 mL 浓盐酸的175 mL的水溶液中水解,此时有乳白色絮状物产生。减压蒸馏除去苯,过滤水洗得到米色粒状的粗产物,即2,5-二苯甲酰基对苯二甲酸(4)和4,6-二苯甲酰基间苯二甲酸(5)混合物。将混合物加入到200 mL 1.0 mol/L KOH溶液中,过滤除去少量不溶杂质,滤液用稀盐酸酸化至pH=3~4,过滤后再用蒸馏水洗净,80 ℃下干燥8 h后,得白色固体。用乙酸重结晶,得到2,5-二苯甲酰基对苯二甲酸(4)。得到4后,蒸除重结晶母液中的乙酸,得到的灰色固体,该固体用丙酮重结晶两次得到白色晶体5(4.3 g, 11.5 mmol),产率:23.1%。熔点:277~279 ℃(文献值[7]:277~278 ℃)。1H NMR (DMSO,500 MHz):δ ppm 7.49 (s, 1H),7.50~7.57 (m, 4H),7.64 (t, 2H), 7.70(d, 4H),8.56 (s, 1H),13.66 (s, 2H)。
(2)假-4,6-二苯甲酰基-1,3-苯二甲酰氯(3)的合成
将4,6-二苯甲酰基-1,3-间苯二甲酸(12.0 g,32.1 mmol),SOCl2(50 mL), N,N-二甲基甲酰胺(0.1 mL),三者依次加入到100 mL的四口烧瓶中,在76~78 ℃下搅拌反应2 h,反应中溶液逐渐变澄清。反应结束后,减压蒸馏除去过量的SOCl2,然后再加入苯(2×30 mL),继续减压蒸馏用以除去微量的SOCl2,得到白色固体3(13.0 g, 31.6 mmol),收率:98.4%。1:1环己烷/二氯甲烷混合溶剂重结晶,熔点为181~183 ℃(文献值:183~185 ℃)。1H NMR (CDCl3, 500 MHz): δ ppm 7.47~7.49 (m, 6H),7.66~7.68 (m, 4H), 7.79 (s, 1H), 8.46 (s, 1H)。
(3)4,6-二苯甲酰基-1,3-苯二甲酰胺(2)的合成
往中间体3中加入N-甲基-2-吡咯烷酮(50.0 mL),加热搅拌至溶解,得到红棕色溶液;在0~5 ℃条件下,再将该溶液在30 min内缓慢加入到由浓氨水(45.0 mL)和NMP(60.0 mL)组成的混合溶液中,滴加完毕后,撤去冰浴,在室温下,将反应混合物搅拌24 h,再用蒸馏水(80 mL)稀释,析出白色沉淀。白色沉淀经过滤,热水(100 mL)洗涤,80 ℃下干燥8 h,干燥后得到白色粉末4,6-二苯甲酰基间苯二甲酰胺(2)(11.2 g, 30.1 mmol),收率为95.1%。甲醇重结晶,熔点为289~293 ℃(文献值[7]:290~295 ℃)。1H NMR (DMSO, 500 MHz): δ ppm 7.01 (s, 2H), 7.10 (d,1H), 7.20~7.26 (m, 6H), 7.37~7.39 (m, 4H), 7.74 (d, 1H), 9.37 (s, 2H)。
(4)4,6-二苯甲酰基-1,3-苯二胺(1)的合成
将中间体2(25.0 g, 67.2 mmol)溶于300 mL 2.08 mol/L 的KOH 溶液中,得到悬浊液,冰水浴冷却。在5~7 ℃条件下,往上述溶液中滴加5.25%的次氯酸钠溶液(215 mL, 249.8 mmol),约0.5 h 滴完。然后移除冰水浴,此时反应液为黄色透明溶液。再用热水浴加热反应,在76~80 ℃下反应2 h,反应液变为红棕色,并出现红色沉淀,过滤收集沉淀,用热水彻底洗涤(3×500 mL),再次过滤,干燥,得到1的粉红色粗产物(16.9 g, 53.5 mmol),收率为79.6%。粗产物先后用氯仿和无水甲醇重结晶,得到淡黄色粉末1,熔点为253~254 ℃(文献值[7]:255~257 ℃)。1H NMR (DMSO, 500 MHz):δ ppm 6.02 (s, 1H),7.34~7.42 (m, 6H),7.44~7.46 (m, 6H),7.56 (s, 1H),7.59 (s, 4H)。
2 结果与讨论
2.1重结晶溶剂的选择
第一步傅克酰基化反应中,根据文献,用冰乙酸和水(1:3)的混合溶剂对中间体5进行重结晶提纯,用文献这个方法是可以进行提纯的,但是不能得到较纯的化合物5。经过研究摸索发现,用丙酮来进行提纯,可以得到较纯的化合物5。最终确定先用冰乙酸对4和5的混合物分步重结晶两次,分离得到中间体4,蒸除重结晶母液中的乙酸,再用丙酮进行重结晶得到了5。
2.2水分的影响
第二步氯代反应中,要注意反应整个过程无水操作。反应结束后,尽量蒸除微量的氯化亚砜,氯化亚砜的存在对下一步反应影响很大。
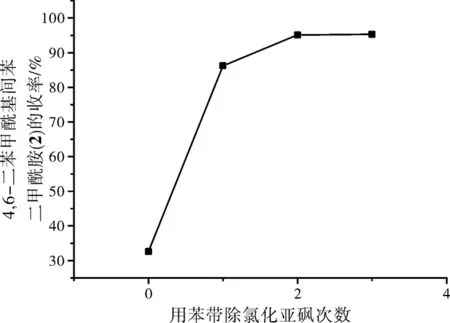
图2 用苯带除氯化亚砜次数对化合物(2)收率的影响Fig.2 The effect of the number of thionyl chloride removing with benzene on the yield of compound (2)
从图2中可以看出,用苯带除氯化亚砜两次后,第三步4,6-二苯甲酰基间苯二甲酰胺(2)收率就很高了,达到95%。带除氯化亚砜后的产物应尽快投入第三步反应,可以不提纯,直接用于第三步酰胺化反应,因为酰氯易水解。
2.3反应温度的影响
第三步酰胺化反应制备4,6-二苯甲酰基间苯二甲酰胺(2)中,改变滴加浓氨水时的温度,得到4,6-二苯甲酰基间苯二甲酰胺(2)收率与滴加温度的关系图,如图3所示。
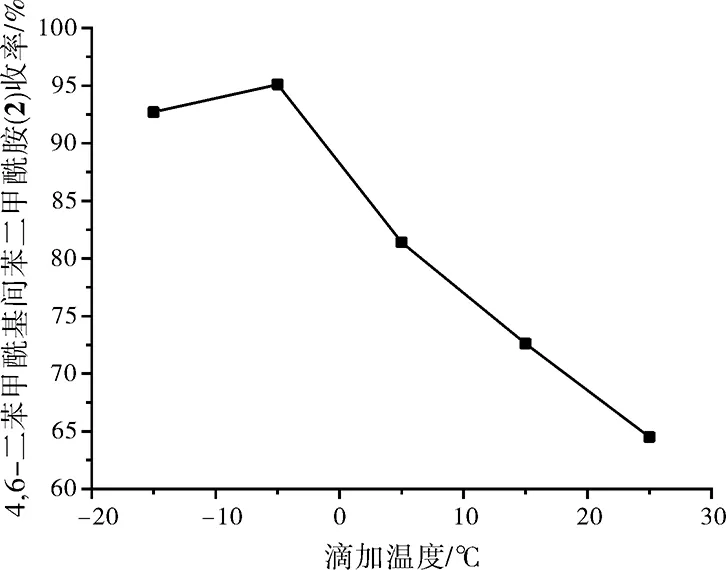
图3 滴加温度对化合物2收率的影响Fig.3 The effect of titration temperature on the yield of compound (2)
从图3可以看出,滴加温度在5 ℃,反应温度控制在室温时,4,6-二苯甲酰基间苯二甲酰胺(2)收率比较高。在室温下滴加收率较低,是由于反应放热使浓氨水挥发,故反应滴加温度不宜过高。
第四步Hofmann 降级反应中,滴加次氯酸钠溶液时,需要将温度控制在5~7 ℃。次氯酸钠溶液滴加结束后,需迅速升温。通过改变反应温度,得到4,6-二苯甲酰基-1,3-苯二胺(1)收率与反应温度的关系图,如图4所示。从图4中可以看出,反应温度应控制在80 ℃左右,此时收率较高。
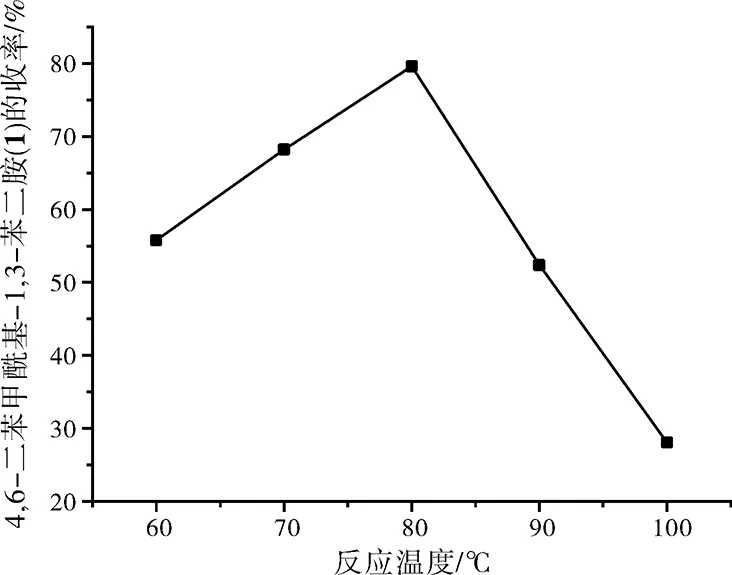
图4 反应温度对4,6-二苯甲酰基-1,3-苯二胺(1)收率的影响Fig.4 The effect of reaction temperature on the yield of 4,6- dibenzoyl-1,3-phenylenediamine(1)
3 结 论
通过傅克酰基化反应、氯代反应、酰胺化反应和Hofmann 降级反应,合成得到4,6-二苯甲酰基-1,3-苯二胺,并用熔点和1H NMR等手段进行了表征,结果表明所得化合物结构与预期结构一致。
第二步氯代反应和第三步酰胺化反应要一起做,否则化合物2的产率较低。
[1]Jullian V, Courtois F, Bolbach G. Carbon carbon bond ligation between β-cyclodextrin and peptide by photo-irradiation[J].Tetrahedron Letters, 2003, 44(34):6437-6440.
[2]Ulbricht M,Riedel M,Marx U.Novel photochemical surface functionalization of polysulfone ultrafiltration membranes for covalent immobilization of biomolecules[J]. Journal of Membrane Science,1996,120(2):239-259.
[3]Nakamura Y,Ukita T.Construction of heterocyclic compounds by use of α-diazophos-phonates:new one-pot syntheses of indoles and isocoumarins[J]. Organic Letters,2002,14(4):2317-2320.
[4]Qin Z Q,Jennings M C,Puddephatt R J.Self-assembly of polymer and sheet structures in palladium(II) complexes containing carboxylic acid substituents [J].Inorganic Chemistry, 2002, 41(20):5174-5186.
[5]Pika J,Konosonoks A,Rachel M R,et al.Photoenolization as a means to release alcohols[J].Journal of Organic Chemistry,2003,68(5):1964-1972.
[6]Martin B S,Valente J E.4-and 5-nitro-2-benzoylbenzoicacid[J].Journal of Chemical Crystallography,1998,28(3):203-207.
[7]Imai Y, Johnson E F, Katto T, et al. Synthesis of aromatic polymers containing anthrazoline and isoanthrazoline units [J]. Journal of Polymer Science Polymer Chemistry Edition, 1975,13(10): 2233-2249.
Study on Synthesis of 4,6-dibenzoyl-1,3-phenylenediamine*
ZHOUYuan-yuan1,WUHong-chen1,WUYa-ming1,CHENYun1,ZHANGQin2,ZHUHong-jun2
(1 Department of Applied Chemistry, Nanjing Polytechnic Institute, Jiangsu Nanjing 210048;2 Nanjing Tech University, Jiangsu Nanjing 211816, China)
The compound of 4,6-dibenzoyl-1,3-phenylenediamine was synthesized from pyromellitic dianhydride. Firstly,4,6-dibenzoylisophthalic acid was synthesized by Friedel-Crafts acylation. Secondly,pseudo-4,6-dibenzoylisophthaloyl chloride was synthesized by chlorination. Thirdly, 4,6-dibenzoylisophthalamide was synthesized by amidation. Lastly, the target compound was synthesized by Hofmann degradation. Target compounds were characterized by melting point and1H NMR.1H NMR for pseudo-4,6-dibenzoylisophthaloyl chloride was obtained.
Friedel-Crafts acylation; chlorination; amidation; Hofmann degradation; aromatic amines
2014年江苏省高等学校大学生实践创新训练计划项目(项目编号201412920003Y);2014年南京科技职业学院院级课题(项目编号NHKY-2014-03)。
周园园(1992-),女,学生,南京科技职业学院工业分析与检验1321。
吴弘辰(1996-),男,学生,南京科技职业学院生物技术与化学制药1522。
朱红军。
O625.63+2
A
1001-9677(2016)08-0051-03
