施硅对水稻白叶枯病抗性及叶片抗氧化酶活性的影响
2016-08-30刘红芳宋阿琳范分良李兆君梁永超
刘红芳, 宋阿琳, 范分良, 李兆君, 梁永超,2*
(1中国农业科学院农业资源与农业区划研究所, 农业部植物营养与肥料重点实验室, 北京 100081;2浙江大学环境与资源学院, 杭州 310058)
施硅对水稻白叶枯病抗性及叶片抗氧化酶活性的影响
刘红芳1, 宋阿琳1, 范分良1, 李兆君1, 梁永超1,2*
(1中国农业科学院农业资源与农业区划研究所, 农业部植物营养与肥料重点实验室, 北京 100081;2浙江大学环境与资源学院, 杭州 310058)
【目的】水稻白叶枯病是一种细菌性枯萎病害,是限制水稻生产的重要生物因素之一。通过田间接种白叶枯病菌,研究施硅对水稻叶片中丙二醛含量及抗氧化系统酶活性的影响及其抗白叶枯病的机理,为安全有效的防治病害提供理论依据。【方法】以唐粳2号水稻品种为材料,2013年在河北省秦皇岛市进行田间试验,试验在两个施氮水平 [N 180 kg/hm2(正常供氮,N180), 450 kg/hm2(高量供氮,N450)]下设3个硅处理[不施硅(-Si),施硅酸钠(Si1, 以SiO2计,70 kg/hm2), 施硅钙肥(Si2, 以SiO2计,70 kg/hm2)],在水稻孕穗期采用剪叶法接种白叶枯病菌,研究硅对接种后30 d水稻病情指数和第1 d、 3 d、 5 d、 7 d和10 d水稻叶片中丙二醛(MDA)含量、 超氧化物歧化酶(SOD)活性、 过氧化氢酶(CAT)活性、 抗坏血酸过氧化物酶(APX)活性的影响。【结果】接种白叶枯病菌后,正常供氮水平,施硅处理的病情指数比不施硅处理平均降低17.8%(P<0.05); 高量供氮水平,施硅钙肥的病情指数比不施硅降低15.1%(P<0.05),而施硅酸钠的病情指数差异不显著。接种白叶枯病菌后,施硅处理的水稻叶片MDA均低于不施硅处理,且在正常供氮水平第7 d和高量供氮水平第3 d、 第7 d差异达显著水平。接种白叶枯病菌后,正常供氮水平第1 d、 第7 d和高量供氮水平第1 d、 第5 d,施硅处理的水稻叶片中SOD活性均显著高于不施硅处理,且第1 d施硅钙肥的叶片SOD显著高于施硅酸钠处理; 接种白叶枯病菌后,施硅处理的水稻叶片中CAT活性均高于不施硅处理,但未达显著水平; 高量供氮水平第1 d、 第7 d和第10 d施硅处理的水稻叶片中APX活性均显著高于不施硅处理。【结论】施硅能提高感病水稻叶片中SOD、 CAT和APX的活性,降低水稻叶片中MDA含量,有效清除植物体内活性氧(ROS),从而增强了水稻抗白叶枯病的能力; 在高量供氮水平下,硅钙肥抵御白叶枯病效果好于硅酸钠。
硅; 氮; 水稻; 白叶枯病; 抗氧化酶活性
水稻白叶枯病是由野油菜黄单胞菌水稻致病变种(Xanthomonascampestrispv.oryzae, Xoo)引起的一种世界性的细菌性枯萎病害。为了控制该病的发生,研究者在化学处理、 改变耕作方式和降低氮肥使用量等方面进行了大量尝试,但这些措施在规模和地域上不同程度地受到了限制。目前,有关水稻白叶枯病的研究大多集中于抗源筛选、 抗性遗传及抗性育种等方面。
硅是地壳中最丰富的元素之一,其含量仅次于氧。1840年,德国化学家李比希提出植物不但能吸收铵和磷酸,还能吸收硅酸等,并将硅列为与氮、 磷、 钾同等重要的植物必需营养元素[1]。1926年,Sommer最早提出硅与水稻的正常生长发育有关,硅是必需营养元素,只是因无法实现纯净的无硅培养而难以证实[2]。硅对植物生长发育的有益作用已是不争的事实,在抵御病害方面,已有学者[3-4]研究提出,硅能促进植物生长和诱导植物抗病性,且能显著提高水稻抵御稻瘟病的能力,只是其抗病机制并不是很清楚。对于硅抵御病害的研究,多集中在以真菌引起的稻瘟病、 纹枯病等方面[5],而对于以细菌引起的白叶枯病的研究甚少。目前,仅有薛高峰等[6]通过水培试验研究并提出硅可以对水稻白叶枯病有防御效果,认为硅可通过参与植株体内代谢,调节抗氧化系统酶活性,增强植株对白叶枯病抗性。在大田条件下,不同氮水平下硅对水稻白叶枯病的抗病效果还未见报道。因此,本研究通过田间接种白叶枯病菌,设置正常和高量2个供氮水平,选用硅酸钠和硅钙肥,研究不同氮水平条件下硅对水稻叶片相关抗氧化系统酶活性影响及其白叶枯病抗性机理的探讨,为有效、 安全防治白叶枯病提供理论依据。
1 材料与方法
1.1供试材料
试验于2013年510月在河北省秦皇岛市抚宁县留守营镇张各前村进行,试验田土壤理化性质为有机质含量21.0g/kg、 碱解氮157.0mg/kg、 有效磷61.0mg/kg、 速效钾112.0mg/kg、 土壤pH7.5、 有效硅130.0mg/kg。试验用水稻品种为唐粳2号。
基肥选用复混肥料(N-P2O5-K2O15-15-15),氮肥选用尿素(N46.0%)。硅肥选用分析纯试剂硅酸钠(Na2SiO3·9H2O)和硅钙肥,其中硅钙肥由领先生物农业股份有限公司提供,有效硅(SiO2)含量21.0%、 氧化钙(CaO)含量25.0%。
NA培养基采用的是肉汁胨培养基[7]。
1.2试验设计
小区面积15m2(4.2m×3.6m),小区之间用双层厚塑料膜围起,将塑料膜插入地下约20cm,地上部用竹竿支起(高出水面1020cm),留1.5m宽的水道(即保护行),在小区保护行两侧的水面以上的塑料膜上均匀地各打4个小孔,作为灌、 排水的通道,保证每个小区单排单灌。
试验采取随机区组排列,设正常和高量供氮2个水平为N180kg/hm2(N180)和N450kg/hm2(N450); 3个硅处理为不施硅(-Si),施硅酸钠(Si1),施硅钙肥(Si2)。每个处理设3次重复,水稻于5月13日移栽,并于水稻孕穗期接种白叶枯病菌。田间精细管理,除不使用防治白叶枯病的药剂外,其他管理与普通大田相同。
基肥为复混肥料(N-P2O5-K2O为15-15-15),用量为600kg/hm2; 硅酸钠和硅钙肥用量为70kg/hm2(以SiO2计),于移栽一周后按1 ∶1分别与干燥土壤掺混,按试验方案将硅酸钠和硅钙肥分别均匀抛洒于水田相应小区中,氮肥分别以基肥(50%)、 分蘖肥(30%)和穗肥(20%)3次施用。
1.3菌液制备与接种
28℃条件下,将菌株在NA斜面培养基上活化培养2d,在液体培养基上于28℃水浴中震荡培养1d。然后收集菌体,用无菌水离心洗涤2次后,配制成109cfu/mL的细菌悬浮液,供接种用。
在水稻孕穗期,用剪刀沾菌液剪去水稻上部健康叶的叶尖12cm(即采用剪叶法)[8],每沾一次菌液剪12片叶,每株剪56片叶。
1.4样品采集与处理
分别于分蘖期、 拔节期和成熟期采集水稻植株,将鲜样叶片装于液氮罐中运输,并于-80℃超低温冰箱中贮存,用于检测蛋白质、 丙二醛和相关酶活性; 将不同时期采集的植株茎秆及收获期的籽粒,用蒸馏水冲洗干净,于鼓风干燥烘箱中80℃杀青30min,然后降温至65℃烘干,用于检测植株养分含量。
1.5病情调查

1.6测定项目
分别于接种后第1、 3、 5、 10 d采集水稻叶片,放在布袋中用液氮冷冻,于-80℃冰箱中保存,用于测定丙二醛、 超氧化物歧化酶、 过氧化氢酶、 抗坏血酸过氧化物酶和蛋白质含量。
1.6.1 丙二醛(MDA)含量的测定参照李云锋等[10]的方法提取粗酶液; 丙二醛(MDA)含量的测定参照赵世杰等的测定方法[11]。
1.6.2 超氧化物歧化酶(SOD)、 过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)活性的测定参照Sato等[12]的方法提取粗酶液; SOD活性的测定参照李合生等[13]的测定方法; CAT活性的测定参照Cakmak等[14]的测定方法; APX活性的测定参照Nakano等[15]的测定方法。
1.6.3 蛋白质含量的测定参照Bradford[16]的测定方法,以牛血清蛋白(BSA)为标准蛋白,采用考马斯亮蓝G-250法测定蛋白含量。
1.7数据分析
试验数据用Microsoft Excel 2007进行数据汇总和计算,用SPSS 18.0软件进行统计分析,采用LSD法进行差异显著性比较,SigmaPlot 11.0作图。
2 结果与分析
2.1硅对水稻白叶枯病情指数的影响
图1显示,接种白叶枯病菌,无论正常供氮水平(N180),还是高量供氮水平(N450),施硅对水稻白叶枯病的抗性表现出明显差异。施氮与施硅对水稻白叶枯病病情指数不存在交互作用。正常供氮水平,施硅处理比不施硅处理的白叶枯病病情指数平均降低了17.8%,且均达显著水平; 高量供氮水平,施硅酸钠的病情指数比不施硅降低了7.4%,差异不显著,施硅钙肥的病情指数比不施硅降低了15.1%,差异显著。结果说明,施硅能显著提高水稻对白叶枯病的抵抗能力,高量供氮水平,硅钙肥效果好于硅酸钠。
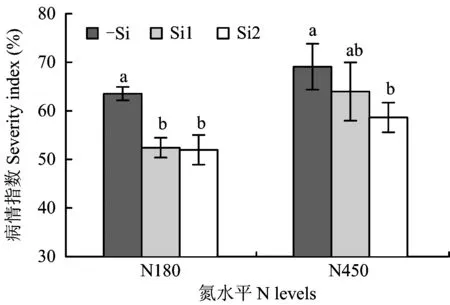
图1 正常和高量供氮水平下硅对水稻白叶枯病病情指数的影响Fig.1 Effects of Si on bacterial blight development in leaves of rice under normal and nigh levels of nitrogen supply[注(Note): 方差分析Variance analysis: N** (F=17.06), Si**(F=11.78), N×Si(F=0.92).]
2.2硅对感病水稻叶片MDA含量的影响
由图2可以看出,无论施硅与否,水稻接种白叶枯病菌后,第1 d叶片丙二醛(MDA)含量快速升高,第3 d后又急剧下降,第5 d施硅处理维持平稳,而不施硅处理快速升高,第7d后施硅处理快速升高,不施硅处理缓慢升高。而在整个变化过程中,施硅处理的MDA含量均低于不施硅处理,正常供氮水平第7 d施硅与不施硅处理差异达到显著水平; 高量供氮水平第3 d和第7 d施硅与不施硅处理均达显著水平。结果说明,接种白叶枯病菌后,水稻叶片中丙二醛(MDA)含量急剧上升是一种应激响应,施硅可以降低叶片中MDA的含量。
2.3硅对感病水稻叶片SOD活性的影响
超氧化物歧化酶(SOD)通过歧化反应清除超氧阴离子自由基,形成过氧化氢和分子氧。图3表明,无论正常供氮水平,还是高量供氮水平,水稻接种白叶枯病菌后,施硅处理的SOD活性均高于不施硅处理,正常供氮水平第1 d和第7 d达显著水平,高量供氮水平第1 d和第5 d达显著水平,而且第1 d时施硅钙肥的叶片SOD活性显著高于施硅酸钠处理。结果表明,水稻接种白叶枯病菌后,超氧化物歧化酶(SOD)活性急剧下降,是一种植物本能的应激反应,与不施硅比较,施硅能提高叶片超氧化物歧化酶(SOD)活性,硅是通过提高SOD 的活性,积累H2O2来提高植物的抗病性。
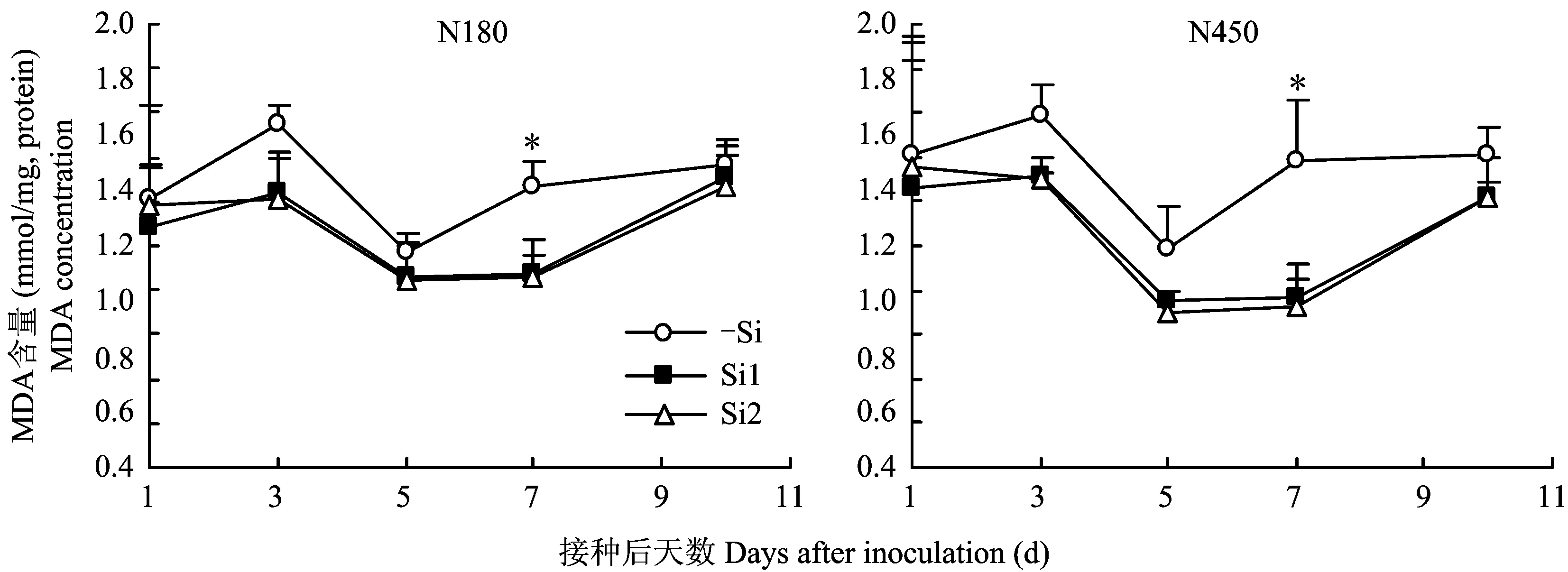
图2 正常和高量供氮水平下硅对接种后水稻叶片丙二醛含量的影响Fig.2 Effects of Si on MDA concentration in leaves of Xoo-infected rice under normal and nigh levels of nitrogen supply
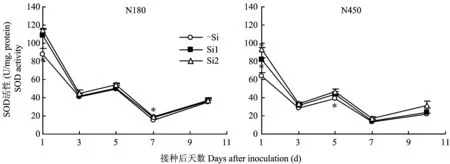
图3 正常和高量供氮水平下硅对接种后水稻叶片超氧化物歧化酶活性的影响Fig.3 Effects of Si on SOD activity in leaves of Xoo-infected rice under normal and high levels of nitrogen supply[注(Note): *表示同一时间,施硅与否在P<0.05水平下差异显著 Denotes significant difference at P<0.05 between the + Si (Si1 or Si2) and -Si treatments at the same time point.]
2.4硅对感病水稻叶片CAT活性的影响
如图4所示,无论施硅与否,接种水稻白叶枯病菌后,叶片中过氧化氢酶(CAT)活性均是先急剧下降,第3 d后保持平缓下降,第5 d后仍然保持平缓直至第10 d仍变化不大。在生长过程中,施硅处理的CAT活性均高于不施硅处理,但未达显著水平。水稻接种白叶枯病菌,施硅提高了水稻叶片中过氧化氢酶(CAT)的活性,这有助于清除植株体内的过氧化氢(H2O2),从而提高水稻对白叶枯病菌的抗性。
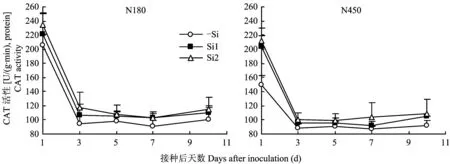
图4 正常和高量供氮水平下硅对接种后水稻叶片过氧化氢酶活性的影响Fig.4 Effects of Si on CAT activity in leaves of Xoo-infected rice under normal and high levels of nitrogen supply[注(Note): *表示同一时间,施硅与否在P<0.05水平下差异显著 Denotes significant difference at P<0.05 between the + Si (Si1 or Si2) and -Si treatments at the same time point.]
2.5硅对感病水稻叶片APX活性的影响
图5表明,无论施硅与否,水稻叶片中抗坏血酸氧化物酶(APX)活性的变化趋势均是先急剧下降,第3 d后缓慢下降,一直持续到第10 d降到最低点。在生长过程中,施硅处理的APX活性均高于不施硅处理,高量供氮水平,第1、 7和10 d均达显著水平。结果表明,在高量供氮水平下,硅可显著提高水稻叶片APX的活性,有利于清除H2O2,从而提高水稻对白叶枯病菌的抗性。

图5 正常和高量供氮水平下硅对接种后水稻叶片抗坏血酸氧化物酶活性的影响Fig.5 Effects of Si on APX activity in leaves of Xoo-infected rice under normal and high levels of nitrogen supply[注(Note): *表示同一时间,施硅与否在P<0.05水平下差异显著Denotes significant difference at P<0.05 between the + Si (Si1 or Si2) and -Si treatments at the same time point.]
3 讨论
有关硅增强水稻对病害的抵御作用机制有物理屏障作用和诱导抗病作用两种,其中一种是硅在细胞壁积累起到了物理屏障的作用,另一种是硅通过激活寄主防卫基因,提高由病原菌诱导的系统抗病的作用[17-21]。在植物与病原菌互作过程中,过氧化氢产生和积累与植物抗病反应密切相关,过氧化氢具有直接抑制和毒害病原菌, 促进寄主细胞壁的木质化和细胞壁结构蛋白的交联, 引发寄主膜脂过氧化作用和诱导植保素的合成等作用[6]。
丙二醛(MDA)是膜质过氧化产物,逆境胁迫时,植物体内MDA含量升高,因此,可将MDA含量作为植物抗逆性的生理指标[22-24]。薛高峰等[30]水培试验研究结果表明,接种白叶枯病菌后,施硅能显著提高MDA在植物体内积累量,诱导膜脂过氧化作用。本研究通过田间接种白叶枯病菌试验研究结果表明,接种白叶枯病菌,3天内无论加硅与否,MDA均快速升高,3天后急剧下降,第5天后又开始升高,施硅处理的MDA均低于不施硅处理。本试验施硅与不施硅对水稻叶片中MDA含量的影响与薛高峰等[30]研究的72 h后的结果基本一致,说明接种白叶枯病菌后,水稻叶片中丙二醛(MDA)先急剧上升是一种应激响应,上升的时间因水稻品种及试验条件等不同而有所不同,施硅可以降低叶片中MDA的含量,说明施硅通过降低叶片脂质过氧化作用(MDA含量),来降低白叶枯病对水稻的伤害,以此增强水稻抗白叶枯病能力。
活性氧(ROS)是植物体内一种重要的信号分子,但是它也会对植物造成毒害。而植物自身形成了响应和防御氧化胁迫的回避和清除机制[25],清除机制包括酶促和非酶类两大清除系统,其中酶促清除系统主要包括抗坏血酸过氧化物酶(APX)、 超氧化物歧化酶(SOD)、 过氧化氢酶(CAT)、 谷胱甘肽还原酶(GR)和过氧化物酶(POD)等[26]。豇豆接种锈菌后,施硅可显著提高叶片POD、 SOD和CAT活性,降低MDA含量[27]。水稻接种纹枯病菌后,施硅的MDA含量总体上低于不施硅处理,其SOD活性高于不施硅处理,接种后第4天,施硅的SOD活性较低,而对CAT活性无显著影响[28]。薛高峰等[29]研究结果表明,在水培试验条件下,水稻接种白叶枯病菌后,施硅能显著提高其SOD活性,降低CAT、 POD和APX的活性,72 h后施硅水稻叶片的CAT活性高于不施硅,且96 h达显著水平。本研究中大田试验的结果表明,接种白叶枯病菌后施硅处理显著提高了水稻体内SOD、 CAT和APX的活性,施硅对SOD活性的影响与薛高峰等[29]的研究结果一致,对于CAT活性的影响与其72 h后的结果基本一致,而对于POD和APX活性的影响恰好相反,可能与水稻品种、 接种时期和试验条件等有关。
本试验采用剪刀沾菌液剪去水稻上部健康叶的叶尖1 2 cm进行接种(即剪叶法),细菌通过伤口经过木质部浸入植株体内,这一接种方法完全不同于将高浓度病菌喷洒于叶面的接种方法(通常用于真菌病害的研究)。在本研究中,基本上可以排除由于硅以SiO2·nH2O形态在叶片表皮细胞壁上淀积从而阻止病菌从叶片表面侵入细胞体内的可能性。因此,硅的物理或机械屏障作用的这一抗病机制在本研究中不是主要原因,硅提高水稻对白叶枯病抗性的机制主要是诱导防卫机制[29-30]。本研究结果表明,水稻接种白叶枯病菌后,SOD活性急剧下降,是一种植物本能的应激反应; 与不施硅比较,施硅能提高叶片SOD活性,硅通过提高SOD的活性,清除活性氧,以提高植物的抗病性。水稻接种白叶枯病菌后,施硅在一定程度上提高了CAT活性,有利于清除H2O2,提高了抵御白叶枯病菌的能力。接种白叶枯病菌后高量供氮水平硅可显著提高APX的活性,有助于清除植株体内的过氧化氢(H2O2),从而提高水稻对白叶枯病菌的诱导抗性。因此,本研究在田间试验条件下进一步验证了薛高峰等[29]在水培条件下硅对水稻抗白叶枯病的研究结论,即硅是通过参与寄主与防卫反应有关的代谢过程的生理抗病作用,是植物抗氧化系统及其它代谢过程共同作用的结果,而不仅仅是简单的物理屏障作用。
另外,试验结果还显示,接种白叶枯病菌后,在高量供氮水平施硅钙肥的病情指数显著低于硅酸钠的处理,可能硅钙肥中的钙元素也在起作用,具体原因及机理还有待进一步研究。
4 结论
1)田间试验接种白叶枯病菌的试验表明,施硅能显著减轻水稻的白叶枯病,增强了水稻抗白叶枯病的能力。
2)施硅还能提高感病水稻叶片中超氧化物歧化酶(SOD)、 过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)的活性,降低水稻叶片中丙二醛(MDA)的含量,从而有效清除植物体内活性氧(ROS),增强植株抗白叶枯病能力。
3)施硅水稻的病情指数比不施硅的显著降低,且高量供氮水平下硅钙肥效果好于硅酸钠。
[1]王继朋.硅在几种植物中的吸收、 分配及其作用探讨[D]. 北京: 中国农业大学博士学位论文, 2003.
Wang J P. Silicon uptake, distribution and its subsequent function in several plants[D]. Beijing: PhD Dissertation of China Agricultural University, 2003.
[2]孙万春.硅提高水稻对稻瘟病抗性的生理与分子机理[D].北京: 中国农业科学院博士学位论文, 2008.
Sun W C. The physiological and molecular mechanisms of silicon-enhanced resistance to rice blast [D]. Beijing: PhD Dissertation of Chinese Academy of Agricultural Science, 2008.
[3]Rodrigues F A, Vale F X R, Komdorfer G H,etal. Influence of silicon on sheath blight of rice in Brazil[J].Crop Protection, 2003, 22: 23-29.
[4]Sun W C, Zhang J, Fan Q H,etal. Silicon enhanced resistance to rice blast is attributed to silicon-mediated defence resistance and its role as physical barrier[J]. European Journal of Plant Pathology, 2010, 128: 39-49.
[5]Seebold K W, Datnoff L E, Correa Victoria F J,etal. Effects of silicon and fungicides on the control of leaf and neck blast in upland rice[J].Plant Disease, 2004, 88: 253-258.
[6]薛高峰.硅提高水稻对白叶枯病抗性的生理与分子机理[D]. 北京: 中国农业科学院博士学位论文, 2009.
Xue G F. The physiological and molecular mechanisms of silicon-enhanced resistance to bacterial blight in rice [D]. Beijing: PhD Dissertation of Chinese Academy of Agricultural Science, 2009.
[7]李欣, 李红玉, 庞新跃,等. 互作对水稻白叶枯病菌JXOⅢ和JXOⅤ超氧阴离子释放的调控[J]. 生态学报, 2006, 26(12): 4192-4197.
Li X, Li H Y, Pang X Y,etal. Regulation on superoxide anion production inXanthomonasoryzaepv.oryzae, JXOIII and JXO V by host-pathogen interaction[J]. Acta Ecologica Sinica, 2006, 26(12): 4192-4197.
[8]Kauffman H E, Reddy A P K, Hsieh S P Y, Merca S D. An improved technique for evaluating resistance of rice varieties toXanthomonasoryzae[J]. Plant Disease Reporter, 1973, 57: 537-541.
[9]方中达, 许志刚, 过崇俭, 等. 中国水稻白叶枯病菌致病型的研究[J]. 植物病理学报, 1990, 20(2): 81-88.
Fang Z D, Xu Z G, Guo C J,etal. Study on pathotypes ofXarrthomonascampestrispv.oryzaein China[J]. Acta Phytopathologica Sinica, 1990, 20(2): 81-88.
[10]李云锋,王振中.稻瘟菌GP66激发子诱导的水稻膜脂过氧化及其保护酶活性变化[J]. 植物病理学报,2005,35(1): 43-48.
Li Y F, Wang Z Z. Membrane lipid peroxidation and protective enzymes activity induced in rice leaves by GP66 elicitor fromMagnaporthegriseac[J]. Acta Phytopathologica Sinica, 2005, 35(1): 43-48.
[11]赵世杰,李德全.现代植物生理学实验指南[M].北京: 科学出版社,1999. 305-306.
Zhao S J, Li D Q. Experimental manual of modern plant physiology[M]. Beijing. Science Press, 1999. 305-306.
[12]Sato Y, Murakami T, Funatsuki H,etal. Heat shock-mediated APX gene expression and protection against chilling injury in rice seedlings[J]. Journal of Experimental Botany, 2001, 52 (354): 145-151.
[13]李合生,孙群,赵世杰,等. 植物生理生化实验原理与技术[M].北京: 高等教育出版社, 2000.167-169.
Li H S, Sun Q, Zhao S J,etal. Pinciples and techniques of plant physiological biochemical experiment[M]. Beijing: Higher Education Press, 2000: 167-169.
[14]Cakmak I, Marschner H. Magnesium deficiency and high light intensity enhance activities of superoxide dismutase, ascorbate peroxidase, and glutathione reductase in bean leaves[J]. Plant Physiology, 1992, 98: 1222-1227.
[15]Nakano Y, Asada K. Hydrogen peroxide is scavenged by ascorbate-specific peroxidase in spinach chloroplasts[J]. Plant & Cell Physiology, 1981, 22 (5): 867-880.
[16]Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J]. Analytical Biochemistry, 1976, 72: 248-254.
[17]Cherif M, Bélanger R R. Use of potassium silicate amendments in recirculating nutrient solutions to suppressPythiumultimumon long English cucumber[J]. Plant Disease, 1992, 76 (10): 1008-1011.
[18]Cherif M, Asselin A, Belanger R R. Defense responses induced by soluble silicon in cucumber roots infected byPythiumspp[J]. Phytopathology, 1994, 84 (3): 236-242.
[19]Datnoff L E, Deren C W, Snyder G H. Silicon fertilization for disease management of rice in Florida[J]. Crop Protection, 1997, 16 (6): 525-531.
[20]Rodrigues F A, McNally D J, Datnoff L E,etal. Silicon enhances the accumulation of diterpenoid phytoalexins in rice: a potential mechanism for blast resistance[J]. Phytopathology, 2004, 94: 177-183
[21]Ning D F, Song A L, Fan F L,etal., Effects of slag-based silicon fertilizer on rice growth and brown-spot resistance[J]. Plos One, 2014, 9(7): e102681-e102681.
[22]Choudhary M, Jetley U K, Abash Khan M,etal. Effect of heavy metal stress on proline, malondialdehyde and superoxide dismutase activity in the cyanobacterium Spirulina platensis-S5[J]. Ecotoxicology & Environmental Safety, 2007, 66(2): 204-209.
[23]豆长明.超积累植物美洲商陆锰累积与耐性机制研究[D]. 杭州: 浙江大学博士学位论文, 2009.
Dou C M. Mechanisms of accumulation and tolerance of manganese inPhytolaccaamericanaLinn [D]. Hangzhou: PhD Dissertation, Zhejiang University, 2009.
[24]Li G, Wan S, Zhou J,etal. Leaf chlorophyll fluorescence, hyperspectral reflectance, pigments content, malondialdehyde and proline accumulation responses of castor bean (RicinuscommunisL.) seedlings to salt stress levels[J]. Industrial Crops & Products, 2010, 31(1): 13-19
[25]Mittler R. Oxidative stress, antioxidants and stress tolerance[J]. Trends in Plant Science, 2002, 7(9): 405-410.
[26]岳晓翔,陈敏,段迪,等. 绿色和紫红色表型盐地碱蓬叶片抗氧化系统比较研究[J]. 山东师范大学学报(自然科学版), 2008, 23(1): 121- 124.
Yue X X, Chen M, Duan D,etal. Comparative study on antioxidant system of green and red-violet phenotypeSuaedasalsaleaves[J]. Journal of Shandong Normal University (Natural Science), 2008, 23(1): 121-124.
[27]李国景,刘永华,朱祝军,等. 外源硅对长豇豆锈病抗性的影响及其生理机制[J]. 浙江大学学报(农业与生命科学版), 2007, 33(3): 302-310.
Li G J, Liu Y H, Zhu Z Jetal. Effect of exogenous silicon on resistance of asparagus bean rust and its physiological mechanism[J]. Journal of Zhejiang University (Agric.& Life Sci.), 2007, 33(3): 302-310.
[28]张国良,戴其根,张洪程.施硅增强水稻对纹枯病的抗性[J]. 植物生理与分子生物学学报, 2006, 32(5): 600-606.
Zhang G L, Dai Q G, Zhang H C. Silicon application enhances resistance to sheath blight(Rhizoctoniasolani) in rice[J]. Journal of Plant Physiology and Molecular Biology, 2006, 32(5): 600-606.
[29]薛高峰, 宋阿琳, 孙万春, 等. 硅对水稻叶片抗氧化酶活性的影响及其与白叶枯病抗性的关系[J]. 植物营养与肥料学报, 2010, 16(3): 591-597.
Xu G F, Song A L, Sun W C,etal. Influences of silicon on activities of antioxidant enzymes in rice leaves infected byXoostrain in relation to bacterial blight resistance[J]. Plant Nutrition and Fertilizer Science, 2010, 16(3): 591-597.
[30]薛高峰,孙万春,宋阿琳,等. 硅对水稻生长、 白叶枯病抗性及病程相关蛋白活性的影响[J]. 中国农业科学, 2010, 43(4): 690-697.
Xue G F, Sun W C, Song A L,etal. Influence of silicon on rice growth, resistance to bacterial blight and activity of pathogenesis-related proteins[J]. Scientia Agricultura Sinica, 2010, 43(4): 690-697.
Effects of silicon application on resistance against bacterial blight and antioxidant defense activities of rice leaves
LIU Hong-fang1, SONG A-lin1, FAN Fen-liang1, LI Zhao-jun1, LIANG Yong-chao1,2*
(1InstituteofAgriculturalResourcesandRegionalPlanning,ChineseAcademyofAgriculturalSciences,Beijing100081,China;2CollegeofEnvironmental&ResourceSciences,ZhejiangUniversity,Hangzhou310058,China)
【Objectives】 Bacterial blight of rice is a bacterial wilt disease in the world, which is one of the important biological factors limiting rice yield. By inoculatingXoointo leaves of field-grown rice, we investigated the effect of silicon on concentration of malondialdehyde and activities of antioxidant defense enzymes in rice leaves and the underlying mechanism ofXooresistance to provide theoretical basis for safe and effective prevention and control measures for the disease. 【Methods】 A field experiment was conducted in Qinhuangdao, Hebei province in 2013. Rice was grown with no Si (-Si), sodium silicate at 70 kg/hm2(Si1, SiO2) and calcium silicon fertilizer at 70 kg/hm2(Si2, SiO2) at two nitrogen levels, i.e. 180 kg/hm2(N180, normal N) and 450 kg/hm2(N450, high N). The rice variety used was a japonica (Oryzasativacv. Tang No.2). Five to six of the uppermost fully expanded leaves of each rice plant at the booting stage were inoculated by using leaf clipping method, in which the leaf blade was cut with a pair of scissors pre-dipped in the bacterial suspension. The effect of silicon on rice disease index was examined 30 days after inoculation, and the effect of silicon on the concentration of malondialdehyde and the activities of superoxide dismutase (SOD), catalase (CAT) and ascorbic acid peroxidase (APX) in rice leaves was analyzed at 1, 3, 5, 7 and 10 days after inoculation. 【Results】 After inoculation with leaf blight pathogen, under the normal N level, on the average disease index of Si-treated plants was 17.8% lower than that of Si-untreated plants (P<0.05), while under the high N level, the disease index of calcium silicate-treated plants was 15.1% lower than that of Si-untreated plants (P<0.05), and the index of sodium silicate-treated plants was statistically insignificant. The concentration of malondialdehyde (MDA) in silicon-treated plants was lower than that in silicon-untreated plants 7 days after inoculation under the normal nitrogen level (P>0.05), and so was it at 3 and 7 days after inoculation under the high nitrogen level. The activity of super oxide dismutase (SOD) in silicon-treated plants was significantly higher than that in silicon-untreated plants 7 days after inoculation under the normal N level, and so was it 1 and 5 days after inoculation under the high N level. The SOD activity was significantly higher in calcium silicate-treated plants than in sodium silicate-treated plants 1 day after inoculation. The activity of catalase (CAT) in the Si-treated plants was higher than that in the Si-untreated plants, though the difference was not statistically significant. The activity of ascobic peroxidase (APX) in the Si-treated plants was significantly higher than that in the Si-untreated plants 1, 7, and 10 days after inoculation under the high N level.【Conclusions】 Addition of silicon fertilizer can enhance the activities of SOD, CAT and APX and reduce the concentration of MDA of rice leaves in the field condition, thus effectively eliminating reactive oxygen species and improving resistance against bacterial blight. Under the high N level, calcium silicate is more effective in increasing resistance against bacterial blight than sodium silicate.
silicon; nitrogen; rice; bacterial blight of rice; activities of antioxidant defense enzymes
2015-12-28接受日期: 2016-02-04
国家“十二·五”科技支撑计划“钢渣农业资源化利用技术研究与示范”(2013BAB03B02)资助。
刘红芳(1973—),女,北京平谷人,副研究员,博士研究生,主要从事植物逆境生理与分子生物学研究。 E-mail: liuhongfang@caas.cn
E-mail: ycliang@zju.edu.cn
Q945.78; S432.2+4
A
1008-505X(2016)03-0768-08
