胱硫醚-β-合成酶在脑缺血-再灌注大鼠模型中表达变化的研究
2016-08-29周晓璐王国川谭安超刘杰麟
周晓璐 王国川 谭安超 刘杰麟 张 华
(贵州医科大学附属人民医院输血科,贵阳550002)
胱硫醚-β-合成酶在脑缺血-再灌注大鼠模型中表达变化的研究
周晓璐王国川①谭安超刘杰麟②张华①
(贵州医科大学附属人民医院输血科,贵阳550002)
①贵州医科大学附属人民医院检验科,贵阳550002。
②贵州医科大学基础医学院免疫教研室,贵阳550004。
目的:观察缺血-再灌注(Ischemia-reperfusion,IR)大鼠模型脑组织中胱硫醚-β-合酶(Cystathionine β-synthase,CBS)表达的变化及意义。方法:采用改良线栓法制备大鼠大脑中动脉栓塞(Middle cerebral artery occlusion,MCAO)模型。分别应用RT-PCR及Western blot法检测SHAM组大鼠、I组大鼠以及IR组3 h、6 h、12 h和24 h大鼠脑内CBS mRNA和CBS蛋白的表达变化;采用ELISA法检测大鼠血中同型半胱氨酸含量变化;采用CBS抑制剂羟胺抑制CBS活性后,Western blot法检测氧化应激相关蛋白HO-1的表达,并用光镜观察脑组织的病理学变化。结果:IR大鼠脑组织CBS mRNA和蛋白表达水平显著高于假手术组(P<0.01),于再灌注12 h表达至峰值。和假手术组相比,血中同型半胱氨酸含量在再灌注12 h时水平最低(5.73±1.17 vs 2.88±0.93,F=25.56,P=0.001)。应用HA抑制CBS活性后,CBS及氧化应激相关蛋白HO-1表达显著减少,光镜下神经元损伤进一步加重。结论:缺血-再灌注后,脑组织中CBS表达上调可能对神经元产生保护效应。
脑卒中;缺血-再灌注;同型半胱氨酸;胱硫醚-β-合成酶;氧化应激
脑血管疾病尤其是脑卒中,是导致人类死亡的第三常见疾病,也是成人致残的主要原因。其发病逐渐年轻化且发病率渐高,已成为家庭和社会的负担。因此,对引发卒中的危险因素进行识别和干预,进而降低发病率和死亡率就显得尤为重要[1]。近年来多项研究证实,高同型半胱氨酸(Homocysteine,HCY)血症可作为脑卒中的独立危险因素[2,3]。HCY是蛋氨酸脱甲基形成的含硫氢基的氨基酸;体内的HCY可被胱硫醚-β-合酶(Cystathionine β-synthase,CBS)催化后缩合为胱硫醚[4]。若CBS的含量或活性发生变化,会引起同型半胱氨酸血浆浓度异常。本研究动态观察了脑缺血-再灌注(Ischemia-reperfusion,IR)大鼠模型脑组织中CBS的变化,为探索其在IR脑损伤中的作用提供依据。
1 材料与方法
1.1材料
1.1.1仪器与试剂RIPA裂解液购自北京百泰克生物技术有限公司,Trizol RNA 提取试剂以及CBS和β-actin引物购自美国Invitrogen公司,逆转录试剂盒购自日本TOYOBO公司,实时荧光定量PCR试剂盒购自美国KAPA公司,HCY ELISA试剂盒、CBS抗体和HO-1抗体购自美国Abcam公司,β-actin-HRP和HRP二抗购自美国Santa Cruz公司,羟胺(Hydroxyla mine,HA)购自美国Sigma公司。微孔板检测仪(SpectraMax M2)购自加拿大Molecular Devices公司。
1.1.2实验动物分组健康SD大鼠30只,体重250~280 g,鼠龄3~4个月,雌雄不拘,购自上海西普尔-必凯实验动物有限公司。每个分组5只,随机分成:(1)SHAM组:即假手术对照组,对大鼠进行10%水合氯醛(0.35 ml/100 g)腹腔注射麻醉后仅暴露颈总动脉不进行血管夹闭;(2)I组:即单纯缺血组,对大鼠行麻醉手术后夹闭血管使缺血2 h;(3)IR组:即缺血再灌注组,夹闭血管使大鼠缺血2 h后松开血管夹使恢复血流,根据再灌注时间又分为再灌注3、6、12和24 h组;(4)HA组,缺血2 h再灌注6 h后,按照12.5 mg/kg的剂量腹腔注射CBS抑制剂HA[5],再灌注至12 h。实验结束时处死大鼠,眼眶取血及开颅取脑后进行相关指标的检测。
1.2方法
1.2.1动物模型制备参照Belayev等[6]改良的Longa方法,选用颈外动脉插入线栓法制备大鼠大脑中动脉栓塞(Middle cerebral artery occlusion,MCAO)模型。术中严密观察,保持大鼠肛温在36.5~37.5℃。
1.2.2神经功能评价经麻醉的大鼠清醒后,其神经功能评定参考Longa 5分制评分标准[7]。0分:无神经损伤症状;1分:不能完全伸展对侧前爪;2分:向右侧转圈;3分:向右侧倾倒;4分:不能自发行走,意识丧失。
1.2.3脑组织中总mRNA的提取和CBS cDNA的RT-PCR不同时间点取的脑组织暂时放于-196℃液氮罐保存,样本收齐后,脑组织总mRNA提取操作按照Trizol试剂说明书进行。按照逆转录试剂盒说明书操作,将提取的mRNA逆转录为cDNA。β-actin引物序列为F:5′-ATGGATGACGATAT-CGCTGCG-3′和R:5′-TCGTCCCAGTTGGTGACA-ATG-3′;CBS引物序列为F:5′-GAACCAGACGGAGCAAACAG-3′和R:5′-TGTAGAGGACTTTGCAGACT-3′。用1%琼脂糖凝胶对RT-PCR产物进行电泳分离后凝胶成像照相。用Bandscan5.0凝胶图像处理软件进行灰度分析,CBS mRNA相对表达量=CBS扩增产物条带灰度值/β-actin扩增产物条带灰度值。
1.2.4蛋白提取和Western blot检测用RIPA裂解液裂解组织收取蛋白上清液。定量30 μg总蛋白,并用10% 聚丙烯酰胺凝胶电泳分离,湿转法将目的蛋白转印至聚偏二氟乙烯膜。用含有5%脱脂牛奶的TBST室温封闭2 h后孵育一抗,4℃摇床轻摇过夜;用TBST洗膜3次后,室温孵育辣根过氧化物酶(Horseradish peroxidase,HRP)标记二抗1 h。ECL化学发光后,测定反应条带灰度值,以β-actin作为内参,计算各种蛋白的相对表达量。
1.2.5ELISA验证血清HCY的表达按照ELISA试剂盒说明书进行操作,检测各组大鼠血中HCY的含量。1.2.6脑组织学检查大鼠脑组织用10 %中性甲醛固定后进行石蜡包埋,制成5 μm厚切片行HE染色,光镜下观察脑组织病理变化。

2 结果
2.1大鼠神经功能评定结果IR组大鼠麻醉清醒后均出现明显的眼球下陷,肢体无力等症状,神经功能评分为平均为(3.40±0.55)分,且肢体瘫痪症状以缺血2 h再灌注24 h最明显;I组2只不能伸展前肢,2只出现向左侧划圈,1只出现向左倾倒,神经功能评分为(1.80±0.84)分;HA组出现1只不能伸展前肢,1只出现向左侧划圈,3只出现向左倾倒,神经功能评分为(2.40±0.89)分;而假手术组动物则无明显的神经功能障碍。
2.2脑组织中CBS mRNA表达的变化CBS mRNA在SHAM组和I组大鼠脑组织中表达无差异(P>0.05)。与SHAM组相比,脑组织中的CBS mRNA在缺血-再灌注3 h后开始上调(P<0.01),12 h表达至峰值(P<0.01),见图1。
2.3脑组织中CBS蛋白表达的变化Western blot实验结果显示,CBS蛋白在SHAM组和I组大鼠脑组织中表达无差异(P>0.05)。与SHAM组相比,脑组织中的CBS蛋白在缺血-再灌注6 h后开始上调(P<0.01),12 h表达至峰值(P<0.01),见图2。应用HA抑制CBS,至再灌注12 h时,CBS的表达量相
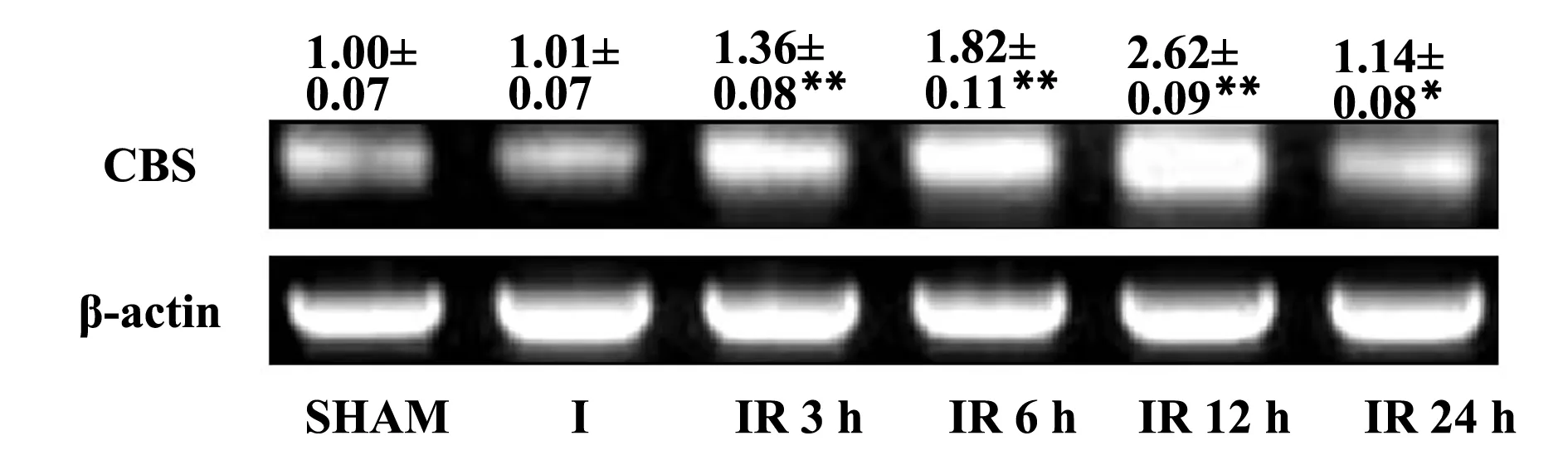
图1 缺血-再灌注各时间点大鼠脑组织中CBS mRNA的表达Fig.1 Expression of CBS mRNA in rat brain during cerebral ischemia-reperfusionNote: Compare with SHAM group,*.P<0.05,**.P<0.01.

图2 缺血-再灌注各时间点大鼠脑组织中CBS 蛋白的表达Fig.2 Expression of CBS protein in rat brain during cerebral ischemia-reperfusionNote: Compare with SHAM group,*.P<0.05,**.P<0.01.
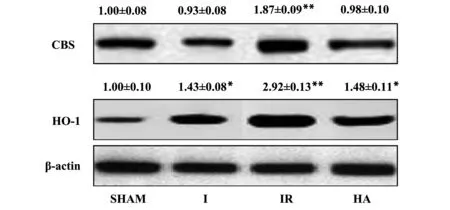
图3 各组大鼠脑组织中CBS和HO-1的表达Fig.3 Expression of CBS and HO-1 in rat brain between different groupsNote: Compare with SHAM group,*.P<0.05,**.P<0.01.

图4 各组大鼠大脑皮质的组织形态学改变(HE染色,×400)Fig.4 Morphological changes of cerebral cortex in different groups(HE staining,×400)

表1 各组大鼠缺血-再灌注时血中HCY含量的变化Tab.1 Concentration of plasma HCY in rat during cerebral ischemia-reperfusion
较于IR组显著下调,同时观察到HO-1发生协同性变化,差异有统计学意义,见图3。
2.4血HCY含量的变化SHAM组和I组大鼠血中HCY含量没有统计学差异。与SHAM组相比,缺血-再灌注12 h后血中HCY显著下调(5.73±1.17 vs 2.88±0.93,F=25.56,P=0.001);应用HA抑制CBS活性,血中HCY含量则无明显改变(P>0.05),见表1。
2.5脑组织形态学的变化光镜下可见SHAM组脑组织结构清晰,未发现病理性改变。I组脑组织病理损伤轻,少量神经元胞核、胞体增大,着色变浅。与SHAM组相比,IR组大脑皮质部分神经病理损伤进一步加重,细胞周围出现水肿裂隙。应用HA抑制CBS活性,光镜下可见HA组较IR组病变减轻,固缩的神经元数目减少,见图4。
3 讨论
根据世界各国死亡报告统计表明,全球每年死于脑卒中者约59.8%为缺血性脑卒中[8]。持续脑缺血可引起神经细胞不可逆的损伤从而导致脑功能的降低或损坏,而短暂性脑缺血后,机体会做出防御反应,主动产生神经保护作用相关因子或大分子蛋白,这种内在对抗机制使机体能耐受一定程度的缺血损伤[9]。本研究运用大鼠大脑中动脉栓塞(MCAO)模型,观察脑缺血-再灌注脑组织中CBS含量的动态变化。研究发现,缺血-再灌注后CBS水平呈时间依赖性增加,在12 h时可达高峰,相反血中HCY水平则降至最低,表明缺血-再灌注发生时,体内CBS和HCY可能参与了疾病过程;对IR大鼠使用CBS抑制剂HA后,CBS表达量减少,HCY水平较未使用HA大鼠有显著升高,且HO-1的表达则减少,提示CBS在脑卒中的发生发展中发挥了举足轻重的作用,细胞氧化应激亦可能参与其中。
IR发生后,脑组织内诱导产生大量的诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)及其产物NO,同时血液中超氧阴离子等各种自由基含量也急剧上升,NO与超氧阴离子快速结合生成氧化性更强的过氧亚硝基阴离子(ONOO-),使脑内的自由基反应进一步增强,损伤加重[10]。组织细胞可产生多种抗氧化酶抵御氧化性损伤,其中血红素氧合酶(Hemeoxygenase,HO)亚型HO-1是细胞对抗应激反应和抗氧化损伤的重要组成部分。Robert等[11]研究指出,由CBS缺乏引起的高半胱氨酸血症和肝脏细胞的氧化应激相关。Han等[12]则进一步证实,在热惊厥小鼠模型中使用CBS抑制剂HA后,HO-1的表达下调,细胞抗氧化损伤能力减弱。此外,王瑜玲等[13]应用大鼠肢体缺血-再灌注模型观察大脑皮层和海马区CBS表达量的变化,发现12 h时CBS的表达量最高,其调控的具有神经元保护作用的硫化氢(H2S)水平相应增高;当抑制CBS的表达时,光镜下可见神经元的病变进一步加重,证实CBS对神经元有一定的保护效应。CBS作为同型半胱氨酸代谢的限速酶,其含量和活性的变化直接决定了血液中HCY的水平。Baumbach等[14]通过检测CBS基因缺陷鼠中HCY的含量,发现相比于野生型CBS+/+鼠,CBS+/-鼠中HCY的水平升高了近60%,同时观察到小鼠大脑血管壁显著增厚,提示CBS及其调控的HCY在血管疾病的发病中发挥了重要作用。
1969年McCully[15]首次提出高同型半胱氨酸与心脑血管疾病存在关联,此后,大量研究表明高同型半胱氨酸血症是脑卒中的独立危险因素。HCY是一种含巯基的氨基酸,是甲硫氨酸代谢的中间产物,在正常情况下HCY维持在较低水平(5~15 mmol/L),其生成和代谢保持动态平衡[16]。HCY每升高50 μmol/L,脑血管病的风险将增加50%。CBS参与同型半胱氨酸的代谢,在CBS的催化下,丝氨酸与同型半胱氨酸结合使之清除。CBS水平明显降低可引起高同型半胱氨酸血症,后者进一步促进动脉硬化的形成。高HCY致脑卒中的发病机制可能是多方面的,HCY可促使过氧化氢和氧自由基生成,对血管内皮细胞造成损伤和毒性作用;其次,它还可以促进动脉平滑肌细胞的增生;通过加速低密度脂蛋白氧化、增加泡沫细胞的形成和激活血小板黏附、聚集,亦可导致脉粥样硬化和梗死[17]。
本研究初步证实了CBS表达上调在缺血-再灌注损伤中对神经元有保护作用,我们将进一步研究CBS在IR脑损伤过程中确切的抗氧化应激机制。
[1]Go AS,Mozaffarian D,Roger VL,etal.AHA statistical update [J].Circulation,2013,127:e62-e245.
[2]陈旭彬,周艳霞,王洋.同型半胱氨酸与脑卒中相关性研究 [J].海南医学院学报,2013,19(3):326-328.
[3]程丽妞,白树风,杜敢琴,等.高同型半胱氨酸对脑梗死的影响[J].中国实用神经疾病杂志,2013,16(5):16-18.
[4]Sen S,Kawahara B,Gupta D,etal.Role of cystathionine β-synthase in human breast cancer [J].Free Radical Bio Med,2015,86:228-238.
[5]王瑜玲,马华民,王冰,等.大鼠肢体缺血-再灌注后脑 CBS 表达的变化及意义[J].中国病理生理杂志,2015,31(2):213-218.
[6]Belayev L,Alonso OF,Busto R,etal.Middle cerebral artery occlusion in the rat by intraluminal suture neurological and pathological evaluation of an improved model[J].Stroke,1996,27(9):1616-1623.
[7]何甜,闫超群,曾祥红,等.针刺对卒中后痉挛大鼠纹状体和脊髓中氨基酸含量的影响[J].中华中医药杂志,2015,30(9):3015-3017.
[8]吴升平,李世绰,王文志.中国城乡四社区人群脑卒中类型分布[J].中华预防医学杂志,1998,32(z1) :14.
[9]Sheng R,Qin Z.The divergent roles of autophagy in ischemia and preconditioning [J].Acta Pharmacol Sin,2015,7(36):411-420.
[10]Prajapa K,Roy N.Ischemia and Reperfusion Injury;The killer of the Modern Times [J].Quest,2013,1(1):10-13.
[11]Robert K,Nehmé J,Bourdon E,etal.Cystathionine β synthase deficiency promotes oxidative stress,fibrosis,and steatosis in mice liver [J].Gastroenterology,2005,128(5):1405-1415.
[12]Han Y,Qin J,Chang X,etal.Hydrogen sulfide and carbon monoxide are in synergy with each other in the pathogenesis of recurrent febrile seizures [J].Cell Mol Neurobiol,2006,26(1):101-107.
[13]王瑜玲,马华民,王冰,等.大鼠肢体缺血-再灌注后脑 CBS 表达的变化及意义[J].中国病理生理杂志,2015,31(2):213-218.
[14]Baumbach GL,Sigmund CD,Bottiglieri T,etal.Structure of cerebral arterioles in cystathionine β-synthase-deficient mice[J].Circ Res,2002,91(10):931-937.
[15]McCully KS.Vascular pathology of homocystinemia:implications for the pathogenesis of atherosclerosis [J].Am J Pathol,1969,56(1):111-128.
[16]Chambers JC,Seddon MD,Shah S,etal.Homocysteine--a novel risk factor for vascular disease [J].J Roy Soc Med,2001,94(1):10-13.
[17]申丽萍.同型半胱氨酸与脑卒中[J].临床合理用药杂志,2013,6(29):176-177.
[收稿2015-11-16修回2016-01-27]
(编辑张晓舟)
Dynamic change of cystathionine β-synthase during cerebral ischemia-reperfusion and its effect in rats
ZHOU Xiao-Lu,WANG Guo-Chuan,TAN An-Chao,LIU Jie-Lin,ZHANG Hua.Department of Hematology,the Affiliated People′s Hospital of Guizhou Medical University,Guiyang 550002,China
Objective:To observe the dynamic change of cystathionine β-synthase during cerebral ischemia-reperfusion and its effect in rats.Methods: The ischemic model was established with line embolism to block the middle cerebral artery.The reverse transcription-polymerase chain reaction(RT-PCR) and Western blot assay were used to assess the expression of cystathionine β-synthase(CBS) in SHAM group,I group,and IR group.ELISA assay was performed to detected the homocysteine(HCY) level in plasma.After treating with the inhibitor of cystathionine β-synthase called hydroxyla mine(HA),the expression of hemeoxygenase 1(HO-1) and the pathologic change of the brain was evaluated.Results: As compared to sham group,the expression of CBS was significantly up-regulated in ischemia-reperfusion group at 12 h post-reperfusion.Meanwhile,it existed the lowest level of HCY at 12 h post-reperfusion,comparing to sham grouzp(5.73±1.17 vs 2.88±0.93,F=25.56,P=0.001).When inhibited the activity of CBS via using HA,the down-regulation of HO-1 protein and further damage in neuron were observed.Conclusion: Cystathionine β-synthase serves as an protective factor during cerebral ischemia-reperfusion.
Stroke;Ischemia-reperfusion;Homocysteine;Cystathionine β-synthase;Oxidative stress
10.3969/j.issn.1000-484X.2016.08.012
R743.31文献标志码A
1000-484X(2016)08-1141-04
周晓璐(1984年-),女,硕士,主管技师,主要从事免疫学、输血检验方面的研究,E-mail:zhouxiaolu293@163. com。
及指导教师:刘杰麟(1963年-),男,博士,教授,主要从事基础免疫学方面的研究,E-mail:ljll282@163.com。
张华(1970年-),女,博士,主任技师,主要从事临床免疫学方面的研究,E-mail:zhanghua937@163.com。
