酸改性碳纳米管-再生纤维素膜的制备及表征*
2016-08-25张明新朱天容胡思前杨自然
张明新, 朱天容,2,唐 开, 胡思前,2,王 亮,2,杨自然
(1江汉大学化学与环境工程学院,湖北 武汉 430056;2光电化学材料与器件教育部重点实验室(江汉大学),湖北 武汉 430056)
酸改性碳纳米管-再生纤维素膜的制备及表征*
张明新1, 朱天容1,2,唐开1, 胡思前1,2,王亮1,2,杨自然1
(1江汉大学化学与环境工程学院,湖北武汉430056;2光电化学材料与器件教育部重点实验室(江汉大学),湖北武汉430056)
通过醋酸和混酸(V浓硫酸:V浓硝酸=3:1)两种方法对碳纳米管进行改性,然后在制备再生纤维素的基础上,制备改性碳纳米管-再生纤维素膜。通过红外、XRD和结构等对碳纳米管及其碳纳米管改性再生纤维素膜进行了性能表征,混酸能使碳纳米管表面接上羟基和羧基,同时去除表面杂质,引入碳纳米管能改变再生纤维素膜的结构和结晶性能。
碳纳米管;改性;再生纤维素;表征
纤维素是众多天然高分子化合物中的一种,其主要来源于自然界的植物,纤维素主要是由许多葡萄糖酐以糖酐键连接起来的直链多糖[1-3]。在纤维素分子的结构中,每个重复单元存在三个醇羟基,其中一个是伯羟基,而另外两个是仲羟基,由于羟基与水可以形成羟基,故纤维素具有高度亲水性。再生纤维素指的是将天然纤维素用各种方法溶解后再沉淀析出,而得到的纤维素。它不同于天然纤维素的地方在于分子量很低,结晶度狠低,分子缠结很少[4-7]。制备纤维素膜,首先要将其溶解,铜氨法,由于溶解纤维素的能力十分强,所以将纤维素溶解在铜氨溶液中时会发生配位反应形成纤维素醇化物或是分子化合物[8-11];新的溶解纤维素的主要方法有NaOH/尿素体系和环胺氧化物溶剂体系[12]。纤维素膜主要应用在电泳、亲水离子交换剂、渗透与透析、反渗透、电渗析、纳米过滤和作为包装材料等[13]。纤维素膜的改性方法主要由Ce4+引发的自由基聚合对纤维素纤维进行改性,多活性基阳离子无碱改性,二氧化硅纳米粒子改性及生物酶改性[14]。
碳纳米管,众所周知是以碳为基础的,以形成平面六边形的石墨单层为基础的,卷曲成的空心小管,其中碳是以sp2轨道杂化的方式成键。碳纳米管以层数的多少,可以分为多壁碳纳米管(MWNT)和单壁碳纳米管(SWNT)。即使制备的碳纳米管经过了纯化处理,其仍然不能直接用来制备复合材料,这是由于其比表面积极大,长径比大,表面呈惰性,不易与材料结合,管与管之间有范德华力,制备复合材料时,会在复合材料基体和溶液中产生缠结与团聚,将妨碍其发挥优异性能,也妨碍其创造良好的界面,不利于聚合物均匀分散[15-17]。因此,为了增加碳纳米管与聚合物更好的结合,需要对碳纳米管进行表面改性。目前来说,碳纳米管的改性方法主要有2种:共价键改性(化学改性)和非共价改性(物理改性)。共价键改性是利用氧化、接枝等手段,直接在碳纳米管的侧壁上引入小分子化合物、活性官能基团(如-NH2、-COOH和OH)等,从而提高碳纳米管的活性,增加其在溶液和聚合物中的相容性和分散度[18-19]。基于以上研究,本文准备采用溶胶-凝胶法,用改性后的碳纳米管制备复合膜,以期获得吸水性能优良的膜。
1 实 验
1.1试验药品和仪器
1.1.1试验药品
短棉绒;氢氧化钠固体(分析纯),武汉联碱厂;脲(尿素)(分析纯),国药集团化学试剂有限公司;95%乙醇(分析纯),天津市富宇精细化工有限公司;65%~68%硝酸(分析纯),开封东大化工有限公司试剂厂;36%~38%盐酸(化学纯),武汉市中南化学试剂厂;冰醋酸(化学纯),湖北省沙市市化学试剂一厂;98%浓硫酸(分析纯),信阳市化学试剂厂。
1.1.2试验仪器
分析天平;烧杯;JJ-1精密增力电动搅拌器;DF-101s集热式恒温加热磁力搅拌器,上海豫康科教仪器设备有限公司;0.22 μm有机滤膜,上海市新亚净化器件厂;循环式真空水泵泵,巩义市予华仪器有限责任公司;TENSOR 27傅里叶变换红外光谱仪,德国布鲁克公司;X’Pert Powder X射线衍射仪,荷兰PANaiytial;HITACHI SU8010超高分辨冷场发射扫描电子显微镜。
1.2实验内容
1.2.1改性的碳纳米管以及复合膜的制备
1.2.1.1再生纤维素膜的制备
在50 mL烧杯中准确称取28.8 g 7wt%NaOH/12wt%尿素溶液,加入1.2 g短棉绒(4wt%),搅拌一段时间后放入冰箱冷藏室中(-12 ℃)。12 h后,烧杯拿出,待溶液解冻后置于冰水中机械搅拌30 min,再次放入冰箱冷藏室中。12 h后,再次将烧杯拿出,待溶液解冻后置于冰水中机械搅拌30 min,然后将烧杯放入冰箱上层,静置脱气30 min后,将溶液倒在已经洗干净的玻璃板上,用缠绕有一定厚度的玻璃棒将溶液铺平。接着将玻璃板放入5wt%的浓硫酸中,待膜自行脱落后,排除膜中的气泡,将膜用蒸馏水洗至中性。最后,将膜平铺在另一洗净的玻璃板上,四角用粘胶粘住,自然晾干1.5 d。
1.2.1.2碳纳米管的改性
将0.1 g多壁碳纳米管放入三角烧瓶中,加入6 mL浓硫酸,2 mL浓硝酸(浓硫酸的体积与浓硝酸的体积比为3:1)(或者加入10 mL冰醋酸),70 ℃(或100 ℃)回流12 h[20]。将酸溶液大量稀释后,用有机滤膜过滤,洗涤后,70 ℃干燥。
1.2.1.3改性碳纳米管-再生纤维素膜的制备
在50 mL烧杯中准确称量28.8 g 7wt%NaOH/12wt%尿素溶液,分别加入0 g、0.012 g、0.036 g、0.06 g改性后的碳纳米管(碳纳米管的质量与短棉绒的质量比分别为1wt%,3wt%,5wt%),搅拌后加入1.2 g短棉绒(4wt%),制备复合膜。
1.2.2改性碳纳米管及复合膜的表征
用傅里叶变换红外光谱仪(波长:4000~600 cm-1)、X射线衍射仪(2θ:10°~80°)、扫描电子显微镜等仪器对未改性的碳纳米管、醋酸改性的碳纳米管和混酸改性的碳纳米管等3个固体试样进行了红外、晶体衍射以及结构等表征,同时也对纯的再生纤维素膜、含1wt%未改性的碳纳米管-再生纤维素膜和含1wt%混酸改性的碳纳米管-再生纤维素膜等3个膜进行了红外、晶体衍射和结构等进行了表征。
2 结果与讨论
2.1膜和碳纳米管的外部颜色及内部结构的比较
2.1.1复合膜外观比较
图1为纯的再生纤维素膜、含1wt%未改性的碳纳米管-再生纤维素膜、含3wt%未改性的碳纳米管-再生纤维素膜和含5wt%未改性的碳纳米管-再生纤维素膜颜色的比较图。由图1可知,随着未改性的碳纳米管的含量的增加,复合膜的颜色由白色到黑色逐渐加深,并且在膜的表面能明显看到未改性的碳纳米管,故未改性的碳纳米管与再生纤维素的结合较差。

图1 再生纤维素(RC)-未改性碳纳米管(MWNTs)复合膜的表面照片
图2为纯的再生纤维素膜、含1wt%混酸改性的碳纳米管-再生纤维素膜、含3wt%混酸改性的碳纳米管-再生纤维素膜和含5wt%混酸改性的碳纳米管-再生纤维素膜颜色的比较图。由图2可知,随着用混酸改性的碳纳米管的含量的增加,复合膜的颜色也由白色到黑色逐渐加深,但含3wt%混酸改性的碳纳米管复合膜与含5wt%混酸改性的碳纳米管复合膜和颜色差不多,故3wt%已达饱和。并且在膜的表面未能明显看到碳纳米管,故混酸改性的碳纳米管与再生纤维素的结合较好。将图1与图2中含量相同的未改性碳纳米管-再生纤维素膜与混酸改性碳纳米管-再生纤维素膜的颜色作对比,可看到混酸改性碳纳米管-再生纤维素膜的颜色要深,其进一步证明了酸改性的碳纳米管与再生纤维素的结合比未改性的碳纳米管与再生纤维素的结合要好。

图2 再生纤维素(RC)-改性碳纳米管(MWNTs)复合膜的表面照片
2.1.2复合膜及碳纳米管内部结构比较
图3为含1wt%未改性碳纳米管-再生纤维素膜和含1wt%混酸改性碳纳米管-再生纤维素膜在2.00 μm分辨率下的扫描电镜图。由图3可以看出,含1wt%混酸改性碳纳米管-再生纤维素膜比1wt%未改性碳纳米管-再生纤维素膜表面要光滑,故混酸改性的碳纳米管与再生纤维素结合的要好。图4为未改性的碳纳米管和混酸改性的碳纳米管在200 nm分辨率下的扫描电镜图。由图4可以看出,混酸改性后的碳纳米管,其管状半径会增大,缠绕现象减少,这将有利于与纤维素的结合。故用混酸改性碳纳米管效果较好。

图4 未改性碳纳米管(a)和改性碳纳米管(b)的SEM图谱
2.2改性碳纳米管及复合膜的表征
2.2.1红外分析特征峰
图5为未改性的碳纳米管、醋酸改性的碳纳米管和混酸改性的碳纳米管的红外光谱图。由图5可以看出,用醋酸改性的碳纳米管与未改性的碳纳米管的红外峰基本一样,且在3500 cm-1左右没有出现羟基的特征峰值。用混酸改性的碳纳米管在3755 cm-1出现了O-H的伸缩振动峰,1689 cm-1出现了C=O的伸缩振动峰,1547 cm-1出现了C-O-H的弯曲振动峰,1147 cm-1出现了C-O的伸缩振动峰。故混酸能够氧化碳纳米管,使其出现羟基和羰基,而醋酸不行。图6为纯的再生纤维素膜、含1wt%未改性的碳纳米管-再生纤维素膜以及含1wt%混酸改性的碳纳米管-再生纤维素膜的红外光谱图。由图6可知,含1wt%未改性的碳纳米管-再生纤维素膜的谱图与纯的再生纤维素膜的谱图差不多。在再生纤维素红外光谱图中,在3319 cm-1出现了宽而强的O-H伸缩振动吸收峰,2915 cm-1出现了C-H伸缩振动吸收峰,1648 cm-1出现了较弱的由于纤维素吸水所致的吸收峰,1388 cm-1出现了中强度的 C-H弯曲振动吸收峰,1019 cm-1出现了较强的C-O-C伸缩振动肩带峰,891 cm-1出现了-CH2弯曲振动吸收峰。而在含1wt%混酸改性的碳纳米管-再生纤维素膜的红外光谱图中,O-H伸缩振动吸收峰减弱和C-H伸缩振动吸收峰,由于纤维素吸水所致的吸收峰和C-H弯曲振动吸收峰几乎消失。这是由于纤维素的羟基与改性后碳纳米管的羰基作用,使羟基的数量降低。故改性后的碳纳米管能够很好的与再生纤维素结合。

图5 未改性、醋酸和混酸改性碳纳米管的红外光谱图
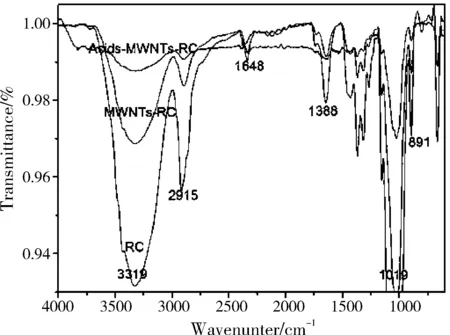
图6 纯的再生纤维素膜、含1wt%未改性的碳纳米管及含1wt%混酸改性的碳纳米管-再生纤维素膜的红外光谱图
2.2.2晶体衍射分析结晶度
图7为未改性的碳纳米管、醋酸改性的碳纳米管和混酸改性的碳纳米管的X-射线衍射图。由图7可以看出未改性的碳纳米管的X-射线衍射图与醋酸改性的碳纳米管基本一样,故醋酸对碳纳米管改性效果很差,几乎无改性效果。且其特征衍射峰2θ位于26.1°和42.9°。混酸改性的碳纳米管的X-射线衍射特征峰2θ位于25.6°,其位置降低,这可能与氧化后生成的羰基与羧基有关。且可能由杂质引起的峰值42.9°消失了。故混酸对碳纳米管的改性效果较好。图8为纯的再生纤维素膜、含1wt%未改性的碳纳米管-再生纤维素膜、含1wt%醋酸改性的碳纳米管-再生纤维素膜和含1wt%混酸改性的碳纳米管-再生纤维素膜的X-射线衍射图。由图8可知,4条线的差别不大。纯的再生纤维素膜的特征衍射峰2θ位于11.9°、15.3°、22.4°、26.3°、29.3°、35.6°、39.4°、43.1°、47.4°和48.5°。查阅文献可知[21],再生纤维素膜的X-射线衍射特征峰2θ位于12.0°、20.0°和22.0°左右等3个,同时由图7可知碳纳米管的特征峰位于26.0°左右。故图8前4个为复合膜的特征峰,后6个为测量时,所用双面胶引起的。混酸改性的碳纳米管-再生纤维素膜的X-射线衍射特征峰2θ位于11.7°、15.0°、22.3°和26.3°。对比可知,纤维素的特征峰值相应有所减低。这是由于纤维素上的羟基与碳纳米管上的羧基结合后,纤维素链排列规整度降低,结晶度降低。

图7 未改性的碳纳米管、醋酸改性的碳纳米管和混酸改性的碳纳米管的X-射线衍射图
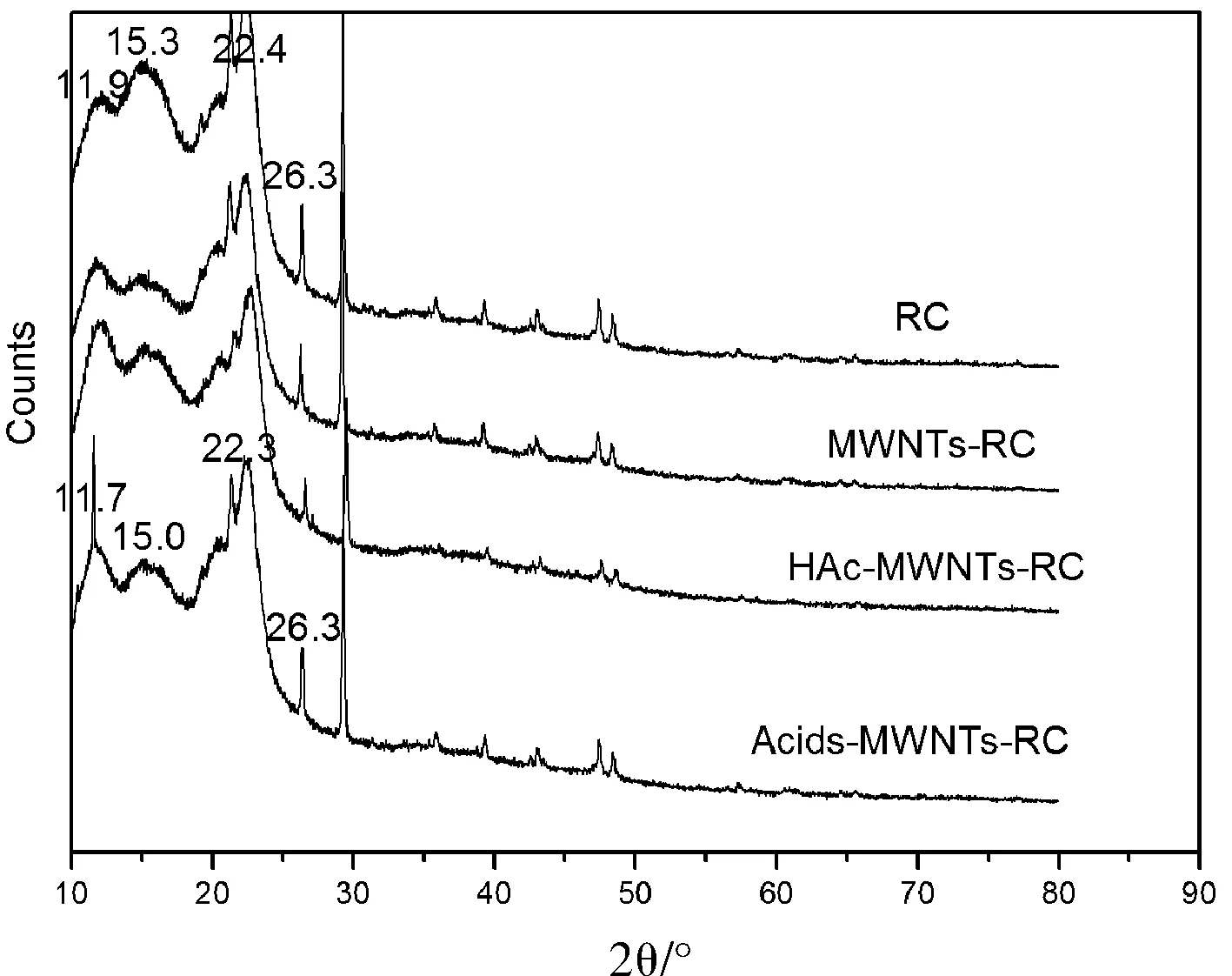
图8 纯的再生纤维素膜、含1wt%未改性的碳纳米管-再生纤维素膜、含1wt%醋酸改性的碳纳米管-再生纤维素膜和含1wt%混酸改性的碳纳米管-再生纤维素膜的X-射线衍射图
3 结 论
(1) 醋酸对碳纳米管几乎没有改性效果。混酸(V浓硫酸:V浓硝酸=3:1)改性的碳纳米管,通过红外及XRD可以看出,其表面增加羟基和羧基;通过扫描电镜可以看出,管状半径增大,缠绕现象降低。故混酸对碳纳米管的改性效果很好。
(2) 混酸改性的碳纳米管-再生纤维素膜的吸水性能比纯再生纤维素膜,以及醋酸改性的碳纳米管-再生纤维素膜的吸水性能都要好。故最后确定用混酸(V浓硫酸:V浓硝酸=3:1)改性碳纳米管。
[1]李娜,刘忠洲,续曙光.再生纤维素分离膜制备方法研究进展[J].膜科学与技术,2001,21(6): 27-33.
[2]王碟,王中珍.纤维素纤维鉴别方法简介[J].国际纺织导报,2010(11): 58-62.
[3]唐莹莹,潘玉娟.再生纤维素纤维的结构与力学性质的研究[J].国外丝绸,2009(3):10-12.
[4]张金梅,柳卫莉,张俐娜,等.花生壳纤维素制备再生纤维素膜[J].暨南大学学报(自然科学版),1996,17(1):59-63.
[5]杨光,张俐娜.再生纤维素/聚乙烯醇共混膜的研究[J].高分子学报,1994(2): 176-181.
[6]郑连爽,张甲耀,张俐娜,等.再生纤维素膜的微生物降解[J].环境科学,1996,17(2): 6-9.
[7]张俐娜,杨光,钟文德.再生纤维素膜及其微孔膜性能的比较[J].膜科学与技术,1992,12(1): 59-63.
[8]张俐娜,肖玲,聂学先,等.再生纤维素膜孔性研究[J].高分子材料科学与工程,1991(1): 109-113.
[9]蒋昌武,何喜庆,吴琳俐,等.再生纤维素荧光膜[J].应用化学,1995,12(1): 30-33.
[10]张领,孙晓锋,景占鑫,等.半纤维素/碳纳米管复合凝胶的溶胀性能[J].化工进展,2013,32(8): 1881-1886.
[11]杨光,张俐娜.再生纤维素膜对聚苯乙烯的截留性[J].应用化学,1991,8(3): 17-21.
[12]杨鹏飞.纤维素在膜科学中的研究进展[J].河北化工,2009,32(4): 9-12.
[13]韩天龙.纤维素膜的应用研究[J].吉林工程技术师范学院学报(工程技术版),2004, 12 (20): 54-56.
[14]雷乐颜.纤维素纤维的改性方法[J].科技与向导,2011(26): 28.
[15]付昱,孙立,田春贵,等.酸功能化碳纳米管对多孔碳材料储能活性及稳定性的增强作用[J].应用化学,2013,30(9): 1065-1072.
[16]林锐,李丽丽,何佳,等.羧酸化单壁碳纳米管对盐酸表柔比星吸附与释放行为的研究[J].药学学报,2011,34(2): 30-33.
[17]宫斌,黄据芹,王怀友.碳纳米管的修饰研究进展[J].化学分析计量,2009,18(5): 89-91.
[18]程亚玮,李欢军,张公正.碳纳米管基聚合物水凝胶研究进展[J].中国科学论文,2013,8(9): 89-91.
[19]任丙南,耿静.酸处理对碳纳米管催化剂载体的影响[J].广东化工,2013,40(11): 23-25.
[20]闵嘉康.碳纳米管改性方法及其在复合材料制备中的应用[J].科研论坛,2010,5(下): 118-120.
[21]李传峰,邵怀启,钟顺和.有机无机杂化膜材料的制备技术[J].化学进展,2004,16(1): 83-89.
Preparation and Characterization of Acid Modified Carbon Nanotubes-regenerated Cellulose Membrane*
ZHANG Ming-xin1, ZHU Tian-rong1,2, TANG Kai1, HU Si-qian1,2, WANG Liang1,2, YANG Zi-ran1
(1 School of Chemistry and Environmental Engineering, Jianghan University, Hubei Wuhan 430056;2KeyLaboratoryofOptoelectronicChemicalMaterialsandDevices(JianghanUniversity),MinistryofEducation,JianghanUniversity,HubeiWuhan430056,China)
Carbon nanotubes were modified by two methods of acetic acid and mixed acid (Vsulfuric acid:Vnitric acid=3:1). On the basis of the preparation of regenerated cellulose, the modified carbon nanotubes-regenerated cellulose membrane was prepared. By IR, XRD and structure properties of carbon nanotube characterization, mixed acid can make the surface of carbon nanotubes grafted in hydroxyl and carboxyl, at the same time to remove surface impurities. The structure and crystalline properties of regenerated cellulose membranes can be changed by the introduction of carbon nanotubes.
carbon nanotubes; modification; regenerated cellulose membrane; characterization
湖北省教育厅科学研究计划项目(B2014066);光电化学与器件教育部重点实验室开放基金项目(JDGD-201609);江汉大学博士科研启动经费项目(2012021)。
张明新(1994-),男,本科生,从事材料化工。
朱天容(1985-),女,讲师,博士,研究方向:膜分离材料,光电薄膜材料。
O636.9
B
1001-9677(2016)014-0055-04
