抗肿瘤植入剂在直肠癌根治术中应用的可行性探讨
2016-08-25战祥青胡朝奇芜湖先声中人药业有限公司安徽芜湖4080山东省莒县中医院神经外科山东莒县76800
徐 刚 战祥青 胡朝奇▲.芜湖先声中人药业有限公司,安徽芜湖 4080;.山东省莒县中医院神经外科,山东莒县 76800
抗肿瘤植入剂在直肠癌根治术中应用的可行性探讨
徐刚1战祥青2胡朝奇1▲
1.芜湖先声中人药业有限公司,安徽芜湖241080;2.山东省莒县中医院神经外科,山东莒县276800
目的 探讨术中植入抗肿瘤植入剂在直肠癌手术治疗中的可行性。方法 回顾性分析莒县中医院收治的60例接受直肠癌手术治疗的患者的临床资料,依据术中是否植入抗肿瘤植入剂分为两组,比较两组患者的手术情况、不良反应、术后近期治疗效果及远期治疗效果。结果 两组患者的一般手术情况、不良反应和术后近期治疗效果无统计学意义(P>0.05);观察组患者远期治疗效果优于对照组(P<0.05)。结论 抗肿瘤植入剂具有操作方便、安全、可行的特点,对于降低术后癌症的复发和转移均具有重要的临床意义,值得推广应用。
抗肿瘤植入剂;氟尿嘧啶;直肠癌;可行性
[Abstract]Objective To explore the feasibility of antitumor implants for rectal carcinoma.Methods Clinical data of rectal carcinoma who had been operative in Juxian Hospital of Tradition Chinese Medicine were collected and analyzed. They were divided into two groups based on the usage of antitumor implants.Operation condition,side effects,shortterm effects and long-term effects were compared.Results There were no significant differences between the two groups in the operation time,bleeding volume and short-term effects(P>0.05).The long-term effect of the observation group was better than that of the control group(P<0.05).Conclusion The features of Antitumor inplants are easy to operate,and safe feasible.Antitumor implants can reduce the recurrence rates after treatment.It is safe and feasible.It is worth for clinical application.
[Key words]Antitumor implants;Fluorouracil;Rectal carcinoma;Feasibility
直肠癌是临床上常见的一种恶性肿瘤疾病,目前临床上该病的治疗主要以手术根治术为主[1],虽然手术根治术可将肿瘤瘤体大部切除,但是由于手术仍然可能残留部分瘤体组织,残留的瘤体细胞可快速进行复制,进而导致肿瘤的复发,严重影响了治疗效果,因此如何有效抑制残留瘤体的复制对于提高直肠癌根治术的治疗效果具有重要意义[2]。术中植入抗肿瘤植入剂是临床上治疗食管癌、胃癌的常用辅助治疗方式,本研究旨在考察直肠癌根治术中植入抗肿瘤植入剂的可行性,以为直肠癌临床治疗提供科学、合理的辅助治疗方法,现报道如下。
1 资料与方法
1.1一般资料
回顾性分析莒县中医院2011年1月~2014年7月收治的接受直肠癌根除术的60例患者临床资料,并依据术中是否植入氟尿嘧啶植入剂将患者分为两组,其中30例患者术中未植入氟尿嘧啶植入剂,作为对照组,30例患者术中植入氟尿嘧啶植入剂,作为观察组。观察组中男17例,女13例,年龄37~58岁,平均(45.7±5.9)岁,上段肿瘤9例,中段10例,下段11例,TNMⅠ期 6例,TNMⅡ期 17例,TNMⅢ期7例,高度分化6例,中度分化16例,低度分化8例;对照组中男 16例,女14例,年龄35~57岁,平均(46.5±6.3)岁,上段肿瘤12例,中段8例,下段10例,TNMⅠ期 8例,TNMⅡ期 16例,TNMⅢ期6例,高度分化5例,中度分化15例,低度分化10例,两组患者一般资料组间差异无统计学意义(P>0.05),具有可比性。
1.2纳入标准及排除标准
纳入标准:①患者年龄30~60岁;②直肠是原发病灶部位;③仅存在单一病灶部位;④患者术前无明显肝肾功能异常;排除标准:①肿瘤已广泛扩散;②伴有重要器官严重合并症;③曾患有其他肿瘤疾病;④氟尿嘧啶过敏者。
1.3方法
1.3.1治疗方法两组患者均接受常规直肠癌根除术,即采用腹部正中或左旁正中切口入膜,先将患者直乙结肠左侧系膜进行分离,再分离右侧系膜,于腹膜的折返处会师,并对肠系膜下方血管根部进行结扎,以完整切除原发性肿瘤作为手术原则,切除过程中保证肿瘤远端至少有2 cm安全切缘,使用TME术式对肿瘤的淋巴引流区进行清扫,在保证患者肿瘤完全根治的基础上尽可能保留患者泌尿生殖功能和肛门括约肌功能,术中严格执行无瘤原则,肿瘤标本取出时注意保护手术切口,术后常规缝合手术切口,并留置引流管。观察组患者采用术中植入抗肿瘤植入剂进行辅助治疗,即采用氟尿嘧啶植入剂(管剂,芜湖先声中人药业有限公司,规格0.1 g,批号:20100904、20110704、20120201),观察组患者在完成直肠癌手术后将600 mg氟尿嘧啶植入剂分4~6点分别均匀植入患者的瘤床、肠系膜血管根部和相应的淋巴引流通路中,每一个植药点的植入量不超过150 mg,每个植药点距离吻合口的距离应>3 cm[3]。对照组患者仅接受常规直肠癌根治术,且两组患者术后均依据NCCN直肠癌治疗规范进行术后的辅助治疗,并对患者疾病的转归情况进行随访。
1.3.2评价指标以两组患者的一般手术情况、毒副作用、术后近期治疗效果及远期治疗效果作为观察指标,其中手术情况考察两组患者的手术时间和术中出血量;毒副作用主要考察两组患者手术治疗前后红细胞计数(RBC)、白细胞计数(WBC)、肌酐含量和谷丙转氨酶(ALT)含量的变化;术后近期治疗效果主要考察术后排气时间、进食时间、尿管留置时间、下床时间、术后住院时间和术后4周内并发症发生率(吻合口漏、腹膜炎、切口感染和肠梗阻);远期治疗效果考察患者接受治疗12个月后血CEA升高、局部复发、远处转移和死亡的发生率。
1.4统计学方法
使用SPSS13.0统计学软件包进行分析,其中计量资料以(x±s)表示,采用独立样本t检验,计数资料以[n(%)]表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1两组患者一般手术情况比较
两组患者的手术时间和术中出血量比较,差异无统计学意义(P>0.05),见表1。
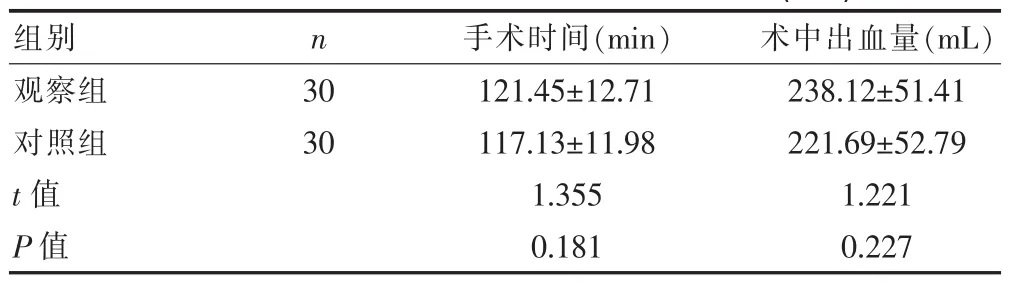
表1 两组患者手术时间和术中出血量比较(x±s)
2.2两组患者治疗前后RBC、WBC、肌酐和ALT含量变化比较
治疗前两组患者的各项指标值均没有显著性差异,治疗后两组患者的WBC、肌酐和ALT含量均明显高于治疗前,观察组:t(WBC)=-10.034,P=0.000;t(肌酐)= -4.437,P=0.000;t(ALT)=-6.934,P=0.000;对照组:t(WBC)= -11.455,P=0.000;t(肌酐)=-3.887,P=0.000;t(ALT)= -6.872,P=0.000;但是组间差异无统计学意义(P>0.05)。见表2。
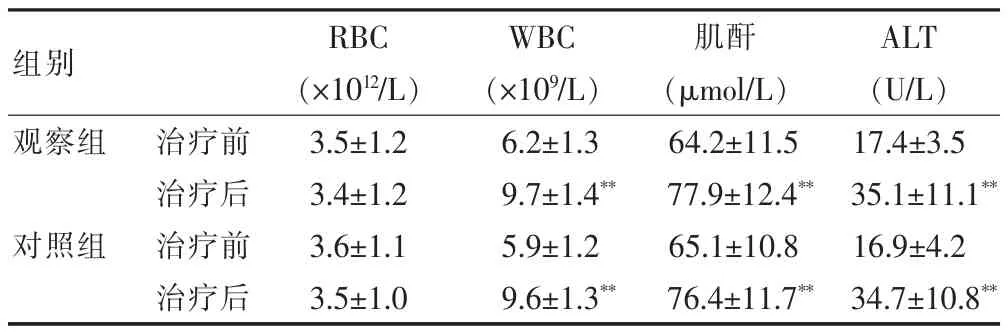
表2 两组患者治疗前后RBC、WBC、肌酐和ALT含量变化比较(x±s,n=30)
2.3两组患者术后近期治疗效果比较
两组患者术后一般恢复情况和并发症发病率比较,组间差异无统计学意义(P>0.05),见表3、4。
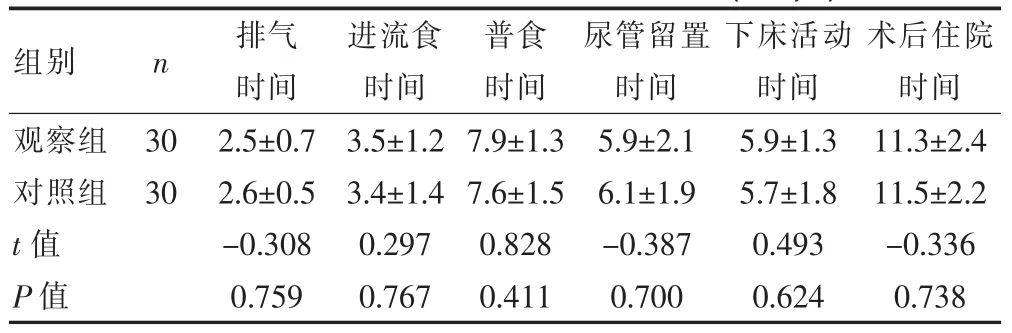
表3 两组患者术后一般恢复情况比较(x±s,d)
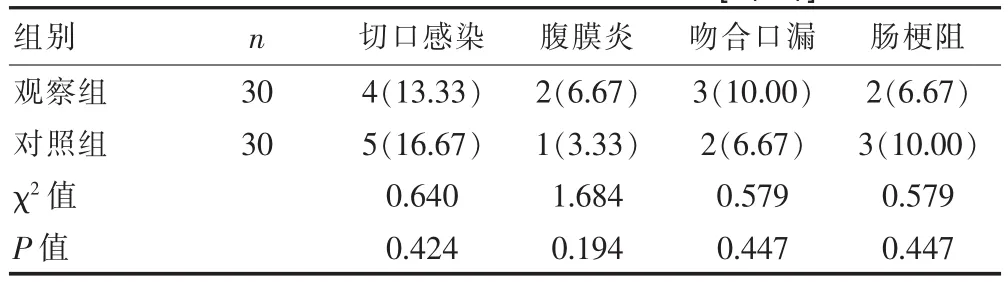
表4 两组患者术后并发症结果比较[n(%)]
2.4两组患者术后远期治疗效果比较
观察组患者CEA升高例数、局部复发例数及远处转移例数明显少于对照组(P<0.05)。见表5。
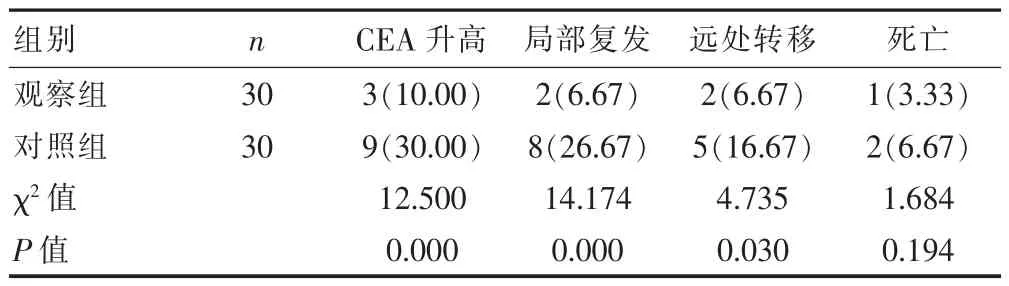
表5 两组患者术后远期治疗效果比较[n(%)]
3 讨论
进展期直肠癌术后转移、复发率较高,进而造成患者的预后效果较差[4],临床研究发现,进展期直肠癌术后患者5年的生存率小于30%。造成术后转移、复发的主要因素有以下两个方面:①术中肿瘤细胞的脱落种植[5];②微小转移灶的残留。因此如果可以在术后对患者的手术切除部位及时给予化疗药物进行治疗,将有效的抑制术后的转移、复发[6],从而有效提高直肠癌的手术治疗效果。抗肿瘤植入剂是临床上治疗恶性肿瘤的一种新剂型,其通过以高分子材料作为释药骨架,从而可有效发挥局部控制给药的目的。5-Fu是临床上常用的抗肿瘤药物[7],其可抑制肿瘤细胞胸腺嘧啶核苷酸合成酶的活性,从而有效抑制肿瘤细胞的DNA 和RNA的合成。但是由于5-Fu半衰期较短,给药后血药浓度维持时间较短,因而需要大剂量、多次给药,从而导致患者治疗过程中不良反应较多[8],氟尿嘧啶植入剂是以高分子材料硅橡胶作为载体的抗肿瘤缓释植入剂,其通过在术中病灶部位植入药物,一方面可以维持术后病灶部位及周围组织较高的5-Fu浓度[9],避免因全身给药给患者带来的严重不良反应,提高患者的治疗效果;同时5-Fu在外周血液循环中也可以维持较长时间的血药浓度,可有效预防术后局部复发[10]。目前氟尿嘧啶植入剂作为恶性肿瘤根除术的辅助治疗方式[11],在消化系统恶性肿瘤治疗中应用较为广泛,王霁[12]、尹会义等[13]通过在直肠癌术中植入氟尿嘧啶植入剂发现,患者的肝肾功能和免疫功能无明显影响,患者的并发症也未出现明显增加,但是术后局部复发率较之未术中给药组的患者明显降低;郝永胜等[14]在胃癌治疗中使用氟尿嘧啶植入剂发现,患者3年的生存率明显高于未给药组,同时患者的复发率也明显低于未给药组。
本次临床通过比较两组患者的手术情况结果发现,两组患者的手术时间和术中出血量无显著性差异(P>0.05),说明术中植入氟尿嘧啶植入剂操作较为方便、安全,不会增加手术难度。两组患者的白细胞计数值均明显高于术前,这是由于患者术后的应激反应和炎症反应所致,且组间差异无统计学意义(P>0.05),说明术中植入氟尿嘧啶植入剂不会增加患者术后的炎症反应。两组患者术后肌酐、ALT含量明显高于手术前,可能与手术对组织的损伤、药物使用有关[15],但是两组患者均未出现严重的肝肾功能异常,这与王霁[12]、尹会义等[13]的研究结果一致。说明了术中植入氟尿嘧啶植入剂的安全性。两组患者术后身体恢复时间和并发症的发生率无显著性差异(P>0.05),进一步说明了氟尿嘧啶植入剂使用的安全性,不会对患者术后身体身体恢复产生不良影响。CEA是临床上预测直肠癌预后和复发的重要指标之一,CEA含量越高,患者肿瘤预后效果越差,复发的可能性越高[16],本次研究发现,观察组患者CEA升高患者数、局部复发患者数、远处转移患者数均明显低于对照组患者(P<0.05),初步说明了术中植入氟尿嘧啶植入剂可有效预防直肠癌根除术后恶性肿瘤的转移和复发。本次临床研究中,两组患者的死亡率无显著性差异(P>0.05),因此尚不能明确术中植入氟尿嘧啶植入剂是否可以降低直肠癌术后患者的死亡率,需要进行进一步的临床研究。
总之,术中植入氟尿嘧啶植入剂具有操作方便、安全、可行的特点,对于降低术后癌症的复发和转移均具有重要的临床意义,具有推广应用价值。
[1]华进,朱广伟,张晓岚.结直肠癌患者术后5-FU腹腔灌注与5-FU缓释剂术后腹腔植入的临床疗效分析[J].牡丹江医学院学报,2010,31(6):34-36.
[2]殷保兵,马保金,陈进宏.大肠癌术中腹腔植入氟尿嗜咤植入剂的临床观察[J].中国临床医学,2006,13(5):767-768.
[3]陆雪明,王树钦.直肠癌术中植入氟尿嘧啶缓释剂的临床观察[J].中国普外科基础与临床杂志,2014,21(4):495-497.
[4]赵泉,罗开元,王明春,等.缓释氟尿嘧啶组织间植入治疗大肠癌的疗效观察[J].云南医药,2007,28(5):447-448.
[5]邓立春,沈伟生,张瑶,等.化疗对晚期结直肠癌患者血清VEGF水平的影响[J].实用临床医药杂志,2010,14(5):90-92.
[6]吴志海,吴大英,郭予武,等.卡培他滨维持治疗转移性结直肠癌的疗效及安全性观察[J].实用临床医药杂志,2012,16(7):85-87.
[7]郭基珍,王晓俊,王向.腹腔镜直肠癌根治术19例临床分析[J].实用临床医药杂志,2011,15(5):63-65.
[8]徐刚,胡朝奇.正交试验设计优化氟尿嘧啶植入剂制剂工艺研究[J].中国医药导报,2015,12(19):19-20.
[9]郭迅,裴明祥,张文新,等.氟尿嘧啶植入剂在乳腺癌术中应用的对比研究[J].中国医药导报,2010,7(14):55-56.
[10]徐刚,胡朝奇.术中植入氟尿嘧啶植入剂在原发性肝癌切除术治疗中的应用价值[J].中国现代医生,2015,53(11):112-115.
[11]王培红,杜军,夏蕊琪,等.直肠癌手术中植入缓释药物的安全性与有效性观察[J].实用医院临床杂志,2015,12(1):148.
[12]王霁.直肠癌术中腹腔置入5-氟尿嘧啶缓释剂的疗效及安全性分析[J].中国医药指南,2015,13(4):69-70.
[13]尹会义,于洋.术中局部植入氟尿嘧啶缓释剂在胃肠道肿瘤治疗中的应用体会[J].现代诊断与治疗,2015,26 (3):579-580.
[14]郝永胜,李凤晓,范伟.进展期胃癌术中植入5-氟尿嘧啶缓释剂的疗效观察[J].中国药物与临床,2016,16 (4):558-560.
[15]陈宏,陈军.原发性肝癌患者接受根治性手术联合5-Fu缓释剂术中植入的预后评估[J].海南医学院学报,2016,22(7):712-715.
[16]王正冬,周爱明,金根培.进展期结直肠癌患者术中行氟尿嘧啶腹腔区域性量化缓释化疗的效果观察[J].山东医药,2012,52(27):84-85.
Feasibility study on antitumor implants for rectal carcinoma
XU Gang1ZHAN Xiangqing2HU Chaoqi1
1.Wuhu Simcere Sino-implant Pharmaceutical Co Ltd,Wuhu241080,China;2.Department of Neurosurgery,Juxian Hospital of Tradition Chinese Medicine in Shandong Province,Juxian276800,China
R730.5
B
1673-9701(2016)17-0129-03
安徽省芜湖市科技计划项目(2013hm43)
▲
(2016-03-27)
