临床应用血浆地高辛浓度危急值的效果评价
2016-08-22彭琼
彭琼
·论著·
临床应用血浆地高辛浓度危急值的效果评价
彭琼1
目的 评价临床应用血浆地高辛浓度危急值的效果。方法 从湖北省荆门市第一人民医院实验室的信息系统中选出自2013年3月至2015年2月血浆地高辛浓度危急值的相关数据,并通过对数据进行处理,进而统计临床应用血浆地高辛浓度危急值的科室分布、时间段分布及发生率,分析血浆地高辛的危急值范围以及报告的周转时间。结果 血浆地高辛危急值发生率为3.19%,下午15时至17时是血浆地高辛浓度危急值发生率最高时间段,在3 h内将报告送到相关科室的有51例,占82.3%,临床指征和血浆地高辛浓度危急值的符合率为67.7%。结论 持续改进血浆地高辛浓度危机值报告程序,并进行定期分析评估,可以有效提高临床和检验科的工作质量和效率,给予患者更好的安全保障。
质量改进;危急值;血浆地高辛浓度
危急值是临床上极度异常的检验结果,若患者没有得到及时有效的治疗,很可能面临死亡的危险[1]。危险值的报告工作涉及临床医生、护理部以及实验室等[2],因其直接关系到患者的生命安全,因此,越来越受到重视和关注。中国医院协会2007年制定的患者安全目标第四点明确指出要建立健全完善的危急值报告制度[3],这表明,我国相关研究学者对危急值的概念、项目设置、作用以及意义已有了一定的认识和重视。College of American Pathologists有关的危急值范围的调查报告和标准指南和第三版《全国临床检验操作规程》等,均可作为实验室和临床的基准来对危急值项目进行有效的设置和调整[3]。如何设定危急值限值,如何第一时间向临床提供检验结果,更好地满足临床需求,还需进一步的研究和分析。
1 资料与方法
1.1资料来源 从湖北省荆门市第一人民医院实验室的信息系统中选出自2013年3月至2015年2月血浆地高辛浓度危急值的相关数据,内容包括科室、标本号、年龄、接收时间、结果、报告时间等。
1.2血浆地高辛的检测方法 患者入院24 h内及出院前24 h用肝素锂管抽取肘静脉血3 ml,摇匀,放入离心机中以4000转/min的转速离心5 min,取上层清液滴入试纸上静置15 min,试纸放入FIA8000系列免疫定量分析仪(南京普朗医用设备有限公司提供)中测定地高辛浓度(仪器检测范围为100~15000 pg/ml)。
2 结果
2.1血浆地高辛浓度危急值发生率 我院检验科免疫室自2013年3月至2015年2月血浆地高辛浓度测试数为1945次,其中,有62个符合危急值报告条件的测试数,血浆地高辛危急值发生率为3.19%。
2.2血浆地高辛浓度危急值发生率与发生时间的关系 经过数据分析发现,下午15时至17时是血浆地高辛浓度危急值发生率最高时间段,占40.3%,其次是上午10时,占19.4%,其中,住院患者占89.8%(表1)。
2.3血浆地高辛浓度危急值临床科室的具体分布情况 通过对数据进行统计,分析血浆地高辛浓度危急值在临床科室分布,结果显示高干病房和心内科为血浆地高辛浓度危急值发生的主要科室,占61.5%(表2)。
2.4血浆地高辛浓度危急值与年龄分布的关系 通过数据统计,分析血浆地高辛浓度危急值年龄分布,结果显示,大于55岁的老年患者为血浆地高辛浓度危急值发生的主要年龄段。在62例血浆地高辛浓度危急值患者中,年龄最小的患者为21岁,两名均为慢性肾功能衰竭患者;年龄最大的患者96岁;其中,以75岁~85岁年龄组为主,占46.8%,其次为85~96岁年龄组,占22.6%(表3)。
2.5地高辛浓度检测的周转时间 对于危急值的报告,地高辛浓度检测的周转时间相当重要,在30 min内将标本送到实验室的24例,占38.7%,而在3 h内将报告送到相关科室的51例,占82.3%,而11例患者标本超过3 h才报告给相关的临床科室,占17.7%(表4)。
2.6临床指征和血浆地高辛浓度危急值的符合率在62例血浆地高辛浓度危急值患者中,有42例患者在检测出危急值前后24 h出现地高辛中毒症状,其中有7例患者出现消化道反应包括腹泻、呕吐、恶心、厌食;有10例患者出现视觉障碍包括视力模糊、绿视、黄视;有8例患者出现心脏反应包括各种心律失常;有17例患者出现神经系统症状包括精神错乱、谵妄、失眠、头痛、眩晕。其中,在调整用药后48 h,有32例患者症状有所缓解,临床指征和血浆地高辛浓度危急值的符合率为67.7%。
3 讨论
迅速、准确地为临床医生提供具有诊断意义的检测数据是实验室的主要职能[4],因此,对危急值的报告就显得相当重要。危急值,即提示患者可能处在极其危险的状态[5],此时,若临床医生可及时得到危急值信息,并对患者做出适当的处理和治疗,可挽救患者的生命,否则将会失去最佳的治疗或抢救时机。因此,对于危急值报告制度的建立和改进十分重要[6]。
Lundberg最早提出危急值报告制度,并逐渐被各国采纳和使用。有些实验结果即使出现异常,也不会对患者的生命造成威胁[7],如肿瘤标志物实验、补体、抗体、血脂以及血浆蛋白等;当实验结果出现异常,对患者的生命造成威胁时,需要对其进行积极治疗和处理时,才将其列入危急值报告列表中,如血钠、血钾和血气分析[8]等,但是,危急值项目的检测结果出现异常时,并不意味着患者面临生命危险,当危急值项目的检测结果高于或低于一定值时,才会对患者的生命安全造成威胁[9],而这个临界值,即为危急值,血浆地高辛作为实验室常见的药物浓度危急值,也被加入到危急值项目中。

表1 血浆地高辛浓度危急值发生率与发生时间的关系

表2 血浆地高辛浓度危急值临床科室的科室分布及发生率

表3 血浆地高辛浓度危急值的年龄分布以及发生率
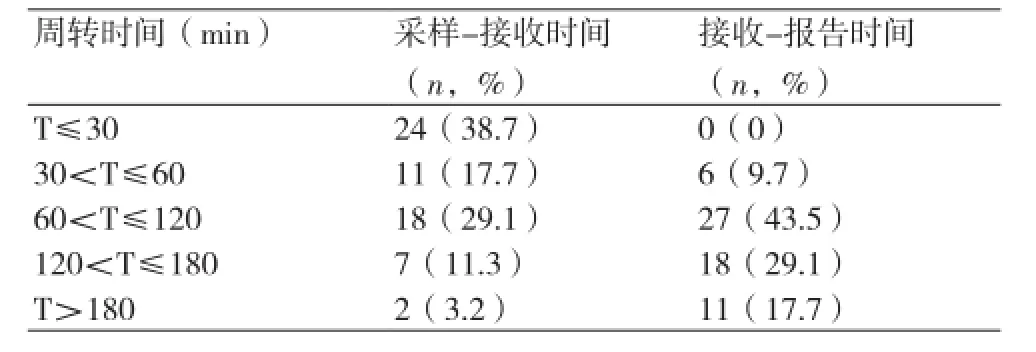
表4 地高辛浓度检测的周转时间
地高辛能增加心肌收缩力,通常用于治疗多种心律失常以及充血性心衰等[10],但是地高辛的治疗指数较低,药效学和药动学个体差异较大,安全范围较窄,给予常规剂量也可能达不到理想的疗效甚至中毒等[11]。尽管药物剂量标准化因为晶体地高辛的出现成为可能,但有患者即使维持量也出现中毒[12],如电解质紊乱(如地高辛敏感性可因低血钾增加而出现中毒症状)以及老年患者等,地高辛本身用于治疗心律不齐,然而地高辛中毒症状也类似于心律不齐[13]。
从血浆地高辛浓度危急值的临床科室分布和发生时间发现,如表2所示,高干病房和心内科病房是血浆地高辛浓度危急值发生率较高的主要科室;住院患者是危急值的主要来源,占89.8%,而血浆地高辛浓度危急值的发生时间分布也有一定规律性,如表1所示,主要发生在下午,这与药代动力学、患者服药时间以及本院的工作流程有一定相关性。如表3所示,血浆地高辛浓度危急值主要集中在55岁以上的老年患者,推测可能与联合用药、老年人肾功能减退以及服用地高辛的疾病类型有一定关系。通过查阅病史发现,部分患者在使用地高辛的同时,还使用了钙离子通道阻断剂以及抗菌药等。
血浆地高辛浓度危急值标本检测的周转时间对患者的安全有很大的影响,因此缩短周转时间至关重要,其涉及到培训、教育、工作流程及仪器设备等的改善和提高[14],每个流程都可能对周转时间造成影响,如表4所示,对于危急值的报告,地高辛浓度检测的周转时间相当重要,在30 min内将标本送到实验室的24例,占38.7%,而在3 h内将报告送到相关科室为51例,占82.3%,由此可见,标本运输时间是不可忽视的因素之一,改进的方法有加强临床科室培训及增加运输人员,而11例患者的标本超过3 h才报告给相关科室,占17.7%,主要原因是检验科肿瘤标志物项目检测和血浆地高辛浓度项目检测为同一台仪器,标本一般在上午采集,因此当大量标本送到实验室时,血浆地高辛浓度检测的速度明显减慢,因此,应提高工作效率,同时医院可配备高效率自动化仪器以及优化工作流程等来提高检测标本的能力和速度。
本院通过实验室信息系统对患者进行实时监测,当患者的血浆地高辛浓度危急值发生时,检测人员则会尽可能在第一时间完成重复测试危急值项目。根据《医学实验室质量和能力认可准则》,实验室相关人员应在检验科危急值结果登记本上记录:患者姓名、检测日期、病历号、临床联系人、检测结果、标本的接收、检测以及报告的具体时间以及报告人等。对于门诊的急诊患者[15],可通过门诊办公室的信息系统查询患者或者患者家属的联系方式,由相关负责人通知患者进行复诊,以防患者出现危险情况。
对于血浆地高辛浓度危急值的调整,首先一定要慎重,每一次调整都应与临床协作进行严谨的调整和改进,第二是尽可能减少不必要的危急值和使真正的危急值能够危急起来,第三是危急值经过调整后的一定期限内,进行临床随访,保证患者生命安全。本研究显示,血浆地高辛危急值发生率为3.19%,临床工作可以接受,联合部分临床科室进行评估,临床指征和血浆地高辛浓度危急值的符合率为67.7%。因此将血浆地高辛浓度大于2.5 ng/mL作为危急值界限可继续使用。
[1] Eyer F,Steimer W,Nitzsche T,et al. Intravenous application of an anticalin dramatically lowers plasma digoxin levels and reduces its toxic effects in rats[J]. Toxicol Appl Pharmacol, 2012,263(3):352-9.
[2] Neuhoff S,Yeo KR,Barter Z,et al. Application of permeability-limited physiologically-based pharmacokinetic models: Part I-digoxin pharmacokinetics incorporating P-glycoprotein-mediated efflux[J]. J Pharm Sci,2013,102(9):3145-60.
[3] 林瑶,胡尧. 血浆地高辛浓度危急值的应用与评估[J]. 标记免疫分析与临床,2014,21(6):770-2.
[4] Cawello W,Mueller-Voessing C,Andreas J,et al. Effect of lacosamide on the steady-state pharmacokinetics of digoxin: Results from a phase I, multiple-dose, double-blind, randomised, placebocontrolled, crossover trial[J]. Clin Drug Investig,2014,34(5):327-34.
[5] 曾蓉,王薇,王治国,等. 临床实验室危急值报告制度的建立[J]. 中华检验医学杂志,2012,35(4):380-1.
[6] 刘灿,王炳龙,林寿榕,等. 临床实验室危急值的应用研究[J]. 中华检验医学杂志,2013,36(6):565-8.
[7] Shojiro O,Hiroshi O,Shinji N,et al. Relation of n-Value to Critical Current for Local Sections and Overall Sample in a SmBCO Coated Conductor Pulled in Tension[J]. Mater Trans,2014,55(3):549-55.
[8] 朱铭. 常规检验中危急值复查结果及回报时间分析[J]. 山东医药,2014,54(25):94-6.
[9] Ochiai S,Okuda H,Fujimoto M,et al. Analysis of the correlation between n-value and critical current in bent multifilamentary Bi2223 composite tape based on a damage evolution model[J]. Supercond Sci Tech,2012,25(5):54016-25.
[10] 孙杰,徐炜新,任军,等. 信息化管理背景下建立检验危急值报告追踪预警机制的研究[J]. 检验医学,2014,29(4):380-3.
[11] Jingli X,Zhiguo L. Existence of three distinct solutions to boundary value problems of nonlinear differential equations with a p-Laplacian operator[J]. Appl Math Lett,2014,27(12):101-6.
[12] Oga EF,Sekine S,Horie T,et al. Ex vivo and in vivo investigations of the effects of extracts of Vernonia amygdalina, Carica papaya and Tapinanthus sessilifolius on digoxin transport and pharmacokinetics:Assessing the significance on rat intestinal P-glycoprotein efflux[J]. Drug Metab Pharmacokinet,2013,28(4):314-20.
[13] 陈淑琴,李雪姣,米东,等. 危急值报告制度在妇产科医院临床中的应用分析[J]. 山东医药,2013,53(44):49-51.
[14] ThangaMariappan T,Kurawattimath V,Gautam SS,et al. Estimation of the unbound brain concentration of P-glycoprotein substrates or nonsubstrates by a serial cerebrospinal fluid sampling technique in rats[J]. Mol Pharm,2014,11(2):477-85.
[15] 宋世平,陈建魁,马红雨,等. 应用危急值报告制度促进检验科质量管理[J]. 国际检验学杂志,2012,33(20):2519-21.
本文编辑:杨新颖,姚雪莉
Effects evaluation of critical value of digoxin concentration in plasma
PENG Qiong. Clinical Laboratory, Jingmen First People's Hospital, Jingmen, Hubei, 448000, China.
Objective To evaluation effects of critical value of digoxin concentration in plasma. Method Clinical data of critical value of digoxin concentration in plasma was screened out from laboratory information system of Jingmen First People's Hospital. The occurrence rate, department distribution and daily distribution of critical value of digoxin concentration in plasma were calculated. The range and turnaround time for critical value of digoxin concentration in plasma was analyzed. Results The occurrence rate of critical value of digoxin concentration in plasma was 3.19%, and was highest between 3pm and 5pm. The department of cardiology was department with highest occurrence rate. Laboratory turnaround time of 51 patients (82.3%) were less than 3 hours, and coincidence rate was 67.7%. Conclusion Continuous improvement of report procedures of critical value of digoxin concentration in plasma and regular evaluation are important to improve efficiency and provide safety guarantee.
Quality improvement; Critical value; Digoxin concentration in plasma
R541
A
1674-4055(2016)06-0733-03
1448000 荆门,荆门市第一人民医院检验科
doi:10.3969/j.issn.1674-4055.2016.06.27
1.3地高辛浓度危急值设定 血浆地高辛浓度危急值设定参照第三版《全国临床实验操作规程》和College of American Pathologists有关的危急值范围的调查报告以及相关文献,包括Critical Lab Values(Saint Joseph Health System)、Critical Value Notification(MCLNO Pathology Services)、Critical Values(Department of Laboratory Medicine University of Washington)、Critical Value (Massacheusetts General Hospital)等,在结合相关科室专家的意见和建议,将血浆地高辛浓度危急值设定为大于2.5 ng/mL。
1.4统计学方法 所有数据均采用SPSS 17.0和Excel软件进行分析,计数资料采用例数(构成比)表示。
