香石竹RNAi载体的转化体系对转基因抗性芽分化的影响
2016-08-10徐笑寒李枝林蒋亚莲卢珍红余蓉培周旭红
徐笑寒,李枝林,蒋亚莲,卢珍红,余蓉培,周旭红*
(1.云南农业大学 园林园艺学院,云南 昆明 650201;2.云南省农业科学院 花卉研究所,云南 昆明 650205;3.国家观赏园艺工程技术研究中心,云南 昆明 650601)
香石竹RNAi载体的转化体系对转基因抗性芽分化的影响
徐笑寒1,李枝林1,蒋亚莲2,3,卢珍红2,3,余蓉培2,3,周旭红2,3*
(1.云南农业大学 园林园艺学院,云南 昆明 650201;2.云南省农业科学院 花卉研究所,云南 昆明 650205;3.国家观赏园艺工程技术研究中心,云南 昆明 650601)
摘要:将已构建的与减数分裂相关的OSD1基因的RNAi载体通过农杆菌转化香石竹品种‘Nogalte’,通过正交试验,筛选得出如下最佳转化条件:预培养4 d、黑暗下共培养5 d、农杆菌菌液浓度OD600=0.5、共培养基中AS浓度30 mg/L、农杆菌侵染时间30 min。
关键词:基因工程;农杆菌介导;正交试验;香石竹
香石竹(Dianthuscaryophyllus),又名麝香石竹和康乃馨,为石竹科多年生草本植物,是世界四大切花之一,被誉为“母亲节”之花,在花卉市场中占有重要的地位[1]。随着经济和社会的发展,人们对花卉的需求量日益增大,对花卉的色、香、形等奇异的新品种的需求也日益强烈。在农作物新品种育种中,转基因技术具有高效、快捷、目标明确、性状稳定、育种年限短等特点,相比于传统的育种手段有着较大的优势。植物基因工程,又称植物遗传工程(plant genetic engineering)、植物遗传转化(plant genetic transformation)等,是指利用DNA重组(DNA recombination)、细胞组织培养等技术,将外源基因导入植物细胞或组织,进而获得转基因植株的技术方法[3]。正交试验设计和分析方法是目前最常用的工艺优化试验设计和分析方法[2]。我们在研究香石竹转基因体系的建立中,通过正交试验的方法提高了试验效率,得到了令人满意的结论。
已知的研究在单细胞真菌、非洲爪蟾和老鼠的卵母细胞中发现, APC/C(后期促进复合物)是关键的细胞周期修饰物,它同时作用于有丝分裂和减数分裂[4]。OSD1基因家族是在拟南芥中发现的,拟南芥OSD1(At3g57860)基因是有丝分裂APC/C的抑制剂[5],OSD1突变能导致2n配子的形成。2n配子在花卉多倍体育种中起重要作用[6]。利用转基因技术,可沉默与2n配子形成相关的OSD1基因,培育高频2n配子的种质,为香石竹多倍体育种打下基础。
本研究利用已构建的香石竹OSD1基因RNAi载体,通过农杆菌介导的方法对乙酰丁香酮浓度、预培养的时间、菌液浓度、侵染时间及共培养时间对香石竹抗性芽分化的影响进行了优化,建立了最佳转基因再生体系,为香石竹的遗传育种打下了基础。
1材料与方法
1.1正交试验设计
选定影响转基因抗性再生植株频率的5个因素:预培养时间、AS终浓度、共培养时间、菌液浓度、侵染时间,选用L18(37)正交表,绘制了因素水平表(见表1)。
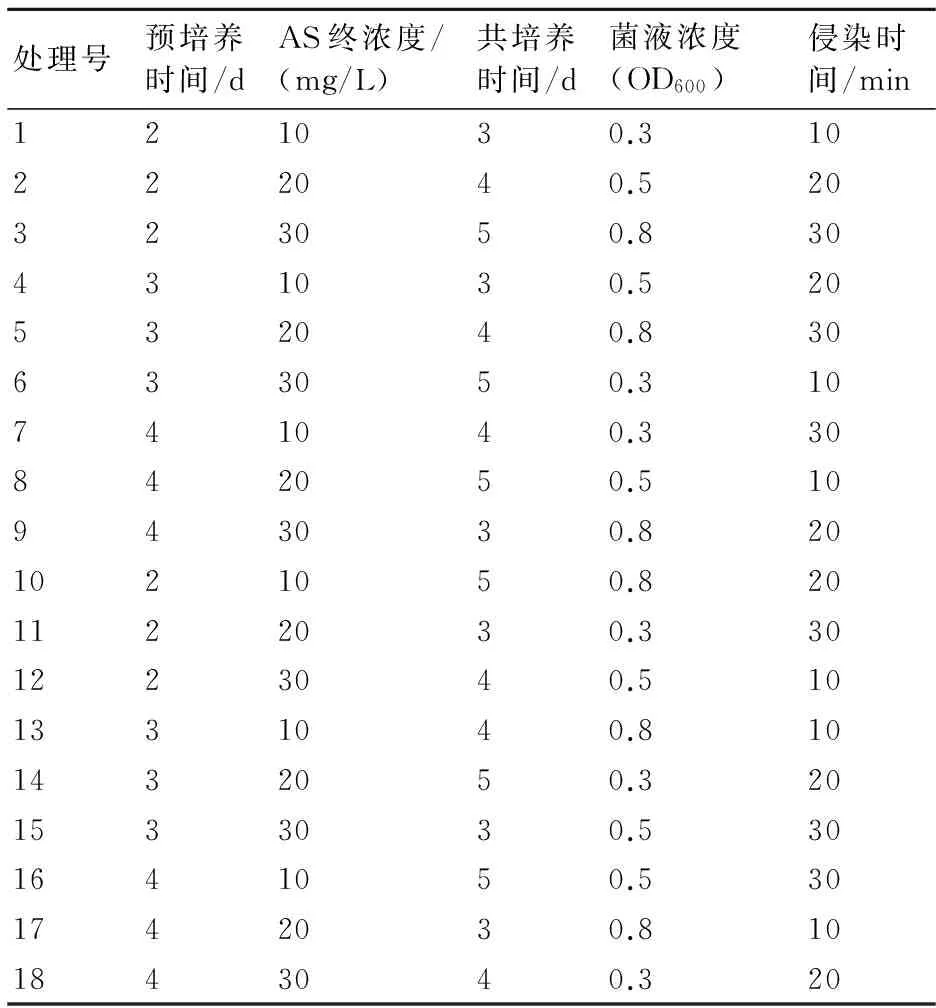
表1 正交试验设计表L18(37)
1.2试验材料和试验仪器
试验材料:香石竹品种‘Nogalte’为云南省农科院花卉研究所基地种植培养。试验仪器:超净工作台、摇床、紫外分光光度计、接种器、镊子、手术刀等。试验试剂: AS(乙酰丁香酮)、TDZ(植物生长调节剂)、NAA(萘乙酸)、MS培养基、km(卡那霉素)、YEB培养基。
1.3试验过程
1.3.1预培养配制含0.22 mg/L TDZ和0.50 mg/L NAA的MS培养基,作为香石竹‘Nogalte’外植体的预培养基。在超净工作台中,切下香石竹茎尖部分约1 cm的两小段(去掉茎尖生长点)作为外植体,将其放入配制好的预培养基中,分别标记好处理号,每个试验设置3个重复,每个重复中放置10个外植体。依据不同的试验组合,放入组培室(23 ℃)中分别光照培养2~4 d。
1.3.2菌液配制将OSD1基因的RNAi干扰载体导入农杆菌EHA105菌株,吸取1 μL的菌液至50 μL的YEB液体培养基中,并加入km(终浓度为50 mg/L),分别放入摇床(28 ℃)中,以200 r/min培养约12、24、40 h,经过紫外分光光度计测试,分别得到OD600=0.3、0.5、0.8这3种新鲜菌液。
1.3.3侵染在超净工作台上将预培养结束的外植体取出,放入10 mL的离心管中,分别加入上述OD600为0.3、0.5、0.8的3种菌液, 在摇床(28 ℃、80 r/min)中侵染10~30 min。
1.3.4共培养在上述预培养基中加入终浓度为10~30 mg/L的AS,作为共培养基。在超净工作台中将侵染完成的外植体从离心管中取出,在吸水纸上先将多余的农杆菌菌液吸干,再根据试验组合放入含不同浓度AS的共培养基中。标记好处理号,依据不同试验组合在培养箱(23 ℃)中暗培养3~5 d。
1.3.5筛选培养配制含0.22 mg/L TDZ、0.50 mg/L NAA和50 mg/L km的MS培养基作为筛选培养基。在超净工作台中,将共培养完成的香石竹外植体接入筛选培养基中,放入组培室(23 ℃)继续培养。
2结果与分析
采用SPSS 20.0软件统计香石竹外植体分化形成的愈伤组织数、愈伤组织的状态、愈伤组织分化形成的植株数和分化植株的状态,结果见表2和图1。由图1可见:将经农杆菌侵染的外植体放入筛选培养基上(图1a),2~5 d后,外植体开始膨大(图1b),形成黄色或黄绿色的疏松愈伤组织(图1c~图1d);培养20 d左右时,黄绿色的愈伤组织开始分化成植株(图1e),有些分化植株为正常的绿色植株(图1f),有些植株出现玻璃化和白化现象(图1g),少数植株叶片边缘出现褐化现象(图1h),大多数植株都呈现玻璃化状态(图1i)。
由表2可见,香石竹茎尖愈伤形成率很高,最高可达100%,最低为22.22%,分化植株的愈伤比例从12.50%至73.33%,每个愈伤分化的植株数为1.67~55.00棵。其中,12号处理分化植株的愈伤比例最高,13号处理每个愈伤分化的植株数最多;刚分化出来的愈伤大多数为黄绿色疏松的胚性愈伤,由愈伤分化的植株大多数呈玻璃化状态。
从表3中可以看出:预培养4 d的愈伤形成率和愈伤组织分化植株的比率最高;分化植株数以预培养2 d最高,预培养2、3和4 d间无显著差异。综合考虑,选择预培养4 d为最佳预培养天数。
当AS终浓度为10 mg/L时愈伤形成率和分化植株数最高;当AS终浓度为30 mg/L时愈伤组织分化植株的比率最高。从愈伤组织分化植株比率的角度来看,共培养基中AS浓度以30 mg/L为宜。
当共培养时间为3 d时,愈伤形成率最高;当共培养时间为5 d时,愈伤组织分化植株的比率最高;当共培养时间为4 d时,愈伤组织分化植株数最多。从愈伤组织分化植株比率的角度来看,共培养时间以5 d为宜。
当菌液浓度OD600=0.8时,愈伤形成率最高;当菌液浓度OD600=0.5时,愈伤组织分化植株的比率和愈伤组织分化的植株数最高。综合考虑,菌液浓度OD600=0.5为最佳农杆菌侵染的浓度。
当侵染时间为30 min时,愈伤形成率和愈伤组织分化植株的比率最高;当侵染时间为10 min时,愈伤组织分化的植株数最多。综合考虑,菌液侵染时间30 min为最佳侵染时间。

a:刚开始筛选的外植体; b:外植体开始膨大; c:黄色的疏松愈伤组织; d:黄绿色的疏松愈伤组织; e:黄绿色愈伤组织开始分化形成植株; f:绿色正常的分化植株; g:白化和绿色玻璃化的分化植株; h:绿色玻璃化且边缘褐化的分化植株; i:绿色玻璃化的分化植株。图中标尺长度为1 cm。
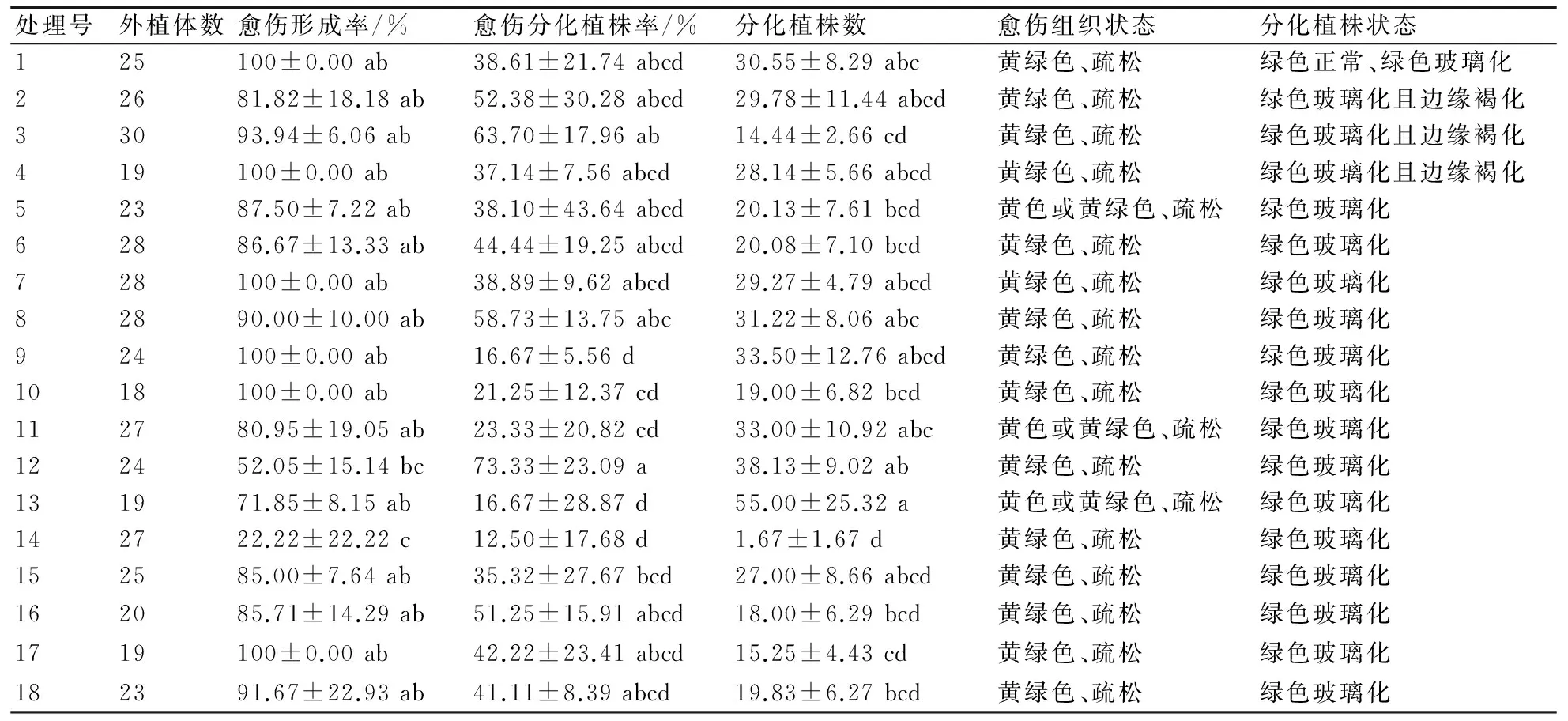
图1 转基因香石竹抗性芽的再生
3讨论
3.1香石竹转化条件的筛选
预培养在提高植物的遗传转化率中发挥重要作用,预培养有利于促进植物创伤口处的细胞分裂,分裂状态的细胞更容易整合外源DNA,从而提高外源基因的瞬时表达和转化率。在根癌农杆菌介导的ACC氧化酶基因转化香石竹幼叶的研究中,最佳转化条件是预培养2 d[7]。Kanwar J K等的试验表明4 d是外植体分化愈伤组织的最佳预培养时间[8]。在本试验中,最佳预培养时间也为4 d。
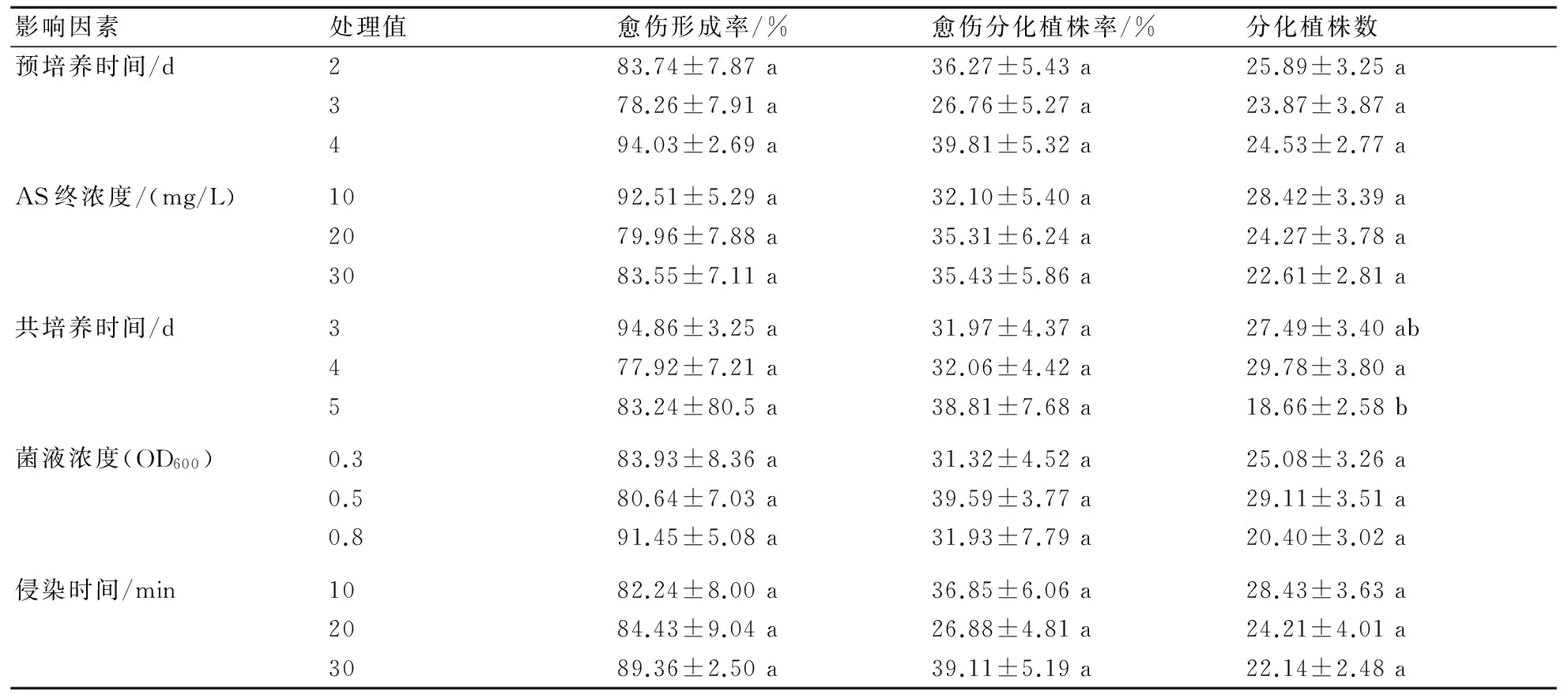
表3 各试验因素对香石竹愈伤组织形成及分化的影响
3讨论
3.1香石竹转化条件的筛选
预培养在提高植物的遗传转化率中发挥重要作用,预培养有利于促进植物创伤口处的细胞分裂,分裂状态的细胞更容易整合外源DNA,从而提高外源基因的瞬时表达和转化率。在根癌农杆菌介导的ACC氧化酶基因转化香石竹幼叶的研究中,最佳转化条件是预培养2 d[7]。Kanwar J K等的试验表明4 d是外植体分化愈伤组织的最佳预培养时间[8]。在本试验中,最佳预培养时间也为4 d。
农杆菌和外植体共培养是整个转化过程中非常重要的环节,它决定着植物细胞与农杆菌是否相互作用。农杆菌附着、T-DNA的转移及外源基因的整合都在共培养时期进行。前人的研究表明适宜的共培养时间为3~4 d[8]。本试验的最佳共培养时间为5 d。
共培养是Ti质粒实现T-DNA转化的途径,而乙酞丁香酮(AS)对Vir区基因的活化具有重要的作用。本实验经过测定,得出在添加30 mg/L AS的培养基中进行共培养,能获得较高的抗性植株百分率。
农杆菌的侵染时间及菌液浓度对遗传转化起着非常重要的作用。若外植体在菌液中浸泡时间太短,则农杆菌尚未接种到伤口面,在培养时无农杆菌生长,不能转化;如果外植体在菌液中浸泡时间太长,则容易出现污染。故要选择合适的农杆菌的浓度及侵染时间。本实验得出菌液浓度OD600=0.5、侵染时间30 min为最佳条件。
3.2外植体材料的选择
香石竹再生体系多选用叶片为外植体[7,9-10]。而本实验以茎尖作为外植体也能获得较高的再生率,而以叶片为外植体获得再生植株的数量少(实验结果未发表)。这可能是因为顶芽主要由分生组织构成,而分生组织是由未分化状态的细胞构成的细胞群体,所以顶芽具有分裂速度快的特点,以茎尖作为外植体能够直接通过器官发生途径产生完整植株,避免经过脱分化和再分化的复杂过程,这样就避免了由于这些复杂过程而引发的突变以及不正常株形的产生。但是也存在着不利因素,由于将农杆菌的T-DNA转入植物细胞中,不能保证转化全部细胞,所以所得到的转基因植株有可能是完全转化的植株,也有可能是部分被转化的嵌合体植株,而嵌合体是不具有遗传功能的,只能在后期再进行筛选观察。
3.3再生植株玻璃化的防治
香石竹再生植株绝大多数会出现玻璃化,可能是因为从愈伤诱导植株时培养基中所含激素水平过高。因此可将再生植株接入激素水平较低的繁殖培养基中,经过2~3轮的培养,可将玻璃化苗培养成正常的绿色植株[11]。
参考文献:
[1] 余义勋,刘娟旭,包满珠.香石竹植株再生及基因工程研究进展[J].植物学通报,2006,23(1):23-28.
[2] 刘瑞江,张业旺,闻崇炜,等.正交试验设计和分析方法研究[J].实验技术与管理,2010,27(9):52-55.
[3] 傅荣昭,刘敏,梁红健,等.通过根瘤农杆菌介导法获得菊花转基因植株[J].植物生理学报,1998,24(1):72-76.
[4] Pesin J A, Orr-Weaver T L. Regulation of APC/C activators in mitosis and meiosis[J]. Cellbio, 2008, 24: 475-499.
[5] Iwata E, Ikeda S, Matsunaga S, et al. GIGAS CELL1, a novel negative regulator of the anaphase-promoting complex/cyclosome, is required for proper mitotic progression and cell fate determination inArabidopsis[J]. Plant Cell, 2011, 23(12): 4382-4393.
[6] d'Erfurth I, Cromer L, Jolivet S, et al. The CYCLIN-A CYCA1;2/TAM is required for the meiosis I to meiosis II transition and cooperates with OSD1 for the prophase to first meiotic division transition[J]. PLoS Genet, 2010(6): e1000989.
[7] 余义勋.根癌农杆菌介导的ACC氧化酶基因转化香石竹的研究[D].武汉:华中农业大学,2004:48-51.
[8] Kanwar J K, Kumar S. Recovery of transgenic plants byAgrobacterium-mediated genetic transformation inDianthuscaryophyllusL. (carnation)[J]. Pelagia Research Library, 2011, 2(2): 357-366.
[9] 苏晓瑜.香石竹再生体系的建立及根癌农杆菌介导的遗传转化体系的研究[D].重庆:西南大学,2007:33-36.
[10] 刘彩霞.香石竹ACC氧化酶基因RNAi载体构建及其遗传转化研究[D].北京:中国林业科学研究院,2007:38-39.
[11] 周旭红,桂敏,莫锡君,等.一种香石竹组培快繁的方法:中国,103461139A [P].2013-12-25.
(责任编辑:黄荣华)
收稿日期:2016-01-04
基金项目:国家自然科学基金项目(31460530、31260491);国家观赏园艺工程技术研究中心项目(2012FU125X10);云南省应用基础研究计划(2014FA044);云南省中青年学术和技术带头人培养计划(2015HB077)。
作者简介:徐笑寒(1989─),男,浙江杭州人,硕士生,主要从事观赏植物资源利用与创新研究。*通讯作者:周旭红。
中图分类号:S681.5
文献标志码:A
文章编号:1001-8581(2016)07-0027-05
Influence of RNAi Vector Transformation System on Differentiation of Transgenic Resistant Buds of Carnation
XU Xiao-han1, LI Zhi-lin1, JIANG Ya-lian2,3, LU Zhen-hong2,3, YU Rong-pei2,3, ZHOU Xu-hong2,3*
(1. College of Horticulture and Landscape, Yunnan Agricultural University, Kunming 650201, China; 2. Flower Research Institute, Yunnan Academy of Agricultural Sciences, Kunming 650205, China; 3. National Engineering Research Center for Ornamental Horticulture, Kunming 650601, China)
Abstract:The RNAi vector of OSD1 gene which was connected with meiosis was constructed and integrated into carnation cultivar ‘Nogalte’ by Agrobacterium-mediated genetic transformation. Through orthogonal test, the optimal transformation conditions were screened out as follows: pre-culture for 4 days, co-cultivation in dark for 5 days, concentration (OD600) of Agrobacterium suspension solution being 0.5, concentration of AS (acetosyringone) in co-cultivation medium being 30 mg/L, and infection time of Agrobacterium being 30 min.
Key words:Genetic engineering; Agrobacterium-mediated transformation; Orthogonal test; Carnation
