新型深度共熔溶剂选择性分离木质素的研究*
2016-08-08常杰刘钧郭姝君王曦付严
常杰 刘钧 郭姝君 王曦 付严
(华南理工大学 化学与化工学院, 广东 广州 510640)
新型深度共熔溶剂选择性分离木质素的研究*
常杰刘钧郭姝君王曦付严
(华南理工大学 化学与化工学院, 广东 广州 510640)
近年来,以胆碱类为代表的生物基离子液体作为木质素的优良溶剂逐渐受到广泛关注.文中基于Hansen溶解理论,设计出一种分别以乳酸(LA)和氯化胆碱(ChCl)为氢键供受体的新型离子液体——深度共熔溶剂(DES)作为木质素分离的溶剂.通过实验考察了常压下ChCl/LA摩尔比、温度、时间对木质素溶解效果的影响,确定了最佳工艺条件为ChCl/LA摩尔比1∶9、温度90 ℃、时间12 h,此时木质素的溶解率达90.1%,再生木质素纯度为96.3%.紫外可见光谱(UV)及红外光谱(FT-IR)分析表明木粉中木质素经DES处理后被大量脱除;X射线衍射分析表明经预处理后的木粉中纤维素结构基本未被破坏;核磁共振谱(13C NMR)分析表明再生木质素由紫丁香基、愈创木基及少量对羟苯基结构单元组成;离子色谱分析结果表明该混合溶液中的综纤维素只有少量发生溶解.
木质素;深度共熔溶剂;氯化胆碱;乳酸;Hansen参数
木质素是自然界中含量仅次于纤维素的生物质资源之一,是唯一可再生的含芳香结构的物质.木质素用途广泛,可用作混凝土减水剂、选矿浮选剂、冶炼矿粉粘结剂、 耐火材料等,应用前景巨大.制浆造纸工业每年要从植物中分离出约1.4亿吨纤维素,同时得到5 000万吨左右的木质素副产品,但迄今为止,超过95%的木质素仍以黑液直接排入江河或直接烧掉,造成了严重的环境污染和资源浪费.木质素结构复杂,一般溶剂难以将其溶解,因此,找到一种能够有效选择性溶解木质素的溶剂,是将其充分利用的重要前提[1- 3].
近些年来,离子液体为预处理木质纤维素开拓了新方向[4].咪唑类离子液体在木质纤维素分离研究中应用最为广泛,也取得了一定的成果.例如,余华明[5]结合离子液体与有机溶剂的优点设计了离子液体1-丁基-3甲基咪唑溴盐[BMIM]Br与乙醇的混合体系选择性分离松木组分,在170 ℃下反应得到了纯度为93%的木质素.然而,这些传统的咪唑类离子液体的生产来源是化石能源,生产过程本身就对环境有一定程度的污染,且其价格高,毒性较大,难以生物降解,工业化前景并不被大家看好[6- 7],因此寻找一种更为绿色、更为廉价的离子液体十分重要.
2001年,由氯化胆碱(ChCl)与氢键供体组成的深度(低温)共熔溶剂(DES)被制备出[8].胆碱类低温共熔溶剂是生物基离子液体,除了具备传统离子液体的优良特性之外,还具有低毒、可生物降解、价格低廉、易于制备等特点,工业前景广阔[9].DES通常是由一定化学计量比的氢键受体(如季铵盐)和氢键供体(如羧酸、多元醇)组合而成的两组分或三组分低温共熔混合物,凝固点显著低于各个组分纯物质的熔点[10].Francisco等[11]以氨基酸、氯化胆碱、苹果酸等为原料,制备出了多种DES溶剂,同时发现某些DES对木质素的溶解性好,对纤维素几乎不溶解,对半纤维素的溶解能力也比较差,且合成方便,将二者以一定比例混合加热搅拌即可获得;此外,DES可以通过改变氢键供受体对的摩尔比来实现对木质纤维素的选择性溶解,操作性较强[12].因此,本研究采用DES作为选择性分离木质素的溶剂.
DES种类繁多,但并非每种DES都能够有效溶解木质素,无针对性的实验尝试会造成浪费,因此本研究采用Hansen 溶解理论作为设计溶剂的理论基础和预测模型.基于Hansen溶解理论,氢键供受体分别选择DL-乳酸(LA)和氯化胆碱.以尾叶桉为原料,分别考察了ChCl/LA摩尔比、 温度、时间等因素对木质素溶解效果的影响,确定了最佳工艺条件,并对此条件下的产物、原料、残渣及溶液分别进行了UV、FT-IR、XRD、13C NMR、IC分析.
1 溶剂的设计
1.1Hansen溶解理论
Hansen溶解理论对极性溶剂具有很强的适用性[13].Hansen认为,分子间相互作用力可以分为色散力、极性力、氢键力.溶剂和溶质的Hansen 溶度参数的3个分量分别接近才可以相溶,相应的溶度参数计算公式为
(1)
式中,Ed、Ep、Eh分别为色散力、极性力与氢键力的内聚能分,V为摩尔体积,δ为Hildebrand溶度参数,δd为色散力参数,δp为极性力参数,δh为氢键力参数.
Hansen[14]提出了一个三维球理论来确定聚合物的溶度参数.由于色散力差别较小,以色散力参数的2倍值2δd、极性力参数δp和氢键力参数δh为球心,以聚合物溶解半径Ro为半径作三维球,若溶剂的这3个参数值所确定的坐标点落在此球内部,则表明溶剂可溶解该聚合,数学公式如下:
(2)
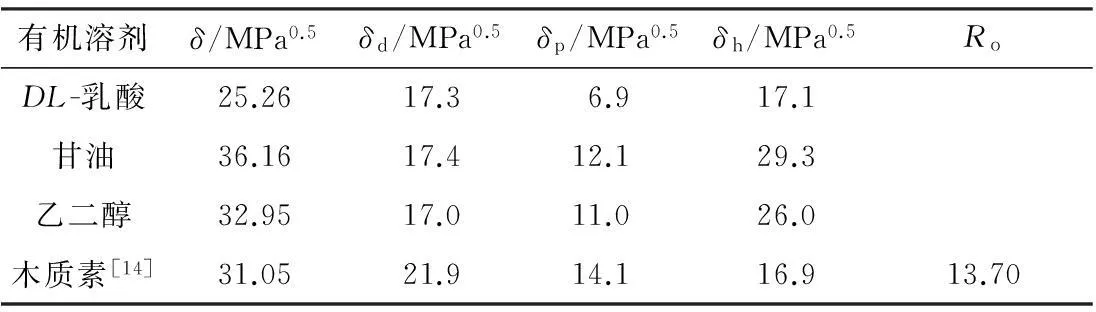
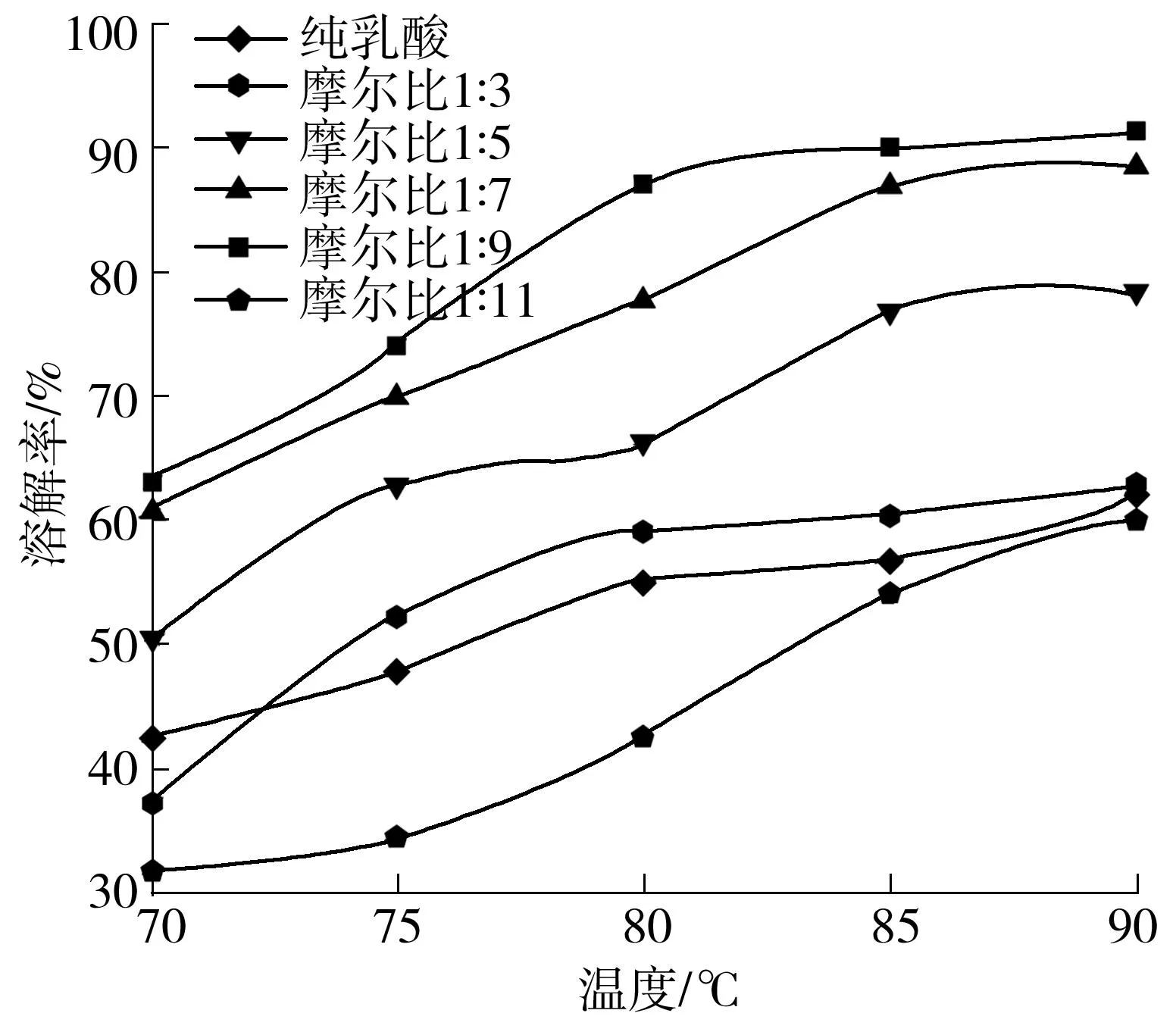
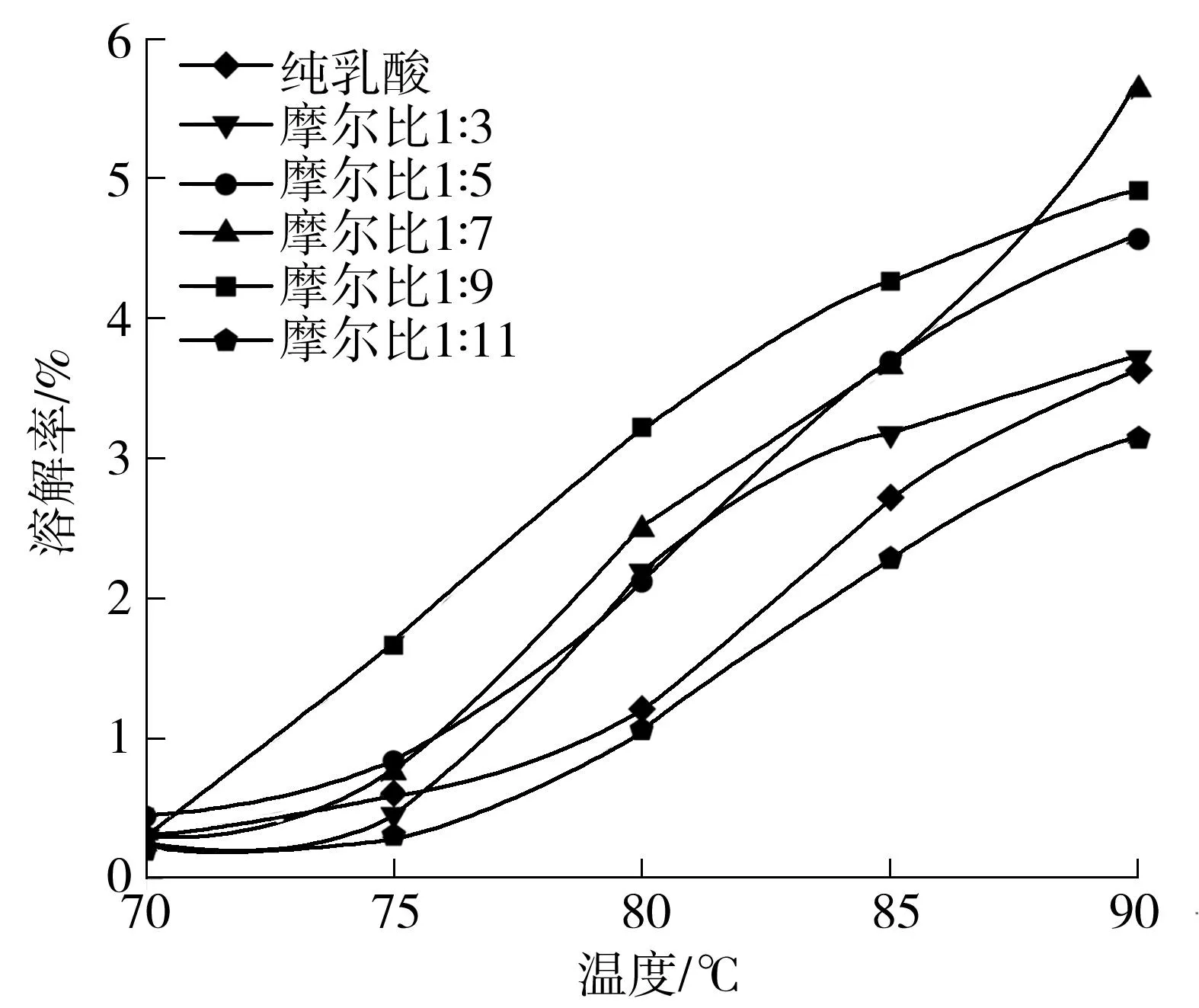
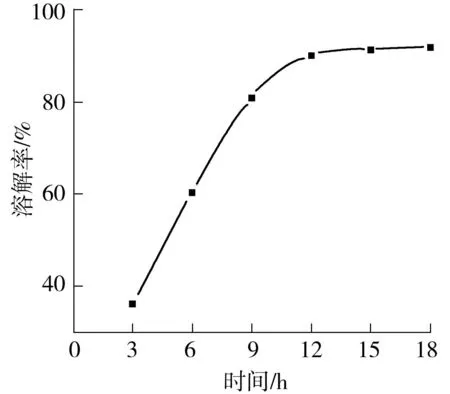
其中,Ri为溶剂与溶质在三维图中的距离,下标s和l分别代表溶剂和聚合物.当Ri 1.2溶剂的选择 氢键供体的选择最重要的是溶解参数值合适.常见的价格低廉的氢键供体有甘油、乙二醇、乳酸等.基于基团贡献法,可分别计算出三者的溶解参数.通过式(3)、(4)及表1,可计算出δ及δd. (3) (4) 式中Fi为第1类基团中基团i的贡献,Sj为第2类基团中基团j的贡献值,mj、ni分别为基团j、i的个数. 表1 第1类基团对δ及δd的贡献值[14]1) 1)甘油、 乙二醇、 乳酸分子中无第2类基团. 对于δp,Wu等[15]给出一个简化的计算公式: (5) 式中,μ为偶极矩. 25 ℃时DL-乳酸、甘油、乙二醇及木质素的Hansen参数值如表2所示. 表2 25 ℃时DL-乳酸、甘油、乙二醇及木质素的Hansen参数值 将表2数值代入式(2),计算得到乳酸、甘油、乙二醇的Ri分别为8.55、15.45、13.73,因此,从理论上讲,25 ℃下只有乳酸(Ri<13.70)可以溶解木质素. 由于本实验在70~90 ℃下进行,温度升高会导致Hansen参数的变化[14].但当温度升高时,木质素的溶解率一般会上升[16];另外,氯化胆碱作为季铵盐,具有相催化转化的性质,能在一定程度上降低固相中溶质的表面能[17],理论上会更加促进木质素的溶解. 2.1材料与仪器 原料:尾叶桉,产自贵港市南郊区,其灰分、木质素、半纤维素、纤维素、抽出物及水分含量分别为1.73%、28.20%、24.32%、42.11%、1.38%和1.81%. 试剂:氯化胆碱(纯度≥98.5%),国药集团化学试剂有限公司生产;DL-乳酸(纯度≥90%),天津科密欧试剂有限公司生产;无水乙醇(纯度≥99%),国药集团化学试剂有限公司生产. 实验装置:DF-101D集热式恒温油浴锅,巩义市予华仪器有限责任公司生产;XF-8均相反应器,烟台市招远松岭仪器设备有限公司生产;DHG-9070A电热恒温鼓风干燥箱,上海一恒科学仪器有限公司生产;CAV114C电子天平,上海奥豪斯仪器有限公司生产. 分析仪器:紫外可见分光光度计,日本岛津公司生产;红外光谱仪,美国Nicolet公司生产;X射线衍射仪,德国Bruker公司生产;AVANCE DRX 400型核磁共振仪,德国Bruker公司生产;Dionex ICS-3000型离子色谱仪,美国安捷伦公司生产. 2.2实验方法 2.2.1DES的合成 分别将不同ChCl/LA摩尔比1∶3、1∶5、1∶7、1∶9、1∶11换算成质量比1∶1.94、1∶3.23、1∶4.52、1∶5.81、1∶7.10后,按质量比准确称取总质量500 g的二组分,分别加入到5个1 L圆底烧瓶中混合,置于油浴锅中,在50 ℃下加热1 h使ChCl充分溶解,冷却后分别倒入1 L锥形瓶中于干燥环境中保存备用. 2.2.2原料预处理 取一定量的尾叶桉木粉(40~60目),按照GB/T 2677.6进行苯-乙醇抽提6 h后,将试样放在105 ℃下烘干. 2.2.3影响因素分析 (1)不同摩尔比及温度的影响 按1∶30(g/g)固液比将绝干木粉与纯乳酸、绝干木粉与摩尔比为1∶3、1∶5、1∶7、1∶9、1∶11的 DES分别混合,然后加入到30 mL均相反应器中,固定转速为100 r/min,以上每种混合液均分别在70、75、80、85、90 ℃下反应15 h.反应完成后,将物料过滤分离,所得残渣用无水乙醇多次洗涤,于105 ℃下干燥后称重.然后根据Klason法测出残渣中木质素质量,按照GB/T 2677.10测出残渣中综纤维素质量.被溶解的木质素及综纤维素质量分数按下式计算: (6) (7) 式中,X1、Y1分别为溶解的木质素、综纤维素的质量分数,mL、mC分别为1g原料中木质素、综纤维素的总质量,m1、m2分别为1g原料的残渣中木质素、综纤维素的总质量. (2)反应时间的影响 确定最佳摩尔比和温度后,按1∶30(g/g)固液比将绝干木粉与所确定摩尔比的DES在此温度下混合,然后加入到30mL的均相反应器中,固定转速为100r/min,分别反应3、6、9、12、15、18h,反应完成后将物料过滤分离,残渣用无水乙醇多次洗涤,105 ℃下干燥后称重.根据Klason法测出残渣中木质素质量,按照GB/T2677.10测出残渣中综纤维素质量,按照式(6)、(7)计算. (3)木质素的再生 确定出最佳摩尔比、温度、时间后,将此条件下反应后的混合溶液加入5倍体积的去离子水,静置5h析出溶解的物质,放在干燥箱中于105 ℃下烘干4h,测量析出物中再生木质素含量,析出的木质素质量分数按下式计算: (8) 式中,X2为析出的木质素质量分数,m0为1g原料中析出的木质素的总质量. 2.2.4表征分析 对原料、残渣、混合液、再生木质素分别进行UV、FT-IR、XRD、13CNMR、IC表征分析. 3.1不同ChCl/LA摩尔比及温度对木质素溶解效果的影响 图1和2分别给出了木质素和综纤维素在不同摩尔比的DES和温度下的溶解率变化,从图中可以看出,随温度升高,综纤维素与木质素的溶解率随之增加,其中ChCl/LA摩尔比为1∶9、温度为90 ℃时,木质素溶解率达91.3%,综纤维素溶解率仅为4.9%.这表明在90 ℃时,DES对综纤维素的溶解能力较差,这与Francisco等[11]的研究结果一致.由图1还可以看出,当ChCl/LA摩尔比为1∶5、1∶7、1∶9时,木质素的溶解率明显高于纯乳酸,这也说明ChCl在溶解过程中确实起到了相催化转移的作用.同时溶解率随ChCl/LA摩尔比的变化为:1∶3<1∶5<1∶7<1∶9,这可能是随着ChCl的减少,其黏度降低,对溶剂与木粉之间的传质有利,因此其溶解效果逐渐增强.而ChCl/LA摩尔比为1∶11时最高溶解率仅为60%,这可能是由于ChCl的量对于这1g木粉而言相催化转移作用不太明显,同时又造成LA的相对含量降低,由此导致溶解效果比纯乳酸还差.另外,温度升高可能使得ChCl相催化转移能力增强,促使木质素溶解[17],但反应温度不宜过高,否则可能会导致综纤维素溶解较多,对后续木质素提取及再生木质素纯度不利.从图1可知,90 ℃、ChCl/LA摩尔比1∶9时木质素溶解率最高,达到91.3%,因此,木质素溶解的最佳温度是90 ℃,最佳的DESChCl/LA摩尔比为1∶9. 图1木质素在不同摩尔比的DES及不同温度下的溶解率变化(15h) Fig.1ChangeofdissolutionrateofligninindifferentmoleratiosofDESunderdifferenttemperatures(15h) 图2综纤维素在不同摩尔比的DES及不同温度下的溶解率变化(15h) Fig.2ChangeofdissolutionrateoftotalcelluloseindifferentmoleratiosofDESunderdifferenttemperatures(15h) 3.2反应时间对木质素溶解效果的影响 图3为ChCl/LA摩尔比为1∶9、温度为90 ℃时,不同反应时间对木质素溶解效果的影响.不难看出,在3~12h内,木质素溶解率逐渐变大,由3h溶解36.2%增大至12h的90.1%,而在12~18h内溶解率也有微小的增加(由90.1%增加至91.8%),但是在该6h内溶解率仅仅上升1.7个百分点,说明此时DES对木质素的溶解几乎达到饱和.随着时间的延长,综纤维素的溶解量也会逐渐增加,这仍然对后续木质素再生过程有不利的影响.因此,综合考虑将最佳反应时间定为12h. 图3 不同反应时间下木质素溶解率的变化 Fig.3Changeofthedissolutionrateofligninindifferentreactiontime 1-乙基-3-甲基咪唑醋酸盐[EMIM][OAc]是溶解木质素效果比较好的离子液体之一.Sun等[18]利用[EMIM][OAc]:H2O溶剂体系在150 ℃下处理甘蔗渣,木质素溶解率为46%.Li等[19]利用[EMIM][OAc]处理松木粉,110 ℃下反应16h,木质素溶解率可达90%以上.而本研究所利用的这种新型DES离子液体在90 ℃下即可达到90%以上的溶解率,一定程度上降低了能耗,显示出了一定的优势. 3.3木质素析出量及纯度 准确称取1g木粉在30g摩尔比为1∶9的DES中于90 ℃下反应12h,将混合溶液用无水乙醇洗涤过滤后,加入5倍去离子水,静置5h,过滤烘干,析出的固体质量为0.243 7g,测得其中木质素为0.236 3g,析出木质素的质量分数为92.1%,纯度约为96.3%. 3.4原料、混合液、残渣及木质素的表征分析 3.4.1UV分析 图4为反应后混合溶液的紫外可见光谱图.典型的针、阔叶材木质素的紫外光谱通常在270~280nm及200~208nm处各有一极大吸收值.木质素紫外光谱在280nm附近出现强吸收峰,这是木质素苯环的特征吸收,针叶材、阔叶材木质素由于苯环上取代基不同,最大吸收波长也略有不同.针叶材木质素在波长为280nm处有最大吸收峰,而阔叶材木质素由于含较多高度对称的紫丁香基单元,其最大吸收峰移至275~277nm处[20].由图可见,在275nm处有一个最大吸收峰,这是典型的阔叶材吸收峰.尾叶桉属阔叶材,其木质素含较多的紫丁香基.而图中200~208nm处无吸收峰,却在221nm处有最大吸收峰,这可能是由于乳酸中羧基与木质素中部分酚羟基发生反应在苯环侧链上加入了羰基不饱和键,使吸收峰产生了红移[21]. 图4 混合溶液的紫外可见光谱图 3.4.2FT-IR分析 图5 原料、残渣及再生粗木质素的红外光谱图 与桉木粉相比,残渣的红外光谱图中3 400、2 900、1 600、1 510、1 460、1 158cm-1等处木质素典型的特征吸收峰[20]强度明显减弱,表明木质素被大量脱除. 在再生的粗木质素谱线中,1 505cm-1处吸收峰强度小于1 460cm-1处,1 325cm-1处的吸收峰较强,表明紫丁香基含量较高,1 505cm-1处的吸收峰强度小于1 460cm-1处,1 130cm-1处的吸收峰最强,830cm-1处只有一个吸收峰等特点都符合典型阔叶材木质素的红外光谱图.不同来源的木质素(尤其是阔叶材木质素)均混杂一定量的半纤维素,因此木质素红外光谱中1 710cm-1处为乙酰基和糖醛酸的酯基[20]. 3.4.3XRD分析 图6是桉木粉溶解前后的X射线衍射图.从图中可以看出,原料和残渣的峰型极为相似,无新峰型出现.纤维素的主要信号峰在2θ=22.5°和16°~17°处[23].这表明桉木粉中纤维素为纤维素Ⅰ晶型.由Segal公式得出桉木粉原料的结晶度为38.67%,经DES处理后,残渣结晶度为45.05%,这说明DES的溶解过程基本不破坏纤维素结构,可见溶解的少量综纤维素多为半纤维素,与Francisco等[11]的研究结果一致. 图6 原料桉木粉和未溶解桉木粉残渣的X射线衍射谱图 Fig.6X-raydiffractionspectrogramsofraweucalyptusmaterialandeucalyptusresidue 3.4.413CNMR分析 粗木质素的13CNMR谱图如图7所示,羰基碳位移值在165~200范围内,苯环或双键上的碳位移值在104~162范围内,苯环侧链上的碳位移值在53~87范围内,甲氧基的碳位移值在54~56范围内[20].紫丁香基(S)信号出现在位移值150.78、105.47、103.00处.145.58是愈创木基(G)单元信号,131.99是非醚化S/G单元,117.00、161.00的小信号峰代表对羟苯基单元(H),这表明分离所得木质素由紫丁香基、愈创木基及少量对羟苯基结构单元组成.115.00的信号为对香豆酸酯,说明对香豆酸与木质素通过酯键连接.123.05、122.14对应阿魏酸酯和阿魏酸醚,表明阿魏酸与木质素通过酯键和醚键连接.83.60、65.05处信号峰表明存在β-O-4单元,54.01处为强峰—OCH3[24]. 图7 粗木质素的13C NMR谱图 3.4.5IC分析 准确称取木糖、阿拉伯糖、半乳糖、葡萄糖和甘露糖标准品,用去离子水配制成各单糖浓度分别为2×10-6、4×10-6、6×10-6、8×10-6、10×10-6的系列标准溶液.按一定色谱条件进行测试,以标样浓度为横坐标、标样的峰面积为纵坐标作标准曲线[25].其回归方程和相关系数见表3.从表中可见,阿拉伯糖、半乳糖、葡萄糖、木糖及甘露糖在此测定条件下呈现良好的线性关系. 表3 几种单糖的标准曲线 移取1mL(1.17g)在最佳条件下反应后的混合溶液,定容至500mL容量瓶中,摇匀.取适量溶液经0.22μm的水系微孔滤膜过滤后,按色谱分析条件进样检测[25].根据标准曲线,计算出混合溶液中各种单糖的相对含量,结果见表4. 表4 混合液中单糖的测定结果 根据表4中数据及表3中公式计算可得,1.17g混合溶液中含0.164mg阿拉伯糖、0.101mg半乳糖、0.595mg葡萄糖、0.337mg木糖.原混合溶液(约30g)中溶解的总糖量约为30.70mg,约占原料中综纤维素总糖量的4.62%,说明半纤维素与纤维素溶解较少.IC定量分析表明,DES对木质素的溶解具有较高的选择性,与Francisco等[11]的研究结果一致. 文中以桉木粉为原料,以深度共熔溶剂体系对木质素进行溶解分离,对反应条件进行了优化,由研究结果得到如下结论: (1)基于Hansen溶解理论,运用一种创新的方法设计出了新型深度共熔溶剂ChCl/LA体系,实验证明此溶剂对木质素有高效选择分离的特性,最佳工艺条件如下:ChCl/LA摩尔比1∶9,温度90 ℃、时间12h. (2)用深度共熔溶剂体系处理桉木粉反应温度为90 ℃时即可使木质素溶解率达到90.1%,一定程度上降低了能耗. (3)分离组分的特性分析结果表明,深度共熔溶剂对木质素具有较高选择性,再生木质素纯度达96.3%,且纤维素几乎不被溶解,所得木质素由紫丁香基、愈创木基及少量对羟苯基结构单元组成,残渣中纤维素结构基本没有遭到溶剂破坏. (4)对于经DES处理后的木粉残渣(主要是纤维素和半纤维素),后续工作将利用水热法水解热稳定性较差的半纤维素,进而制备糠醛;同时对纤维素固体残渣进行酶解糖化的研究. [1]邱学青,楼宏铭,杨东杰,等.工业木质素的改性及其作为精细化工产品的研究进展 [J].精细化工,2005,22(3):161- 167. QIUXue-qing,LOUHong-ming,YANGDong-jie,etal.Researchprogressofindustrialligninmodificationanditsutilizationasfinechemicals[J].FineChemicals,2005,22(3):161- 167. [2]蒋挺大.木质素 [M].2 版.北京:化学工业出版社,2009. [3]郑勇,轩小朋,许爱荣,等.室温离子液体溶解和分离木质纤维素 [J].化学进展,2009,21(9):1807- 1812. ZHENGYong,XUANXiao-peng,XUAi-rong,etal.Dissolutionandseparationoflignocellulosewithroom-temperatureionicliquids[J].ProgressinChemistry,2009,21(9):1807- 1812. [4]李昌志,王爱琴,张涛.离子液体介质中纤维素资源转化研究进展 [J].化工学报,2013,64(1):182- 197.LIChang-zhi,WANGAi-qin,ZHANGTao.Progressofconversionofcelluloseresourceinionicliquids[J].ChineseJournalofChemicalEngineering,2013,64(1):182- 197. [5]余华明.基于离子液体的生物质高效分离和改性研究 [D].广州:华南理工大学化学与化工学院,2012. [6]PUY,JIANGN,RAGAUSKASAJ.Ionicliquidasagreensolventforlignin[J].JournalofWoodChemistry&Technology,2007,27(1):23- 33.[7]FRADERF,AFONSOCA.Impactofionicliquidsinenvironmentandhumans:anoverview[J].Human&ExperimentalToxicology,2010,29(12):1038- 1054. [8]ABBOTTAP,CAPPERG,DAVIESDL,etal.Preparationofnovel,moisture-stable,Lewis-acidicionicliquidscontainingquaternaryammoniumsaltswithfunctionalsidechains[J].ChemicalCommunications,2001,19(19):2010- 2011.[9]ABBOTTAP,CAPPERG,DAVIESDL,etal.Novelsolventpropertiesofcholinechloride/ureamixtures[J].ChemicalCommunications,2003,1(1):70- 71. [10]ZHOUQ,SONGY,YUY,etal.Densityandexcessmolarvolumeforbinarymixturesofnaphthenicacidionicliquidsandethanol[J].JournalofChemical&EngineeringData,2010,55(3):1105- 1108. [11]FRANCISCOM,BRUINHORSTAVD,KROONMC.Newnaturalrenewablelowtransitiontemperaturemixtures(LTTMs):screeningassolventsforlignocellulosicbiomassprocessing[J].GreenChemistry,2012,14(8):2153- 2157. [12]FRANCISCOM,ADRIAANVDB,KROONMC.Low-transition-temperaturemixtures(LTTMs):anewgenerationofdesignersolvents[J].AngewandteChemie,2013,52(11):3074- 3085. [13]YUH,HUJ,CHANGJ.SelectiveseparationofwoodcomponentsbasedonHansen'stheoryofsolubility[J].Industrial&EngineeringChemistryResearch,2011,50:7513- 7519. [14]HANSENCM.Hansensolubilityparameters:auser'shandbook[M].BocaRaton:CRCPress,2007.[15]WUPL,BEERBOWERA,MARTINA.ExtendedHansenapproach:calculatingpartialsolubilityparametersofsolidsolutes[J].JournalofPharmaceuticalSciences,1982,71(11):1285- 1287. [16]BADGUJARKC,BHANAGEBM.Factorsgoverningdissolutionprocessoflignocellulosicbiomassinionicliquid:Currentstatus,overviewandchallenges[J].BioresourceTechnology,2015,178:2- 18.[17]徐寿昌.有机化学 [M].2版.北京:高等教育出版社,2014. [18]SUNYC,XUJK,XUF,etal.Dissolution,regenerationandcharacterisationofformicacidandAlcelllignininionicliquid-basedsystems[J].RSCAdvances,2013,4(6):2743- 2755. [19]LIW,SUNN,STONERB,etal.Rapiddissolutionoflignocellulosicbiomassinionicliquidsusingtemperaturesabovetheglasstransitionoflignin[J].GreenChemistry,2011,3(8):2038- 2047. [20]李忠正.植物纤维资源化学 [M].北京:中国轻工业出版社,2012. [21]王键,王燕.棉秆木质素的光谱分析 [J].林产化学与工业,2009,29(1):115- 119. WANGJian,WANGYan.Studyofinfraredspectroscopicanalysisofcottonstalkfiber[J].Chemistry&IndustryofForestProducts,2009,29(1):115- 119. [22]郭斌,龙金星,王芙蓉,等.亚临界水中离子液体催化蔗渣液化残渣分析 [J].化工学报,2012,63(8):2425- 2430.GUOBin,LONGJin-xing,WANGFu-rong,etal.Analysisofresiduefromcatalyticliquefactionofbagassewithacidicionicliquidinsubcriticalwater[J].ChineseJournalofChemicalEngineering,2012,63(8):2425- 2430.[23]徐绍华,武书彬,尉慰奇.桉木三组分在高温热水预处理及酶解糖化中的规律研究 [J].林产化学与工业,2013,33(1):21- 26. XUShao-hua,WUShu-bin,WEIWei-qi.Thechangesofthree-componentsineucalyptusduringprocessesofpre-processinginhightemperatureliquidwaterandenzymo-lysis[J].Chemistry&IndustryofForestProducts,2013,33(1):21- 26. [24]张斌,武书彬,阴秀丽,等.酸水解木质素的结构及热解产物分析 [J].太阳能学报,2011,32(1):19- 24. ZHANGBin,WUShu-bin,YINXiu-li,etal.Structureandpyrolysisproductsanalysisofacidhydrolysislignin[J].ActaEnergiaeSolarisSinica,2011,32(1):19- 24. [25]彭云云,武书彬,程江娜,等.离子色谱法测定蔗渣半纤维素中的单糖及糖醛酸含量 [J].造纸科学与技术,2009,28(5):10- 12,86. PENGYun-yun,WUShu-bin,CHENGJiang-na,etal.Determinationofmonosaccharidesanduronicacidsinbagassehemicellulosehydrolyzatebyionchromatography[J].PaperScience&Technology,2009,28(5):10- 12,86. InvestigationintoSelectiveSeparationofLignininNovelDeepEutecticSolvent CHANG JieLIU JunGUO Shu-junWANG XiFU Yan (SchoolofChemistryandChemicalEngineering,SouthChinaUniversityofTechnology,Guangzhou510640,Guangdong,China) Inrecentyears,choline,anovelkindofbio-basedILs(IonicLiquids)usedasagoodligninsolvent,hasbeenpaidmoreandmoreattentionto.Inthispaper,basedonHansen’stheoryofsolubility,anovelionicliquidanaloguenamedDES(DeepEutecticSolvent),inwhichlacticacid(LA)andcholinechloride(ChCl)wererespectivelyusedasthedonorandtheacceptorofhydrogenbonds,wasdesignedtoseparatelignin.Then,thedissolutionresultsofligninaffectedbythemolarratioofChCltoLA,thereactiontemperatureandtheinteractiontimewereinvestigatedbyexperiments.Itwasfoundthatthedissolutionrateofligninreachedtheoptimal90.1%andthepurityofregeneratedligninreached96.3%ataChCl-to-LAmolarratioof1∶9,areactiontemperature90 ℃andareactiondurationof12h.TheresultsofUV-VisspectroscopyandFT-IRspectroscopyshowthatthelignininthewoodpowdersisgreatlyremovedafterDEStreatment.XRDresultsshowthatthestructureofcelluloseinthepretreatedwoodpowdersisbarelydamaged.13CNMRresultsindicatethattheregeneratedligninismainlycomposedofsyringyl,guaiacylandalittlep-hydroxylphengl.Moreover,ionchromatographyresultsshowthatonlyasmallamountofholocelluloseisdissolvedinthemixedsolution. lignin;deepeutecticsolvent;cholinechloride;lacticacid;Hansenparameter 2015- 12- 07 国家自然科学基金资助项目(21476090);国家重点基础研究发展计划(973计划)项目(2013CB228104);华南理工大学中央高校基本科研业务费专项资金资助项目 常杰(1968-),男,教授,博士生导师,主要从事生物基材料与能源研究.E-mail:changjie@scut.edu.cn 1000- 565X(2016)06- 0014- 07 TQ 028.9 10.3969/j.issn.1000-565X.2016.06.003 Foundation items: Supported by the National Natural Science Foundation of China(21476090)and the National Program on Key Basic Research Project of China(973 Program)(2013CB228104)
2 原料与实验方法
3 结果与讨论

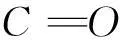

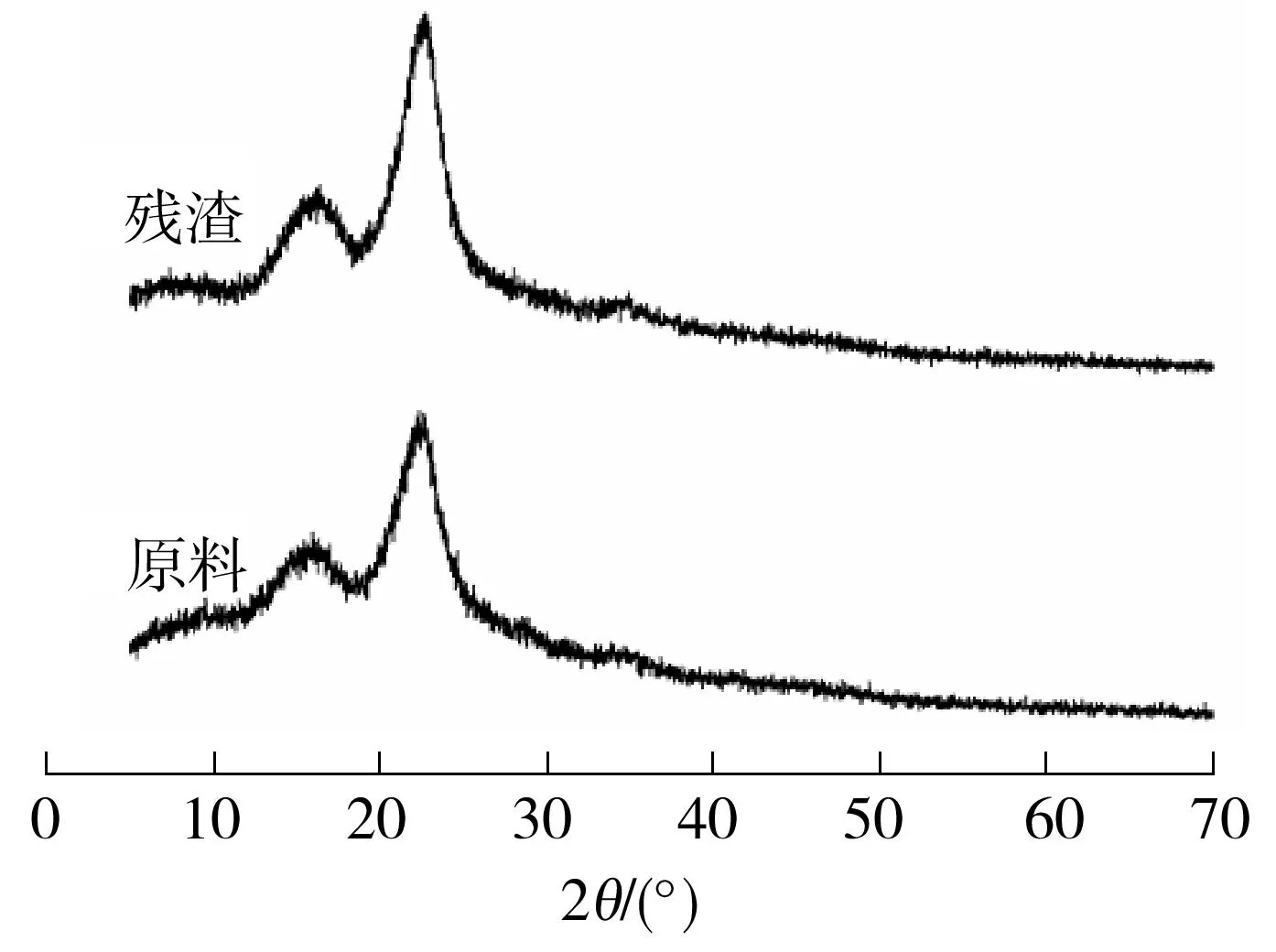
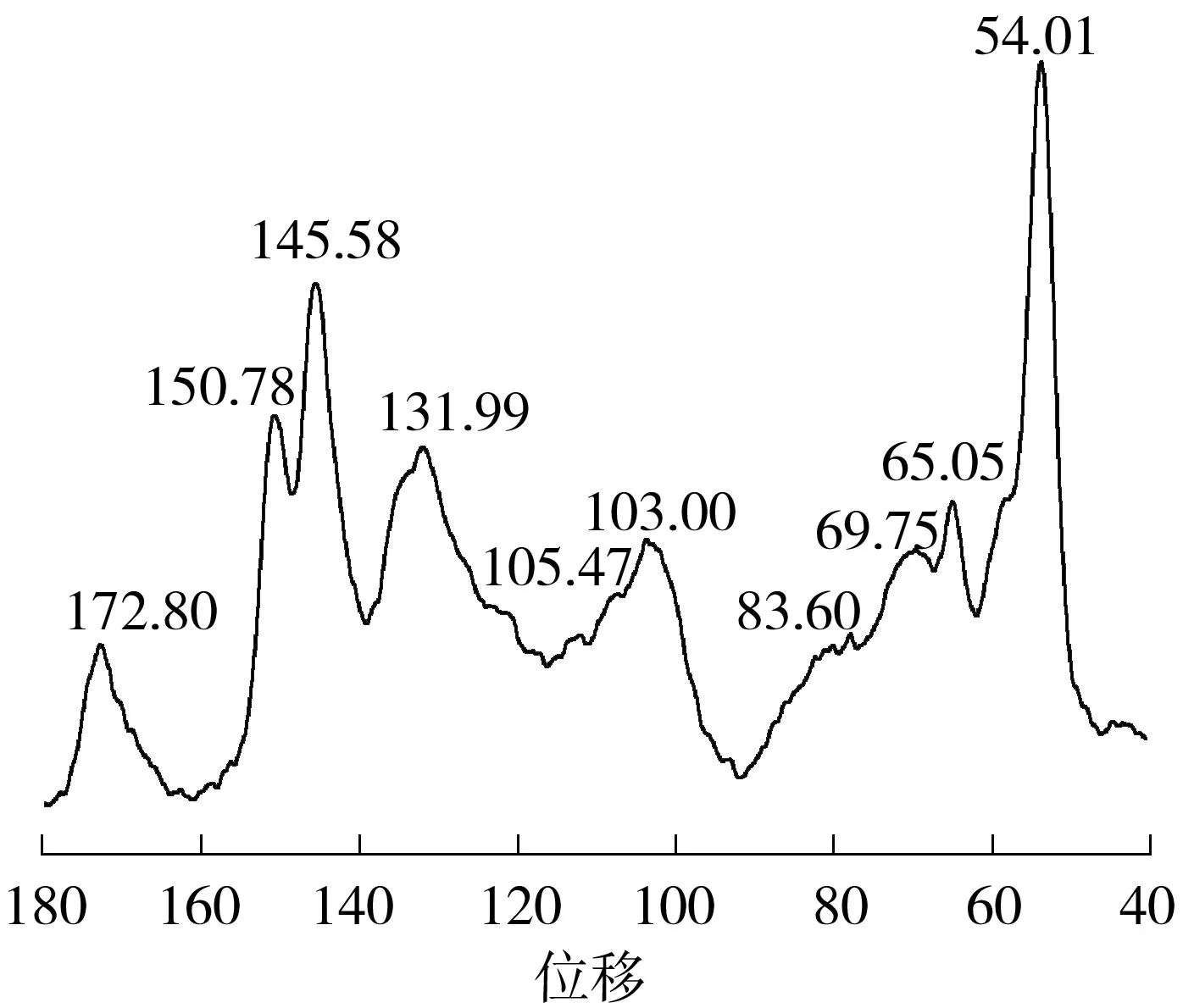


4 结论
