成人特发性膜性肾病血清抗M型磷脂酶A2受体抗体与病情的相关性研究
2016-08-08张丽丽王祥范小丽王晓丽赵军
张丽丽,王祥,范小丽,王晓丽,赵军
(1.潍坊医学院,山东 潍坊 261042;2.山东省潍坊市人民医院,山东 潍坊 261000)
成人特发性膜性肾病血清抗M型磷脂酶A2受体抗体与病情的相关性研究
张丽丽1,王祥1,范小丽1,王晓丽1,赵军2
(1.潍坊医学院,山东 潍坊 261042;2.山东省潍坊市人民医院,山东 潍坊 261000)
目的通过研究成人特发性膜性肾病(IMN)血清抗M型磷脂酶A2受体(PLA2R)抗体的阳性滴度与其他实验室指标的相关性,进一步探讨抗PLA2R抗体对IMN诊断及病情评估的作用。方法选取B超引导下肾穿刺活检证实为IMN患者55例,追踪观察6个月,同时选取15例健康体检者为对照组,应用酶联免疫吸附法(ELISA)检测血清抗PLA2R抗体,同时对IMN患者24 h尿蛋白定量、血清总蛋白、血清白蛋白、血清总胆固醇、血清肌酐进行检测。结果经过3和6个月治疗后,血清抗PLA2R抗体较治疗前降低(P<0.05)。55例IMN患者治疗前血清抗PLA2R抗体阳性患者47例,阳性率为85.45%;治疗3个月后血清抗PLA2R抗体阳性患者36例,阳性率为65.45%,治疗6个月后血清抗PLA2R抗体阳性患者25例,阳性率45.45%。且治疗前血清抗PLA2R抗体滴度与尿蛋白定量呈正相关,与血清白蛋白、总蛋白呈负相关;治疗6个月后血清抗PLA2R抗体滴度与尿蛋白定量呈正相关,与血清白蛋白、总蛋白呈负相关。结论血清抗PLA2R抗体可作为IMN血清学诊断的指标之一,血清抗PLA2R抗体滴度下降与尿蛋白的减少密切相关,与疾病预后、病情转归也可能相关。
特发性膜性肾病;酶联免疫反应;抗M型磷脂酶A2受体抗体
膜性肾病是成人肾病综合征最常见的一组以肾小球基底膜上皮下免疫复合物沉积伴基底膜弥漫增厚为特点的疾病,约占原发性肾病综合征的30%[1]。BECK等[2]发现,人M型磷脂酶A2受体(phospholipase A2 receptor,PLA2R)是存在于人肾小球足细胞膜上的一种跨膜蛋白,是本病的重要靶抗原,并在特发性膜性肾病(idiopathic membranous nephropathy,IMN)患者血循环中检测到抗PLA2R抗体,且阳性率高达70%。国外报道血清抗PLA2R抗体水平与尿蛋白水平、疾病转归及预后密切相系[3]。国内该方面的报道不多,其与病情的相关性有待探讨。本实验通过定期监测血清抗PLA2R抗体滴度变化,来判断治疗疗效及病情转归,进一步证实其在IMN中发挥的重要作用。
1 资料与方法
1.1研究对象
选取2014年1月-2015年1月在潍坊市人民医院肾内科住院行肾穿刺活检证实的特发性膜性肾病55例。其中,男性36例,女性19例;平均年龄(50.45±13.82)岁。所有患者首次入院,无激素及免疫抑制剂应用史,临床资料完整,无吸烟史及重金属接触史。另选取同期15例健康体检者作为对照组。其中,男性9例,女性6例;平均年龄(49.62±15.13)岁。两组数据年龄、性别比较,差异无统计学意义(P>0.05)。
1.2实验方法
1.2.1标本采集收集55例IMN的血清标本及24h尿液标本,治疗3个月后门诊随诊时收集其血清标本及24 h尿液标本,治疗6个月后门诊随诊时再次收集其血清标本及24 h尿液标本。治疗方案包括保守治疗应用血管紧张素转化酶抑制剂或血管紧张素受体拮抗剂、利尿消肿、抗血小板聚集、降脂、中成药、激素联合细胞毒药物或钙调磷酸酶抑制剂(环磷酰胺、他克莫司、环孢素等)。治疗原则参考改善全球肾脏病预后组织(Kidney Disease:Improving Global Outcomes,KDIGO)肾小球肾炎临床实践指南[4]。所有入组对象早晨空腹采集静脉血,3 000 r/min低温离心10 min,分离血清,置于-75℃冰箱中冷冻保存备用。
1.2.2实验室指标的检测使用本院罗氏示差脉冲极谱法全自动生化仪对所有入组对象标本完成血清总胆固醇、总蛋白、白蛋白、尿素氮、肌酐、24 h尿蛋白定量的检测。
1.2.3血清抗PLA2R抗体的酶联免疫吸附法检测实验原理:应用双抗原夹心法测定标本中人抗PLA2R水平。用纯化的人肺炎衣原体IgG抗原包被微孔板,制成固相抗原,往包被的微孔中依次加入Anti-PLA2R,与辣根过氧化物酶(horseradish peroxidase,HRP)标记的抗原结合,形成抗原-抗体-酶标抗原复合物,经过彻底洗涤后加底物3,3',5,5'-四甲基联苯胺显色,在HRP酶的催化下转化成蓝色,并在酸的作用下最终转化成黄色。颜色的深浅与样品中的Anti-PLA2R呈正相关。用酶标仪在450 nm波长处测定光密度,通过标准曲线计算样品中Anti-PLA2R浓度。操作步骤按试剂盒说明书进行,以15例健康体检者作为对照组。
1.3统计学方法
采用SPSS 17.0统计软件进行数据分析,计量资料以均数±标准差(±s)表示,两组以上资料的组间比较用重复测量方差分析,方差齐时,用独立样本t检验;计数资料用随机区组设计的χ2检验,两变量间关系用Spearman秩相关分析,P<0.05为差异有统计学意义。
2 结果
2.1实验室指标分析
IMN患者治疗前与治疗3个月后尿蛋白定量(t= 4.639,P=0.000)、血清白蛋白(t=-7.933,P=0.000)、血清总蛋白(t=-7.058,P=0.000)、血清总胆固醇(t= 6.927,P=0.000)、血清抗PLA2R抗体滴度(t=5.051,P=0.000)比较,经t检验,差异有统计学意义。IMN患者治疗前与治疗3个月后血清肌酐比较,经t检验,差异无统计学意义(t=0.116,P=0.901)。IMN治疗前与治疗6个月后尿蛋白量定量(t=8.766,P=0.000)、血清白蛋白(t=-8.412,P=0.000)、血清总蛋白(t= -7.646,P=0.000)、血清总胆固醇(t=9.095,P=0.000)、血清抗PLA2R抗体滴度(t=6.220,P=0.000)比较,经t检验,差异有统计学意义。IMN治疗前与治疗6个月后血清肌酐比较,经t检验,差异无统计学意义(t=0.832,P=0.423)。IMN治疗3个月和6个月后尿蛋白定量(t=5.858,P=0.000)、血清白蛋白(t=-2.773,P=0.007)、血清总胆固醇(t=3.393,P=0.003)比较,经t检验,差异有统计学意义。IMN治疗3个月和6个月后血清总蛋白(t=-0.701,P=0.496)、血清抗PLA2R抗体滴度(t=1.514,P=0.105)、血清肌酐(t=0.983,P= 0.288)比较,经t检验,差异无统计学意义。见表1。
2.2治疗前后血清抗PLA2R抗体滴度比较
2.2.1根据2012年KDIGO肾小球肾炎临床实践指南规定标准分组①完全缓解:24h尿蛋白<0.3g,血清白蛋白正常。②部分缓解:24 h尿蛋白<3.5 g且尿蛋白排泄量减少≥50%,血清白蛋白正常或升高。③未缓解:未达到上述缓解标准。参考上述标准,将治疗后6个月IMN患者分为完全缓解组、部分缓解组及未缓解组。完全缓解组:治疗3个月和6个月后与治疗前血清抗PLA2R抗体滴度比较,经t检验,差异有统计学意义(t=5.523和11.182,P=0.000);治疗6个月和3个月血清抗PLA2R抗体滴度比较,经t检验,差异有统计学意义(t=6.103,P=0.000)。部分缓解组:治疗3和6个月后与治疗前血清抗PLA2R抗体滴度比较,经t检验,差异有统计学意义(t=4.707 和5.052,P=0.000);治疗6个月和3个月血清抗PLA2R抗体滴度比较,差异无统计学意义(t=0.378,P=0.725)。见表2。
2.2.2治疗前后血清抗PLA2R抗体阳性率比较以15例健康体检者血清抗PLA2R抗体滴度作为正常参照 [(305.28±119.16)ng/L]。治疗前血清抗PLA2R抗体阳性率为85.45%(47/55),治疗3个月后血清抗PLA2R抗体阳性率为65.45%(36/55),治疗6个月后血清抗PLA2R抗体为45.45%(25/55),经χ2检验,差异有统计学意义(χ2=15.764,P=0.000),治疗后血清抗PLA2R抗体阳性率低于治疗前血清抗PLA2R阳性率。见表3。
2.2.3不同病理分期IMN血清抗PLA2R抗体滴度比较所有患者在B超引导下行肾活检,并行光镜[苏木精-伊红染色、马森三色染色、过碘酸-雪夫染色、过碘酸六胺银染色]、免疫荧光(IgA、IgG、IgM、C3、C1q、FRA)及电镜检查确定病理分期。Ⅰ期:肾小球无明显病变,仅可见基底膜空泡变性,上皮下少量嗜复红蛋白沉淀;Ⅱ期:基底膜向上皮下的沉积物间增生,并包绕沉积物,显示为“钉突”结构;Ⅲ期:增生的基底膜将免疫沉积物完全包裹,基底膜多呈现弥漫不规则增厚,银染色见基底膜呈网状、链环状表现;Ⅳ期:光镜下基底膜高度弥漫性增厚,基底膜内可见空隙,但无典型的连环结构,毛细血管腔狭窄甚至闭塞。本研究对象无Ⅳ期特发性膜性肾病患者。治疗前、治疗3个月及治疗6个月后IMNⅠ/Ⅱ/Ⅲ期血清抗PLA2R抗体滴度比较,差异无统计学意义(P>0.05)。但治疗前血清抗PLA2R抗体阴性者(8例)有5例表现为IMNⅠ期。IMNⅠ期:治疗3和6个月后与治疗前血清抗PLA2R抗体滴度比较,经t检验,差异有统计学意义(t=2.218和3.104,P=0.033 和0.004),治疗6个月与治疗3个月血清抗PLA2R抗体滴度比较,经t检验,差异无统计学意义(t= 1.093,P=0.282);IMNⅡ期:治疗3和6个月后与治疗前血清抗PLA2R抗体滴度比较,经t检验,差异有统计学意义(t=5.310和5.574,P=0.000),治疗6个月与3个月血清抗PLA2R抗体滴度比较,经t检验,差异无统计学意义(t=0.967,P=0.3337);IMNⅢ期:治疗3和6个月后与治疗前血清抗PLA2R抗体滴度比较,经t检验,差异无统计学意义(t=1.493 和1.969,P=0.161和0.072)。治疗6个与3个月血清抗PLA2R抗体滴度比较,经t检验,差异无统计学意义(t=0.517,P=0.299)。见表4。
2.3血清抗PLA2R抗体滴度与生化指标之间的相关性
IMN患者治疗前血清抗PLA2R抗体滴度与尿蛋白定量呈正相关(r=0.452,P=0.001),与血清白蛋白、血清总蛋白呈负相关(r=-0.337和-0.0269,P= 0.012和0.047),与血清总胆固醇、血清肌酐无关(P>0.05)。IMN治疗3个月后血清抗PLA2R抗体滴度与尿蛋白定量、血清白蛋白、血清总蛋白、血清总胆固醇、血清肌酐无关(P>0.05)。治疗6个月后血清抗PLA2R抗体滴度与尿蛋白定量呈正相关(r=0.521,P=0.000),与血清白蛋白、血清总蛋白呈负相关(r= -0.373和-0.358,P=0.005和0.007),与血清总胆固醇、血清肌酐无关(P>0.05)。
表1 治疗前、后相关实验室指标的比较 (n=55,±s)
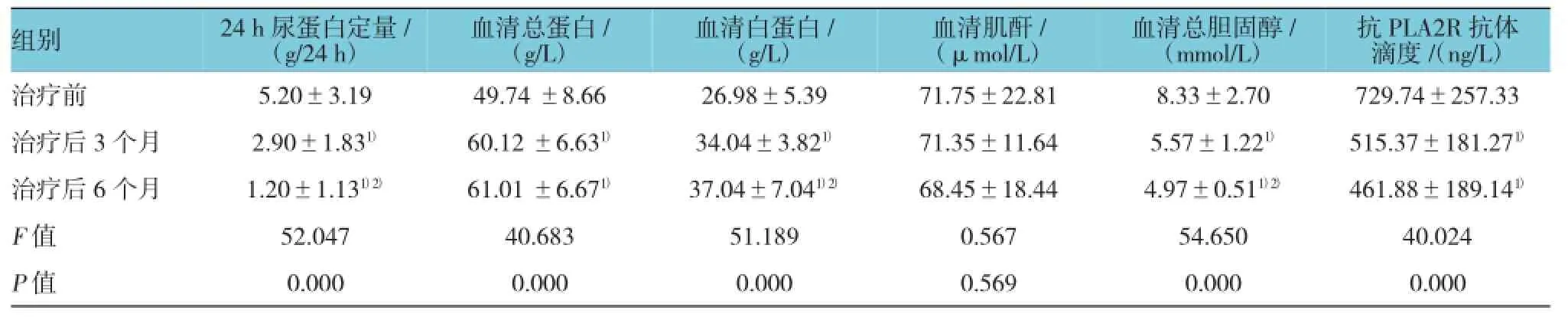
表1 治疗前、后相关实验室指标的比较 (n=55,±s)
注:1)与治疗前比较,P<0.01;2)与治疗后3个月比较,P<0.05
抗PLA2R抗体滴度/(ng/L)治疗前 5.20±3.19 49.74±8.66 26.98±5.39 71.75±22.81 8.33±2.70 729.74±257.33治疗后3个月 2.90±1.831) 60.12±6.631) 34.04±3.821) 71.35±11.64 5.57±1.221) 515.37±181.271)治疗后6个月 1.20±1.131)2) 61.01±6.671) 37.04±7.041)2) 68.45±18.44 4.97±0.511)2) 461.88±189.141)F值 52.047 40.683 51.189 0.567 54.650 40.024 P值 0.000 0.000 0.000 0.569 0.000 0.000组别24 h尿蛋白定量/ (g/24 h)血清总蛋白/ (g/L)?血清白蛋白/ (g/L)血清肌酐/ (μmol/L)血清总胆固醇/ (mmol/L)
表2 3组患者治疗前后血清抗PLA2R抗体滴度比较 (ng/L,±s)

表2 3组患者治疗前后血清抗PLA2R抗体滴度比较 (ng/L,±s)
注:1)与治疗前比较,P<0.01;2)与治疗后3个月比较,P<0.01
组别治疗后3个月完全缓解组(n=8) 791.15±111.18 511.02±90.241)部分缓解组(n=42) 705.11±223.86 502.11±167.281)未缓解组(n=5) 838.39±574.45 631.66±352.63 F值 3.638 P值 0.008治疗前P值258.57±76.091)2) 83.247 0.000 488.43±164.791) 22.493 0.000 564.20±302.21 3.066 0.103治疗后6个月F值

表3 治疗前后血清抗PLA2R抗体阳性率比较
表4 治疗前后IMN不同病理分期血清抗PLA2R抗体滴度比较 (±s)
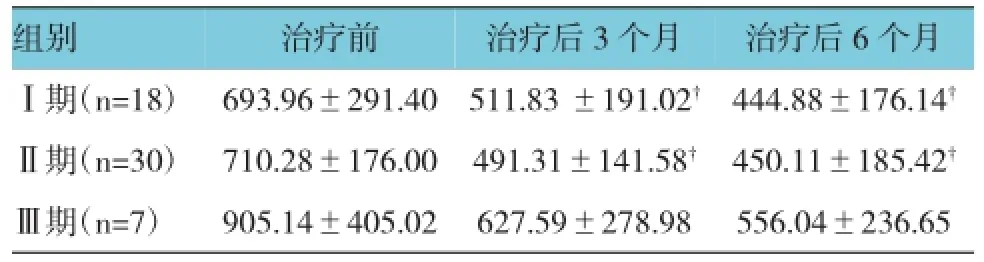
表4 治疗前后IMN不同病理分期血清抗PLA2R抗体滴度比较 (±s)
注:†与治疗前比较,P<0.05
组别治疗后6个月Ⅰ期(n=18) 693.96±291.40 511.83±191.02†444.88±176.14†Ⅱ期(n=30) 710.28±176.00 491.31±141.58† 450.11±185.42†Ⅲ期(n=7) 905.14±405.02 627.59±278.98 556.04±236.65治疗前治疗后3个月
3 讨论
特发性膜性肾病作为肾病综合征常见病理类型之一,其临床表现轻重不一,预后差异较大,部分患者可自发缓解,近半数患者最终进入慢性肾衰竭。其肾小球损伤机制之一为补体膜攻击复合物,激活PLA2,使内质网的完整性受到破坏,肾小球滤过屏障受损出现蛋白尿[4-5]。现已明确在人类足细胞上有M型PLA2R表达,并且证明M型PLA2R与抗PLA2R抗体共表达。BECK等[2]研究发现,抗PLA2R抗体只在特发性膜性肾病中表达,在继发性膜性肾病及其他肾小球疾病中不表达。
通过对55例特发性膜性肾病患者血清抗PLA2R抗体的检测,发现其阳性率高达85.45%,治疗3个月后其阳性率降至65.45%,治疗6个月后其阳性率降至45.45%,说明血清抗PLA2R抗体与IMN密切相关,并随着IMN患者病情好转,血清抗PLA2R抗体阳性率逐渐降低(P<0.01)。同时,治疗前与治疗3个月及6个月后血清抗PLA2R抗体滴度比较,差异有统计学意义,说明经治疗后血清抗PLA2R抗体滴度减少甚至转阴。通过研究笔者发现,IMN患者治疗前、治疗6个月后血清抗PLA2R抗体滴度与尿蛋白定量呈正相关,但治疗3个月后血清抗PLA2R抗体滴度与尿蛋白定量无关。治疗6个月后血清抗PLA2R抗体阴性患者中(30例)有23例患者达到临床蛋白尿缓解(24 h尿蛋白定量<1 g),血清抗PLA2R抗体阳性患者中(25例)仅有7例患者达到临床蛋白尿缓解。
国外研究者发现,血清抗PLA2R抗体是IMN患者体内的主要自身抗体,其阳性率约为75%[2]。通过对中国60例IMN患者的血清PLA2R抗体进行检测,其阳性率为81.7%[6]。国内学者研究52例IMN患者血清抗PLA2R抗体的阳性率高达96.2%[7]。对于治疗前血清抗PLA2R抗体阳性率高于国外,分析其原因可能如下:①存在人种差异;②试剂或检测技术存在不同。本研究中笔者发现,治疗前、治疗3和6个月后血清抗PLA2R抗体滴度逐渐减少甚至转阴,与BECK等[3]的研究结果一致,血清抗PLA2R抗体阳性IMN患者给予利妥昔单抗药物治疗后,多数患者血清抗PLA2R抗体滴度下降甚至消失,临床蛋白尿明显缓解。所以最好定期监测血清抗PLA2R抗体滴度变化来预测治疗疗效。同时笔者发现,IMN患者治疗前、治疗6个月后血清抗PLA2R抗体滴度与尿蛋白定量呈正相关,与国内外多个学者的研究发现血清抗PLA2R抗体水平与尿蛋白量的变化呈现一定的线性关系(正相关)一致[6,8-10],而HOXHA等[11]报道两者无关。本研究中笔者发现,治疗3个月后血清抗PLA2R抗体滴度与尿蛋白定量无关,可能由于治疗有效的IMN患者血清抗PLA2R抗体滴度的下降常先于尿蛋白减少及疾病缓解[5],还需进一步追踪观察。
HOXHA等[12]追踪观察患者27个月(中位数),发现实验初期血清抗PLA2R抗体滴度水平高的患者比血清抗PLA2R抗体滴度水平低的患者肾功能损伤进展快。KANIGICHERLA等[13]追踪观察患者5年,发现实验初期血清抗PLA2R抗体滴度高者比血清抗PLA2R抗体滴度低者血清肌酐值翻倍的比例高,本研究只追踪研究患者6个月时间,发现2例血清抗PLA2R抗体滴度高的患者出现血清肌酐轻度升高,但血清抗PLA2R抗体与血清肌酐比较,差异无统计学意义,需要继续追踪观察。
综上所述,IMN血清抗PLA2R抗体滴度与尿蛋白水平、疾病近期转归存在一定关系。经治疗后出现血清抗PLA2R抗体滴度降低或转阴的IMN患者,尿蛋白明显减少,治疗前后PLA2R抗体滴度持续高的患者不容易缓解或缓解后容易复发。血清抗PLA2R抗体可做为IMN诊断的重要血清学指标,并与IMN的疗效密切相关。
[1]WASSERSTEIN A G.Membranous glomerulonephritis[J].J Am Soc Nephro,1997,8(4):664-674.
[2]BECK L H,BONEGIO R G,LAMBEAU G,et al.M-type phospholipase A2 receptor as target antigen in idiopathic membranous nephropathy[J].N Engl J Med,2009,36(1):11-21.
[3]BECK L H,FERVENZA F C,BECK D M,et al.Rituximab-induced depletion of anti-PLA2R autoantibodies predicts response in membranous nephropathy[J].JAm Soc Nephrol,2011,22(8):1543-1550.
[4]NANGAKU M,SHANKLAND S J,COUSER W G,et al.Cellular responsetoinjuryinmembranousnephropathy[J].AmSoc Nephrol,2005,16(5):1195-1204.
[5]MUNDEL P L,SHANKLAND S J.Podocyte biology and response to injury[J].Am Soc Nephrol,2002,13(12):3005-3015.
[6]QIN W,BECK L H,ZENG C,et al.Anti-phospholipase A2 receptor antibody in membranous nephropathy[J].J Am Soc Nephrol,2011,22(6):1137-1143.
[7]韩丹诺,谌贻璞,王艳艳,等.特发性膜性肾病中血清磷脂酶A2受体抗体的临床意义[J].中国实用内科杂志,2015,35(4):351-354.
[8]SEGARRA-MEDRANOA,JATEM-ESCALANTEE,CARNICER-CÁCERES C,et al.Evolution of antibody titre against the M-type phospholipase A2 receptor and clinical response in idiopathicmembranousnephropathypatientstreatedwith tacrolimus[J].Nefrologia,2014,34(4):491-497.
[9]HOFSTRA J M,DEBIEC H,SHORT C D,et al.Antiphospholipase A2 receptor antibody titer and subclass in idiopathic mem branous nephropathy[J].J Am Soc Nephrol,2012,23(10):1735-1743.
[10]周广宇,金玲,于晶,等.成人膜性肾病患者血清抗PLA2R抗体与病情的相关性[J].中华肾脏病杂志,2012,28(2):111-114.
[11]HOXHA E,KNEIΒLER U,STEGE G,et al.Enhanced expression ofthe M-type phospholipase A2 receptor in glomeruli correlateswith serum receptor antibodies in primary membranousnephropathy[J].Kidney Int,2012,82(7):797-804.
[12]HOXHA E,THIELE I,ZAHNER G,et al.Phospholipase A2 receptor autoantibodies and clinical outcome in patients with primary membranous nephropathy[J].J Am Soc Nephrol,2014,25(6):1357-1366.
[13]KANIGICHERLA D,GUMMADOVA J,MC KENZIE E A,et al. Anti-PLA2R antibodies measured by ELISA predict long-term outcome in a prevalentpopulation of patientswithidiopathic membranous nephropathy[J].Kidney Int,2013,83(5):940-948.
(童颖丹 编辑)
Correlation between serum anti-PLA2R antibody and adult idiopathic membranous nephropathy
Li-li Zhang1,Xiang Wang1,Xiao-li Fan1,Xiao-li Wang1,Jun Zhao2
(1.Weifang Medical University,Weifang,Shandong 261042,China;2.Weifang People's Hospital,Weifang,Shandong 261000,China)
Objective To investigate the relationship between the positive titer of serum anti-phospholipase A2 receptor(PLA2R)antibody and other laboratory indexes in adult patients with idiopathic membranous nephropathy(IMN),and to explore the roles of anti-PLA2R antibody in the diagnosis of IMN and the evaluation of the disease severity.Methods Fifty-five IMN patients were selected,and 15 cases of healthy persons were selected as the control group.Serum anti-PLA2R antibody was detected by ELISA.And 24-h urinary protein,serum total protein,serum total cholesterol and serum creatinine were detected in the IMN patients.Results After 3 months and 6 months,the serum anti-PLA2R antibody was significantly lower than that before treatment(P<0.05).Before treatment 47 of 55 IMN patients were anti-PLA2R antibody positive,the positive rate was 85.45%;3 months after the treatment there were 36 patients with positive anti-PLA2R antibody,the positive rate was 65.45%;6 months after treatment,anti-PLA2R antibody positive rate was 45.45% (25/55).The serum anti-PLA2R antibody titer was positively correlated with urinary protein,but was negatively correlated with serum albumin and total protein before treatment and 6 months after treatment. Conclusions Serum anti-PLA2R antibody can be used as one of the serum indexes of IMN,and serum anti-PLA2R antibody titer is closely related to urine protein,which may be closely related to the prognosis and outcome of the disease.
diopathic membranous nephropathy;enzyme linked immune response;anti-PLA2R antibody
R692
A
10.3969/j.issn.1005-8982.2016.09.009
1005-8982(2016)09-0044-05
2015-11-26
赵军,E-mail:wfsky@163.com
