肝脏二维超声与CT配准技术的临床可行性研究
2016-07-29俊徐利建顾力栩詹维伟
柳 俊徐利建顾力栩詹维伟
肝脏二维超声与CT配准技术的临床可行性研究
柳 俊1徐利建2顾力栩2詹维伟1
【摘要】目的:探讨肝脏二维超声与CT配准技术的临床可行性。方法:5例肝脏二维超声图像与CT图像进行配准,包括超声探头的标定、标记点配准、图像预处理、仿真实验,通过定性定量评价比较超声与CT之间配准的精确性与稳定性。结果:二维超声与CT之间能够100%进行配准。本文方法所得到的两者图像的相似性测度较好。计算所得超声与CT配准后目标点之间的平均误差为4.13±0.44mm。结论:二维超声与CT之间配准的准确性和稳定性较好,临床上可能有很大的应用前景。
【关键词】超声;X线计算机,体层摄影术;配准
目前肝脏常见的超声引导手术如射频消融等主要通过术前规划和术中的二维超声引导,手术期间需要其他医学影像的辅助,操作上尤为不便。同时由于成像原理的不同,有时一些病灶在超声上无法显示或无法清晰显示,但在CT上则可清晰显示[1]。在这几种情况下,术前CT和术中超声图像的配准十分有必要,它可用于改善超声导航的精确度,帮助医护人员降低手术风险和手术时间,最终提高手术的成功率[2-3]。本文通过肝脏的二维超声与CT配准技术的定性定量评估,阐明其在临床上应用的可行性。
方 法
1.一般资料
本研究经过伦理委员会同意并取得患者知情同意权。选取2013年4月间上海交通大学医学院附属瑞金医院肝占位性病灶患者5名,男性3名,女性2名,年龄26~48岁,平均年龄39±5.62岁。病灶大小7.56~4.24cm,平均5.63±1.32cm。所有患者均需首先进行上腹部CT增强检查,之后进行超声检查。
2.仪器与方法
2.1. 仪器:超声仪器选用GE E9,百胜MyLab 90,Aloka 4000,凸阵探头,探头频率3.5Hz。计算机断层扫描(CT)仪器选用GE 64排128层螺旋CT(Lightspeed VCT)。配准软件及仪器由上海交通大学生物工程学院自主研发。该系统使用了电磁追踪设备,超声探头上绑定了一个6D传感器用于将超声图像导入系统。软件用Python 语言和Visualization Toolkit(VTK) 实 现,Compute Unified Device Architecture(CUDA)用于加速核心的算法。导航软件在Dell Precision (Intel Core i5 CPU 2.67GHz, RAM 2.96GB,NVIDIA GeForce GTX 260 graphics card, Microsoft Windows XP Professional 版本2002 Service Pack 3)运行,从GE E9得到的超声图像通过视频采集卡导入计算机中。电磁导航系统(NDI,Northern Digital,Canada)包括场生成器(FG)、空中接口单元(CIU)和四个传感器接口单元(SIU)。
2.2 配准前准备
(1)超声探头的标定: 超声探头的标定通过计算超声图像坐标系和传感器坐标系间的坐标变换矩阵将超声图像融入软件系统中。我们为超声标定制作了一个包含了标定面板的水箱。面板有25个半径为1.5mm、高1mm,且可在超声中清晰成像的圆柱体。超声标定主要分三步:首先,一个6个自由度的传感器固定在超声探头上用于获得探头的空间位置和角度,标定的水箱注满水用于超声成像;然后,调整超声探头将超声图像与标定面板对齐,通过在系统中鼠标和导航针分别在超声图像坐标系和世界坐标系中获取圆柱体的中心位置。最后对两组点计算一个刚体变换使得两者的欧式距离最小。
(2)标记点配准:从CT中分割得到了肝静脉和门静脉,这提供了直观的信息来帮助完成配准过程。我们在CT和超声图像中选取肝脏中若干个相关的血管分叉点作为解剖标记点。此系统支持半自动化地选取标记点,所有的血管分叉点提前从CT图像中计算得到。我们需要交互地从超声图像中识别标记点,完成超声标定和标记点配准,超声图像整合到了系统中,标记点配准得到的初始变换为接下来的图像配准做准备。
(3) 图像预处理:肝脏是实质器官,大量颗粒,需要做平滑处理;同时在超声图像中处理噪声[4],在去噪的同时还能保留边界信息。
(4)仿真实验:从CT图像仿真超声特性是基于超声物理学的原理,我们建立了一个只考虑超声反射和衰减特性的超声束模型。仿真的过程分两个步骤:首先,根据超声探头上绑定的6D传感器获取探头的空间位置和角度,得到二维CT重采样的面数据;然后计算仿真超声束上的每个像素值、插值后的值以及梯度值,迭代更新得到最终值。我们建立了有物理学意义的准确仿真系统,仿真过程中可任意交互改变虚拟探头的参数,包括探头类型(线性或扇形)、探头位置(空间位置和角度)、超声束的初始强度、超声束的频率、视场、穿透深度和斑点噪声。由于超声波的反射特性,组织边界增强;同时骨组织由于表面的高反射率被消减。仿真的结果将作为中间图像用于接下来的图像配准。
2.3 配准及配准后定性定量评估:通过在CT和超声图像中选取标记点和目标点,我们建立了自己的金标准。4个血管分叉点作为基准点,病灶中心点作为目标点。一旦CT和超声图像的基准点选择完毕,并通过计算机计入系统后,系统可自动匹配两者之间的图像,即配准过程完成。我们可以将配准好的CT图像和超声图像旋转-20°~20°以及在X、Y坐标上平移-20~20个像素来初步显示配准的相似性测度作为定性评价。5例患者图像配准后逐一计算超声图像目标点与CT图像目标点之间的误差值,并计算误差平均值(AVG)和标准差(SD),了解配准后的准确性和离散度(即稳定性)。
结 果
5例患者均能实现二维超声图像与CT之间的配准,完成率100%。通过本文方法得到的CT体数据和超声切面的融合效果图,图1数字箭头1、2、3 标记的解剖结构分别为皮下软组织、脊椎和肝脏,可以看到相对应的结构已基本匹配。
图2数字1、2、3标记的箭头分别表示肝叶轮廓、肝脏血管和肝血管瘤,图2A、B显示的特征信息包括肿瘤和血管。本文的配准方法基本匹配所有的特征结构(图2C)。初步的定性实验说明本文提出的配准方法准确性较好。5例患者目标点之间的误差值见表1,平均误差值4.13±0.44mm。
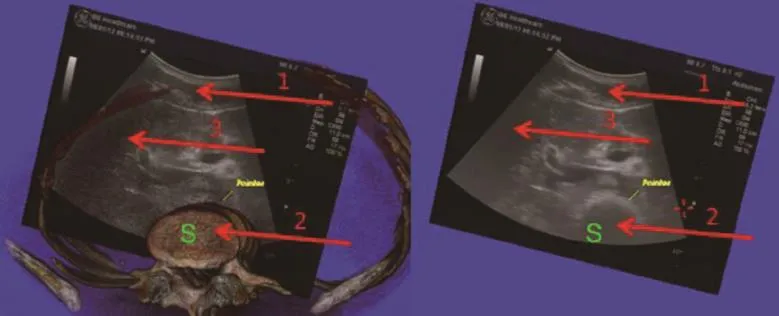
图1 CT数据和超声切面的融合图。1、2、3箭头标记的解剖结构分别为皮下软组织、脊椎和肝脏。
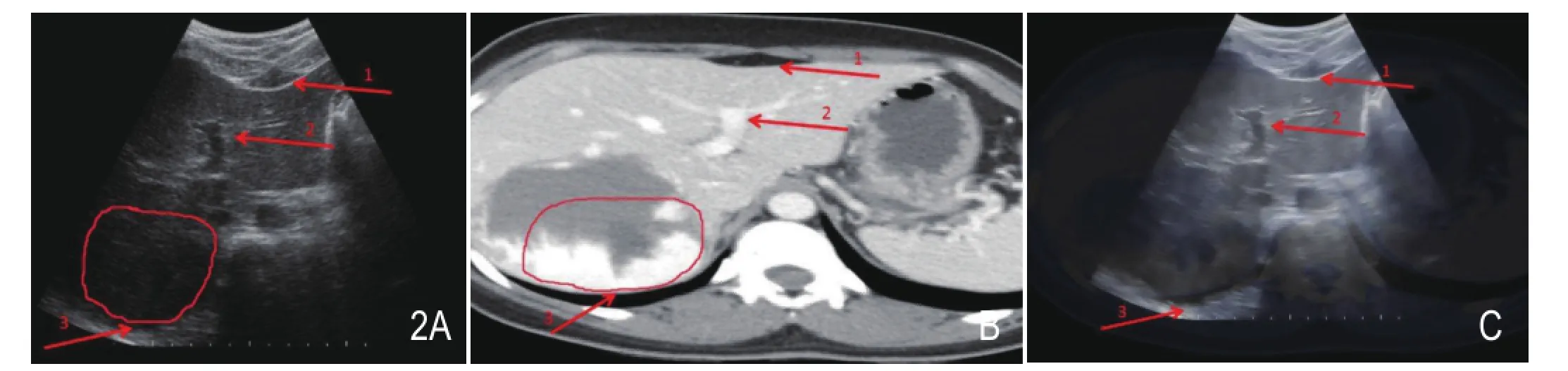
图2 CT切面和超声切面的融合图。1、2、3标记的箭头分别表示肝叶轮廓、肝脏血管和肝血管瘤。A、B.显示的特征信息包括肿瘤和血管。 C.匹配了所有的特征结构。
1

表1 5例患者超声图像与CT图像目标点之间的误差值(单位:mm)
讨 论
CT和超声图像的成像原理完全不同,导致灰阶不匹配,图像差异很大,要在这两种成像模态间建立一个理想的相似性测度并不容易。超声图像中,软组织的边界被增强,骨组织被屏蔽,这与CT图像中是很不一样的,而且超声的图像质量不好(对比度低、噪声高以及伪影)使CT和超声之间的配准更加困难,任何能使这两类图像更相似的办法都可以改善配准的精度[4]。
CT和超声图像由于成像原理不一致很难建立有效的相似性测度,同时由于超声图像对比度和信噪比低,且有斑点噪声,使常见的配准算法无法应用于超声图像的配准。本文提出的CT和超声图像的配准框架针对CT和超声图像本身的成像特性,建立一种结合了灰度信息和几何信息的新相似性测度,这是本文的主要创新点[5]。整个算法框架首先对CT和超声图像预处理来增强两种模态的相似性,超声图像中的斑点被消除,同时保留边界信息。然后建立超声的仿真模型,从CT图像中仿真超声的反射和衰减特性,以及从CT图像中仿真超声特性能增加两种模态的相似性,这是为进一步的配准做准备。仿真后,由于超声的反射特性组织边界增强,骨组织因为组织界面间的高反射率完全消除,仿真得到的这些特性和真实超声是一致的[6-7]。最后,本文提出了一种整合了图像空间信息和灰度信息的相似性测度来配准从CT仿真得到的超声和真实的超声,新的测度对图像的灰度和空间信息的结合方式完全不同于以往提出的方法。初步的实验结果显示新的测度相比于只利用图像灰度信息的测度具有更高的精度,尤其是对于低分辨率的超声图像,本文提出的测度具有更高的准确度[5]。
CT和二维超声图像的自动化配准仍然是一个开放的问题,据我们所知,很少有完全自动化的CT和超声图像的工作流程应用于临床的肝脏病例上。准确的配准依赖于一个良好的初始变换,这就需要临床医生在患者皮肤或图像上选择基准点。本文结合了基准点配准与图像配准方法来提高配准的准确度和稳定性。基准点配准的计算效率高,但是稳定性差[8-9];图像配准能避免过多的人工操作,且能进一步提高配准的精度,它的缺点在于参数寻优过程中容易陷入局部最小点导致配准失败[10-11]。结合以上两种配准方法较好地平衡了整个配准过程的准确度和稳定性。本文提出配准后的定量评估的平均误差值为4.13±0.44mm,说明其准确性和稳定性都是很好的,这样的准确性和稳定性可以适用于临床诊断及介入治疗。
通过CT和超声图像的融合,临床介入治疗的导航系统可以被建立,由于目标区域复杂和超声图像质量差,在一些病例中,只把超声图像用于实时导航的传统方法往往并不能有效帮助临床医生来确定手术的目标区域,我们的系统使用电磁导航和CT、超声的融合图像可以更有效地帮助临床医生准确地确定手术目标区域[5]。
综上所述,本文提出的二维超声与CT配准技术的临床应用是可行的。但是由于CT和超声这两种医学图像差异很大,很难建立这两种模态的理想的相似性测度,并且本文的病例数较少,因此需要做更多的临床实验来验证本文提出的方法。
参 考 文 献
[1]Ferrucci J. Liver tumor imaging: current concepts. AJR, 1990,155:473-484.
[2]Wein W, Khamene A, Clevert D, et al. Simulation and fully automatic multimodal registration of medical ultrasound. Medical Image Computing and Computer-Assisted Intervention-MICCAI, 2007,2007:136-143.
[3]Wein W, Brunke S, Khamene A, et al. Automatic CT-ultrasound registrationfor diagnostic imaging and image-guided intervention. Medical Image Analysis,2008, 12:577-585.
[4]Coupé P, Hellier P, Kervrann C, et al. Nonlocal means-based speckle fltering for ultrasound images. Image Processing, IEEE Transactions on, 2009, 18:2221-2229.
[5]He Y, Gu L. Medical Image Registration Using Normal Vector and Intensity Value[C]//Intelligent Computation and Bio-Medical Instrumentation (ICBMI), 2011 International Conference on. [S.l.]:[s. n.], 2011:46-49.
[6]Kutter O, Shams R, Navab N. Visualization and GPU-accelerated simulation of medical ultrasound from CT images. Computer Methods and Programs in Biomedicine, 2009, 94:250-266.
[7]Reichl T, Passenger J, Acosta O, et al. Ultrasound goes GPU: realtime simulation using CUDA[C]//Proceedings of SPIE. [S.l.]: [s.n.],2009,7261:726116-726116.
[8]Bucholz R, Yeh D, Trobaugh J, et al. The correction of stereotactic inaccuracy caused by brain shift using an intraoperative ultrasound device[C]//CVRMed-MRCAS'97. [S.l.]: [s.n.], 1997:459-466.
[9]Comeau R, Sadikot A, Fenster A, et al. Intraoperative ultrasound for guidance and tissue shift correction in image-guided neurosurgery. Medical Physics, 2000, 27:787.
[10]Aylward S, Jomier J, Guyon J, et al. Intra-operative 3D ultrasound augmentation[C]//Biomedical Imaging, 2002. Proceedings. 2002 IEEE International Symposium on. [S.l.]: [s.n.], 2002:421-424.
[11]Lange T, Papenberg N, Heldmann N, et al. 3D ultrasound-CT registration of the liver using combined landmark-intensity information. International Journal of Computer Assisted Radiology and Surgery, 2009, 4:79-88.
中国医学计算机成像杂志,2016,22:265-268
Chin Comput Med Imag,2016,22:265-268
1 Department of Ultrasonic Diagnosis, Ruijin Hospital, Shanghai Jiao Tong University School of Medicine.
2 Institute of biomedical engineering, Shanghai Jiao Tong University ,
Address: 197 Ruijin NO. 2 Road, Shanghai, 200025, P.R.C
Address Correspondence to ZHAN Wei-wei (E-mail: shanghairuijin@126. com)
中图分类号:R814.42
文献标志码:A
文章编号:1006-5741(2016)-03-0265-04
收稿时间:(2016.01.20 ;修回时间:2016.02.22)
作者单位:1 上海交通大学医学院附属瑞金医院超声诊断科2 上海交通大学生物医学工程学院
通信地址:上海市黄浦区瑞金二路197号 , 上海市200025 The Projects of Medicine Combined with Engineering (Science) of Shanghai Jiaotong University (YG2012ZD06)
通信作者:詹维伟(电子邮箱:shanghairuijin@126.com)
基金项目:上海交通大学“医工(理)交叉研究基金”项目(YG2012ZD06)
The Clinical Feasibility of 2-D Ultrasound and CT Registration Technology About Liver
LIU Jun1, XU Li-jian2, GU Li-xu2, ZHAN Wei-wei1
【Abstract】Purpose: To discuss the clinical feasibility of 2-D ultrasound and CT registration technology about liver. Methods: 2D ultrasound images and CT images of 5 cases liver were registered. The accuracy and stability between the two imaging according to the qualitative and quantitative results were assessed, the process included ultrasonic probe calibration, marks registration, image preprocessing and the simulation experiment. Result: It can be 100% registered between 2-D ultrasound and CT. The imaging similarity was better according to our methods. After registration, the mean and standard deviation of the target error was 4.13 and 0.44 between ultrasound and CT respectively, so the accuracy and stability was good. Conclusion: It can be 100% registered between 2-D ultrasound and CT. Although there were some errors, but it still has a great prospect in the clinic application in the future.
【Key words】Ultrasound, CT, registration
