硫铁矿石热自燃机理研究及其探讨*
2016-07-26董洪芹陈先锋杨海燕刘校
董洪芹 陈先锋 杨海燕 刘校
(武汉理工大学资源与环境工程学院 武汉 430070)
硫铁矿石热自燃机理研究及其探讨*
董洪芹陈先锋杨海燕刘校
(武汉理工大学资源与环境工程学院武汉 430070)
摘要硫铁矿石自燃是矿山开采中面临的重大灾害之一。矿石自燃不仅会造成巨大的资源浪费和经济损失,还将引发一系列的安全与环境问题。通过研究硫铁矿石自燃的化学热力学机理,掌握了导致硫铁矿自燃的主要原因。利用DSC曲线对硫铁矿自燃过程的氧化特性进行研究,通过对比不同粒径的热流曲线及特征温度点的变化趋势,分析硫铁矿自燃特性的变化规律。应用热分析动力学方法计算了硫铁矿的活化能,比较不同粒径下矿样的活化能大小,为判断其自燃可能性和自燃特性研究提供依据。
关键词硫铁矿热自燃热动力学活化能
0引言
我国硫铁矿资源丰富,约有20%~30%的硫铁矿及5%~10%的有色金属或多金属硫化矿山存在自燃火灾的危险。硫铁矿石中主要成分FeS具有很高的自燃氧化性,在常温下与水和氧气共同存在时会发生氧化反应放出大量的热量,当这些热量不断积蓄而无法释放时,会使周围环境的温度不断升高,引起周围易燃物质的燃烧,进而引发火灾,造成经济损失和资源浪费。针对矿样进行实验,利用实验所得DSC曲线分析不同粒径下FeS矿样的热流曲线的变化规律,研究不同条件(样品粒度的改变)对硫铁矿样自燃特性的影响。并采用热分析动力学方法[1],用Ahcar法和Coats-Redfern 法求解反应所需活化能,比较所得结果,从而得出比较可靠的活化能值。根据活化能对硫铁矿自燃特性进行比较性分析,验证实验所得结果。
1实验设计
1.1实验仪器及药品
实验系统主要由同步热分析仪器、电子精密天平、粉碎机、机械振动机、分子筛、真空干燥箱、真空手套箱、稳压电源、液态氮气配气罐和数据输出设备组成。
实验药品采用由天津光复精细化工有限公司生产的纯FeS(含量≥85.0%)进行研究。
1.2实验方法
在30~900 ℃温度范围内,利用热分析仪对FeS颗粒进行热分析。将纯FeS在电热真空干燥箱中干燥,质量衡定后,粉碎机粉碎FeS固体,然后利用机械筛分机,筛分成不同粒径的样品,利用电子天平称出待用的测试样品质量,利用同步热分析仪进行实验。
分别选取5 mg粒径为140~200目,200~240目,240~400目,400~500目的FeS颗粒,采用升温速率5 K/min、空气流量30 mL/min,在30~900 ℃范围内进行动态热分析试验,分析粒径对FeS氧化性质的影响。
2实验结果与分析
分别筛选140~200目、200~240目、240~400目、400~500目4种不同粒径的FeS样品,选取质量5 mg,在5 K/min升温速率、30 mL/min空气流量条件下,在30~900 ℃范围内进行动态热分析试验。所得热流曲线如下图1所示。
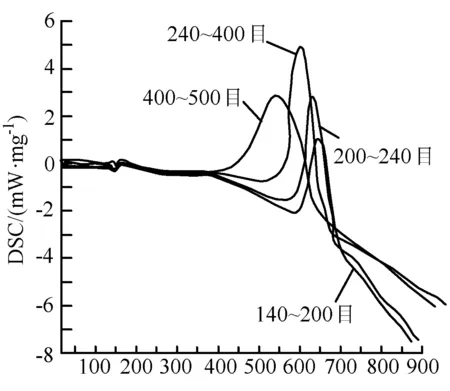
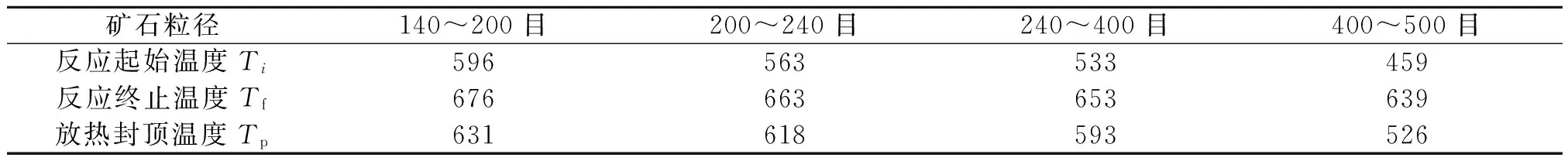
图1 不同粒径矿样热流(DSC)曲线
通过分析图1中不同粒径矿石DSC曲线和表1所列的特征温度点可以看出,随着矿石粒径的减小,DSC曲线有整体前移的趋势,且它们的氧化升温过程经历了3个不同的阶段[2]:
第一阶段:在温度为30~300 ℃之间,不同粒径矿样的DSC曲线基本保持一致,且热流曲线上在150 ℃左右出现一个小的相变吸热峰。这是因为在该阶段FeS发生物理吸附氧的结果。固体表面吸附氧气和脱附氧气处于平衡状态,因此表明粒径的改变对矿样的物理反应过程影响很小。
第二阶段:从300 ℃至放热封顶温度,此阶段主要发生的是化学吸附并伴有化学反应的发生。该过程中随着温度的升高,DSC曲线逐渐上升,且随着温度的不断升高,DSC曲线越来越陡,表明更多的矿石分子不断被激活,吸附的氧份比率增加。另外,随着温度的增加,热流曲线上,粒径为400~500目的样品最先发生化学反应,接着240~400目、200~240目、140~200目的样品依次发生变化,起始温度随着粒径的减小而降低。这表明,随着粒径的减小,矿石越容易发生氧化反应。
第三阶段:从放热封顶温度至反应终止温度,该阶段是吸附的氧分子与矿样发生剧烈化学反应,放出二氧化硫气体和大量的能量。因氧化放出的二氧化硫带走了热量,因此,热流曲线逐渐降低。从表1可得,随着粒径的减小,矿石反应的起始温度、反应终止温度和放热封顶温度均逐渐降低,DSC曲线向低温方向移动。其原因是,矿石粒径越小,其表面积越大,氧气分子与样品接触的面积增大,吸附的氧气量增大,使其氧化的条件变得有利,在较低的环境温度下有更多的分子能被激活,发生氧化反应[2]。
3热动力学分析
3.1Ahcar法
有Ahcar方程[3]:
(1)


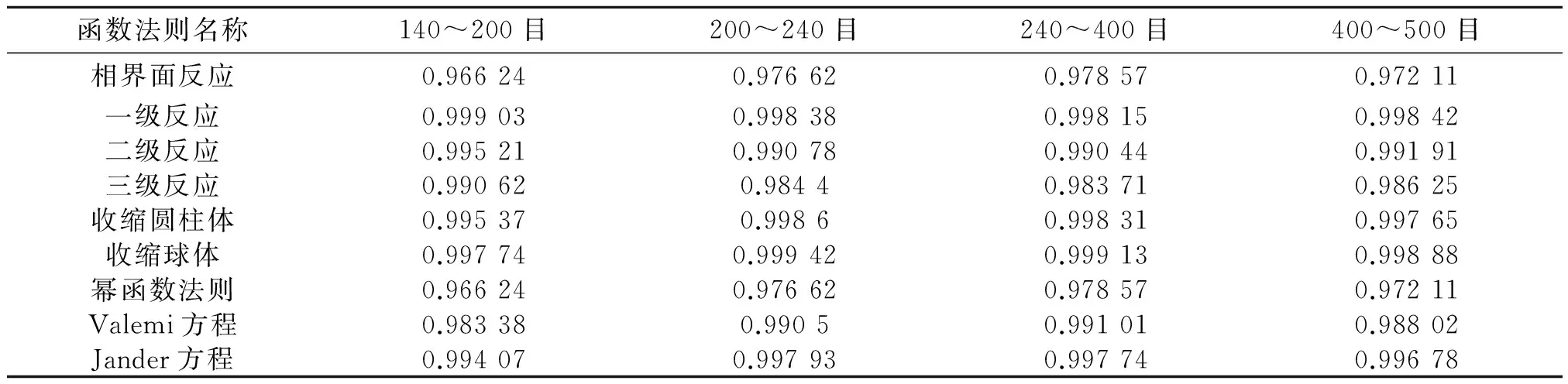
表2 不同粒径FeS相关性系数
对于上述4种粒径FeS的相关性系数,选取每种粒径最大相关性系数时的热流实验数据,进行拟合,所得结果如图2所示。
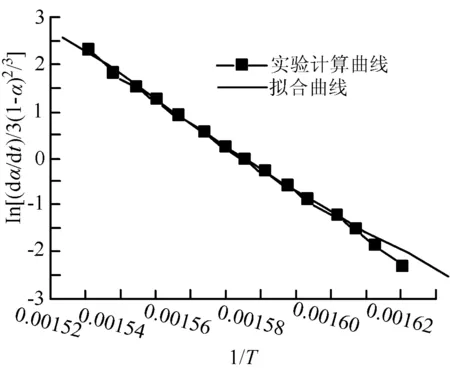
线性拟合方程:y=75.175 03-47 710.400 56x
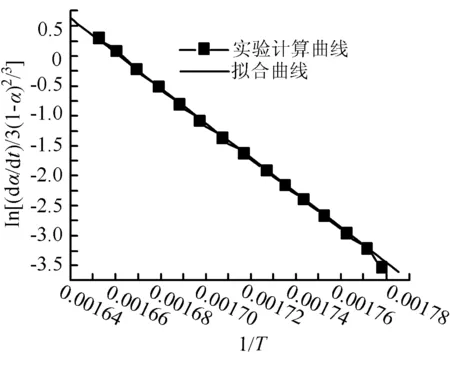
线性拟合方程:y=47.794 66-28 990.131 75x
相关性系数:R=0.998 088
(c)240~400目

线性拟合方程:y=51.916 94-32 896.146 03x
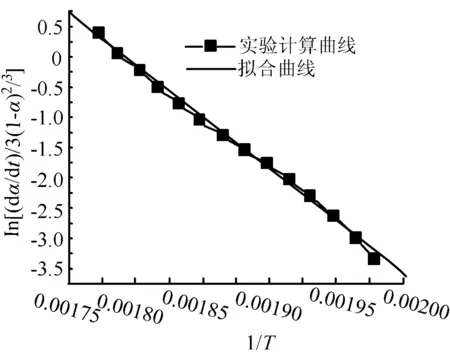
线性拟合方y=29.085 52-16 206.076 94x
利用拟合所得数据,分别计算出不同粒径矿石的活化能E[4],列于下表3中。

表3 不同粒径矿样活化能 kJ/mol
3.2Coats-Redfern法
根据热分析动力学相关原理[5],得出Coats-Redlfern方程:
(2)
利用实验测得的热流实验数据,对不同粒径下的DSC数据进行处理[6],可得,ln[G(α)/T2]对1/T的一系列曲线,对它们进行线性回归分析得到相关性系数,结果如表4所示。
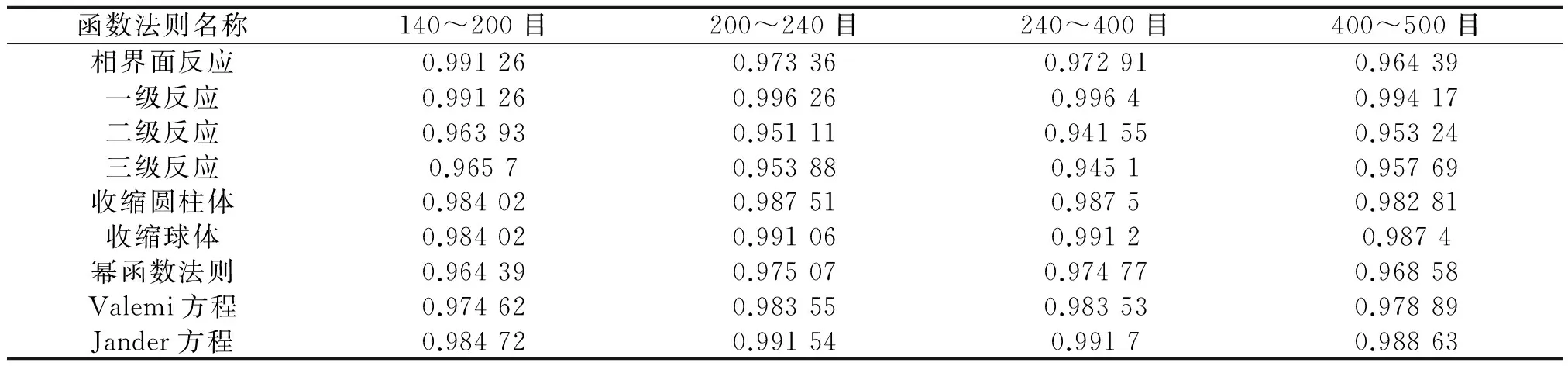
表4 Coats法不同粒径矿样相关性系数
对于上述4种粒径矿样的相关性系数,选取每种粒径最大相关性系数时的热流实验数据,对ln[G(α)/T2]~1/T作图,拟合结果如图3所示。

线性拟合方程为:y=37.527 85-32 314.396 85x
相关性系数:R=0.991 26
(a)140~200目
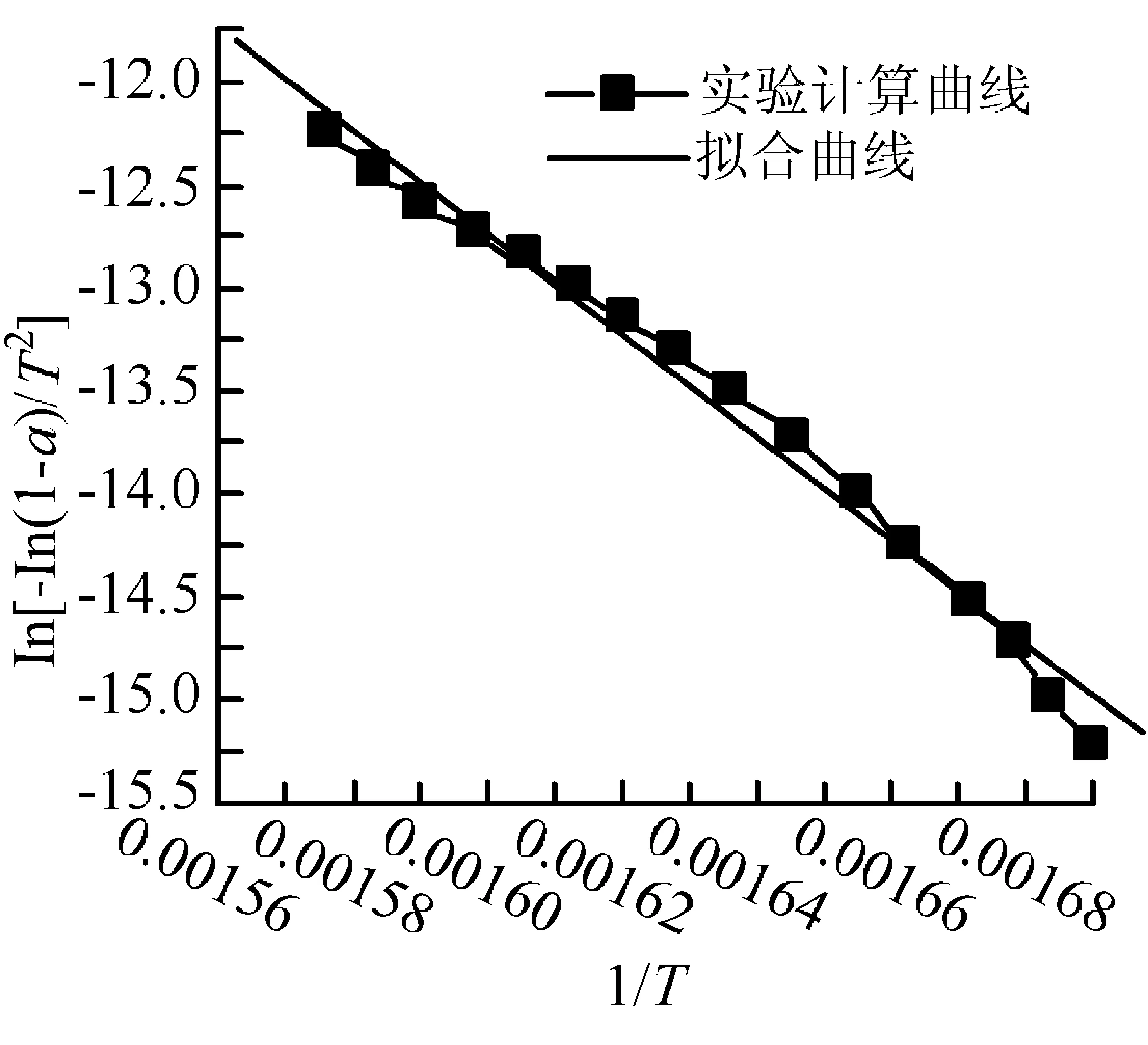
线性拟合方程为:y=29.821 95-26 633.627 13x
相关性系数:R=0.996 26
(b)200~240目
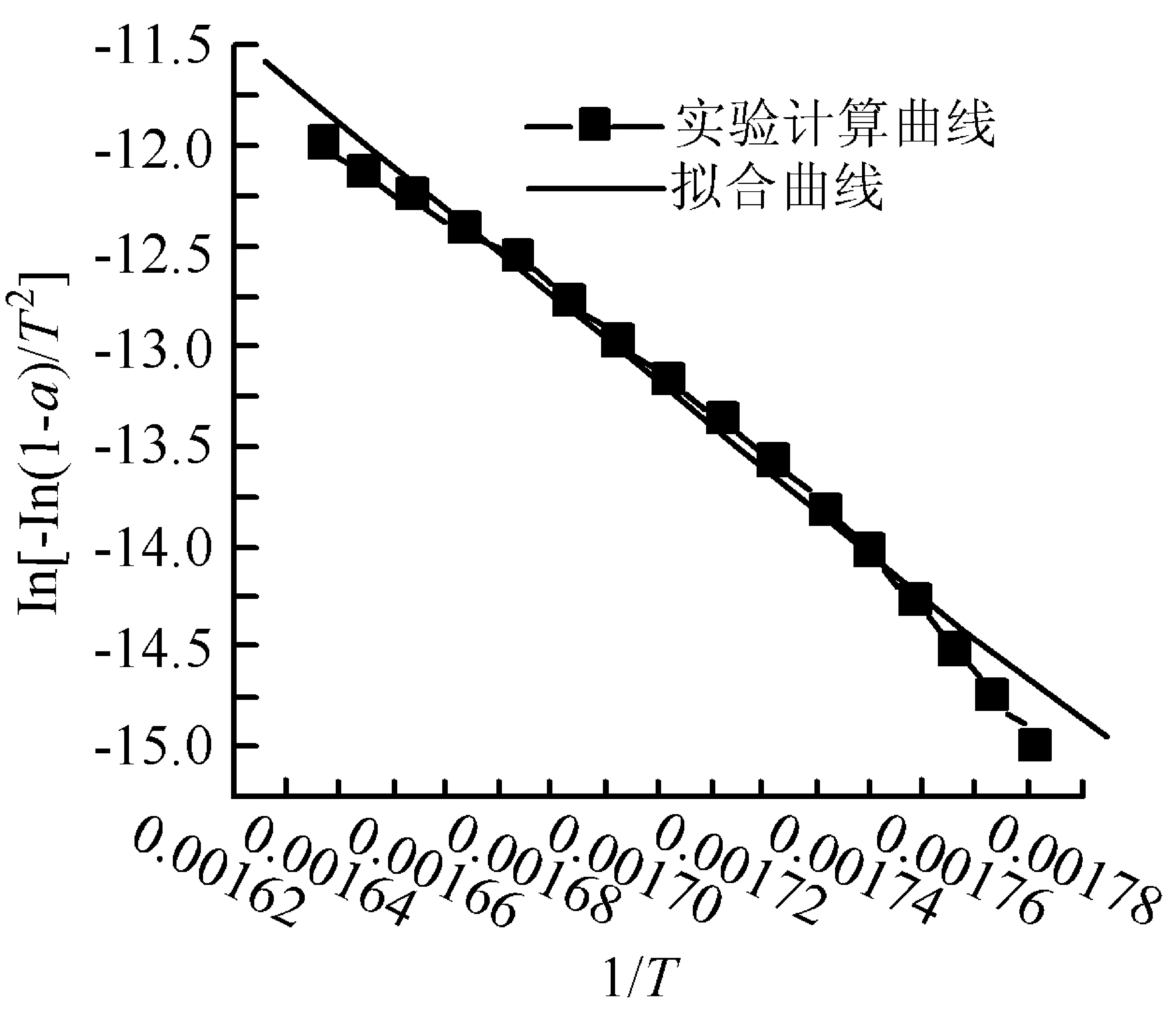
线性拟合方程为:y=26.741 91-23 569.344 49x
相关性系数:R=0.996 4
(c)240~400目

线性拟合方程为:y=10.523 61-12 528.760 42x
相关性系数:R=0.994 17
(d)400~500目
图3不同粒径时动力学相关性分析曲线
利用拟合所得数据,分别计算出不同粒径矿石的活化能E,列于下表5中。
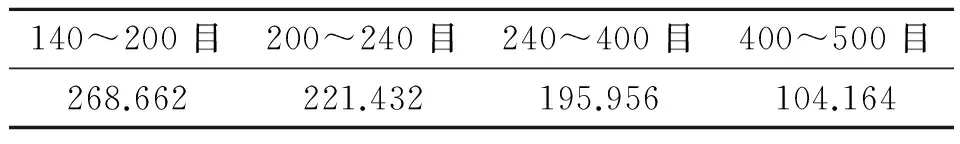
表5 不同粒径矿样活化能 kJ/mol
表3和表5的计算结果显示,由两种方法求出的活化能均显示出相同的趋势。粒径为140~200目的样品反应所需活化能最多,在这4种矿样中最不易自燃,200~240目、240~400目、400~500目反应所需活化能逐渐减小,越容易被氧化,即自燃氧化倾向性越来越大。
通过以上对DSC曲线的分析和反应所需活化能的计算可得:随着粒径的改变,FeS自燃所需的时间和能量也跟着改变。因此,粒径对矿石自燃的影响不能忽略。矿石粒径减小,DSC曲线整体向低温方向移动,硫铁矿自燃所需的能量变小,自燃危险性越大。反之,其自燃危险性越小。
4结论
通过对矿石粒径分析硫铁矿自燃特性,并基于计算得出的活化能参数来描述硫铁矿的自燃规律,比较矿样的自燃可能性大小。
(1)硫铁矿氧化升温过程经历了3个不同的阶段,即矿石与氧气的物理吸附,矿石与氧气的化学吸附,矿石与氧气的化学反应。
(2)相同升温速率下,随着矿石粒径的减小,矿样热流曲线整体向低温方向移动,氧化反应起始温度、终止温度和放热封顶温度都降低,硫铁矿自燃所需活化能降低,其自燃可能性越大。
(3)随着氧化反应的不断进行,转化率不断升高,样品活化能值逐渐降低,更加容易被氧化,自燃危险性越大。
(4)通过采用两种不同方法计算分析FeS矿样反应的热动力学参数知,coats法获得的结果较为接近,活化能的值可信度较高;而Ahcar法计算结果与coats法相比,计算结果偏大。
(5)计算得到的活化能显示出的变化趋势与改变实验条件导致矿样热流曲线发生的变化规律一致。
参考文献
[1]王慧欣,谢传欣,黄飞. FeS自燃特性的分析[J].大庆石油学院学报,2007,31(6):1-4.
[2]李星.硫化亚铁氧化自燃倾向性的试验研究[D]. 武汉:武汉理工大学,2011.
[3]胡荣祖,史启祯.热分析动力学[M]. 北京:科学出版社,2001:126-136.
[4]刘剑,陈文胜,齐庆杰.基于活化能指标煤的自燃倾向性研究[J].煤炭学报,2005,30(1):67-70.
[5]阳富强,吴超.硫化矿石自燃的热分析动力学[J].中南大学学报,2011,42(8):31-38.
[6]李萍,叶威,张振华.硫化亚铁自燃氧化倾向性的研究[J].燃烧科学与技术,2004,10(2):12-15.
*基金项目:国家自然科学基金 (51174153、51374164)。
作者简介董洪芹,女, 硕士。
(收稿日期:2014-12-25)
Research and Discussion on Spontaneous Combustion Mechanism of Pyrites
DONG HongqinCHEN XianfengYANG HaiyanLIU Xiao
(SchoolofResourcesandEnvironmentalEngineering,WuhanUniversityofTechnologyWuhan430070)
AbstractSpontaneous combustion of pyrites is one of the major disasters in mining process. Spontaneous combustion of ore would not only cause a huge of resource wastes and economic losses, but also trigger a series of safety and environmental issues. This paper studies the chemical thermodynamics mechanism of spontaneous combusted pyrites and the main reasons leading to spontaneous combustion of pyrites are found out. The oxidation characteristic in the spontaneous combustion process of pyrite is studied by analyzing the DSC curves and the change rules of spontaneous combustion characteristics are analyzed through comparing the heat flow curves and change tendencies in the characteristic temperature points between different particle sizes of pyrite samples. The activation energies of pyrites are calculated by thermal analysis dynamics methods, and activation energy values of pyrite samples in different particle sizes are compared, providing the basis for the study of the possibilities and characters of spontaneous combustion.
Key Wordspyritespontaneous combustionthermal kineticsactivation energy
