中空结构纳米PtNi催化剂对乙醇电氧化性能研究
2016-07-24周洋李巧霞徐群杰
周洋,李巧霞,徐群杰
(上海电力学院上海市电力材料防护与新材料重点实验室,上海200090)
中空结构纳米PtNi催化剂对乙醇电氧化性能研究
周洋,李巧霞,徐群杰*
(上海电力学院上海市电力材料防护与新材料重点实验室,上海200090)
以H2PtCl6·6 H2O和NiC4H6O4·4 H2O为金属前驱体,XC-72R作为载体,Na3C6H5O7作为络合剂,KBH4作为还原剂,采用两步浸渍还原法合成具有中空结构的PtNi/C纳米催化剂。使用透射电子显微镜法(TEM)、X射线衍射法(XRD)、能量散射X射线谱(EDX)和X射线光电子谱法(XPS)对其进行物理表征,循环伏安曲线(CV)和计时电流曲线对其在酸性乙醇中进行催化氧化性能测试,结果显示PtNi纳米粒子具有中空结构,其对酸性乙醇的催化氧化能力及稳定性较一步浸渍还原法合成的纳米催化剂都有所提高。
PtNi;催化剂;乙醇;中空结构;催化氧化
Pt和Pd作为低温燃料电池催化氧化最好的单金属催化剂有着诸多优点,但也存在着不足,如能量密度不高等缺点。对于此问题很多学者进行了相关研究,例如加入第二种、第三种元素与Pt形成合金或者金属间化合物来提高其催化氧化活性[1]。
中空纳米金属材料与它的实心材料相比存在很多优点,比如低密度、节约原料和降低成本等。具有中空结构的Pt和PtCo催化剂用于甲醇的催化氧化已经有所报道[2]。替代模板法制备中空结构的PtNi催化剂用于氨硼烷制氢也有相关报道[3],这种方法都是在合成了纳米粒子之后移除模板进行的,这样可能会破坏纳米粒子的结构。
本文通过两步浸渍还原法制备具有中空结构的PtNi/C催化剂,对其进行相关的表征和测试,结果显示其具有中空结构,在酸性乙醇中的催化氧化能力以及稳定性较优异。
1 实验
1.1 试剂与仪器
六水合氯铂酸H2PtCl6·6 H2O(国药集团),四水合乙酸镍NiC4H6O4·4 H2O(阿拉丁),纳米活性炭XC-72R(阿拉丁),柠檬酸钠Na3C6H5O7(国药集团),硼氢化钾KBH4(阿拉丁),乙醇C2H5OH(阿拉丁),硫酸H2SO4(国药集团),Nafion溶液(杜邦公司)均为分析纯。溶液用去离子水配制。
使用JEM-2100F场发射透射电镜(JEOL)观察样品的形貌与粒径,HORIBA能谱分析仪(EMAX)分析样品元素组成,D8 Advance X-射线粉末衍射仪(Bruker)分析合金样品结构,PHI X射线光电子能谱分析仪(5000CESCA)分析元素化合价。由玻碳电极(直径D=2 mm)的工作电极、饱和甘汞参比电极和铂片对电极组成三电极体系,采用CHI660C电化学分析仪(上海辰华)测试电极电化学性能。溶液通高纯氮气30 min除溶解氧。
1.2 两步法PtNi/C纳米粒子的制备方法
1.2.1 活性炭预处理
称取一定量的活性炭Vulcan XC-72R在90℃5.0 mol/L HNO3溶液中强力搅拌5 h,冷却至室温,抽滤,水洗,130℃真空干燥6 h,研磨后200目筛分,密封保存。
1.2.2 PtNi纳米粒子的制备
称量0.023 4 g活性炭溶于10 mL无水乙醇,超声分散30 min形成炭浆。将2.65 mL 0.05 mol/L NiC4H6O4·4 H2O溶液和0.134 5 g Na3C6H5O7加入到10 mL去离子水中超声分散,逐滴加到上述炭浆溶液中,磁力搅拌1 h。蠕动泵滴加KBH4溶液(0.05 g KBH4和10 mL去离子水)反应2 h。将2 mL 0.02 mol/L H2PtCl6·6 H2O溶液(Pt负载量20%)和0.142 0 g Na3C6H5O7加入到10 mL去离子水中,重复上述步骤(文中简称TS)。最后抽滤,用乙醇和去离子水反复冲洗,80℃真空干燥6 h。
称取0.023 4 g活性炭溶于10 mL无水乙醇超声分散30 min形成炭浆。将2 mL 0.02 mol/L H2PtCl6·6 H2O溶液、2.65 mL 0.05 mol/L NiC4H6O4·4 H2O溶液和0.268 5 g Na3C6H5O7加入到30 mL去离子水中搅拌(Pt负载量20%),将分散好的前驱体液逐步滴加到炭浆中。室温下磁力搅拌1 h使其充分混合。蠕动泵滴加KBH4溶液(0.1 g KBH4和20 mL去离子水)反应2 h(文中简称OS)。抽滤,用乙醇和去离子水反复冲洗,80℃真空干燥6 h。
1.2.3 电极和测试
工作电极的制备:将2.5 mg PtNi/C催化剂加入0.5 mL乙醇、0.5 mL去离子水和120 μL Nafion溶液,超声分散,制成墨水。移取2.6 μL该墨水于新抛光玻碳电极表面,自然晾干备用。在室温下0.5 mol/LH2SO4+0.5 mol/LC2H5OH溶液中测试电化学性能。
2 结果与讨论
2.1 物理表征
图1是合成的PtNi纳米粒子催化剂的TEM图像,从图中可以看出纳米粒子是单分散的球形,平均粒径大概为16.8 nm。图1c是单个纳米粒子的HRTEM图像,图像显示纳米粒子的中间区域比圆形边框亮很多且边框厚度比较均匀,表明这可能是一个中空的纳米微球[4]。图1b是图1a的粒径统计图,从柱形图可以看出纳米粒子的最小粒径为9 nm,最大粒径为25 nm,平均粒径为17 nm,且纳米粒子的整体粒径分布比较均匀,过大或过小的粒子比较少。图1a显示纳米粒子有小部分的团聚,但总体均匀分布在纳米碳粒上。图2是纳米粒子的EDS图像,从图中可以看出PtNi原子都存在,这与实验的预想比较吻合。
图3是PtNi纳米催化剂和商业JM Pt/C催化剂的XRD谱图,JM商业催化剂Pt的(111),(200),(220),(311)四个特征峰与其面心立方结构的4个基础峰完全吻合。PtNi催化剂的4个特征峰与商业JM的4个特征峰相比,峰面明显变宽,但是没有明显的如Ni或者其氧化物相分离的特征峰,这表明可能形成了PtNi合金。另外,PtNi催化剂的2 θ峰有一定的偏移,这与Vegard定律相吻合[5]。

图1 PtNi/C催化剂TEM图像
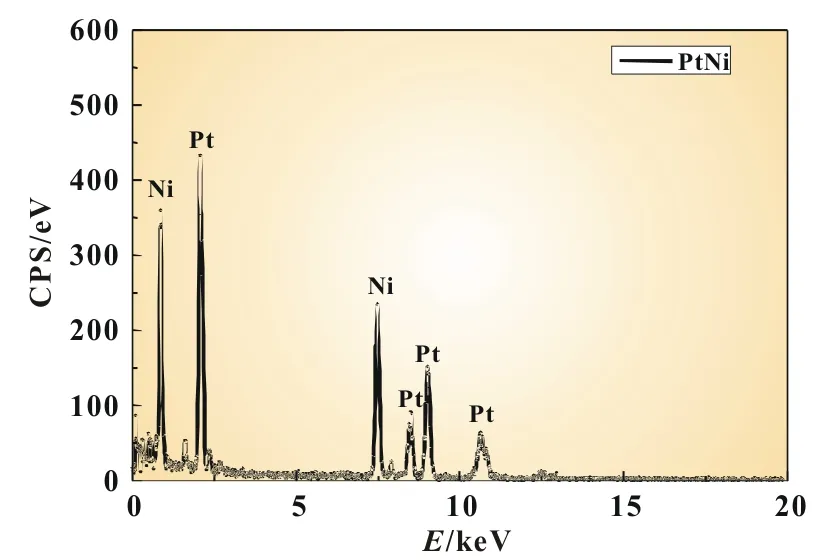
图2 PtNi纳米粒子的EDS图像
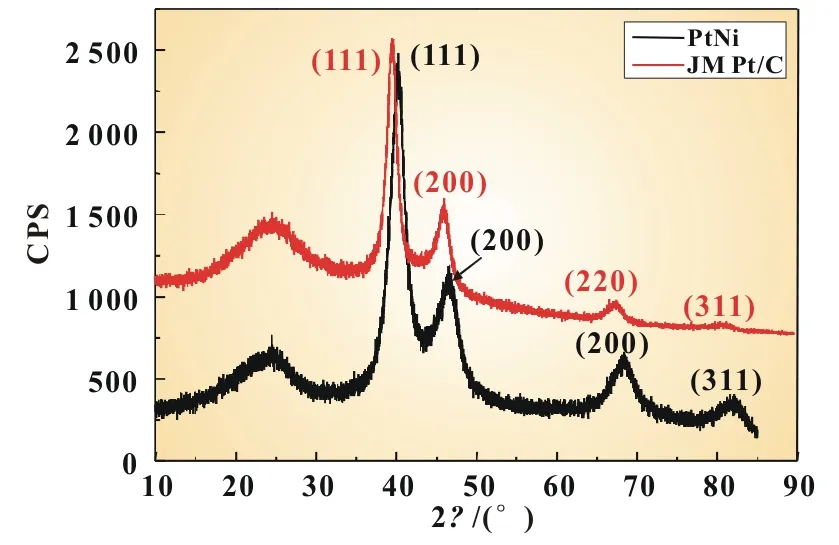
图3 Pt/C和PtNi/C的XRD衍射图
图4是PtNi纳米球Pt 4f的XPS频谱图。Pt 4f7/2和Pt 4f5/2的峰值分别出现在71.5(峰1)和74.6 eV(峰3),这与金属Pt0的峰值相对应。图中72.0(峰2)和75.5 eV(峰4)的峰可能是诸如PtO和Pt(OH)2之类的Pt2+化合物。比较峰的相对强度可以看出0价Pt金属占主要部分。与文献报道的Pt/C纳米粒子中Pt 4f7/2峰值71.40 eV相比,PtNi纳米球Pt 4f7/2峰值出现了一定的右移,表明Pt的电子特性可能有所改变,从而影响发生在低超电位下C-H键的断裂。PtNi中空微球可能的形成机理涉及到Na3C6H5O7微团的形成和具有磁性PtNi纳米粒子的团聚[4]。
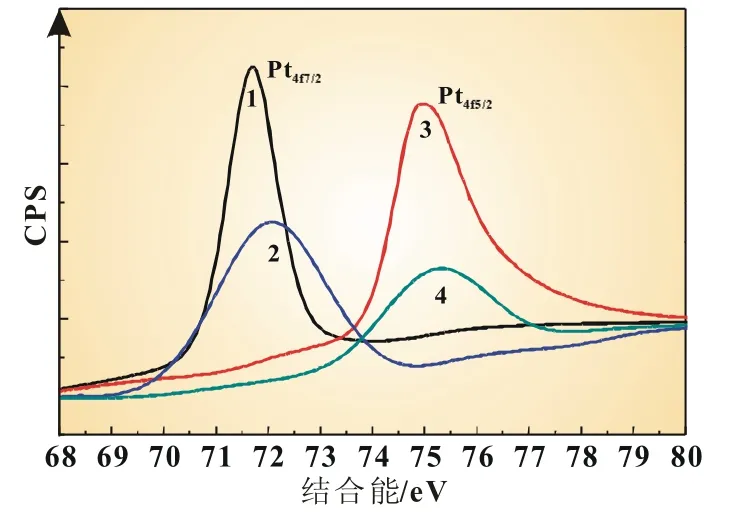
图4 PtNi纳米球Pt 4f的XPS频谱
2.2 电化学测试
图5是PtNi/C催化剂在0.5 mol/L H2SO4溶液中的循环伏安曲线,扫速为50 mV/s。图中曲线表明这是发生在Pt晶体上的典型的吸氢和氧化特征峰[6]。从图中曲线可以看出,与纯Pt/C的催化剂相比,图中曲线表现出了更负的氢低电位沉积电势(UPD),从CV曲线中还可以推断出中空纳米粒子表面富集的是一层Pt,没有其他的非贵金属及其氧化物,因为其特征峰在CV曲线中没有反应,这与前期的一些研究相一致[7]。

图5 室温下PtNi/C催化剂在N2饱和的0.5 mol/L H2SO4溶液中的循环伏安曲线
图6是三种不同的催化剂在0.5 mol/L H2SO4+0.5 mol/L C2H5OH中的循环伏安曲线,从图中可以看出不论是一步法还是两步法合成的催化剂,其催化氧化活性较商业的JM都有所提高,尤其是两步法合成的催化剂其性能较一步法合成的催化剂有较大提高。在这里我们可以用阳极峰电流的前扫值(If)和后扫值(Ib)的比值来描述其在酸性乙醇中对催化氧化过程中吸附中间体的容忍度[8]。If/Ib的比值越低表明其对催化氧化前扫过程中产生的氧化物中间体的氧化能力越差,也就是说氧化物中间体在Pt表面的积累越来越严重[9]。图6中曲线If/Ib值计算表明,两步法合成的PtNi催化剂的If/Ib值最大为0.982,与商业催化剂的0.976相当,高于一步法合成的催化剂的0.960,两步法合成的催化剂的If/Ib值是一步法的1.023倍。If/Ib值表明两步法合成的中空PtNi催化剂较其它两种催化剂拥有更右移的抗中毒能力。

图6 室温下PtNi/C催化剂在N2饱和的0.5 mol/L H2SO4+0.5 mol/L C2H5OH溶液中的循环伏安曲线
图7是三种催化剂在0.5 mol/L H2SO4+0.5 mol/L C2H5OH溶液中的时间电流曲线。两步法合成的中空PtNi催化剂较其它两种催化剂拥有更高且更稳定的电流。图中三条曲线可以看出,一开始电流下降得都比较快,大约500 s趋于平稳。中空PtNi催化剂优异的稳定性可能归结于以下三种原因:双功能机理、Pt电子结构的改变以及中空结构的纳米粒子[10]。
3 结论
通过两步浸渍还原法合成具有中空结构的PtNi纳米粒子,TEM图像显示出其明显的中空结构。循环伏安法和计时电流法测试结果表明其相对于一步法合成的PtNi催化剂和商业催化剂都拥有较好的电化学活性和稳定性。
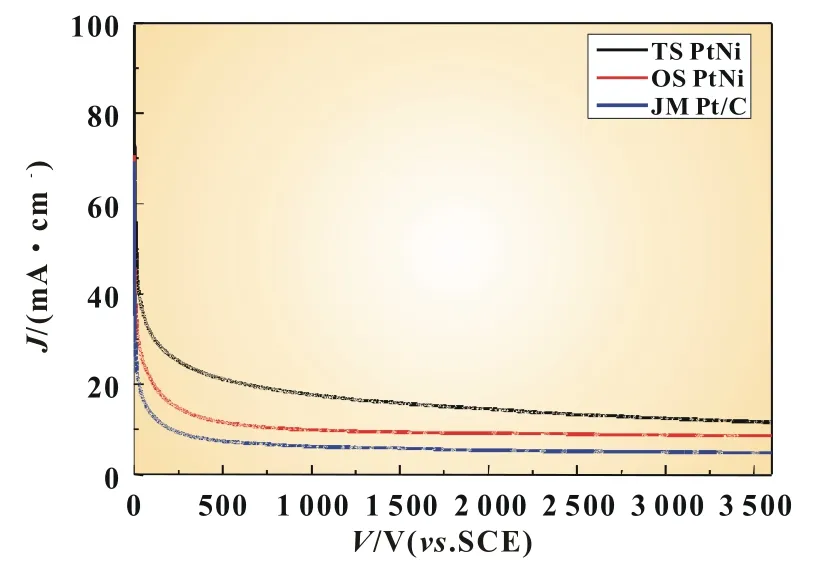
图7 室温下PtNi/C催化剂在N2饱和的0.5 mol/L H2SO4+0.5 mol/L C2H5OH溶液中的时间电流曲线
[1]李巧霞,毛宏敏,徐群杰,等.用不同络合剂制备的Pd-Sn/C催化剂在碱性溶液中对乙醇氧化的电催化性能[J].高等学校化学学报,2014,35(3):602-607.
[2]HERAS D L,ROBERTS E,LANGTON R,et al.A review of metal separator plate materials suitable for automotive PEM fuel cells[J].Energy&Environmental Science,2009,2:206-214.
[3]CHENG F,MA H,LI Y.Ni1-xPtx(x=0~0.12)hollow spheres as catalysts for hydrogen generation from ammonia borane[J].Inorganic Chemistry,2007,46:788-794.
[4]GE C,XIA D G,NIE Z R,et al.Facile synthesis of Co-Pt hollow sphere electrocatalyst[J].Chemistry of Materals,2007,19:1840-1844.
[5]AHRENSTORF K,ALBRECHT O,HELLER H,et al.Colloidal synthesis of NixPt1-xnanoparticles with tuneable composition and size[J].Small,2007,3:271-274.
[6]SCHMIDT T J,GASTEIGER H A,STAB G D,et al.Characterization of high surface area electrocatalysts using a rotating disk electrode configuration[J].Journal of the Electrochemical Society,1998,145:2354-2358.
[7]DUBAU L,DURST J,MAILLARD F,et al.Further insights into the durability of Pt3Co/C electrocatalysts:Formation of“hollow”Ptnanoparticles induced by the Kirkendall effect[J].Electrochimica Acta,2011,56:10658-10667.
[8]WU Y N,LIAO S J,LIANG Z X,et al.High-performance core shell PdPt@Pt/C catalysts via decorating PdPt alloy cores with Pt[J].Journal of Power Sources,2009,194:805-810.
[9]WU J J,TANG H L,WAN Z H,et al.Novel methanol electro-oxidation catalyst assisting with functional phthalocyanine supports[J].Electrochimica Acta,2009,54:1473-1477.
[10]MAYRHOFER K J,JUHART V.Adsorbate-induced surfaces segregation for core shell nanocatalysts[J].Angewandte Chemie International Edition,2009,48:3529-3531.
Research of electrooxidation performance of hollow structure PtNi/C nanocatalyst for ethanol
ZHOU Yang,LI Qiao-xia,XU Qun-jie*
(Shanghai Key Laboratory of Materials Protection and Advanced Materials in Electric Power,Shanghai University of Electric Power,Shanghai 200090,China)
Two step impregnation reduction method was used to prepare PtNi/C nanocatalyst;H2PtCl6·6 H2O and NiC4H6O4·4 H2O was used as the metal precursor;XC-72R was used as the carrier;Na3C6H5O7and KBH4were used as complexing agent and reducing agent,respectively.TEM,XRD,EDX and XPS were used to observe and characterize the morphology and structure of the catalyst.Cyclic voltammetry curves and time current curves were used to characterize the electrochemical performance of the catalyst.The result shows that the hollow catalyst has better catalytic oxidation property and stability than the catalyst prepared by one step impregnation reduction.
PtNi;catalyst;ethanol;hollow structure;catalytic oxidation
TM 911
A
1002-087 X(2016)08-1597-03
2016-01-12
国家自然科学基金项目(21103107)
作者介绍:周洋(1986—),男,江苏省人,硕士,主要研究方向为燃料电池催化剂。
