纳米TiO2富集-石墨炉原子吸收光谱法测定粮食中痕量钼
2016-07-20鲁群苟湖北省产品质量监督检验研究院
□ 鲁群苟 吴 麟 湖北省产品质量监督检验研究院
纳米TiO2富集-石墨炉原子吸收光谱法测定粮食中痕量钼
□ 鲁群苟 吴 麟 湖北省产品质量监督检验研究院
摘 要:笔者建立了纳米TiO2富集-石墨炉原子吸收光谱法测定粮食中痕量钼的分析方法。主要考察了纳米TiO2对钼的分离富集中吸附和洗脱的影响因素,探讨了共存元素对测定Mo的影响。实验结果表明,方法检出限低,精密度好,环境污染小。应用于大米、小麦等粮食样品中痕量Mo的测定,获得了良好的分析结果。
关键词:石墨炉原子吸收光谱法;纳米TiO2;分离富集;粮食;钼
钼是一种人体必需的微量元素,在人体防止龋齿,促进铁的新陈代谢,预防贫血和癌症等方面具有重要作用[1 - 2]。人体中的钼主要来自于食物,建立食品中痕量钼的分析方法具有重要现实意义。钼的测定方法很多,主要有分光光度法[3- 4]、催化极谱法[5]、原子吸收光谱法[6-7]、电感耦合等离子体原子发射光谱法[8- 9]以及电感耦合等离子体质谱法[1 0- 11]等。但由于粮食中钼的含量极低,常规分析仪器较难直接测定。常需要对样品中痕量钼进行预富集。目前,常用的分离富集方法有固相萃取法[1 2- 1 3]、液液萃取法[1 4-1 5]、液膜富集法[1 6]、共沉淀法[1 7]等。固相萃取具有富集效率高、环境污染小、操作简便等优点,所以得到广泛应用。纳米TiO2对一些金属离子具有很强的吸附能力,是痕量金属离子理想的分离富集材料[1 8-21]。
本文以纳米TiO2为吸附剂,以石墨炉原子吸收光谱法为测试手段,建立了纳米TiO2富集-石墨炉原子吸收光谱法测定粮食样品中钼的分析方法。主要考察了纳米TiO2对钼的分离富集中吸附和洗脱的影响因素,探讨了共存元素对测定Mo的影响。实验结果表明,该法检出限低,精密度好,环境污染小、操作简便。应用于大米样品中痕量Mo的测定,获得了良好的分析结果。
1 实验部分
1.1 主要仪器与设备
WFX- 110型原子吸收分光光度计(北京瑞利分析仪器公司),钼空心阴极灯,Milli-Q超纯水系统(美国Millipore公司)、离心机、恒温振荡器、pH计等。仪器工作参数为:分析线313.3 nm,光谱通带0.2 nm,灯电流3.5 mA。石墨炉升温程序见表1。

表1 石墨炉升温程序
Multiwave 3000微波消解仪(Anton Paar),工作条件见表2。

表2 微波消解程序
1.2 主要试剂与溶液
钼标准储备液(ρ(Mo)=400 mg/L):称取0.184 g钼酸铵粉末溶解于50 mL超纯水中,加入10 m L氨水,定容至250 mL。钼工作溶液现用现配。
标准样品:GBW10043(辽宁大米);GBW10044(四川大米);GBW10045(湖南大米);GBW10046(河南小麦)。
氨水溶液(ϕ(NH3·H2O)=10%):移取10 mL浓氨水稀释定容至100 mL。
盐酸溶液(ϕ(HCl)=10%):移取10 mL浓盐酸稀释定容至100 mL。
氢氧化钠溶液(C(NaOH0)=.25 mol/ L):称量5 g氢氧化钠溶解于100 mL超纯水中,溶解定容至500 mL。
硝酸溶液(ϕ(HNO3)=2%):移取20 mL浓硝酸,加超纯水定容至1L。
纳米TiO2(粒径10~100 nm):使用前用5 mol/L HNO3浸泡15 min,然后用超纯水洗至中性,抽滤,于100℃下烘干备用。
盐酸、硝酸、氢氧化钠、氨水等试剂均为分析纯,水为超纯水。
所有器皿均用HNO3溶液(j(HNO3)=10%)浸泡24 h,再用超纯水冲洗3次,烘干备用。
1.3 实验方法
1.3.1 纳米TiO2的预处理
用5 mol/L HNO3浸泡15 min,然后用超纯水洗至中性,抽滤,于100℃下烘干备用。
1.3.2 工作曲线的制作
配置浓度分别为25、50、100、150、200 μg/L的Mo标准系列溶液,用HCl溶液和氨水溶液调节pH=1.5左右,移取10 mL样品溶液到10 mL塑料具塞离心管中,加入0.1 g纳米TiO2,振荡10分钟,静置30分钟后离心,弃去上清液,用盐酸溶液清洗纳米TiO2,然后加入2 mL 0.25 mol/L NaOH,90℃水浴振荡30 min,静置30分钟后移取上清液,用石墨炉原子吸收光谱仪测定。工作曲线见图1。
1.3.3样品测定
准确称取0.05~0.2 g样品于微波消解罐中,加入4 mL HNO3和1 mL H2O2浸泡7 h,按照表2程序进行消解。消解完毕后置于加热套中于120℃赶酸,待溶液基本蒸干时,加少量硝酸溶液(ϕ(HNO3)=2%)溶解,取下冷却至常温,将消解液转移到10 m L塑料具塞离心管中,定容。其余同工作曲线的制作。
2 结果与讨论
2.1 吸附条件的选择
分别移取浓度为5 μg/mL Mo工作溶液1.0 mL于7支10 mL塑料具塞离心管中,加水至2/3左右,用HCl溶液和氨水溶液分别调节酸度为0.25~3.00,再加入纳米TiO20.1 g,振荡吸附10 min。测定上清液中Mo的含量,计算其吸附率。实验结果如图2所示。从图2可看出当pH=1.50左右时,纳米TiO2对Mo的吸附率在90%以上,吸附效果最佳,所以本实验选择吸附酸度为pH=1.50。
2.2 洗脱条件实验
2.2.1 洗脱剂及浓度的选择
从吸附条件实验中可知纳米TiO2吸附Mo时在强酸强碱性条件下吸附率较低,以此作为洗脱剂的选择依据,考虑到纳米TiO2也易吸附其他金属离子,故选择碱性条件进行洗脱。实验选择NaOH溶液作为洗脱剂,考察了不同浓度的NaOH溶液对Mo洗脱率的影响,实验结果见图3。从图3中可以看出,0.20~0.30 mol/L的NaOH洗脱效果较佳,但整体洗脱率偏低,均在55%左右。
2.2.2 洗脱温度的选择
为了提高Mo的洗脱率,进一步实验得知温度对洗脱率影响较大。采用水浴加温的方式进行洗脱,改变水浴温度进行实验,实验结果见图4。从图4可知,洗脱率随水浴温度的提高而增高,90℃时最大值达到80%左右。
2.2.3 振荡时间的选择
为了进一步提高洗脱效率,洗脱的同时进行振荡。并改变振荡时间进行实验,结果见图5。实验结果表明,当振荡时间为30 min时,洗脱率达90%以上。
综上,本法选择的洗脱条件为:NaOH浓度为0.20~0.30 mol/L,在90℃水浴下振荡30 min。
2.3 共存离子的影响
按实验方法,考察了共存离子对Mo测定结果的影响。以测定误差不超过±5%计,2 000倍的Na+、K+、Ca2+、Mg2+,200倍的Al3+、Zn2+、Mn2+、 SO2-,100倍的Fe3+、Cu2+、Cd2+、PO3-
44等不干扰测定。

图1 工作曲线

图2 酸度对Mo吸附率的影响

图3 NaOH浓度对Mo洗脱率的影响
2.4 方法检出限、精密度及线性范围
根据IUPAC的定义,测得本法检出限(k=3s)为0.01 μg/ g,相对标准偏差(RSD)为5.87%。标准曲线回归方程为y=0.0026x-0 .0033(R2=0.9998),在10~200 μg /L范围内有良好的线性关系。
2.5 样品分析结果
按照样品测定方法,对国家粮食标准物质进行了测定,结果见表3。可见分析结果可靠。
参考文献
[1]郑艺梅,胡承孝.食物中的钼与人体健康[J].广东微量元素科学,2005,12(8):1-6.
[2]吴茂江.钼与人体健康[J].微量元素与健康研究,2006,23(5):66-67.
[3]刘奇,李坤威,李永芳.活性炭柱吸附富集-分光光度法测定饮用水中痕量钼(Ⅵ)[J].分析试验室,2004,23(2):68-70.
[4]樊雪梅,王书民,周美,等.抑制动力学分光光度法测定钼尾矿中痕量钼[J].分析试验室,2012,31(11):94-96.
[5]陈志慧,孙洛新,钟莅湘,等.快速催化极谱法测定土壤中的有效态钼[J].岩矿测试,2014,33(4):584-588.
[6]黄仁忠.三乙醇胺增敏火焰原子吸收光谱法测定地质样品中的钼[J].岩矿测试,2009,28(6):587-589.
[7]江文兵,甘志勇.微波消解样品-石墨炉原子吸收光谱法测定土壤中钼量[J].理化检验(化学分册),2013,49(9):1061-1064.
[8]盛献臻,张汉萍,李展强,等.电感耦合等离子体发射光谱法同时测定地质样品中次量钨锡钼[J].岩矿测试,2010,29(4):383-386.
[9]李春香,秦永超,梁沛,等.纳米TiO2分离富集和ICP-AES测定地质样品中的钼和钨[J].分析科学学报,2002,18(3):186-189.
[10]樊祥,韩丽,张润何,等.微波消解-电感耦合等离子体质谱法测定乳制品中铬、钼和硒[J].分析科学学报,2015,31(3):409-412.
[11]侯振辉,王晨香.电感耦合等离子体质谱法测定地质样品中35种微量元素[J].中国科学技术大学学报,2007,37(8):940-944.
[12]罗道成,汪威,安静.阴离子树脂分离富集光度法测定尾矿中微量钼[J].分析试验室,2012,31(3):116-119.
[13]高显会,郭兴家,朱继芬,等.717型阴离子交换树脂分离富集-光度法测定铜精矿和尾矿中微量钼[J].冶金分析,2012,32(4):75-78.
[14]ALD Comitre,BF Reis.Liquid-liquid Extraction Procedure Exploiting Multicommutation in Flow System for the Determination of Molybdenum in Plants[J].Analytica Chimica Acta,2003,479(2):185-190.
[15]M Shamsipur,S Habibollahi.A Highly Sensitive Procedure for Determination of Ultra Trace Amounts of Molybdenum by Graphite Furnace Atomic Absorption Spectrometry After Dispersive Liquidliquid Microextraction[J].Microchimica Acta,2010,171(3):267-273.
[16]王献科,李玉萍,李莉芬.液膜分离富集痕量钼[J].中国钼业,2002,26(5):34-36.
[17]付爱瑞,肖凡,罗治定,等.氢氧化锰共沉淀分离-催化极谱法测定土壤中有效钼[J].理化检验(化学分册),2012,48(4):417-419.
[18]施踏青,梁沛,李静,等.纳米二氧化钛分离富集ICP-AES测定镉、钴、锌的研究[J].光谱学与光谱分析,2005,25(3):444-446.
[19]陈松涛,徐婉珍,闫永胜,等.纳米二氧化钛预富集火焰原子吸收光谱法同时测定锌铜的研究[J].冶金分析,2009,29(3):72-75.
[20]谷晓稳,吕学举,贾琼,等.石墨烯/二氧化钛复合材料富集-石墨炉原子吸收光谱法测定铅和镉[J].分析化学,2013,41(3):417-421.
[21]邓月华,闫永胜,张雯,等.改性纳米二氧化钛对钼(VI)的吸附行为研究[J].冶金分析,2009,29(10):55-59.
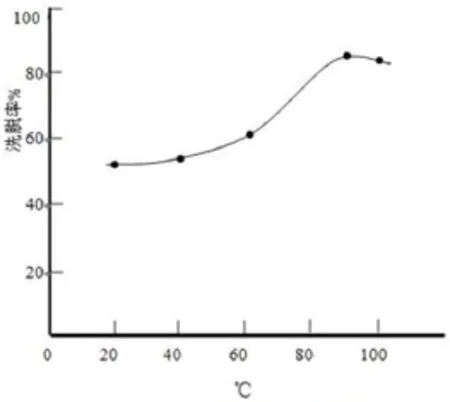
图4 水浴温度对Mo洗脱率的影响

图5 振荡时间对Mo洗脱率的影响
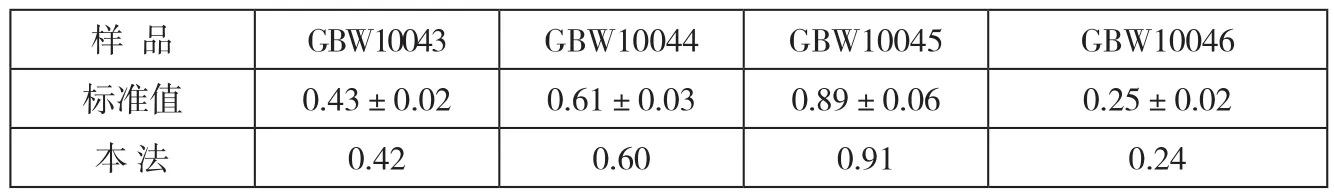
表3 样品分析结果(ω(Mo)10-6,n=5)
