左心瓣膜替换术后三尖瓣功能性关闭不全患者外科再次手术的远期预后分析
2016-07-19佟明汇史艺刘燊骆翔董超杨研王巍许建屏
佟明汇,史艺,刘燊,骆翔,董超,杨研,王巍,许建屏
左心瓣膜替换术后三尖瓣功能性关闭不全患者外科再次手术的远期预后分析
佟明汇,史艺,刘燊,骆翔,董超,杨研,王巍,许建屏
摘要
目的:分析左心瓣膜替换(LSVR)术后出现功能性三尖瓣关闭不全(FTR)患者行再次三尖瓣手术的远期预后,评估FTR患者再次外科手术的适宜时机。
方法:回顾性分析我院1999-01至2013-01期间共59例既往LSVR术后出现FTR而再次进行三尖瓣手术患者的临床资料,对所有患者进行术后随访及统计分析。
结果:59例患者中5例(8.5%)于围术期内死亡,术后总死亡率为11.9%(7/59)。对围术期存活的54例患者均进行随访,平均随访时间为51.1(21~188)个月,其中19例(35.2%)患者出现主要心脏不良事件(MACE),30例(55.6%)患者术后心功能得以改善。单因素分析显示术前纽约心脏协会(NYHA)心功能分级Ⅳ级(P=0.008)、术前右心室功能不全(P=0.037)、合并同期再次左心瓣膜手术(P=0.017)及行TVR术(P=0.002)是患者再次三尖瓣手术后全因死亡的危险因素,进一步行多因素分析显示术前右心室功能不全是影响患者远期免于MACE生存率的唯一独立危险因素[风险比(HR): 3.0;95%可信区间(CI): 1.11~8.2;P=0.031],而再次TVR术(HR:12.80;95% CI:1.53~107.02;P=0.019)及术前NYHA心功能分级Ⅳ级(HR:5.31;95% CI:1.20~24.51;P=0.032)则是影响再次三尖瓣术后患者远期死亡的独立危险因素。
结论:对于右心功能仍处于代偿期的功能性三尖瓣关闭不全的患者,再次三尖瓣手术的远期手术效果较佳。在患者出现右心室功能不全之前积极地进行再次手术治疗三尖瓣病变,可能使患者获益。
关键词 三尖瓣关闭不全;心脏人工瓣膜植入;右心室功能不全
Objective: To analyze the long-term prognosis of re-operation in patients with functional tricuspid regurgitation (FTR) after left sided valve replacement (LSVR) and hence evaluate the optimal timing of mentioned re-operation.
Methods: A total of 59 FTR patients who had re-operation after their prior LSVR in our hospital from 1999-01 to 2013-01 were analyzed. The clinical information and post-operative follow-up results were recorded in all patients.
Results: There were 5/59 (8.5%) patients died in peri-operative period and the overall post-operative mortality was 11.9% (7/59). The follow-up data of 54 survivors were available for the mean time of 51.1 (21-188) months. There were 19/54 (35.2%) patients suffered from MACE and 30 (55.6%) were benefited by improved cardiac function. Uni-variable analysis indicated that pre-operative NYHA class IV (P=0.008), pre-operative right ventricular (RV) dysfunction (P=0.037), concomitant leftsided redo-operation (P=0.017) and TVR operation (P=0.002) were associated with all cause mortality of tricuspid re-operation. Multi-variable Cox regression analysis showed that pre-operative RV dysfunction was the only independent risk factor of long term MACE-free accumulating survival rate (HR=3.0, 95% CI 1.11-8.2, P=0.031); while TVR operation (HR=12.8, 95% CI 1.53-107.02, P=0.019) and pre-operative NYHA class IV (HR=5.3, 95% CI 1.20-24.51, P=0.032) were the independent riskfactors for long-term mortality in patients after tricuspid re-operation.
Conclusion: Patients with compensatory RV function showed better long term prognosis after secondary tricuspid operation. Aggressive re-operation before the occurrence of right ventricular dysfunction could be beneficial for relevant patients.
Key words Tricuspid valve insufficiency; Heart valve implantation, artificial; Ventricular dysfunction, right
(Chinese Circulation Journal,2016,31:376.)
功能性三尖瓣关闭不全(FTR)指无器质性的三尖瓣病变。左心瓣膜病变患者进行左心瓣膜替换(LSVR)手术后出现FTR是心脏外科常见的继发性瓣膜病变。既往观念认为LSVR后继发严重FTR的患者相对罕见,而且FTR在LSVR术后可以得到改善,缺乏外科手术治疗意义。然而国外研究指出:在左心瓣膜术后的患者之中,多达16%~67%的患者可出现远期FTR。若任由FTR进展而不作干预,可导致不可逆性右心衰竭[1, 2]。研究表明[3]FTR是LSVR术后患者预后不良的危险因素。虽然最新的心脏瓣膜外科指南将左心瓣膜病变合并三尖瓣严重关闭不全的患者同期行三尖瓣外科治疗列为I级推荐[4],但对于LSVR术后出现FTR患者的再次手术指证,仍缺乏明确的指引。既往研究报道FTR患者再次手术效果极差,近期手术死亡率高达37%[5]。临床上对于这些患者的再次手术指征未有共识,导致许多FTR患者错失再次手术的最佳时机。本文拟报道我院LSVR术后FTR患者再次手术的远期手术效果,并探讨该类患者的再次手术时机。
1 资料与方法
临床资料:回顾1999-01至2013-01期间,对既往LSVR术后出现FTR并于我院行再次手术治疗三尖瓣病变的患者进行筛选。左心瓣膜疾病的诊断符合现行外科指南标准[4, 6]。FTR被定义为无明确器质性病变或者瓣下组织结构异常的三尖瓣关闭不全。排除标准:先天性、风湿性、退行性三尖瓣病变,合并感染性心内膜炎及冠状动脉疾病患者。所有入选患者术前3个月内均于我院进行超声心动图检查并确诊为中度或以上程度的FTR。患者右心室功能不全的标准为(1)术前超声心动图所见符合:①右心室壁活动异常;②二尖瓣平面下移<2.0 cm;③下腔静脉扩张>2 cm[3, 7]。(2)符合下述临床表现:①患者日常活动明显受限,纽约心脏协会(NYHA)心功能分级Ⅲ~Ⅳ级;②胃纳差并伴有进行性恶液质状态;③依赖利尿剂的静脉系统淤血表现(肝脾淤血性增大、周围性水肿、肝颈静脉返流征阳性、顽固性腹水)。所有患者术前均经药物积极治疗,术前常规行X线胸部计算机断层摄影术(CT)检查以了解胸骨下心脏(心包)的粘连情况。术中行经食道超声心动图(TEE)以评估瓣膜病变及手术效果。所有患者采取胸骨正中切口,手术均在全麻、体外循环下进行。
本研究入选再次三尖瓣手术FTR患者共59例,其中男性17例,女性42例,平均年龄(51.7±8.6)岁;患者术前临床基线资料见表1。为进一步研究根据患者再次三尖瓣术式将患者分为TVP组及TVR组。对所有入选患者于术后5天或出院前复查超声心动图。
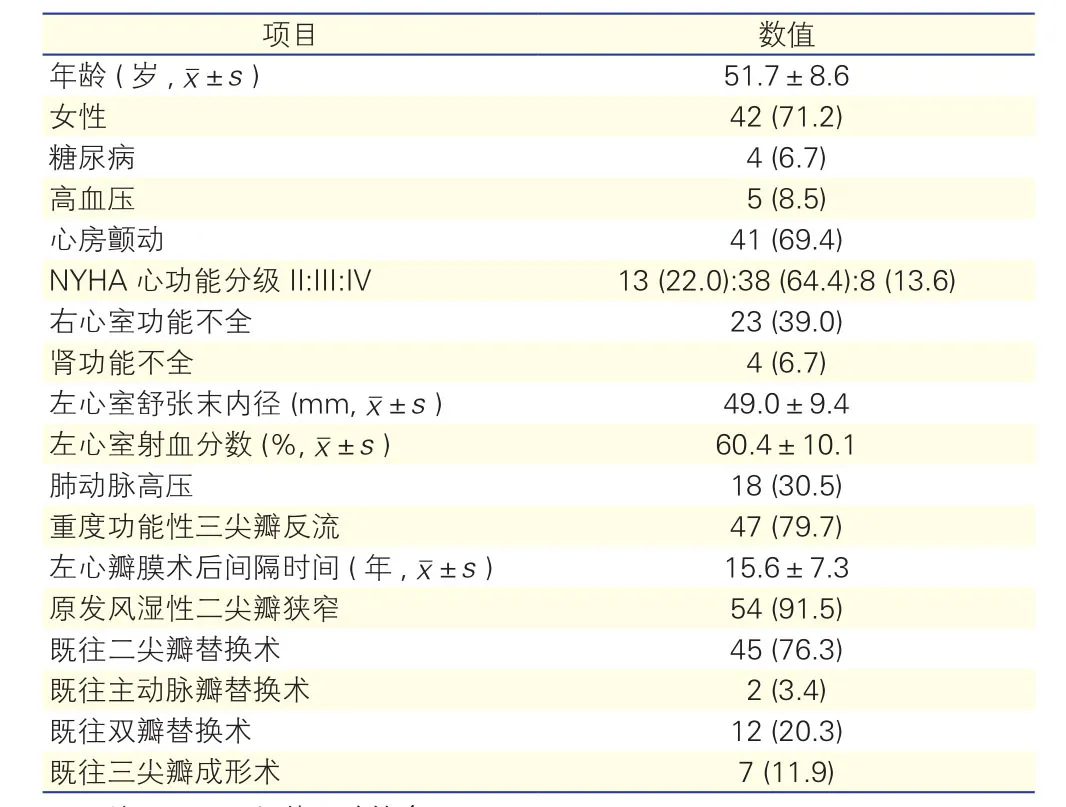
表1 患者术前临床基线资料[n=59,例(%)]
随访:通过门诊复查及电话对所有患者或其家属进行随访。将主要心脏不良事件(MACE)设置为:术后死亡、术后再次出现三尖瓣中量或以上反流、卒中、再次心脏手术、心力衰竭及瓣膜手术相关并发症(术后心内膜炎、心原性重要器官功能衰竭、人工瓣膜功能失灵、血栓形成及出血事件)。
统计方法:所有计量资料采用均数±标准差表示,计数资料以百分数表示。使用SPSS 22.0软件进行统计学分析。计量资料采用t检验比较,计数资料采用卡方检验比较,对不服从正态性或方差齐性的计量资料采用非参数检验。危险因素对预后的影响采用Kaplan-Meier生存分析,生存曲线间差异进行Log-Rank检验,对各危险因素与预后之间的关系采用COX回归分析。双侧P值<0.05被认为差异有统计学意义。
2 结果
手术结果:全部59例再次手术的患者中,40例(68%)行三尖瓣成形术(TVP),其中35例(88%)植入了三尖瓣成形环,其余5例行线性环缩三尖瓣环(De Vega成形术);另外19例患者行三尖瓣替换术(TVR),共植入15枚机械瓣膜及4枚生物瓣膜。同期再次左心瓣膜手术25例,包括8例主动脉瓣替换(AVR)、12例二尖瓣替换(MVR)及5例双瓣替换(AVR+MVR)术。经双极射频消融钳行MAZE Ⅲ型手术1例。
围术期结果:59例患者中围术期死亡5例(围术期死亡率为8.5%)。其中4例死于术后低心排综合征,床旁超声心动图提示右心室功能极度低下,右心功能衰竭;1例死于术后爆发性肺部感染并发多器官功能衰竭。围术期并发症包括二次手术探查2例,低心排综合征7例,胸腔积液、心包填塞各1例,术后切口愈合不良2例。术后早期对全部患者复查超声心动图提示7例出现三尖瓣少量反流,全部患者人工瓣膜功能满意。术后于重症监护室(ICU)的平均住院时间为6.5天,总平均住院天数为32.6天。
随访:对54例存活出院的患者进行随访,平均随访时间为51.1 (21~188)个月。结果如下:(1)心功能分级NYHAⅡ级37例(69%),Ⅲ级15例(28%),Ⅳ级2例(4%)。其中30例(55.6%)患者术后心功能得以改善。(2)死亡2例,其中1例患者于术后2年出现恶性心律失常,猝死;另一例于术后3年死于心功能衰竭。本组患者术后2年生存率及15年累积生存率分别为91.5%及87.1%。(3)共19例(35.2%)患者在随访中出现MACE:11例患者(20.4%)出现再发中到大量三尖瓣反流。2例患者分别于术后3年及4年因传导阻滞而植入心脏永久起搏器,其他并发症包括:肾功能衰竭、瓣膜相关再次手术、血栓形成及卒中各1例。1例患者术后2年因二尖瓣人工瓣瓣周漏及主动脉瓣退行性病变需行第3次心脏手术治疗。随访术后远期免于中到大量三尖瓣反流生存率为(65.9±9.5)%,而远期免于MACE生存率为(40.5±9.0)%。
预后因素分析:(1)术前右心功能不全患者的术后远期累积生存率[(72.5±11.9)% vs (94.2±4.0)%,Log rank P=0.035;图1A]及免于MACE累积生存率[(14.0±12.4)% vs ( 52.5±10.3)%; Log rank P=0.022;图1B]]均明显低于术前无右心室功能不全的患者。(2)根据患者再次三尖瓣术式将患者分为TVP组及TVR组(两组基线资料比较并无统计学差异,表2),分析术式对患者预后的影响:TVR组患者的远期累积生存率明显低于TVP组[(67.5±11.0)% vs (96.9±3.1)%,P≤0.001 ,图2A],但两组的术后远期免于MACE累积生存率并无统计学差异[(44.7±10.4)% vs (30.9±16.0)%,P= 0.725]。(3)根据患者术前有否肺动脉高压分析显示:TVP组和TVR组术后远期免于MACE累积生存率差异无统计学意义 [(40.5±8.2)% vs (39.3±11.2)%, P=0.481]。(4)根据患者术前心功能NYHAⅣ级组的远期累积生存率明显低于术前NYHA心功能分级Ⅱ~Ⅲ级组[(62.5±17.1)% vs (90.9±4.4)%,P=0.007;图2B)]。
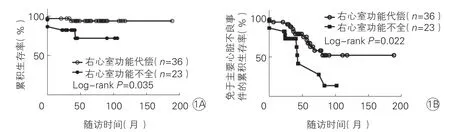
图1 Kaplan-Meier生存曲线显示根据患者术前右心室心功能分组的预后情况
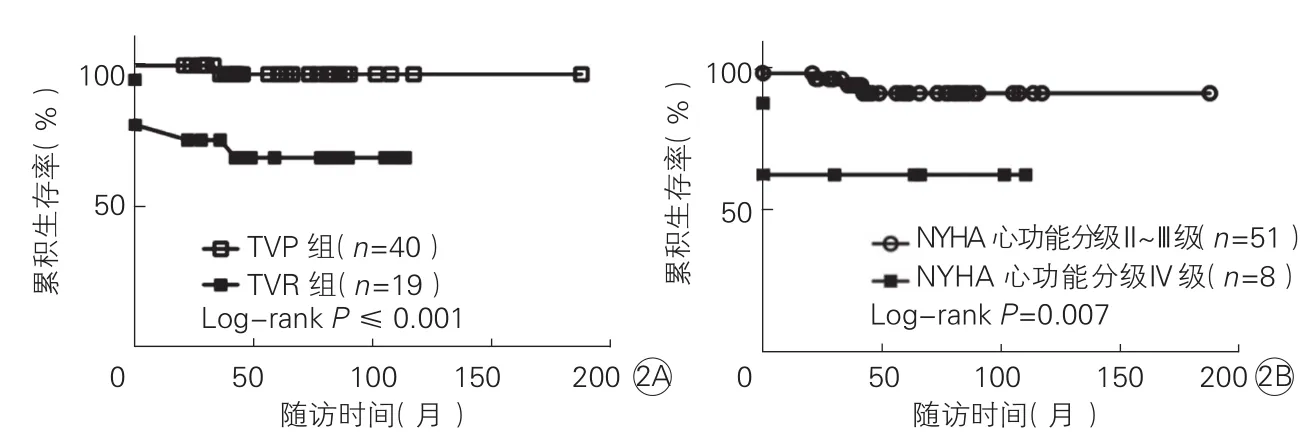
图2 Kaplan-Meier生存曲线显示不同组间患者的术后累积生存率情况
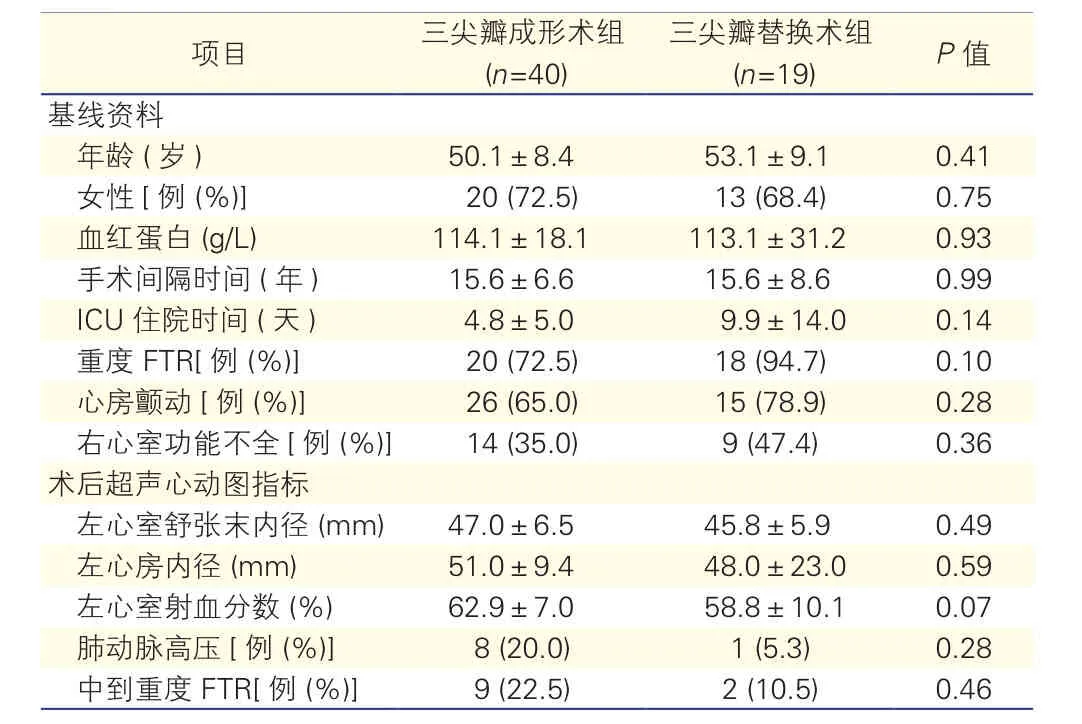
表2 根据患者再次三尖瓣手术术式分组的比较(±s)
对MACE事件的危险因素进行分析(表3):单因素分析结果显示:术前右心室功能不全是FTR患者术后远期发生MACE的危险因素(P=0.03);多因素分析显示:术前右心室功能不全是影响患者远期免于MACE累积生存率的唯一独立危险因素[风险比(HR):3.0; 95% 可信区间(CI):1.1~8.2; P=0.03]。
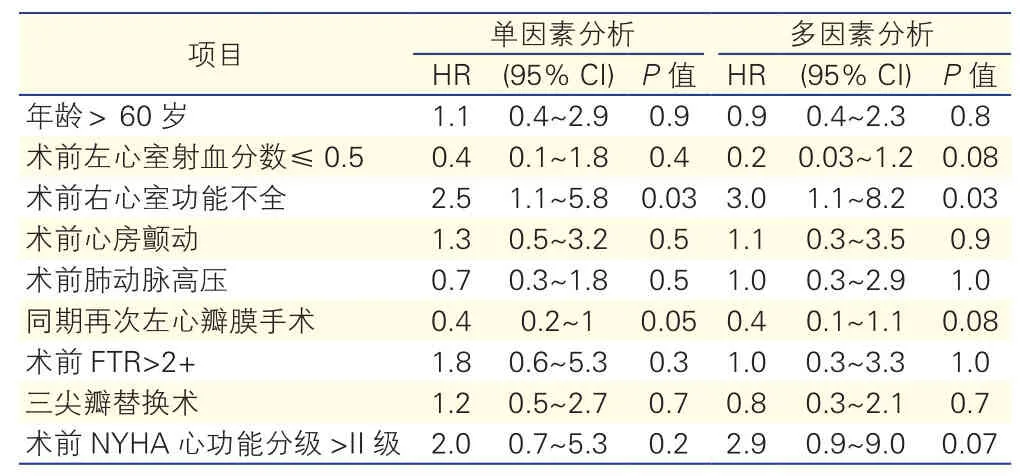
表3 患者术后主要心脏不良事件的危险因素分析
进一步分析患者术后远期死亡事件:术前NYHA心功能分级 Ⅳ级(P=0.008)、术前右心室功能不全(P=0.037)、合并同期再次左心瓣膜手术(P=0.017)及行TVR术(P=0.002)是患者再次术后远期死亡的危险因素。而TVR(HR:12.80; 95% CI:1.53~107.02; P=0.019)及术前NYHA心功能分级Ⅳ级(HR, 5.31; 95% CI:1.20~24.51; P=0.032)则是影响再次三尖瓣术后远期死亡的独立危险因素。
3 讨论
本研究对LSVR术后FTR患者再次行三尖瓣手术的远期效果分析发现:右心室功能不全是影响FTR患者再次手术远期预后的独立危险因素。充分评估患者术前右心室功能情况对选择再次FTR外科手术的适宜时机尤为重要。
3.1 FTR患者再次手术的时机
临床上因为左心瓣膜术后出现严重FTR而寻求再次手术的患者并不少见,此类患者手术风险高,术后预后普遍不良[8]。虽然目前的心脏瓣膜外科指南[6, 9]将左心瓣膜病变合并三尖瓣严重关闭不全的患者同期行三尖瓣手术列为I级推荐,然而有研究发现28%~48%的患者虽然不符合现行的三尖瓣手术指征[10],但于单纯的左心瓣膜术后仍可出现远期严重FTR。早期的研究指出因FTR而再次手术的患者,其术后院内死亡率高达25%,3年及5年生存率仅65%及44%[11]。Staab等[12]对34例FTR患者再次手术预后做出报道:早期死亡率为8.8%,5年生存率为41.6%。然而近期的前瞻性研究指出因FTR而再次手术的患者2年生存率可达91%[13],这与本组患者数据相近,患者预后明显较早期报道的良好。总结国外其他研究指出FTR患者再次手术总体死亡率波动于10%~37%[5, 14, 15],说明患者的得益会随手术时机而截然不同,早期患者的死亡率偏高可能与手术时机偏晚有关。
FTR患者再次外科手术的时机与右心功能评价密切相关。及时在患者右心室功能不可逆性失代偿之前行再次三尖瓣手术,可使右心室功能得以保护。透过右心室形态学重构,改善FTR患者的远期预后及运动耐量。这对左心瓣膜术后的患者而言非常重要。然而当前心脏外科治疗上仍缺乏清晰的右心系统功能分期,主要原因是右心室功能不全症状与三尖瓣反流程度并不一致,许多重度FTR患者临床症状并不典型,而具典型症状的患者往往已进展至右心室功能不可逆性衰竭,再次外科手术的预后极差。因此应该结合临床症状及客观辅助检查指标来对于右心室功能做出综合评估。
由于右心室几何构型复杂,对右心室功能的评估带来极大困难。目前仍未有公认且客观的右心室功能判定指标。欧洲瓣膜指南指出:三尖瓣平面收缩位移(TAPSE <15 mm、三尖瓣收缩期流量<11m/s 及右心室收缩末期面积(RVESA≥20 cm2)可反映右心室功能不全[4]。一项前瞻性研究指出RVESA是影响FTR患者再次手术预后的重要因素,重度FTR患者应在右心室收缩功能不全(RVESA≥20 cm2)及贫血(术前血红蛋白水平≤11.3 g/dl)发生前进行手术干预[13]。FTR患者术前慢性右心功能不全,导致静脉系统淤血、继发性脾功能亢进及红细胞破坏可能是患者术前贫血的主要原因。然而上述反映右心室大小及功能的参数仍未被广泛认可并常规应用于日常临床测量工作上。三维超声心动图及心脏磁共振成像技术的发展与推广,可能会为右心室容量及功能的客观测定带来新希望[16, 17]。
3.2 再次手术术式对预后的影响
由于受右心静脉系统血流动力学因素影响,TVR患者术后存在更高的血栓形成风险,因此患者术后抗凝指标的要求比接受左心瓣膜替换的患者更高,术后抗凝治疗风险也因而上升。国外多个研究表明:TVP组FTR患者的中期生存率可得到明显改善[18-20],因此TVP是目前大部分FTR患者的首选术式。然而,在本研究中两组患者远期免于MACE生存率并无统计学差异,说明两种术式均能有效维持三尖瓣功能。然而,TVR组患者术后远期生存率明显低于TVP组。这可能基于以下原因:第一,死亡患者例数偏少;第二,TVR组患者中,中度以上三尖瓣反流(89.5% vs 75.0%)及右心室功能不全患者的比例(47.4% vs 35.0%)均较高;第三,TVR组患者三尖瓣病变普遍更严重,部分行TVR的患者由于三尖瓣病变进展,已错失行三尖瓣成形的时机。事实上对于那些瓣叶牵拉作用明显、瓣叶对合缘明显低于瓣环水平而瓣环极度扩张的患者,TVP术后效果欠佳,应该进行TVR术治疗。由于患者既往已经植入左心人工瓣膜,患者行TVP术的手术得益可能因为术后仍需抗凝治疗而有所下降,因此,具体术式选择应该综合术中所见三尖瓣病变情况及术前患者整体情况而综合考虑。
综上所述,对于右心功能仍处于代偿期的功能性三尖瓣反流的患者而言,再次三尖瓣手术的远期预后令人满意,术前充分评估患者右心室功能是判断再次手术治疗时机的关键。在出现右心室功能不全之前更积极地进行三尖瓣再次手术可能使患者获益。
参考文献
[1] Czer LS, Maurer G, Bolger A, et al. Tricuspid valve repair. Operative and follow-up evaluation by Doppler color flow mapping. J Thorac Cardiovasc Surg, 1989, 98: 101-110.
[2] Goldman ME, Guarino T, Fuster V, et al. The necessity for tricuspid valve repair can be determined intraoperatively by two-dimensional echocardiography. J Thorac Cardiovasc Surg, 1987, 94: 542-550.
[3] Nath J, Foster E, Heidenreich PA. Impact of tricuspid regurgitation on long-term survival. J Am Coll Cardiol, 2004, 43: 405-409.
[4] Vahanian A, Alfieri O, Andreotti F, et al. Guidelines on the management of valvular heart disease (version 2012). Eur Heart J, 2012, 33: 2451-2496.
[5] Bernal JM, Morales D, Revuelta C, et al. Reoperations after tricuspid valve repair. J Thorac Cardiovasc Surg, 2005, 130: 498-503.
[6] Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC Guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation, 2014, 129: e521-643.
[7] Yock PG, Popp RL. Noninvasive estimation of right ventricular systolic pressure by Doppler ultrasound in patients with tricuspid regurgitation. Circulation, 1984, 70: 657-662.
[8] Jeong DS, Park PW, Mwambu TP, et al. Tricuspid reoperation after left-sided rheumatic valve operations. Ann Thorac Surg, 2013, 95: 2007-2013.
[9] Vahanian A, Alfieri O, Andreotti F, et al. Guidelines on the management of valvular heart disease (version 2012). The Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). G Ital Cardiol (Rome), 2013, 14: 167-214.
[10] Benedetto U, Melina G, Angeloni E, et al. Prophylactic tricuspid annuloplasty in patients with dilated tricuspid annulus undergoing mitral valve surgery. J Thorac Cardiovasc Surg, 2012, 143: 632-638.
[11] King RM, Schaff HV, Danielson GK, et al. Surgery for tricuspid regurgitation late after mitral valve replacement. Circulation, 1984, 70(3 Pt 2): I193-197.
[12] Staab ME, Nishimura RA, Dearani JA. Isolated tricuspid valve surgery for severe tricuspid regurgitation following prior left heart valve surgery: analysis of outcome in 34 patients. J Heart Valve Dis, 1999, 8: 567-574.
[13] Kim YJ, Kwon DA, Kim HK, et al. Determinants of surgical outcome in patients with isolated tricuspid regurgitation. Circulation, 2009, 120: 1672-1678.
[14] Park K, Kim HK, Kim YJ, et al. Incremental prognostic value of early postoperative right ventricular systolic function in patients undergoing surgery for isolated severe tricuspid regurgitation. Heart, 2011, 97: 1319-1325.
[15] Filsoufi F, Anyanwu AC, Salzberg SP, et al. Long-term outcomes of tricuspid valve replacement in the current era. Ann Thorac Surg, 2005, 80: 845-850.
[16] 白文娟, 唐红, 肖锡俊, 等. 实时三维超声心动图定量评价左心瓣膜病变伴随的功能性三尖瓣反流的可行性研究. 中国循环杂志, 2008, 23: 374-377.
[17] Lewis MJ, O'Connor DS, Rozenshtien A, et al. Usefulness of magnetic resonance imaging to guide referral for pulmonary valve replacement in repaired tetralogy of Fallot. Am J Cardiol, 2014, 114: 1406-1411.
[18] Rogers JH, Bolling SF. The tricuspid valve: current perspective and evolving management of tricuspid regurgitation. Circulation, 2009, 119: 2718-2725.
[19] 潘世伟, 胡盛寿, 王巍, 等. 改良三尖瓣成形术对继发性三尖瓣关闭不全的疗效评价. 中国循环杂志, 2011, 26: 46-49.
[20] 潘世伟, 胡盛寿, 许建屏, 等. 成形软环应用于三尖瓣关闭不全修复的疗效评价. 中国循环杂志, 2009, 24: 379-382.
(编辑:梅平)
Long-term Prognostic Analysis of Re-operation in Patients With Functional Tricuspid Regurgitation After Left-sided Valve Replacement
TONG Ming-hui, SHI Yi, LIU Shen, LUO Xiang, DONG Chao, YANG Yan, WANG Wei, XU Jian-Ping.
Department of Cardiac Surgery, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC, Beijing (100037), China
Corresponding Author: XU Jian-Ping, Email: jianpingxu@263.net
Abstract
作者单位:100037 北京市,中国医学科学院 北京协和医学院 国家心血管病中心 阜外医院 心血管疾病国家重点实验室 心外科
作者简介:佟明汇 博士研究生 主要从事心脏瓣膜病外科治疗研究 Email:tongminghui@fuwai.com 通讯作者:许建屏 Email:jianpingxu@263.net
中图分类号:R541.4
文献标识码:A
文章编号:1000-3614(2016)04-0376-05
doi:10.3969/j.issn.1000-3614.2016.04.015
(收稿日期:2015-04-28)
