基于生物效价检测和高效液相色谱法的中药莪术及其炮制品品质评价的研究
2016-07-18王建权徐建中俞旭平孙乙铭
王建权,徐建中,俞旭平,孙乙铭
(浙江省慈溪市中医医院 中药房,浙江 慈溪 315300)
基于生物效价检测和高效液相色谱法的中药莪术及其炮制品品质评价的研究
王建权Δ,徐建中,俞旭平,孙乙铭
(浙江省慈溪市中医医院 中药房,浙江 慈溪 315300)
目的 建立莪术的生物效价检测指标来评价生莪术、醋煮莪术、醋炙莪术的活血化瘀、消炎功效的差异,并建立高效液相色谱法测定莪术及其炮制品中有效成分姜黄素的含量。方法 生物效价测定法将莪术及其炮制品水提取液与牛血纤维蛋白原充分混匀,再加入凝血酶后观察体外凝集反应,并计算莪术活血化瘀效价,高效液相色谱法色谱柱为Waters Cl8(250 mm×4.6 mm,5 μm),流动相为乙腈-0.2%甲酸(47:53),流速为1.0 mL/min,检测波长为420 nm。结果 生莪术抗纤维蛋白原的生物效价为2.07 U,醋煮莪术为2.58 U,醋炙莪术为1.72 U,而生莪术中主要功效成分姜黄素含量为0.03599 mg/g,醋炙莪术、醋煮莪术中姜黄素含量分别为0.03916 mg/g、0.04167 mg/g。结论 以拮抗牛血纤维蛋白原作为生物效价的评价,醋煮莪术的活血化瘀功效高于生莪术和醋炙莪术。
莪术;炮制品;活血化瘀;生物效价
莪术为姜科姜黄属多年生植物蓬莪术、温郁金或者广西莪术的干燥根茎。其性辛、温、苦,具有消积止痛、行气破血的作用,可用于食积胀痛, 也可用于气滞血瘀所致经闭腹痛等症状[1]。根据《中国药典2010年版》及相关文献显示[2],莪术中主要含有挥发油和姜黄素2大类成分,一般采用性状、薄层鉴别及挥发油测定,难以全面评价莪术及其炮制品的品质,而建立适宜的活血化瘀生物活性检测方法和高效液相色谱法用于莪术及其炮制品的质量控制和品质评价,可以体现莪术功效特点,并补充了莪术现有的质控模式的不足。生物效价法试验以牛血纤维蛋白原(FIB)的变化为指标来考察莪术及其炮制品的活血化瘀功效,当牛血纤维蛋白原与凝血酶相互作用生成纤维蛋白,并形成凝胶,以此为指标来评价莪术及其炮制品体外拮抗凝血酶-牛纤维蛋白原凝胶的反应效果,高效液相色谱法试验测定了莪术及其炮制品中主要功效成分姜黄素的含量,结合以上两种方法更接近于评价莪术及其炮制品活血化瘀功效,将生物活性测定法引入中药质量控制和评价体系,更能全面评价莪术及其炮制品的品质。
1 材料与方法
1.1 材料 牛血纤维蛋白原测定试剂盒(FIB)(天津美德太平洋科技限公司,批号201424000);凝血酶(中国食品药品检定研究院,批号S10117-200);同一批次莪术3种炮制品(生莪术、醋煮莪术、醋炙莪术)由浙江省慈溪市中医医院中药房提供并炮制。
R-1001-VN 型旋转蒸发仪(郑州长城科工贸有限公司);DZF-202型真空干燥箱(南京泰康环保科技有限公司)。
1.2 方法
1.2.1 工作缓冲液的制备:pH7. 2 磷酸盐缓冲液(取0.2 mol/L磷酸二氢钾50 mL与0.2 mol/L氢氧化钠溶液35 mL,加新沸过的冷水稀释至200 mL,摇匀,即得) 与生理盐水1:20比例混合。
1.2.2 莪术炮制品的制备
生莪术:称取莪术原药材,浸泡6 h,洗净,置蒸笼内蒸至上气,趁热切成薄片,晾干,筛去灰屑。
醋煮莪术:称取莪术原药材置于制药锅中,加米醋,并加冷水将其浸没,用文火加热至醋汁吸尽,观察莪术药材内无白心时,立即取出,稍微晾干,切厚片,干燥。莪术每10 kg , 用米醋2 kg。
醋炙莪术:称取莪术原药材均匀切片,加40%米醋拌匀,等米醋稍微浸润,置于炒制锅内,用文火慢慢加热,炒至显微黄色,略带焦斑时,取出,放至室温即可。
1.2.3 莪术炮制品供试液的制备:分别称取炮制规范、质量稳定的3种莪术炮制品饮片10 g,分别加入20倍量冷水浸泡4 h,煎煮2次,每次1 h,过120目筛去除药渣。混合2次水煎液,水煎液过滤后浓缩至100 mL。
1.2.4 空白梯度试验:取牛血纤维蛋白原溶液(浓度为5 mg/mL)从加入量20 μL开始,每次试验组加入量增加20 μL,且各组分别加入凝血酶(浓度为5 U/mL)20 μL,充分混匀,立即放入(37±1)℃水浴中,观察成胶情况。试验结果表明当牛血纤维蛋白原溶液加入量大于50 μL时,观察到各组试验结果均形成了一定量的胶块,而当各试验组加入量在50 μL以下时不易形成胶块。因此试验选择牛血纤维蛋白原溶液(浓度为5 mg/mL)加入量从50 μL开始每次增加50 μL的剂量进行空白梯度试验。
1.2.5 生物效价测定方法的建立:将生莪术、醋煮莪术、醋炙莪术供试液分别用工作缓冲液进行稀释,稀释浓度相当于生药量0.5、1、2、3、5、10、15、25、35、40、60、75 mg/L的供试品溶液。取干净试管,分别加入不同浓度的供试液20 μL、牛血纤维蛋白原溶液(浓度为5 mg/mL)50 μL,振摇混匀后加入凝血酶溶液(浓度为5 U/mL)20 μL,立即放入(37±1)℃水浴中,10 min中后观察成胶情况,若无凝胶出现,每次增加50 μL的牛血纤维蛋白原溶液,按上述方法平行测定3次。计算莪术及其炮制品抗凝效价按照《中国药典》2010年版二部附录ⅩⅣ生物检定统计法项下“量反应平行线法”( 3,3) 法[3-5]。
1.2.6 莪术生物效价计算方法:莪术活血化瘀效价(U)=CFIB×VFIB/C供试品×V供试品。
1.2.7 莪术及其炮制品中姜黄素的含量测定
① 色谱条件:Waters C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈-0.2%甲酸(47:53);检测波长:420 nm;流速:1.0 mL/min;柱温35℃。
② 对照品溶液的制备:精密称定姜黄素对照品,加甲醇制成每1 mL含45 μg的对照品溶液,微孔有机滤膜滤过,取续滤液,即得。
③ 供试品溶液的制备: 分别称取生莪术、醋煮莪术、醋炙莪术粉末约1.0 g,精密称定,置于具塞锥形瓶中,精密加入甲醇30 mL,密塞并称取重量,超声提取60 min,冷却放至室温,再称定重量,用甲醇补充,摇匀,过滤,取续滤液,即得。
④ 专属性实验:分别精密吸取对照品溶液,生莪术、醋煮莪术、醋炙莪术供试品溶液各10 μL,注入液相色谱仪,按①项下色谱条件进行测定。
⑤ 线性范围考察:分别精密量取姜黄素对照品溶液(浓度为45 μg/mL)1、2、5、10 1、20 μL注入高效液相色谱仪,照上述色谱条件测定姜黄素的峰面积。以峰面积(A)为纵坐标,进样量(C)为横坐标,绘制标准曲线,并计算回归方程。
⑥ 生莪术、醋煮莪术、醋炙莪术姜黄素含量测定:分别精密吸取上述生莪术、醋煮莪术、醋炙莪术供试品溶液2份各10 μL,按上述色谱条件进行测定,每个样品平行测定2次,外标峰面积法计算。
1.2.8 验证试验
① 精密度试验:按上述色谱条件,取同一份生莪术供试品溶液剂量梯度依照“1.2.4”、“1.2.5”项下方法分6次进行测定,完成后与莪术对照药材溶液进行对比检定;
② 重复性试验:取同一批生莪术分6次进行提取,分别制成其供试品溶液,按上述方法操作,与莪术对照品溶液进行对比检定;
③ 中间精密度试验:为了考察实验室2个不同实验人员对测定结果的影响,按照上述方法进行;
1.2.9 莪术抗凝活性与主要功效成分之间的相关性分析:将莪术及其炮制品抗凝效价与对应的主要化学成分姜黄素含量作图,并按照1.2.7项下方法进行相关性分析。

2 结果
2.1 纤维蛋白原-凝血酶成胶结果 所有未成胶组在5 min之后加入高剂量的凝血酶溶液(浓度为5 U/mL),经(37±1)℃水浴10 min后,仍未观察到继续成胶,表明莪术对凝血酶的直接抑制作用不敏感。试验结果证明,莪术有明显的抑制纤维蛋白原活性的作用。见表1。

表1 生莪术与纤维蛋白原拮抗剂量关系考察
2.2 莪术抗凝活性的量效关系考察 莪术具有明显的抑制血浆纤维蛋白原活性的作用,也就是有明显的抗凝血作用。试验对莪术对照药材的抗凝作用量效关系进行了考察,结果表明,莪术对照药材的对数计量(X)与FIB(Y,牛纤维蛋白原剂量)具有良好的线性关系。线性回归方程:Y=1.335C+0.213(mg),相关系数r=0.9920,线性范围为0.08~1.5 mg, 线性关系良好。说明FIB法可以通过“量反应平行线法”( 3,3)法对莪术生物效价进行检定[4-5]。
2.3 几种莪术炮制品活血化瘀功能生物效价比较 按照上述方法分别测定莪术炮制品醋煮莪术、醋炙莪术,醋炙莪术拮抗牛血纤维蛋白原剂量满足Y=1.392X+0.104,r=0.9940,线性范围为0.1~1.2 mg,平均效价为1.7U;醋煮莪术拮抗牛血纤维蛋白原剂量满足Y=1.554X+0.202,r=0.9820,线性范围0.06~0.7 mg,平均效价为2.58 U。醋炙莪术、醋煮莪术拮抗纤维蛋白原作用数据见表2、表3。

表2 醋炙莪术与纤维蛋白原拮抗剂量关系考察

表3 醋煮莪术与纤维蛋白原拮抗剂量关系考察
2.4 莪术及其炮制品中姜黄素的含量测定结果
2.4.1 专属性实验:结果表明:在本实验色谱条件下,供试品溶液中其他成分与姜黄素分离良好。

图1 姜黄素对照品溶液色谱图Fig.1 Chromatogram of curcumin reference substance solution
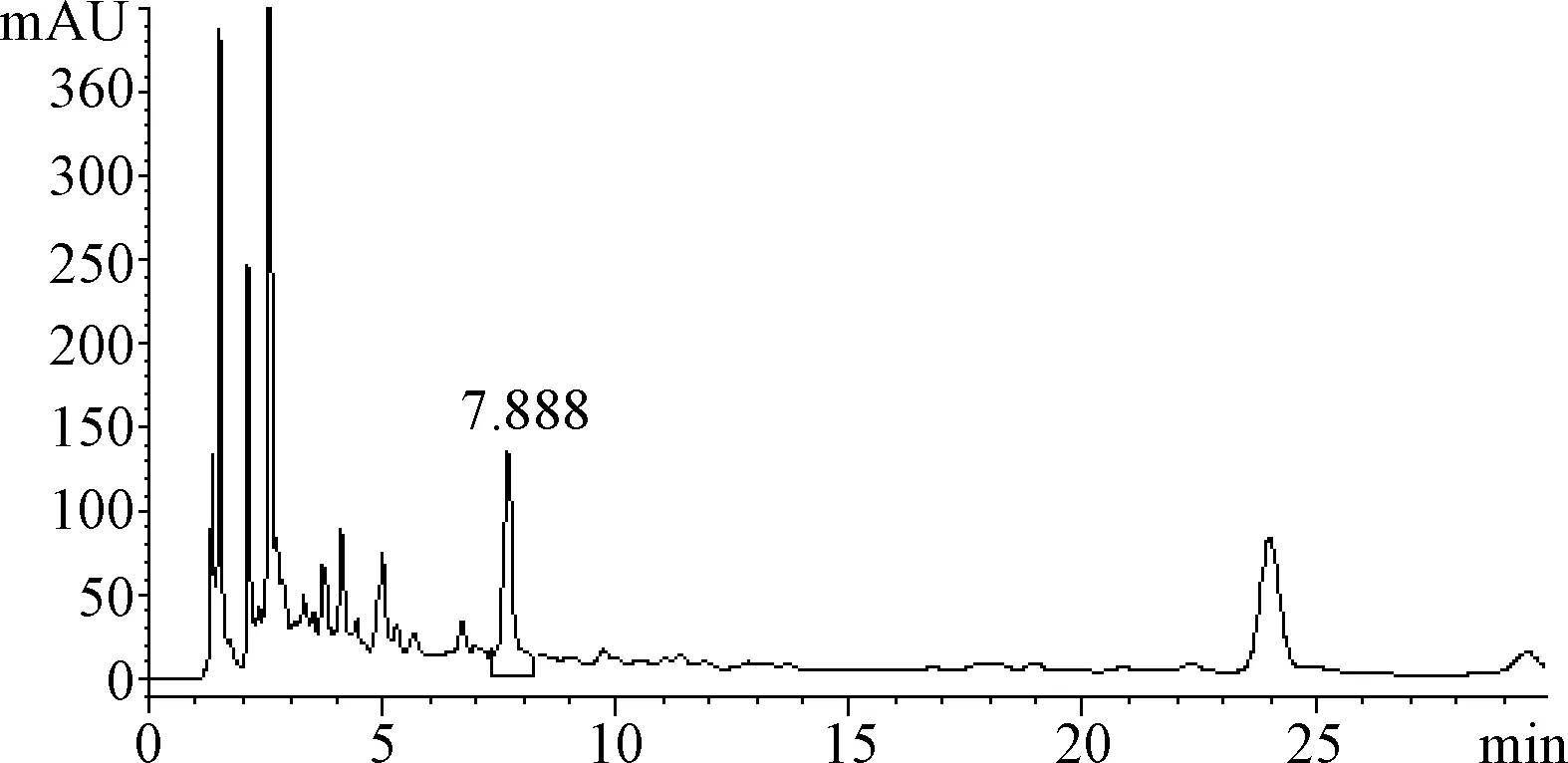
图2 供试品溶液色谱图Fig.2 Chromatogram of test solution
2.4.2 线性范围考察:线性回归方程为A=2973.5C+6.5715(μg/mL),相关系数r=0.9992,线性范围为0.045~55.0 μg/μL, 8次空白测定RSD为0.20%,检出限为0.02 μg/μL。线性关系良好。
2.4.3 精密度试验:与莪术对照药材溶液进行对比检定,计算得到其平均效价分别为2.12 U,RSD分别为 5.8%。表明仪器的精密度良好。
2.4.4 重复性试验:与莪术对照品溶液进行对比检定,计算平均效价分别为1.97U,RSD分别为 4.2%。
2.4.5 中间精密度试验:结果表明,生莪术平均效价分别为2.14 U,RSD分别为3.6%。说明不同实验人员对测定结果影响较小,该方法稳定性较好。
2.4.6 生莪术、醋煮莪术、醋炙莪术姜黄素含量测定结果:每个样品平行测定2次,外标峰面积法计算。见表4。

表4 样品分析结果
2.5 莪术抗凝活性与主要功效成分之间的相关性分析 将莪术及其炮制品抗凝效价与对应的主要化学成分姜黄素含量作图,见图3,并按照1.2.7项下方法进行相关性分析,结果表明,莪术及其炮制品抗凝效价与姜黄素质量分数之间未见显著性相关。

图3 姜黄素含量与抗凝效价相关性图Fig.3 Correlation between content of curcumin and anticoagulant potency
3 讨论
本试验从莪术及其炮制品醋炙莪术与醋煮莪术活血化瘀药理作用的相关文献[6-7]得到启发,对中药莪术及其炮制品活血化瘀功效的检测方法做了一定的探索,本实验将生物效价法及高效液相色谱法进行对比[8-11],建立莪术及其炮制品的评价体系,不仅可以测定其姜黄素含量,而且还可以评价莪术及其炮制品的活血化瘀药效。《中国药典2015年版》提出了中药的质量控制标准要逐步由单一性指标成分向活性有效成分及生物活性测定的综合性检测指标过渡,因此中药及中成药生物活性测定法代表着质量评价的一种发展趋势。而活血化瘀类中药及其炮制品一般会选择几种指标和药理研究方向进行生物活性的考察。本课题组通过前期的试验对凝血4项进行了筛查,最终选择了拮抗FIB(牛血浆纤维蛋白原)的效应[12-13]作为考察指标,并比较了莪术不同提取组分的活血化瘀活性,其中主要功效成分姜黄素的活血化瘀最好,并结合高效液相色谱法对莪术及其不同炮制品中姜黄素含量与活血化瘀活性相关性进行了考察,方法简单、准确,并能构建量效关系,对中药莪术及其炮制品的质量控制和临床疗效的关联更具有实际意义。
[1] 李勇,孙秀燕,林翠英,等. 三个品种莪术挥发油的化学成分研究[J].中草药,2005,36(12):1785-1787.
[2]成晓静,刘华钢,赖茂祥. 莪术的化学成分及药理作用研究概况[J].广西中医学院学报,2007,10(1):79-81.
[3]刘星星,董莉,张晓红,等.止血生物效价用与白及品质的研究[J].中国中药杂志,2014,39(19):3764-3767.
[4]中华人民共和国国药典[S].2010,VolⅡ(二部)附录ⅪV:107.
[5]陈广云,吴启南,王新胜,等.生物效价测定发用于活血化瘀中药三棱品质评价的研究[J].中国中药杂志,2012,37(19):2913-2917.
[6]王普霞,周春祥,陆兔林.莪术不同炮制品活血化瘀作用研究[J].中成药,2004,26(11):905-906.
[7]黄臣虎,陆茵,孙志广,等.莪术抗癌作用机制研究进展[J].中草药,2010,41(10):1745-1747.
[8]唐霞,辛华雯.常见中草药及其有效成分对CYP3A和P-gp代谢与转运的影响[J].中国药师, 2013,16(10):1588-1591.
[9]郑敏霞,沈洁,丰素娟.生物效价检测研究进展[J].中国现代应用药学,2011,28(5):511-514.
[10]刘莹,曹军皓.纤维蛋白原临床研究进展[J].华南国防医学杂志,2010,24(1):557-558.
[11]马会利,冯军,陈纪林,等.人纤维蛋白原结构与功能研究进展[J].四川生理科学杂志,2002,24(2):153-156.
[12]廖共山,班建东. 一种检测凝血酶、类凝血酶的新方法——纤维蛋白原平板法[J].广西医科大学学报,2008,25(6):967-969.
[13]黄青,陆益红,史清水,等. 高效液相色谱法测定缩宫素注射剂含量及其与生物效价测定法比较和应用[J].药物分析杂志,2015,35(6):1115-1121.
(编校:王冬梅)
Study on quality evaluation of curcuma and its processed products by biopotency determination method and HPLC method
WANG Jian-quanΔ, XU Jian-zhong, YU Xu-ping, SUN Yi-ming
(Pharmacy of Traditional Chinese Medicine, Zhejiang Cixi Chinese Medicine Hospital, Cixi 315300, China)
ObjectiveTo establish a method for determining anticoagulation potency of Curcuma,Vinegar boiled Curcuma,Vinegar sunburned Curcuma on promoting blood circulation and removing blood stasis,and the establishment of a HPLC method for content determination of effective ingredients of zedoary turmeric curcumin and its processed products.MethodsBy the full mixture water extracts of these Curcuma and Processed Products and full mixing of fibrinogen, prothrimbin was added into the mixture to from the gel reaction in the nature state and the antagonism titer of Curcuma and Processed Products was calculated. HPLC column for waters C18(250 mm×4.6 mm, 5 μm) , the mobile phase is acetonitrile 0.2% formic acid (47:53). The flow rate was 1.0 mL/min and the detection wavelength was 420 nm.ResultsThe biological potency of antifibrin Curcuma for 2.07 U, Vinegar boiled Curcuma was 2.58U and Vinegar sunburned Curcuma was 1.72 U. And zedoary main efficacy components of the content of curcumin 0.03599 mg/g, vinegar Rhizoma Zedoariae and vinegar boiled the content of curcumin in Rhizoma Curcumae respectively 0.03916 mg/g and 0.04167 mg/g.ConclusionEvaluation of the antagonistic activity of fibrinogen as a biological activity, the Vinegar boiled Curcuma’s effection of activating blood circulation is higher than the Vinegar sunburned Curcuma and the Curcuma.
curcuma; processed products; blood stasis; bioavailability
王建权,通信作者,男,本科,主管中药师,研究方向:中药分析,E-mail:2189920600@qq.com。
R284.1
A
10.3969/j.issn.1005-1678.2016.03.58
