重组赖脯胰岛素与赖脯胰岛素治疗T2DM的疗效比较
2016-07-15乔旭霞
乔旭霞,徐 成
(1.重庆市巴南区人民医院内分泌科 401320;2.重庆医科大学附属第二医院内分泌科 400010)
重组赖脯胰岛素与赖脯胰岛素治疗T2DM的疗效比较
乔旭霞1,徐成2
(1.重庆市巴南区人民医院内分泌科401320;2.重庆医科大学附属第二医院内分泌科400010)
[摘要]目的探讨重组赖脯胰岛素注射液与赖脯胰岛素注射液在2型糖尿病(T2DM)治疗中的临床疗效和安全性。方法将血糖控制不佳的T2DM患者48例按2∶1比例随机分为重组赖脯胰岛素组(观察组,n=32)和赖脯胰岛素组(对照组,n=16),在睡前给予1次重组甘精胰岛素注射的基础上,三餐前分别给两组患者进行1次重组赖脯胰岛素或赖脯胰岛素注射,治疗周期16周。比较两组患者治疗前、后糖化血红蛋白(HbA1c)、空腹血糖(FPG)、餐后2 h血糖(2hPG)变化水平,并评估不良事件。结果44例完成研究,其中观察组28例,对照组16例。治疗16周后,两组患者HbA1c、FPG和2hPG水平均明显降低(P<0.05),观察组和对照组HbA1c下降幅度分别为(1.55±1.50)%、(1.06±1.30)%,FPG下降幅度分别为(2.07±5.01)、(1.09±3.18)mmol/L,2hPG下降幅度分别为(3.28±5.71)、(3.60±5.89)mmol/L。以HbA1c为主要评价指标,0.40为非劣效界值,重组赖脯胰岛素注射液非劣效于赖脯胰岛素注射液(P<0.05)。观察组HbA1c≤6.50%的达标率为14.29%,HbA1c<7.00%的达标率为28.57%;对照组HbA1c≤6.50%的达标率为18.75%,HbA1c<7.00%的达标率为43.75%,两组患者在HbA1c两个水平达标率比较差异无统计学意义(P>0.05)。结论重组赖脯胰岛素注射液治疗T2DM患者在有效性方面非劣效于赖脯胰岛素注射液,且具有相同的安全性。
[关键词]糖尿病,2型;重组赖脯胰岛素;治疗结果;安全性
随着中国经济发展,人们生活方式和环境改变,人口老龄化等因素,2型糖尿病(type 2 diabetes mellitus,T2DM)的患病率逐年上升。Yang等[1]研究调查中国糖尿病患病率,结果提示糖尿病总患病率和糖尿病前期患病率分别为9.7%(男性约10.6%,女性约8.8%)和15.5%(男性约16.1%,女性约14.9%);新近的一项流行病学研究发现,通过有代表性的样本估计中国成年人中的糖尿病总患病率约为11.6%(男性约12.1%,女性约11%),而糖尿病前期患病率高达50.1%(男性约52.1%,女性48.1%)[2]。糖尿病在中国普通成年人群高度流行,特别是T2DM最为多见,在糖尿病患者中占95%以上。因此,T2DM已成为中国重要的公共健康问题之一。
胰岛素作为机体惟一能降低血糖的激素,英国糖尿病前瞻性研究(UKPDS)证实随着病程进展,T2DM患者胰岛β细胞的胰岛素分泌功能逐渐衰退,导致口服降糖药物不能控制血糖达标,此时胰岛素分泌不足便成为T2DM的主要病理、生理机制[3]。而大部分T2DM患者随着病情的发展,最终都需要使用胰岛素治疗。胰岛素类似物作为最新一代的胰岛素,具有作用迅速、消除快、减少低血糖风险等优点。胰岛素类似物还具有模拟第一时相胰岛素分泌,更好的管理餐后血糖;注射时间灵活,提高患者依从性及生活质量;高效且更经济等优势[4]。赖脯胰岛素是由Lilly公司于1996年研发的一种胰岛素类似物,符合人体胰岛素分泌的特点,有明确的疗效和安全性[5-7]。随着药物国际专利保护期结束,国内多家药企都将能生产胰岛素类似物,打破外企行业垄断将为广大糖尿病患者提供质优价廉的治疗用药。本研究采用餐时速效胰岛素联合睡前基础胰岛素的降糖方案;在睡前皮下注射重组甘精胰岛素的基础之上,以赖脯胰岛素餐时皮下注射为对照,评价江苏万邦公司生产的重组赖脯胰岛素注射液治疗T2DM的疗效和安全性。
1资料与方法
1.1一般资料选择2014年1~10月重庆医科大学附属第二医院门诊和住院病房收治的T2DM患者48例,男26例,女22例。入选标准:(1)符合1999年WHO糖尿病诊断标准,诊断为糖尿病;能够理解试验的全过程自愿参加本次研究并签署知情同意书;年龄为18~75岁,性别不限。(2)体质量指数(BMI)在18~35 kg/m2。(3)确诊糖尿病6个月以上。(4)降糖方案为两种或两种以上口服降糖药或胰岛素治疗剂量不变3个月以上,血糖控制不佳[糖化血红蛋白(glycosylated hemoglobin,HbA1c)7.5%~13.0%)]。(5)能够并愿意利用血糖仪进行空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(postprandial 2 hours blood gloucose,2hPG)检测。排除标准:(1)已知对胰岛素过敏者;(2)继发性糖尿病者;(3)有严重的低血糖病史者;(4)6 个月内有糖尿病急性并发症,包括糖尿病酮症酸中毒、非酮症高渗性昏迷等;(5)肌酐(Cr)>177 μmol/L 者;(6)肝脏功能损害,丙氨酸氨基转移酶(ALT)或天门冬酸氨基转移酶(AST)为正常值上限的3倍以上;(7)妊娠(在第一次访视时通过尿妊娠试验进行确定)或哺乳;(8)有药物滥用史或酗酒;(9)确定恶性肿瘤者;(10)接受长期类固醇激素、免疫抑制剂及细胞毒性药物治疗者,尤其是最近3 个月内连续使用该类药物 2 周以上者;(11)其他系统严重疾病,包括呼吸系统、心血管系统、神经系统、消化系统等;(12)贫血患者(血红蛋白小于100.0 g/L);(13)每日注射胰岛素大于或等于3次,且日剂量在60 IU以上者;(14)已参加其他的试验;(15)依从性差,不能按照要求完成试验研究的。本研究遵循赫尔辛基宣言和药物临床试验质量管理规范(GCP)指导原则,并得到本院临床药物试验伦理委员会的批准,所有研究对象在纳入之前均充分知情,并签署了书面知情同意书。
1.2方法
1.2.1治疗方案本试验总研究治疗周期为18周(2周导入期,4周剂量调整期,12周稳定治疗期),筛选后符合入排标准的患者给予个体化的饮食及运动管理,同时在2周的导入期内保持原治疗用药(口服降糖药或胰岛素)不变。将2周后仍符合入选标准(7.5%≤HbA1c≤13.0%)的受试者44例随机分为观察组(n=28)和对照组(n=16)。观察组和对照组患者在睡前给予1次重组甘精胰岛素注射(长秀霖)的基础上,三餐前分别进行1次重组赖脯胰岛素注射液或赖脯胰岛素注射液注射,同时停用原有降糖治疗方案,进入为期4周的胰岛素剂量调整期,12周的稳定治疗期;治疗期间保持饮食控制和运动治疗不变。
1.2.2起步剂量多次皮下注射胰岛素的起步剂量主要分为以下3种情况:(1)单纯口服药联用或口服药联合每天注射胰岛素小于3 次的受试者,按 0.4 IU·kg-1·d-1的剂量给予起步胰岛素每天注射总剂量。其中,基础胰岛素占全天剂量的40%左右,剩余的剂量中,餐前胰岛素按 1/3 比例各分配到三餐中。(2)每天注射胰岛素大于或等于3次,且每天剂量在 40 IU 以下的受试者,起步剂量保留原剂量不变,胰岛素用量为基础胰岛素占全天剂量的40%左右,剩余的剂量中,餐前胰岛素按 1/3 比例各分配到三餐中。(3)每天注射胰岛素大于3 次,且每天剂量为 40~60 IU 的受试者,将起步给药日剂量调整为 40 IU,胰岛素用量为基础胰岛素占全天剂量的 40%左右,剩余的剂量中,餐前胰岛素按 1/3 比例各分配到三餐中。
1.2.3调整方法FPG的调整方案:FPG目标值为4.4~6.1 mmol/L;2hPG的调整方案:2hPG目标值为 8.0~10.0 mmol/L。睡前长效胰岛素剂量调整方法及餐时胰岛素调整方法,见表1。

表1 FPG及2hPG目标值调整方案
1.2.4基础和餐前胰岛素调整顺序调整胰岛素顺序原则:(1)先调整基础胰岛素,根据连续3次FPG测定的最低值调整胰岛素,使FPG接近目标值,根据患者的血糖需求每 3~5 天调整1次。(2)餐时胰岛素按早餐前→晚餐前→午餐前的顺序每次调一段,根据连续3次2hPG测定的最低值调整胰岛素,每 3~5 天调整1次。
1.2.5资料收集与评价(1)数据收集:基线和治疗16周后均对患者进行身高、体质量、血压、心率等指标的测量,所有操作由一指定人员进行测量,操作方法固定、统一。患者隔夜空腹8~12 h来医院,早上8:00开始采集空腹静脉血,测定FPG、HbA1c、胰岛素抗体、血脂及尿酸等相关指标,然后给予患者标准方便面餐(康师傅红烧牛肉面76 g,去油包),2 h后抽取血液检测2hPG。(2)疗效评价指标:主要疗效指标为治疗前、后HbA1c变化及治疗后HbA1c自基线值下降的绝对值。次要疗效指标包括治疗前、后FPG、2hPG的变化;治疗后两组患者HbA1c<7.0%、≤6.5%的百分比;治疗前、后两组患者体质量、血脂变化情况。(3)安全性评价指标:治疗前、后体质量、血压、心率、血脂、胰岛素抗体、尿酸等变化;低血糖和其他不良事件的发生率。
2结果
2.1研究整体完成情况本研究共入组48例患者,其中脱落3例(撤销知情同意书),剔除1例(依从性差)。最终共44例完成研究,其中观察组完成28例,对照组完成16例。
2.2两组患者治疗前相关指标比较两组患者治疗前性别、年龄、BMI、收缩压(SBP)、舒张压(DBP)、心率、体脂百分比(FAT)、HbA1c、FBG、2hPG,以及胰岛素抗体、尿酸等指标比较,差异均无统计学意义(P>0.05),见表2。

表2 两组患者治疗前的各项指标比较
2.3治疗效果评价
2.3.1两组患者HbA1c、FPG、2HPG水平比较经治疗16周后,观察组HbA1c为(7.70±1.13)%,平均下降(1.55±1.50)%;对照组HbA1c为(7.51±1.77)%,平均下降(1.06±1.30)%。观察组治疗后HbA1c水平下降幅度非劣效于对照组治疗后HbA1c水平下降幅度,非劣效界值设定为0.40(t=1.98,P=0.03)。观察组、对照组FPG下降幅度分别为(2.07±5.01)、(1.09±3.18)mmol/L。两组患者治疗前、后FPG变化值组间比较差异无统计学意义(P=0.42)。观察组治疗前、后FPG变化值比较差异有统计学意义(P<0.05)。观察组、对照组2hPG下降幅度分别为(3.28±5.71)、(3.60±5.89)mmol/L。两组患者治疗前、后2HPG变化值组间比较差异无统计学意义(P=0.30)。观察组及对照组治疗前、后2HPG变化值比较差异有统计学意义(P<0.05),见表3。
2.3.2两组患者HbA1c达标率的比较治疗后患者HbA1c<7.00%达标率观察组8例(28.57%),对照组7例(43.75%),两组患者HbA1c<7.0%达标率比较,差异无统计学意义(χ2=1.04,P=0.31)。治疗后患者HbA1c≤6.50%达标率观察组4例(14.29%), 对照组3例(18.75%),两组患者HbA1c≤6.50%达标率比较差异无统计学意义(χ2=0.00,P=1.00)。
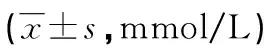
表3 两组患者治疗前、后FPG、2HPG水平比较
2.4两组患者治疗前后不良事件发生情况比较观察组共有5例(17.86%)发生不良反应,1例(3.57%)双下肢轻度水肿患者(自行缓解),4例(14.29%)轻度低血糖(进食后缓解);对照组有6例(37.50%)发生不良反应,均为轻度低血糖(进食后缓解),两组低血糖发生率比较差异无统计学意义(χ2=0.00,P=0.79)。两组患者均无夜间低血糖和严重低血糖发生,均无严重不良事件发生。
3讨论
T2DM是由于胰岛素抵抗和胰岛素相对分泌不足的一种慢性、进展性、全身性代谢紊乱疾病。当β细胞分泌的胰岛素不足以代偿机体胰岛素抵抗时,血糖逐步升高发展为T2DM[10]。两项经典的大型临床研究糖尿病控制与并发症试验(DCCT)和UKPDS结果表明,良好的血糖控制能明显延缓糖尿病慢性并发症(特别是微血管病变)发生与发展[11-12]。胰岛素作为治疗糖尿病最有效的手段,在糖尿病治疗领域具有不可替代的作用,糖尿病的治疗水平因应用胰岛素而达到质的飞越。
中国糖尿病发病率较高,糖尿病相关的治疗费用给患者家庭和社会带来了严重经济负担[13]。跨国制药企业因技术专利长期垄断我国药品市场,随着药物专利期结束,国内的多家药厂将能生产物美价廉的药品,在疗效和安全性相近的情况下,糖尿病患者可根据自身情况选择合适的治疗药物。胰岛素在临床应用中常被认为是治疗T2DM阶梯化治疗的最后一步,它是在改变生活方式治疗和口服药物治疗后血糖仍控制不佳之后的选择。但值得指出的是,美国糖尿病协会(ADA)/欧洲糖尿病研究协会(EASD)建议将胰岛素作为控制血糖一线药物的组合之一[14]。与人胰岛素相比,赖脯胰岛素吸收快、起效快、消除快、使用灵活,能有效降低HbA1c,控制餐后血糖[15]。本研究结果提示,治疗16周后观察组和对照组HbA1c分别由入组时的(9.25±1.11)、(8.57±1.27)%下降为(7.70±1.13)、(7.51±1.77)%,两组下降幅度分别为(1.55±1.50)、(1.06±1.30)%,观察组非劣效于对照组(P<0.05)。观察组和对照组FPG下降幅度分别为(2.07±5.01)、(1.09±3.18)mmol/L,观察组和对照组2hPG下降幅度分别为(3.28±5.71)、(3.60±5.89)mmol/L,组间比较差异均无统计学意义(P>0.05)。观察组HbA1c≤6.5%达标率为14.29%,HbA1c<7.0%达标率为28.57%,对照组HbA1c≤6.5%达标率为18.75%,HbA1c<7.0%达标率为43.75%,两组患者在HbA1c两个水平达标率比较差异均无统计学意义(P>0.05)。研究结果提示,在血糖控制不佳的T2DM患者中,重组赖脯胰岛素改善糖代谢治疗作用非劣效于赖脯胰岛素。低血糖是胰岛素治疗过程中常见的不良反应之一,表现为交感神经兴奋和中枢神经症状为主要特点的综合征,严重时还可引起意识丧失,甚至有死亡风险。多数糖尿病患者因恐惧发生低血糖事件拒绝或延迟胰岛素治疗,这已成为启动胰岛素治疗的障碍之一[12]。赖脯胰岛素独特的药代动力学,药物作用持续时间较人胰岛素短,其低血糖发生风险降低,尤其是严重低血糖及夜间低血糖[15]。本研究发现在16周的治疗期间,观察组共发生轻度低血糖事件4例(14.29%),对照组发生6例轻度低血糖事件(37.50%),两组低血糖发生率比较差异无统计学意义(P>0.05),两组患者中均未发生夜间低血糖和严重低血糖事件。本研究结果提示,低血糖发生风险低与既往研究一致。老年人由于机体反应能力及神经功能减退,低血糖发作时缺乏机体报警症状(心慌、出汗、饥饿、颤抖等),低血糖发作风险较年轻人更高。因此,赖脯胰岛素是老年患者管理血糖的理想选择之一。
观察组中出现1例双下肢轻度水肿,患者既往无下肢水肿病史,亦无心血管系统、消化系统及泌尿系统病史,既往未使用过胰岛素,故此例患者双下肢轻度水肿可能是由于胰岛素治疗引起。胰岛素水肿是胰岛素引起少见的不良反应,可能由于未控制血糖前常有失水和失钠表现,而使用胰岛素治疗后水钠潴留而引起水肿;此外,水肿也可能与胰岛素促进钠离子在肾小管重吸收有关。本研究出现的1例下肢轻度水肿,未进行性加重,观察随访后水肿消退。本研究存在的不足之处为研究时间短,纳入研究的样本量小,还需要纳入更大样本量和长期研究评估重组赖脯胰岛素的疗效和安全性。
综上所述,赖脯胰岛素作为第一个胰岛素类似物在临床实践中治疗糖尿病,其疗效显著并符合人体胰岛素的生理分泌模式,吸收迅速,用药灵活,利于改善患者生活质量和提高患者依从性,并能更好的控制餐后血糖水平;并具有良好的耐受性和安全性,低血糖发生率低,是糖尿病患者控制血糖的理想选择之一。国产重组赖脯胰岛素与进口赖脯胰岛素同样能有效控制T2DM患者血糖,低血糖的发生率相似,疗效和安全性相当,值得临床上进一步的推广验证。
参考文献
[1]Yang WY,Lu JM,Weng JP,et al.Prevalence of diabetes among men and women in China[J].N Engl J Med,2010,362(12):1090-1101.
[2]Xu Y,Wang LM,He J,et al.Prevalence and control of diabetes in Chinese adults[J].JAMA,2013,310(9):948-958.
[3]Wright A,Burden AC,Paisey RB,et al.Sulfonylurea inadequacy:efficacy of addition of insulin over 6 years in patients with type 2 diabetes in the U.K.Prospective Diabetes Study (UKPDS 57)[J].Diabetes Care,2002,25(2):330-336.
[4]Cameron CG,Bennett HA.Cost-effectiveness of insulin analogues for diabetes mellitus[J].CMAJ,2009,180(4):400-407.
[5]Jia W,Xiao X,Ji Q,et al.Comparison of thrice-daily premixed insulin (insulin lispro premix) with basal-bolus (insulin glargine once-daily plus thrice-daily prandial insulin lispro) therapy in East Asian patients with type 2 diabetes insufficiently controlled with twice-daily premixed insulin:an open-label,randomised,controlled trial[J].Lancet Diabetes Endocrinol,2015,3(4):254-262.
[6]Thrasher J,Bhargava A,Rees TM,et al.Insulin lispro with continuous subcutaneous insulin infusion is safe and effective in patients with type 2 diabetes:a randomized crossover trial of insulin lispro versus insulin aspart[J].Endocr Pract,2015,21(3):247-257.
[7]Rees TM,Curtis BH,Gaskins KA,et al.Efficacy and safety of insulin lispro in obese patients with type 2 diabetes:a retrospective metaanalysis of 7 randomized controlled trials[J].Endocr Pract,2014,20(5):389-398.
[8]张丽蓉,潘晓平,陈卫中,等.用SAS编程进行定量资料的等效检验[J].现代预防医学,2008,35(7):1214-1215,1218.
[9]张新佶,贺江南,任建玲,等.阳性药对照临床试验中非劣效性检验的统计分析方法及相关问题[J].数理统计与管理,2010,29(2):372-379.
[10]Janikiewicz J,Hanzelka K,Kozinski K,et al.Islet β-cell failure in type 2 diabetes--Within the network of toxic lipids[J].Biochem Biophys Res Commun,2015,460(3):491-496.
[11] Rosenqvist U.The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus[J].N Engl J Med,1993,329(14):977-986.
[12]Turner R,Holman R,Cull C,et al.Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes(UKPDS33)[J].Lancet,1998,352(9131):837-853.
[13]Farag YM,Gaballa MR.Diabesity:an overview of a rising epidemic[J].Nephrol Dial Transplant,2011,26(1):28-35.
[14]Inzucchi SE,Bergenstal RM,Buse JB,et al.Management of hyperglycemia in type 2 diabetes:a patient-centered approach:position statement of the american diabetes association (ADA) and the european association for the study of diabetes (EASD)[J].Diabetes Care,2012,35(6):1364-1379.
[15]Holleman F,Hoekstra JB.Insulin lispro[J].N Engl J Med,1997,337(3):176-183.
A comparison of effects between recombinant insulin lispro and insulin lispro in treating type 2 diabetes mellitus
QiaoXuxia1,XuCheng2
(1.DepartmentofEndocrinology,Ba′nanDistrictPeople′sHospital,Chongqing401320,China;2.DepartmentofEndocrinology,SecondAffiliatedHospitalofChongqingMedicalUniversity,Chongqing400010,China)
[Abstract]ObjectiveTo compare the efficacy and safety of recombinant insulin lispro and insulin lispro in the treatment of type 2 diabetes mellitus(T2DM).MethodsForty-eight T2DM patients with poor blood glucose control were randomly assigned to the recombinant insulin lispro group (observation group,n=32) and insulin lispro group (control group,n=16) according to the ratio of 2∶1.On the basis of injection of the recombinant insulin glargine once daily before sleep,the two groups were given the recombinant insulin lispro injection or insulin lispro injection once before each meal.The period of treatment was 16 weeks.The levels of HbA1c,2 h postprandial blood glucose(2hPG) and fasting plasma glucose(FPG) before and after treatment were measured and compared between the two groups.The adverse events were evaluated at the end of treatment.ResultsForty-four cases finished the study,28 cases in the observation group and 16 cases in the control group.The levels of HbA1c,FPG and 2hPG after 16-week treatment in the two groups were decreased significantly(P<0.05).The decrease amplitudes of HbA1c in the observation group and the control group were (1.55±1.50)% and(1.06±1.30)% respectively,which of FPG were (2.07±5.01)mmol/L and(1.09±3.18)mmol/L respectively,and which of 2hPG declined (3.28±5.71)mmol/L and(3.60±5.89)mmol/L respectively.With HbA1c as the main evaluation index and 0.40 as the non-inferiority critical value,non- inferiority was found in the recombinant insulin lispro injection as compared with the insulin lispro injection(P<0.05).The standard-reaching rate of HbA1c less than 6.50% in observation group was 14.29%,and which of HbA1c less than 7.00% was 28.57%;in control group,these two standard-reaching rates were 18.75% and 43.75% respectively,and there were no statistically significant differences between two groups(P>0.05).ConclusionThe recombinant insulin lispro injection has non-inferiority effects in the aspect of effectiveness compared with the lispro insulin injection,moreover they have the same safety.
[Key words]diabetes mellitus,type 2;recombinant insulin lispro;treatment outcome;safety
doi:论著·临床研究10.3969/j.issn.1671-8348.2016.18.022
作者简介:乔旭霞(1975-),副主任医师,本科,主要从事内分泌专业糖尿病方向研究。
[中图分类号]R589.1
[文献标识码]A
[文章编号]1671-8348(2016)18-2518-04
(收稿日期:2015-11-18修回日期:2016-03-06)
