电子级三酚A的合成工艺研究
2016-07-14张智勇关金涛尹俊霞
王 坤,申 烦,张智勇,关金涛,尹俊霞
(武汉轻工大学 化学与环境工程学院,湖北 武汉 430023)
电子级三酚A的合成工艺研究
王坤,申烦,张智勇,关金涛,尹俊霞
(武汉轻工大学 化学与环境工程学院,湖北 武汉 430023)
摘要:探究了A,A,A-三(4-羟苯基)-1-乙基-4-异丙苯(三酚A)新的合成方法和合成工艺。以α-甲基苯乙烯为原料,经过烷基化、酰基化、酯化、缩合、水解的过程合成出三酚A;并且着重探索了关键步骤以硫酸为催化剂合成三酚A的反应温度、反应时间、酚酮物质的量比、催化剂及助催化剂的用量的反应工艺条件;并且探索了三酚A的精制工艺条件,得到了纯度达到99.872%的电子级三酚A;此方法原料易得,产品纯度高,在工业上容易实施且效率较高。
关键词:三酚A;合成;工艺研究;电子级
1引言
三酚A全称A,A,A-三(4-羟苯基)-1-乙基-4-异丙苯,它主要广泛应用于塑胶、电子及纺织等行业。三酚A在塑胶行业广泛应用于婴儿的奶瓶、奶粉的容器、水杯、饮料瓶等很多坚硬透明的塑料容器制品中,其具有耐用、轻巧和防摔等特性,是双酚A较好的替代原料[1];在电子行业方面主要用做光刻胶的主要原料, 三酚A的使用使得光刻胶的粘附性和光敏性得到了大大的提高[2];此外,三酚A还是纺织行业中的新型替代型印染助剂,印染助剂的使用可提高加工效率和产品质量,并可节约能源、降低加工成本,还能赋予纺织品优异的功能或风格,改善使用性能和提高纺织品的附加值[3]。
传统的三酚A的合成方法主要是异丙烯基苯乙酮与苯酚反应制得,由于异丙烯基苯乙酮具有活性的烯烃基,不易保存且价格高、产率低[4]。因此为解决传统三酚A合成的问题,笔者提供了一种性质稳定且易获得的原料,并且在工业上容易实施且高效率、高纯度的三酚A合成方法,并对此方法的合成工艺进行了研究。三酚A的合成线路如图1所示。

图1 三酚A的合成线路
2实验部分
2.1仪器与试剂
主要仪器:红外光谱仪,Nicolet iS10,Thermo公司; 核磁共振仪,INOVO 400 MHz,Varian公司; 投射偏光熔点测定仪,XPN-100E,上海长方公司;高效液相色谱仪,Agilent 1220,Agilent公司;电感耦合等离子体质谱仪,ICP-MS-2000,天瑞仪器。
主要试剂:α-甲基苯乙烯,阿拉丁试剂(上海)有限公司;苯酚,天津市致远化学试剂有限公司;冰醋酸、磷酸、甲苯,天津市天力化学试剂有限公司;三氯化铝、乙酰氯,天津市福晨化学试剂厂;β-巯基丙酸,武汉格奥化学技术有限公司;浓硫酸(98%),上述试剂均为分析纯。
2.24-枯基苯酚的合成[5-7]
在装有冷凝管、温度计、恒压低液漏斗磁子搅拌的三口瓶中加入熔融的苯酚37.6 g(0.4 mol)和(n(HAc):n(H3PO4)=1∶1)体系的混合催化剂5 g,升温至90 ℃缓慢滴加入α-甲基苯乙烯11.6 g(0.1 mol)。1 h左右滴加完毕,继续反应6 h,TLC跟踪至反应结束。待反应结束后,溶液澄清无色,加入甲苯150 mL溶解,水洗(100 mL)4次至中性,无水Na2SO4干燥,减压蒸馏除去甲苯和苯酚,再加入100 mL石油醚加热溶解,冷却重结晶,得白色针状固体。产率为67.4%,mp:73—75 ℃(文献值:72—74 ℃)。FT-IR ν:3278 cm-1,3020 cm-1,296l cm-1,1599 cm-1,1512 cm-1,1442 cm-1,1368 cm-1,1179 cm-1,829 cm-1;1H NMR(CDCl3) δ:1.65(S,6H),4. 65(s,1H),6. 70(d,2H),7. 10 ~ 7. 30(m,7H);元素分析(C15H16O):C 84.81,H 7.57 (计算值C 84.87,H 7.60)。
2.34- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮的合成[8-9]
在装有恒压滴液漏斗、冷凝管、搅拌机、低温温度计的500 mL四口烧瓶中导入三氯化铝91.8 g (0.69 mol)与二氯甲烷 137.7 g(相对于氯化铝为1. 5倍重量),氮气置换体系内的空气,并且将之冰浴冷却至-5 ℃。冷却后,通过滴液漏斗将乙酰氯70.65 g (0.9 mol)1 h滴加完毕,形成络合物。络合物在-5 ℃中不溶解于二氯甲烷,体系内成为浆体溶液。
形成络合物后,将烧瓶内温度维持在-5 ℃的同时,向溶液中滴加由4-枯基苯酚63. 6 g (0.3 mol)溶解于DCM 130 g而成的溶液,3 h滴加完毕,滴加结束保温15 min后升温至5—10 ℃之间,保温反应2 h。
反应结束后,拆去装置,将反应液缓慢倾倒入冰盐酸水溶液中(200 g浓盐酸∶500 g冰∶500 g水),同时快速搅拌,待倾倒完毕反应液后,搅拌10 min,静置分液,水层用50 ml×3萃取后,合并有机相,再将有机相洗涤至中性,用无水Na2SO4干燥5 h,旋蒸除去DCM,再加入150 mL石油醚,搅拌,加热溶解,冷却析出白色产品80.8 g,产率90.93%。HPLC检测纯度为99.8%;mp:92—93 ℃ 。1HNMR(CDCl3)δ:7.86(d,2H),7.32(d,2H,),7.20(d,2H),6.99(d,2H),2.57(s,3H),2.28(s,3H),1.69(s,6H);元素分析(C19H20O3):C 76.89,H 6.83 (计算值C 77.00,H 6.80)。
2.4三酚A的合成
在500 mL四颈瓶中依次加入4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮29.6 g (0.1 mol),苯酚75.3 g (0.1×8 mol)及等质量的甲苯(75.3 g),2.9 g β-巯基丙酸,N2保护,开动搅拌,控温在30 ℃,15分钟后,缓慢从100 mL 恒压滴液漏斗中滴加15.7 g浓硫酸,大约0.5—1 h滴完,随着滴加的进行反应液变为棕红色。滴完浓硫酸后,继续控温30 ℃,搅拌15 min。开始加热,控制温度在55 ℃左右,加热搅拌10 h后(TLC跟踪),停止反应。
加入75 g甲苯,再加入50.0 g水65 ℃搅拌水解30 min,而后静止分液;滴加15%的NaOH水溶液,调节PH至中性,反应液呈乳白色悬浮液,再升温至90 ℃后,等反应液变澄清后,将反应液倒入预热的分液漏斗中趁热分液。得紫红色的有机层,再向其中加入3%NaOH 30 g水溶液洗涤,除去颜色,得浅黄色溶液,在用热水50 g洗涤2次至中性,将有机层转入烧杯中,冷却、缓慢搅拌重结晶,抽滤、干燥后得白色粉末状固体35.2 g,产率82.9%。
精制过程:用2-丁酮∶甲苯=1∶5的混合液300 mL将所得的产品加热溶解,用200 mL 80 ℃二次纯净水洗涤萃取5—6次,收集有机层,再补加甲苯120 mL搅拌均匀后,冷却待产品析出,抽滤、烘干得到32.3 g白色产品,精制收率91.8%,HPLC检测纯度:99.887%。mp:228—229 ℃,FT-IR ν:3358.70、3023.68、2963.24、1597.58、1507.03、1440.99、1378.31、1298.56、1013.15、774.42 cm-1;1H-NMR(400MHz,(CD3)2SO)9.19-9.26(3H,d),7.01-7.10(4H,m)、6.92(2H,d,J=7.81Hz)、6.85(4H,d,J=7.81Hz)、6.63-6.67(6H,m)、1.98(3H,s)、1.57(6H,s);元素分析(C29H28O3):C 81.96,H 6.67 (计算值C 82.05,H 6.65)。
3结果与讨论
3.1三酚A反应条件探索
3.1.1原料的物料比对三酚A产率的影响
固定反应温度55 ℃,催化剂98%浓硫酸15.7 g,助催化剂β-巯基丙酸2.9 g,反应时间10 h。取4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮29.6 g(0.1 mol),调整苯酚和4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮的物质的量比(r),实验结果如图1所示。

r =n苯酚/n4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮图1 酚酮物质的量比对三酚A收率的影响
由图1可见,酚酮物质的量的比r对三酚A的合成收率有较大影响。随着酚酮摩尔比r的增加,收率明显增加,当酚酮比为收率达到8时,继续增加酚酮摩尔比,收率反而略微下降。这是因为,反应体系原料的浓度变低,反应受到影响,收率降低。同时r过高会造成苯酚浪费,增加回收成本,故选择酚酮最佳物质的量的比为8∶1,即r=8。
3.1.2温度对三酚A反应产率的影响
固定酚酮物质的量比r=8,改变反应温度,其他反应条件同3.1.1,实验结果如图2所示。如图2可以看出,温度较低时,反应速度较慢, 三酚A收率较低,随着温度升高,反应速度加快, 三酚A收率增加。但是温度高于60 ℃时,收率反而略微下降,这可能是反应温度高,副产物增加所致。故反应温度以55 ℃为宜。
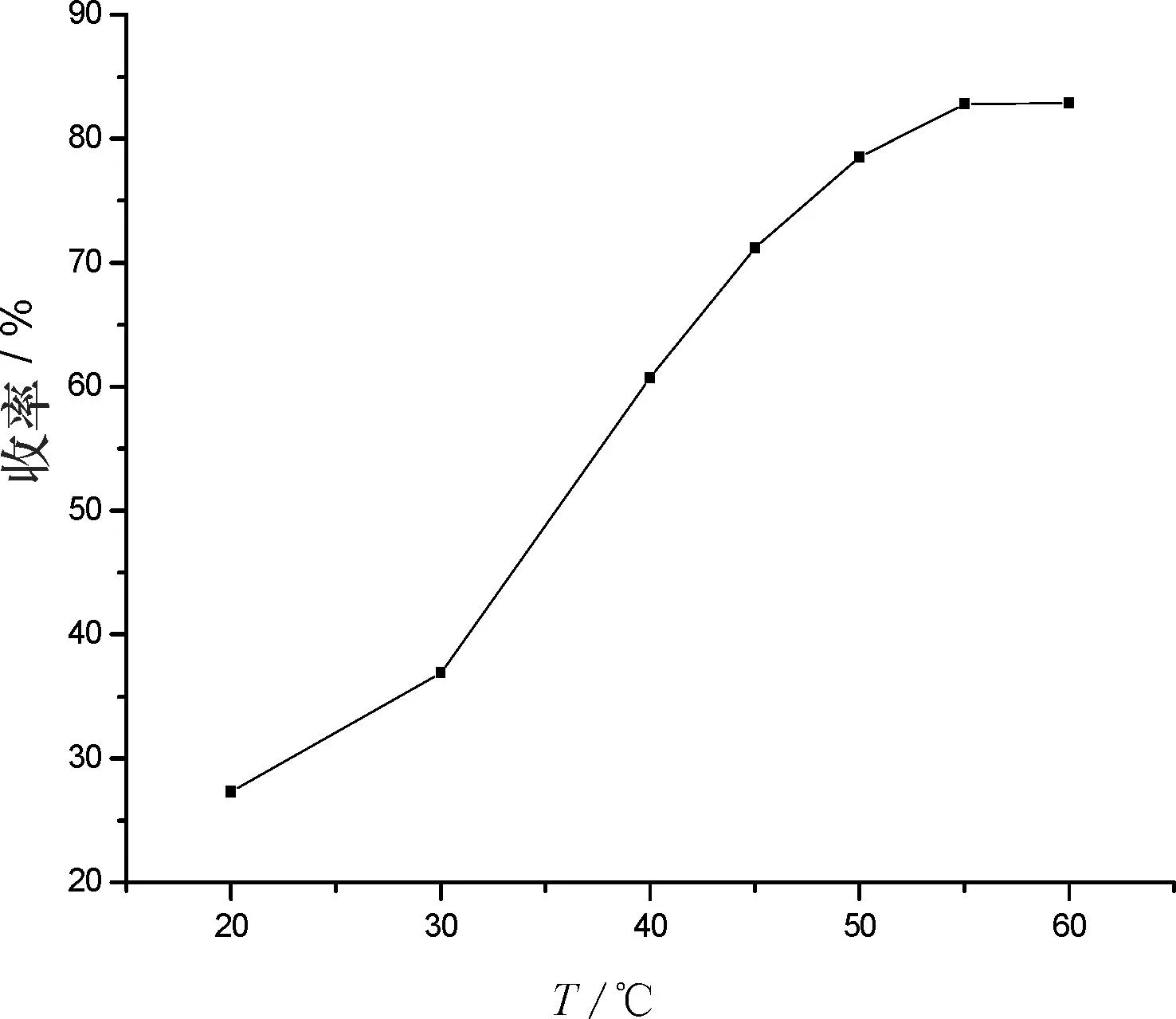
图2 温度对三酚A反应产率的影响
3.1.3反应时间对三酚A产率的影响
固定酚酮物质的量比r=8反应温度定为55 ℃,改变反应时间,其他反应条件同3.1.1,实验结果如图3所示。由图3可知,在1—10 h之间,随着时间的增加,三酚A收率逐步增加,在4—6 h反应较为剧烈,但反应时间超过10 h后,继续延长反应时间收率变化不大,考虑到延长反应时间可能会产生较多副反应,综合分析后,选择最佳反应时间为10 h。

图3 反应时间对三酚A产率的影响
3.1.4催化剂与助催化剂用量对三酚A产率的影响
固定酚酮物质的量比r=8,反应温度定为55 ℃,反应时间为10 h,分别改变催化剂98%浓硫酸的用量(催化剂的质量∶酚酮质量之和)和催化剂β-巯基丙酸的用量(助催化剂的质量∶酚酮质量之和),实验结果如图4、图5所示。
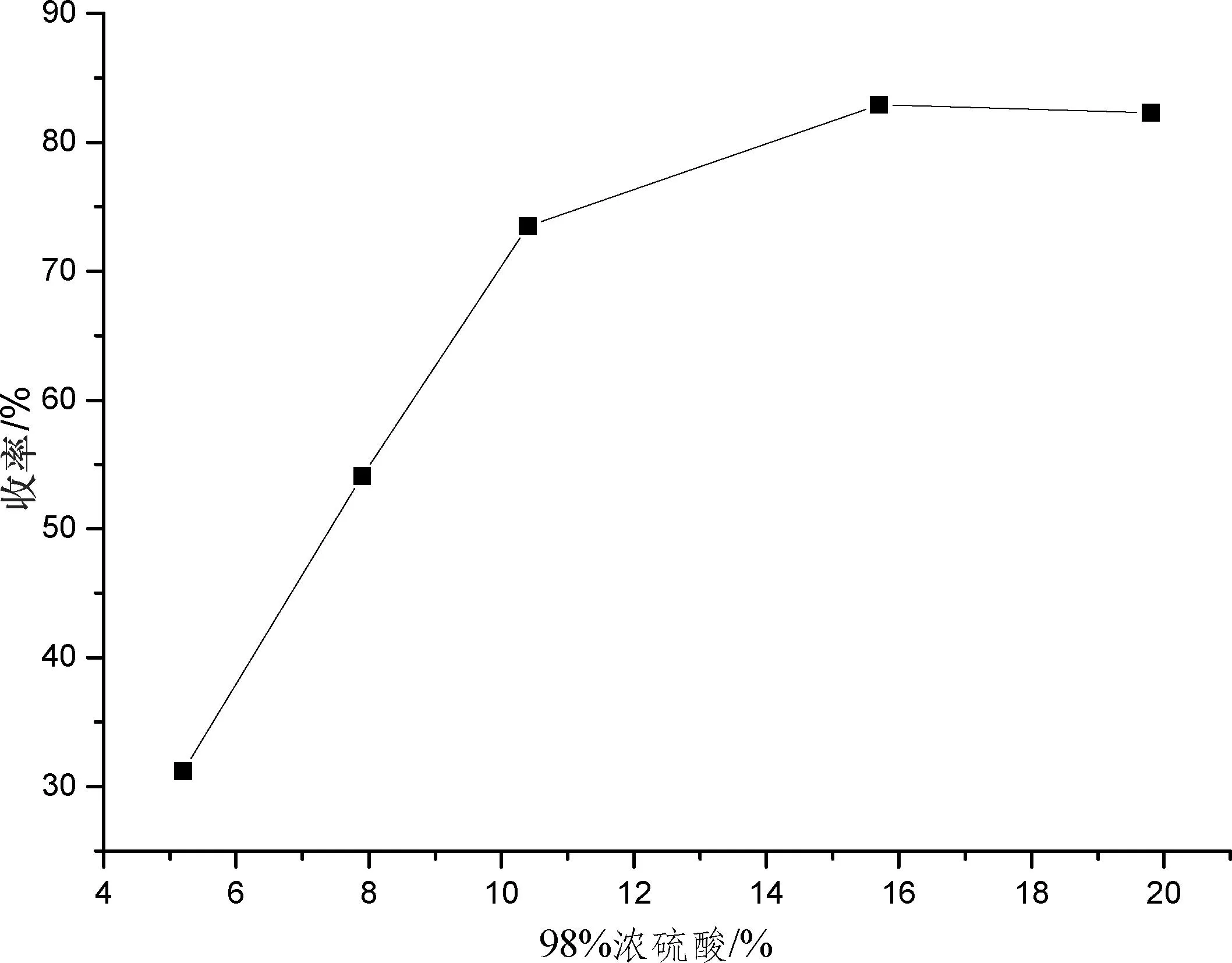
图4 催化剂用量对三酚A产率的影响

图5 助催化剂用量对三酚A产率的影响
由图4可以清楚地看到,催化剂的用量对三酚A收率影响较大。随着催化剂用量的增加收率增加,当催化剂用量为15.7%时收率最高,之后再多加入催化剂收率反而略微下降,这可能是由于高含量的浓硫酸使得部分产物被氧化。过量的催化剂不利于反应进行,因此催化剂最佳用量为15.7%。
由图5可以看出,助催化剂β-疏基丙酸的用量对三酚A收率也有较大影响,助催化剂的用量从1‰—3‰之间,三酚A收率显著增加,继续增加其用量收率变化不大,考虑到助催化剂的回收处理及成本,我们选择最佳助催化剂用量为3‰。
3.2三酚A的精制条件探索
3.2.1溶剂比对三酚A产品晶析收率的影响
在多次试验,尝试了多种溶剂和混合溶剂体系对三酚A进行重结晶,发现2-丁酮—甲苯体系重结晶效果较好,之后对其重结晶的溶剂比进行了探索。取合成出的粗产品10 g,用2-丁酮10 mL将其溶解,分别缓慢加入下列对应比例的甲苯(溶剂比=2-丁酮∶甲苯),加热溶解,缓慢冷却,待得产品析出后,抽滤、干燥、称重,计算其晶析的收率,结果如表1所示。
由表1可以发现,溶剂比在大于1∶3时,三酚A无法析出晶体;当溶剂比在1∶3—1∶7之间,随着溶剂比的减小,三酚A晶析收率逐步增大;当溶剂比小于1:7后,晶析收率变化不大,同时,重结晶过程中的杂质除去效果不佳,溶解三酚A需要的温度大大提升,这使得在工业化中耗能变大,生产成本增大。故选择1∶7的2-丁酮/甲苯体系时,重结晶效率较高。
表1重结晶时,溶剂比对三酚A晶析收率的影响

溶剂比1∶11∶31∶51∶61∶71∶81∶10收率/%0058.380.191.891.992.1
3.2.2精制时重结晶次数对纯度的影响
在生产过程中,我们需要纯度高于99.5%的三酚A产品,根据需求,对重结晶次数进行了探索(表2)。HPLC检测条件:250 mm色谱柱,流动相为75%甲醇,检测波长为280 nm,进样量为5 μL,流速1 mL/min。
由表2可以清晰地看出产品纯度,随着重结晶的次数增加而增加,当重结晶两次时,产品的纯度就高于99.5%,此时就可以达到高纯度化学品的要求;当重结晶3次时,三酚A产品的的纯度已经达到99.872%,再增加重结晶次数,产品的纯度增加不明显,成本也随之而增加,不利于工业生产,因而根据需求重结晶3次可得到高纯度的三酚A产品。
表2重结晶次数对产品纯度的影响

次数01234纯度/%97.54299.13899.73599.87299.887
3.2.3超纯水洗涤次数对钠离子含量的影响
在精制时,将10 g三酚A粗产品用2-丁酮/甲苯(1∶7)加热溶解后,加入60 ℃的电导率为11 MΩ的超纯水震荡洗涤,分液,静置、冷却重结晶,干燥后用IPC-MS检测其钠离子的含量,检测标准为JY/T 015-1996。根据不同洗涤次数,获得的三酚A产品,钠离子含量检测结果如图6所示。
由图6可知,随着洗涤次数的增加,钠离子含量在急剧减少,当洗涤5次之后,钠离子含量减少的程度趋于平缓,此时钠离子的含量仍高于500×10-9,此时的产品虽然达到电子级含量的级别,但是其含量依旧较高,仍有较大的提升空间。分析原因是实验室环境的洁净度达不到要求,需要在洁净实验室环境下,进行多次洗涤。在洁净实验室,再次进行更精细的精制后产品可达到10×10-9的级别。

图6 超纯水洗涤次数对三酚A中钠离子含量的影响
4结论
笔者以α-甲基苯乙烯为原料与苯酚偶联得到4-枯基苯酚,再酰基化、酯化得到4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮,之后与苯酚缩合得到三酚A,通过FT-IR、1HNMR确认其结构正确,4-枯基苯酚是常见的工业原料。着重探索了硫酸法催化合成电子级三酚A的最佳工艺条件,最佳工艺条件是苯酚与4- (1- (4-乙酰氧基苯基)-1-甲基乙基)苯乙酮的物质的量的比为8∶1,催化剂浓硫酸用量为15.7%,助催化剂β-疏基丙酸用量为3‰,在55 ℃环境下反应10 h, 三酚A的产品收率82.9%,产率较高,实验室环境下用2-丁酮/甲苯=1∶7的混合溶剂溶解三酚A,用60 ℃超纯水洗涤5次可使钠离子含量达10-9级别,通过洁净车间可得到电子级三酚
A产品,重结晶3次可得到纯度高达99.872%的三酚A。本实验工艺流程简单,具有较强的工业化生产的可行性。
参考文献:
[1]华文,袁征. 塑料奶瓶安全存争议[J].中国保健营养,2009:79.
[2]郑金红. I-Line光刻胶材料的研究进展.[J] 影像科学与光化学.2012,30(2),81-90
[3]宋肇棠,国晶.环境保护与环保型纺织印染助剂[J].印染助剂,1998,15(3):1-9
[4]尾尻明彦,辻上隆章,丹波孝一.三酚类及其单酯取代物的制造方法及4-烷基芳烷基苯酚衍生物:CN102428061 A.[P]. 2012,
[5]沈之芹,王芳.α-甲基苯乙烯与苯酚的烷基化反应研究[J].合成化学,2006,14(2),196-199.
[6]由君,刘波,段聪文,等. 4-枯基苯酚与2,4-二枯基苯酚联产工艺[J].化工学报,2012,63(5),1429-1436.
[7]钟晓萍,孟宪梅,徐龙鹤. 2,4-二枯基苯酚的合成 [J].沈阳化工学院学报,2009,23(4),309-312.
[8]Akihiko Ojiri, Wakayama, Takafumi Tsujiami. Method for producing trisphenols and monoes- -tersubstituted products thereof, and4-acylaralkylphenol derivatives: US108853A1[P].2012.
[9]尾尻明彦,辻上隆章,丹波孝一.4-酰基芳烷基苯酚衍生物: CN104211588A[P]. 2014.
[10]Zheng Shao-Liang, Gembicky Milan, Marc Messerschmidt,et al. Effect of the Environment on Molecular Proper- -ties: Synthesis, Structure, and Photoluminescence of Cu (I) Bis-(2,9-dimethyl-1,10-ph-enan- -throline) Nanoclusters in Eight Different Supramolecular Frameworks [J]. Inorganic Chem- -istry. 2006, 45(23), 9281-9289.
Study on the synthesis process of electronic grade Trishydroxyphenylethylisopropylbezene
WANGKun,SHENFan,ZHANGZhi-yong,GUANJin-tao,YINjunxia
(School of Chemistry and Environmental Engineering,Wuhan Polytechnic University, Wuhan 430023, China)
Abstract:To explore the new method for synthesizing trishydroxyphenylethylisopropylbezene (TPP) and study on the synthesis process, in this paper, we used α-methyl-styrene as raw materials, and adopted method of alkylation, acylation, esterification, condensation reaction, hydrolysis to obtain the TPP. In addition, we focused on the key steps and used sulfuric acid as the catalyst for TPP and explored the reaction temperature, reaction time, phenol ketone molar ratio, the amount of catalyst and co-catalyst reaction conditions; And explored the TPP’s purification process conditions to obtain the electronic level, high purity product reaching 99.872%; What’s more, this method was easily available in raw materials, easy to implement in industrial and high efficiency, high purity, which has yet to see reports at present.
Key words:Trishydroxyphenylethylisopropylbezene;synthesis; technology research; electronic grade
收稿日期:2016-03-09.
作者简介:王坤(1988-),男,硕士研究生,E-mail,253689413@qq.com. 通信作者:张智勇(1962-),男,教授,E-mail:zzy6211@126.com.
文章编号:2095-7386(2016)02-0040-05
DOI:10.3969/j.issn.2095-7386.2016.02.007
中图分类号:O 621.3
文献标识码:A
