汉滩病毒包膜糖蛋白假病毒的构建及特性研究
2016-07-14李金林陈良君杨占秋
钟 研,李金林,陈良君,杨占秋
(武汉大学医学病毒学研究所,病毒学国家重点实验室, 湖北 武汉 430071)
汉滩病毒包膜糖蛋白假病毒的构建及特性研究
钟研,李金林,陈良君,杨占秋
(武汉大学医学病毒学研究所,病毒学国家重点实验室, 湖北 武汉 430071)
【摘要】目的:研究汉滩病毒包膜糖蛋白与宿主细胞作用的分子机制,构建含有汉滩病毒(HTNV)标准株76~118株包膜糖蛋白的假病毒,并对其进行检测. 方法:将表达汉滩病毒包膜糖蛋白的质粒和以VSVΔG为骨架的假病毒颗粒,与293T细胞共转染,构建汉滩病毒的假病毒,用中和实验,受体抑制实验,免疫共沉淀和Western Blot对其抗原性、中和反应、受体作用等进行检测. 结果:汉滩病毒假病毒与活病毒有相似的抗原特性,汉滩病毒假病毒可以模拟活病毒进入细胞的方式,其糖蛋白是以二聚体形式存在的. 结论:成功构建含有汉滩病毒标准株包膜糖蛋白的假病毒,它与活病毒的抗原特性和受体作用的方式相似,这为进一步研究汉滩病毒包膜糖蛋白与宿主细胞作用的分子机制提供了很好的工具.
【关键词】汉滩病毒;包膜糖蛋白;假病毒;水泡性口炎病毒
0引言
汉坦病毒属于布尼亚病毒科,主要引起肾综合征出血热(hemorrhagic fever with renal syndrome,HFRS)和肺综合征出血热(hantavirus pulmonary symdrome, HPS)两种疾病[1]. 包括我国在内的亚洲地区主要以汉滩病毒(hantaan virus, HTNV)和汉城病毒(seoul virus, SEOV)引起的HFRS为主,欧洲地区以普马拉型(puumala virus,PUUV),多布拉伐型(dobrava virus,DOBV)引起的HFRS为主,美洲地区主要由辛诺柏病毒(sin nombre virus,SNV)引起的HPS为主[2]. 汉坦病毒为单负链RNA病毒,由 L,M,S三个片段组成,L片段编码病毒的RNA聚合酶,M片段编码包膜糖蛋白(GN和GC),S片段编码核壳蛋白(NP). 其中包膜糖蛋白对病毒感染早期入胞,膜融合,晚期出胞等阶段均具有重要作用,但其与宿主细胞相互作用的分子机制仍未完全明了,需要进一步研究. 目前,利用水泡性口炎病毒(vesicular stomatitis virus,VSV)为骨架构建的假病毒系统已经广泛应用于研究RNA病毒的复制,外源糖蛋白的功能以及筛选药物,疫苗评价等[3-7],假病毒系统也已开始运用于汉坦病毒的研究[2,8-9]. 但是这些假病毒是否能完全模拟汉坦病毒的生物学活性及功能尚未见报道. 本研究制备了以水泡性口炎病毒为骨架的汉滩病毒标准株的假病毒,为深入研究汉坦病毒包膜糖蛋白与宿主相互作用机制及评价抗病毒药物和疫苗效果提供手段.
1材料和方法
1.1材料汉滩病毒标准株76~118株活病毒由本实验室长期保存. 293T细胞;Vero-E6细胞;Opti-MEM/LF2000(Invitrogen),宾夕法尼亚大学的Robert Doms教授和Connie S.Schmaljohn 实验室赠送了抗VSV-G和抗HTNV Gc的单克隆抗体HCO2和11E10. 新墨西哥大学医院和智利的汉坦病毒研究组分别提供了抗SNV血清和抗ANDV的患者血清. 田纳西大学的Michael Whitt教授和Robert Doms教授分别赠送了VSVΔG-GFP-VSVG和VSVΔG-luc-VSVG假病毒,pCMV-VSV-G质粒. 中质粒提取试剂盒(Omega). FLAG肽,M2抗 FLAG 抗体(Sigma).
1.2方法
1.2.1汉滩病毒包膜蛋白质粒的表达根据汉滩病毒标准株M片段的基因序列,对编码区的密码子优化之后,由公司(Menlo Park, CA,USA) 合成相应的序列,其含有KpnI和NotI酶切位点,以此酶切位点将M片段克隆到真核表达载体 pCDNA3.1中,形成表达汉坦病毒包膜糖蛋白的质粒,同时在GC蛋白的C末端加入了FLAG标签便于检测 .
1.2.2质粒扩增鉴定①将pHTNVMDNA质粒进行转化扩增. 将连接好的质粒热休克后加入37℃预热的300 μLLB培养基(不含抗生素)轻轻混匀,然后固定到摇床上37℃震荡1 h,取上述转化混合液200 uL滴到含合适抗生素的固体LB培养皿中,用无菌玻璃棒涂布均匀,放入37℃恒温培养箱过夜. 挑取固体培养基上的白色单菌落,接种于含有相应抗生素的20 mL LB液体培养基中,37℃,250 g振荡培养过夜. 取培养物离心后,试剂盒提取质粒. ②用KpnI和NotI双酶切后进行琼脂糖凝胶电泳方法鉴定质粒.
1.2.3假病毒的制备①接种293T细胞到6孔板中,待细胞80%左右融合后,进行转染;②按LF2000说明书将LF2000与Opti-MEM,汉滩病毒表达质粒与Opti-MEM液分别混匀稀释,然后再将两种稀释液混合均匀,室温放置5 min;③将96孔板换新鲜培养基,然后将混合转染液轻轻的滴入到平皿中,继续培养6 h;④6 h后,去除转染培养基以减少LF2000对细胞的毒性,加入新鲜的培养基(不含抗生素)到6孔板中;⑤继续培养72 h后,将VSVΔG-GFP或VSVΔG-rLuc加入到DMEM原液中稀释,更换细胞培养液,加入VSVΔG病毒稀释液,37℃孵育2 h后,去除病毒稀释液,用DMEM 原液洗细胞两次,然后加入不含抗生素的2%DMEM的培养液,37℃继续培养24 h;⑥从6孔板中收取上清到离心管后,2000 rpm,10 min离心,收取上清,然后加入Tris;⑦用滤器过滤后,分装,待用.
1.2.4假病毒对VeroE6细胞的感染性的检测①将veroE6细胞接种到96孔板中,待细胞长到单层后开始实验;②将制备好的带有Luciferase标签的假病毒按照不同浓度进行稀释后感染VeroE6细胞,孵育2 h;③弃去病毒液,用DMEM原液洗一遍,然后加入含2% DMEM维持液继续培养16 h;④检测细胞内Luciferase的量(RLU)即可反映假病毒对VeroE6细胞的感染性.
1.2.5血清或抗体对假病毒的中和作用的检测①将veroE6细胞接种到96孔板中,待细胞长到单层后开始实验;②先将Anti-VSV抗体mAb VSV稀释到1 μg/mL,1∶50稀释倍数稀释患者血清,然后将带GFP标签的假病毒与血清或抗体稀释液等体积混合,37℃水浴1 h;③将混合液加入细胞孔板中,培养24 h;④将培养液上清吸入EP管中,用胰酶消化细胞,将消化的细胞吸入到相应上清的EP管中;⑤1000 rpm,10 min离心后去除上清液,加入200 μL的稀释液混匀;⑥流式细胞仪检测感染假病毒细胞的量.
1.2.6抗β3整合素受体药物Reopro对汉滩病毒假病毒的抑制作用①将Vero-E6细胞接种到96孔板中,待细胞长到单层后开始实验;②将Reopro药物用DMEM原液倍比稀释后分别加入细胞培养板中50 μL/孔,孵育1 h;③将带GFP的假病毒稀释后加入等体积假病毒稀释液到细胞培养孔,孵育1 h;④去除孵育液,洗2遍后,加入2% DMEM 细胞维持液,37℃,5% CO2继续培养16 h;⑤在荧光显微镜下计算GFP 阳性细胞的个数.
1.2.7用免疫共沉淀方法检测包膜糖蛋白是否以二聚体形式存在①将已制备好的汉滩病毒假病毒颗粒VSVG-luc用辛基糖苷裂解,然后用包被有抗 FLAG 的珠子进行免疫共沉淀,②沉淀洗脱后用抗FLAG 和抗GN抗体进行Western Blot试验.
2结果
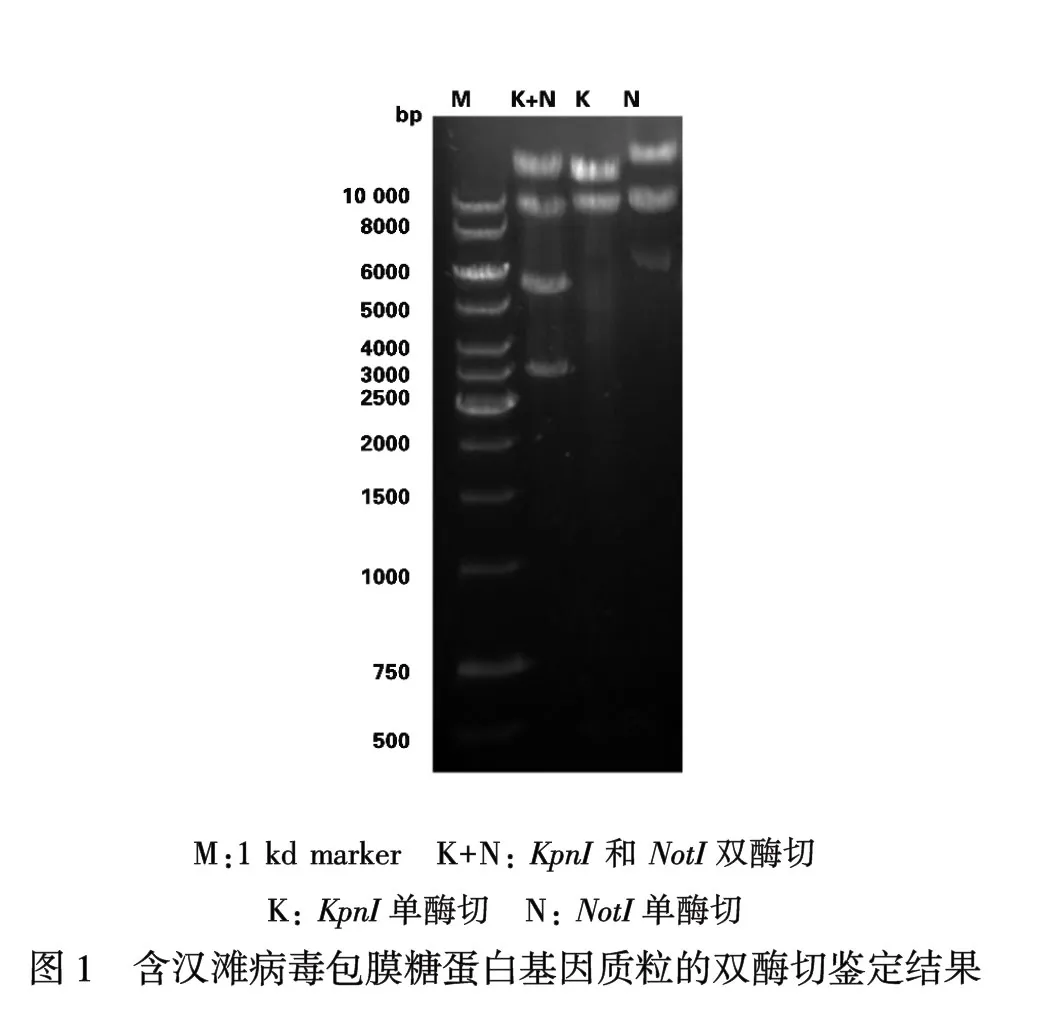
2.1汉滩病毒假病毒质粒的鉴定用KpnI和NotI酶进行双酶切鉴定,结果琼脂糖凝胶电泳跑出的片段与设计的质粒片段相符(图1). 汉滩病毒标准株76~118 M片段质粒M片段长3616 bp,pCDNA3.1(-)为5428/5427 bp,总长度约为9044 bp,条带K+N为双酶切条带,共有4个条带,分别大概位置在3600 bp,5400 bp,9000 bp,11 000 bp左右,11 000 bp片段应该为质粒开环的构型,结果与预期一致,说明质粒构建成功.
2.2汉滩病毒带GFP标签假病毒制备通过上述的假病毒的制备方法,可以得到带GFP绿色荧光的假病毒(图2 A,B),图A为汉滩病毒标准株包膜糖蛋白的假病毒(VSVG-HTNV-GFP),滴度约为3.5×105IU/mL图B为VSV与自身G蛋白质粒构建的假病毒(VSVG-VSV-GFP).滴度约为2×107IU/mL. 可以从图中看出VSVG-HTNV-GFP比VSVG-VSV-GFP的滴度低,原因可能为VSV自身G蛋白可以更有效率的与VSV骨架组装,VSV包膜糖蛋白的构象与汉滩病毒构象不同可能也影响其滴度.
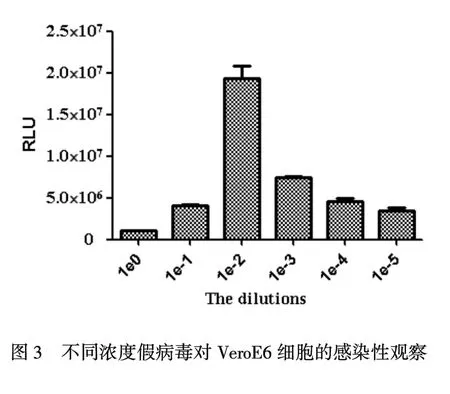
2.3假病毒对易感细胞Vero E6的感染性的观察假病毒稀释成不同的滴度感染Vero E6细胞时,在10-2稀释倍数其对vero-E6的感染量最高,约1.92×107,随后随着稀释倍数增加,感染量逐渐降低,因此选用10-2的稀释倍数进行后续实验(图3).
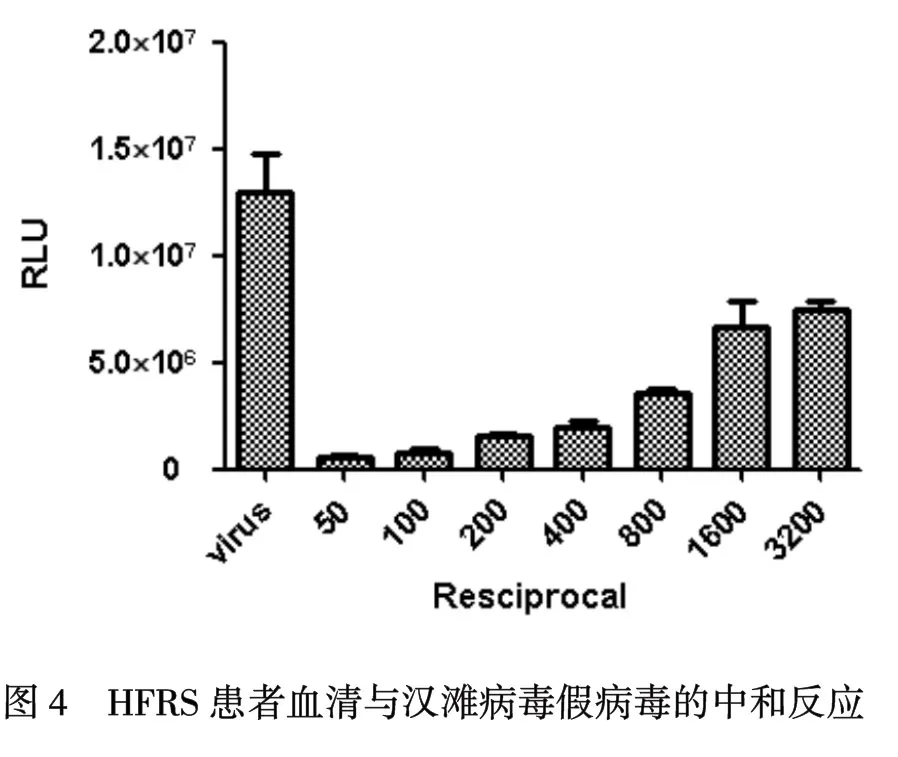
2.4汉坦病毒假病毒与HFRS患者血清的中和反应研究本研究用带Luciferase标签的假病毒与不同稀释浓度的HFRS患者血清进行中和反应,其中患者血清已经用ELISA方法证实有抗体(图4),在稀释1∶50时血清几乎可以中和所有的假病毒,随着稀释度增加,假病毒中和的量也随之越来越少. 这说明汉滩病毒假病毒与活病毒一样可以与HFRS患者血清进行中和反应.
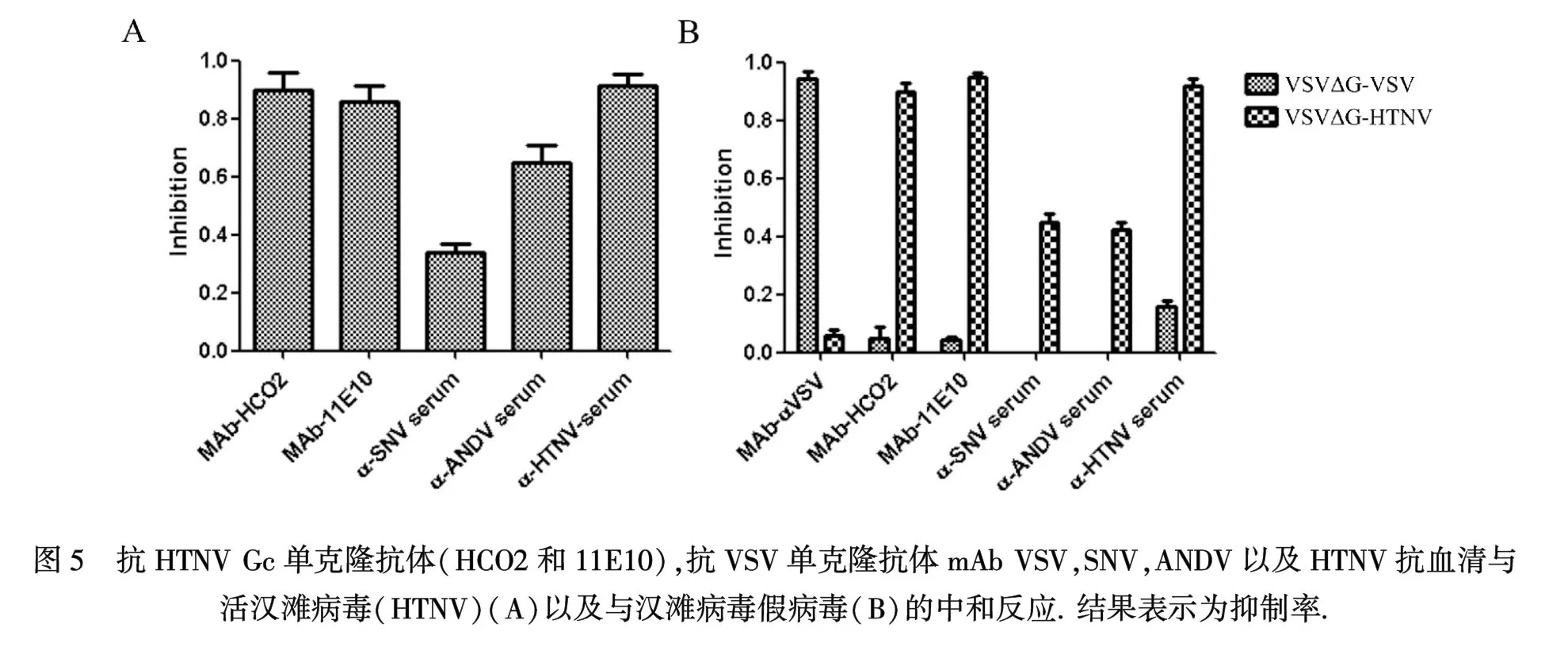
2.5汉滩病毒假病毒的抗原性研究将汉滩病毒活病毒,假病毒,分别与抗汉滩型汉坦病毒 Gc的单克隆抗体(HCO2和11E10),抗VSV单克隆抗体 mAb VSV,SNV,ANDV以及 HTNV 抗血清(来源于HPS/HFRS患者的血清)进行反应(图5)A与B比较观察可知,假病毒与活病毒对单克隆抗体和HFRS患者血清表现出相似的抗原性,另外从图中可观察到抗VSV单克隆抗体mAbVSV对汉滩病毒假病毒基本没有中和作用,仅对VSVΔG-VSV 有抑制作用,这就表明假病毒中的VSV骨架蛋白对汉滩病毒表面蛋白所产生的中和作用没有明显影响.
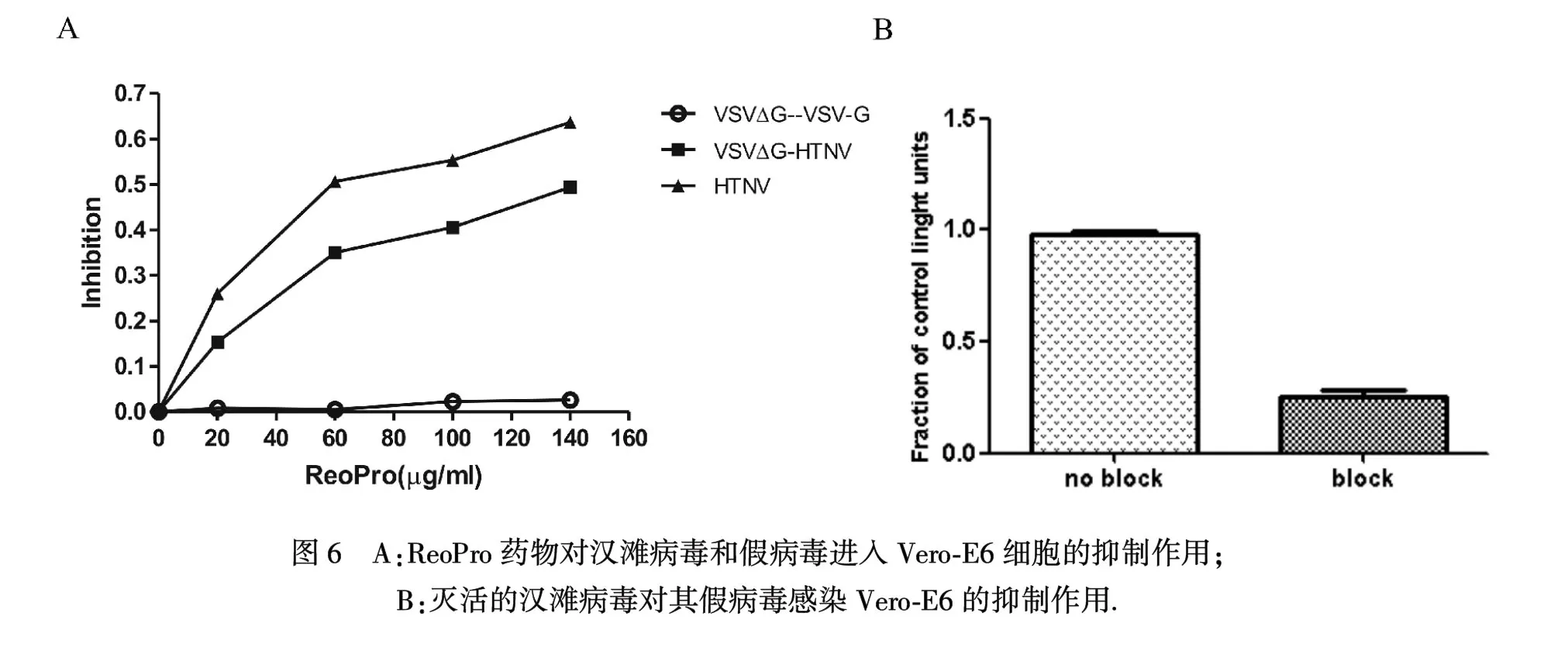
2.6 汉滩病毒假病毒与活病毒受体研究有研究[10]表明β3整合素受体在致病性汉坦病毒进入细胞中发挥了重要作用,但假病毒是否也可以利用β3整合素进入细胞尚不明确,因此我们用抗β3整合素的 Reopro药物预先处理细胞(图6A),ReoPro药物对汉滩病毒进入E6细胞的抑制率可达60%,对汉滩病毒假病毒的抑制率可达45%,说明ReoPro药物可以同时减少致病性活汉滩病毒和假病毒进入细胞,但是观察发现ReoPro药物对VSVΔG-GFP-VSV并没有抑制作用,说明假病毒的骨架对其利用受体进入细胞没有影响. 另外我们用紫外UV灭活的HTNV 汉滩病毒预先与Vero-E6 细胞相互作用,处理组的假病毒进入细胞的量明显被抑制(图6B). 这说明假病毒与其活病毒利用相同的受体进入细胞.
2.7 汉滩病毒假病毒的包膜糖蛋白是以二聚体形式存在有研究[1]表明不同型别的包膜糖蛋白超微结构略有不同,但均以GN,GC二聚体形式存在,而汉滩病毒假病毒表达的包膜糖蛋白是否也是二聚体形式尚不清楚,本研究用抗FLAG 的M2 抗体结合到 6 μm 珠子上,然后用去捕捉Gc,然后用Western Blot的方法进行检测,成熟的Gn和Gc分子量分别为68 kD和55 kD(图7),本研究用对沉淀洗脱后检测,检测到了Gn和Gc,表明汉滩病毒假病毒中Gn和Gc 是以二聚体形式存在.

3讨论
近年来,HFRS的流行趋势发生了变化,新的汉坦病毒的型别和亚型不断出现,病毒的基因变异可能是其根本原因,而M片段编码的GP蛋白承受来自宿主的免疫压力最大,变异最为显著,M基因编码的GP蛋白在病毒进入宿主细胞,中和抗体形成,逃避机体免疫反应等与致病相关的环节密切相关[1]. 汉坦病毒感染与其他有包膜病毒相同,均是由包膜糖蛋白与宿主细胞膜上的受体特异性结合后启动的. 所以研究包膜糖蛋白与受体的识别结合机制,对于后续寻找特异性药物和疫苗抑制汉坦病毒感染起始,从源头阻断其进入细胞复制有着很重要的意义. 本研究利用VSV为骨架构建的假病毒系统带有荧光标签,可以更为方便的进行检测,本研究中我们成功构建了汉滩病毒标准株的假病毒,并对其进行了鉴定,结果表明假病毒对易感细胞VeroE6具有很高的感染性,并且能与单克隆抗体和HFRS血清发生中和反应,假病毒中的GN和GC是以二聚体形式存在的,这是与活病毒的结构一致,这是发挥生理活性的基础. 汉滩病毒与其假病毒不仅具有相同的抗原性,并且还利用相同
的受体进入细胞,这为应用假病毒来筛选抗汉坦病毒药物及疫苗效果评价,研究G蛋白在致病中的分子机制都提供了很好的工具.
【参考文献】
[2] Ogino M, Ebihara H, Lee BH, et al. Use of vesicular stomatitis virus pseudotypes bearing hantaan or seoul virus envelope proteins in a rapid and safe neutralization test[J]. Clin Diagn Lab Immunol,2003,10(1):154-160.
[3] Burns JC, Friedmann T, Driever W, et al. Vesicular stomatitis virus G glycoprotein pseudotyped retroviral vectors: concentration to very high titer and efficient gene transfer into mammalian and nonmammalian cells[J]. Proc Natl Acad Sci USA,1993,90(17): 8033-8037.
[4] Lawson ND, Stillman EA, Whitt MA, et al. Recombinant vesicular stomatitis viruses from DNA[J]. Proc Natl Acad Sci USA,1995,92(10):4477-4481.
[5] Schnell MJ, Buonocore L, Kretzschmar E, et al. Foreign glycoproteins expressed from recombinant vesicular stomatitis viruses are incorporated efficiently into virus particles[J]. Proc Natl Acad Sci USA,1996,93(21):11359-11365.
[6] Bácsi A, Ebbesen P, Szabo J, et al. Pseudotypes of vesicular stomatitis virus-bearing envelope antigens of certain HIV-1 strains permissively infect human syncytiotrophoblasts cultured in vitro:implications for in vivo infection of syncytiotrophoblasts by cell-free HIV-1[J]. J Med Virol,2001,64 (4):387-397.
[7] Maruyama J, Miyamoto H, Kajihara M, et al. Characterization of the envelope glycoprotein of a novel filovirus, lloviu virus[J]. J Virol,2014,88(1):99-109.
[8] Higa MM, Petersen J, Hooper J, et al. Efficient production of Hantaan and Puumala pseudovirions for viral tropism and neutralization studies[J]. Virology,2012,423(2):134-142.
[9] Ray N, Whidby J, Stewart S, et al. Study of Andes virus entry and neutralization using a pseudovirion system[J]. J Virol Methods,2010,163(2):416-423.
[10] Gavrilovskaya IN, Brown EJ, Ginsberg MH, et al. Cellular entry of hantaviruses which cause hemorrhagic fever with renal syndrome is mediated by beta3 integrins[J]. J Virol,1999,73(5):3951-3959.
Construction and identification of hantaan pseudovirions
ZHONGYan,LIJin-Lin,CHENGLiang-Jun,YANGZhan-Qiu
Institute of Medical Virology/State Key Laboratory of Virology, School of Medicine of Wuhan University, Wuhan 430071, China
【Abstract】AIM: To study the molecular mechanism of hantaanvirus (HTNV) envelope glycoprotein with host cell, and constructe pseudovirions of HTNV 76-118 strains. METHODS: It was constructed by incorporating of HTNV glycoproteins onto replication-defective vesicular stomatitis virus(VSV) cores in which the gene for the surface G protein has been replaced by the reporter gene. Antigenicity, neutral reaction and receptor function were detected by neutralization test, co-immunoprecipitation and flow cytometry. RESULTS: There was good concordance of the antigenicity and the way inside host cells between HTNV and its pseudovirions. Also, the glycoprotein GNand GCof pseudovirions existed as heterodimers. CONCLUSION: The pseudovirions are successfully constructed and the pseudovirions can be used to simulate the way of HTNV entry and antigenicity. This study provides a good stool for study on molecular mechanism of hantaan virus envelope glycoprotein.
【Keywords】hantaan virus; pseudovirions; vesicular stomatitis virus(VSV); glycoprotein
文章编号:2095-6894(2016)04-01-05
收稿日期:2016-03-04;接受日期:2016-03-20
基金项目:国家自然科学基金资助项目(81371865)
作者简介:钟研. 硕士. 研究方向:汉坦病毒感染与免疫. E-mail:zy20160217@163.com 通讯作者:杨占秋. 教授. 研究方向:病毒进化与变异. E-mail:zqyang@whu.edu.cn
【中图分类号】R373.9
【文献标识码】A
·基础与转化医学·
