不同剂量附子单煎乌头类生物碱煎出量分析
2016-07-11李学林吴红展
李学林,吴红展,许 真
(1.河南中医学院第一附属医院,河南 郑州 450000;2.郑州大学第二附属医院,河南 郑州 450014)
不同剂量附子单煎乌头类生物碱煎出量分析
李学林1,吴红展1,许真2
(1.河南中医学院第一附属医院,河南 郑州 450000;2.郑州大学第二附属医院,河南 郑州 450014)
摘要目的:考察附子在汤剂中不同质量分数时指标性成分的含量煎出规律,为临床使用附子时合理选择剂量提供依据。方法:采用RP-HPLC法,色谱柱为AgiLent C18SB-Aq柱(4.6 mm×150 mm,5 μm),流动相为乙腈-0.1 moL/L醋酸铵溶液、流速0.4~0.6 mL/min,检测波长235 nm,柱温30 ℃。结果:随着质量分数的增加,附子单煎水煎液中苯甲酰类乌头生物碱煎出增长率逐渐降低;单位质量药材中苯甲酰类乌头生物碱煎出量随附子用量增加呈降低趋势。结论:附子中苯甲酰生物碱的煎出率与附子的剂量有密切关系;随着剂量的增加,单味煎出量渐渐变小,而在达到100 g之后较为明显,而附子毒性成分煎出量随着用量的增加其增长值渐渐趋于平缓;因此,在临床使用附子时应正确辨证,合理使用。
关键词附子;剂量;乌头生物碱;含量测定
附子为毛茛科植物乌头AconitumcarmichaeliiDebx.的子根的加工品,主产于四川、陕西等地。生物碱类成分是附子的主要有效成分和毒性成分,包括双酯型、单酯型、氨醇型和其他种类生物碱。其中双酯型生物碱如乌头碱、次乌头碱、新乌头碱等既是主要的有效成分,又是毒性成分。现代研究证实口服乌头碱0.2 mg即发生不良反应,口服3~4 mg即可导致死亡[1]。有关附子临床应用的不良反应常被报道。本研究探究了不同剂量附子在加水量一定时,其水煎液中乌头类生物碱质量分数的变化规律,为临床安全、合理使用附子提供依据。
1药品、试剂与仪器
附子饮片由河南中医学院第一附属医院提供,经药学部陈天朝主任药师鉴定,符合《中国药典》2010版一部附子项下规定。甲醇(色谱纯)和乙腈(色谱纯),均为DIMA TECHNOLOGY INC产品,批号依次为70134,70129;甲醇(色谱纯),天津市四友精细化学品有限公司产品,批号371762-11384;苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱对照品均购自天津马克生物技术有限公司提供,批号依次为:WT-20100704-6、WT-20100704-4、WT-20100704-5、WT-20100704-3、WT-20100704-2、WT-20100704-1。 Waters e2695高效液相色谱仪(在线脱气系统、四元泵、自动进样系统、Waters 2996型二极管阵列检测器),美国Waters公司产品;Sartorius-CP225D十万分之一电子天平,德国赛多利斯公司产品;YFY 13/3A型密闭三连体煎药机,北京华东原医疗设备有限责任公司产品。
2方法与结果
2.1单味附子剂量组设定
通过对医院处方中附子的调查分析可以看出:附子在超剂量使用时,20 g和30 g的使用频次较高,最大使用剂量可数百克。为了使本实验的结果能够给读者直观明了的感觉,简单设定可以明显比较的附子剂量组,使其涵括剂量范围上下差值达200余克,并能够明显看出其变化趋势,设定30 g、50 g、100 g、150 g、200 g、250 g 6组剂量为实验对象。
2.2附子汤液煎煮制备
设定附子30 g、50 g、100 g、150 g、200 g、250 g剂量组,各取其5倍量,即150 g、250 g、500 g、750 g、1 000 g、1 250 g,每组平行3次。将各剂量组附子分别按加水量公式Q=K×W+R+V×T加入自来水[其中Q为加水量(mL),K为吸蓄量(mL/g),W为药物质量(g),R为预期得药量(mL),V为蒸发系数(mL/min),T为煎煮时间(min)]。设定总得液量为2 000 mL(单次每剂服两次,共400 mL)。浸泡30 min后,将附子药材连同浸泡液放入三连体煎药机中,高压密闭加热。从高温(110 ℃)时开始计时,煎煮110 min,其中理论先煎时间为60 min[2],一煎时间为30 min,二煎时间为20 min[3]。因为附子是毒性中药,所以煎煮时间均以上限设定。将煎煮液收集到容器中,放至室温,吸取100 mL,加0.3 g苯甲酸钠混匀,冷藏放置,作为供试品。每剂量组平行试验3次。由于为密闭煎煮,蒸发系数可不考虑,附子吸蓄量测定为0.932 7 mL/g。
2.3色谱条件
AgiLent C18SB-Aq色谱柱(4.6 mm×150 mm,5 μm),流动相为乙腈-0.1 moL/L醋酸铵溶液(每1 000 mL 中加冰醋酸0.5 mL),流速0.4~0.6 mL/min,检测波长235 nm,柱温30 ℃,进样量10 μL。在上述色谱条件下,苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱分离度大于1.5,峰形较好,满足定量要求,混合对照品及50 g附子水煎液色谱图见图1。

1.苯甲酰新乌头原碱;2.苯甲酰乌头原碱;3.苯甲酰次乌头原碱
2.4对照品溶液的制备
分别精密称定苯甲酰新乌头原碱对照品3.78 mg、苯甲酰乌头原碱对照品1.02 mg、苯甲酰次乌头原碱对照品1.94 mg,置同一个50 mL棕色量瓶中,加甲醇定容至刻度,摇匀,即得含苯甲酰新乌头原碱75.6 mg/L、苯甲酰乌头原碱20.4 mg/L和苯甲酰次乌头原碱38.8 mg/L的混合对照品溶液。
2.5供试品溶液的制备
精密吸取2.2项下制备的样品溶液5mL,置10 mL量瓶中,用甲醇定容至刻度,放置后吸取上清液用0.2 μm微孔滤膜过滤,即得。
2.6线性关系的考察
精密移取混合对照品溶液0.5,1.5,2.0,2.5,3.0 mL分别置5 mL容量瓶中,用甲醇定容至刻度,摇匀,配制不同质量分数的混合对照品溶液。吸取上述混合对照品溶液各20 μL注入高效液相色谱仪,按2.3项下方法进行分析。分别以对照品进样量(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线并进行回归计算。结果见表1。
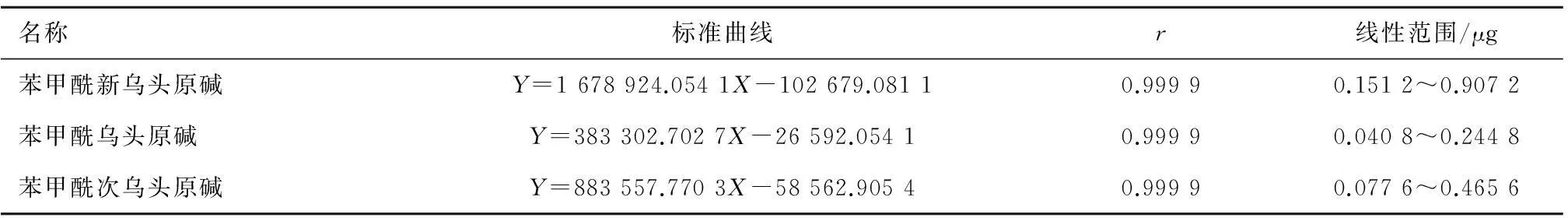
表1 线性范围考察
2.7精密度试验
精密吸取混合对照品溶液10 μL,连续进样5次,记录峰面积。结果:苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱的RSD值分别为0.51%、0.54%、0.65%。结果表明:精密度良好。
2.8重复性试验
取2.2项下制备的同一样品溶液,按2.5项下方法平行制备5份样品溶液,按2.3项下色谱条件进行测定。结果:苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱的平均含量分别为0.139,0.036,0.062 g/L,RSD值依次为0.59%、2.91%、1.17%。结果表明:重复性良好。
2.9稳定性试验
取同一供试品溶液,室温放置,分别于0,2,4,8,16,24 h,按2.3项下方法进样分析。结果:苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱峰面积的RSD值分别为1.03%、1.15%、2.05%。结果表明:供试品溶液在24 h内稳定。
2.10回收率试验
精密吸取已知含量的50 g剂量组附子煎液5.0 mL,置于10 mL量瓶中,加入2.4项下混合对照品溶液适量,按2.3项下方法测定。结果表明回收率良好。
2.11含量测定
按2.5项下制备30,50,100,150,200,250 g组供试品溶液,精密吸取10 μL,注入高效液相色谱仪,按2.3项下条件测定样品含量。结果见表2。同时为了能够更直观地反映在实际使用过程中病人在不同附子剂量下服用的含毒性成分(有效药理成分),分别计算出含毒性成分不同剂量煎煮时的每克药材煎出含量和一般每次服用量,分别见表3和表4。

表2 附子单煎液中苯甲酰类成分质量分数 mg·L-1

表3 单位药材中3种苯甲酰成分煎出含量 mg·L-1

表4 附子单煎液中苯甲酰类成分每次服用量
3讨论
附子属毒性药范畴,对其剂量的使用历来医家都比较谨慎。本实验采用不同视角,以固定实验的条件,只改变附子用量的方法进行研究,主要考察附子中指标性成分受其质量分数的影响。通过研究,初步得出:随着质量分数的增加,附子单煎水煎液中苯甲酰类乌头生物碱煎出增长率逐渐降低;单位质量药材中苯甲酰类乌头生物碱煎出量随附子用量增加呈降低趋势。还可以看出:附子30 g与50 g剂量组的单独煎煮出的单位药材含量相近;随着剂量的增加,单味煎煮出的量渐渐变小,在100 g以后较为明显,这与附子处方在汤剂使用时最高多为100 g,超过100 g时多不为汤剂使用的情况相符。附子毒性成分煎出量随着附子用量的增加渐渐趋于平缓,单位药材煎出量随着剂量增加逐渐下降,30 g剂量组与250 g剂量组变化显著,可能是受到不同剂量煎煮液质量分数的影响,从而限制了部分药物理论上的煎出。附子剂量在30~100 g时受质量分数影响变化不太明显,提示在此剂量段时应谨慎使用。
4参考文献
[1]周金黄.中药药理学[M].上海:上海科学技术出版社,1986.
[2]高学敏.中药学[M].北京:中国中医药出版社,2007.
[3]李财坐.论中药汤剂煎煮与疗效[J].时珍国医国药,1999,40(9):655-655.
(编辑陶珠)
文章编号:1001-6910(2016)05-0070-04·药学研究·
中图分类号:R284
文献标志码:B
doi:10.3969/j.issn.1001-6910.2016.05.34
收稿日期:2015-02-26;修回日期:2016-01-25
