HPLC同时测定地榆升白片中没食子酸和(+)-儿茶素的含量
2016-07-02胡佳王泽宇广兵康敏李鸿翔邓赟
胡佳,王泽宇,广兵,康敏,李鸿翔,邓赟
HPLC同时测定地榆升白片中没食子酸和(+)-儿茶素的含量
胡佳1,王泽宇1,广兵2,康敏1,李鸿翔1,邓赟1
[摘要]目的:建立HPLC同时测定地榆升白片制剂中没食子酸和(+)-儿茶素的含量方法。方法:采用Inertsil ODS-3色谱柱 (250 mm×4.6 mm,5 μm,GL Sciences lnc.),以甲醇-0.05%磷酸为流动相,梯度洗脱;检测波长280 nm;体积流量1 mL.min-1;柱温30 ℃。结果:没食子酸和(+)-儿茶素的线性范围分别为20.82~187.38 μg.mL-1(r=0.9996)、20.90~188.10 μg.mL-1(r=0.9998),平均加样回收率分别为98.99%(RSD=1.88%)和101.09%(RSD =0.58%)。结论:该方法操作简便、灵敏、准确,可作为地榆升白片的质量控制方法。
[关键词]地榆升白片;没食子酸;(+)-儿茶素;高效液相色谱法;含量测定
[作者单位]1. 成都中医药大学药学院 中药材标准化教育部重点实验室 四川省中药资源系统研究与开发利用重点实验室省部共建国家重点实验室培育基地,成都 611137;2.成都地奥制药集团有限公司,成都 610041
Tel:15828612471 Email:627441426@qq.com
Tel:15198277136 Email:15198277136@163.com
赟,男,研究员,博士生导师,主要从事中药化学成分与质量标准化研究
Tel:(028)61800232 Email:dengyun2000@hotmail.com
地榆升白片是由地榆单味药加工制成的片剂,具有升高白细胞的作用,用于白细胞减少症[1]。临床上常作为化疗期间的辅助用药[2],也可用于治疗精神病药所致的白细胞减少症[3]、干扰素治疗乙型肝炎所致的白细胞减少症[4]。处方中地榆是蔷薇科植物地榆Sanguisorba officinalis L.或长叶地榆Sanguisorba officinalis L.Var. longifolia(Bert.)Yü et Li的干燥根,具有凉血止血,解毒敛疮的功效[5]。地榆中主要含有多酚类、皂苷类和黄酮等化学成分,多酚类成分主要有没食子酸、(+)-儿茶素、鞣花酸、没食子儿茶素等[6-8]。2010版《中华人民共和国药典》中地榆药材含量测定项下对没食子酸含量进行了测定。地榆升白片未收录于2010版《中华人民共和国药典》;地榆升白片现有标准收录于《国家中成药标准汇编》,在含量测定项下为采用高效液相色谱法对没食子酸进行含量测定[1]。
现代药理学表明,地榆中所含的没食子酸具有抗肿瘤、抗氧化、抗辐射和抗病原微生物等广泛的药理作用[9];此外地榆中所含另一主要活性成分儿茶素也具有抗肿瘤、抗氧化、抗辐射等作用[10],Takano等[11]研究表明儿茶素对5-氟二氧嘧啶引起的小鼠骨髓抑制所造成的血液毒性有极强的药理作用,能促进其白细胞和血小板数量的恢复和增长,同时提高脾脏指数,具有促进骨髓细胞增殖的作用。石卫民等[12]研究证明儿茶素具有降低辐射对造血组织的损伤,促进造血功能恢复的作用。儿茶素是升高白细胞的确切活性成分,而现有的地榆升白片的含量测定指标仅对没食子酸进行测定。为有效的控制产品质量,本实验首次建立了高效液相色谱法同时测定地榆升白片中没食子酸和儿茶素的含量,该法简便、灵敏、准确,为进一步完善地榆升白片的质量评价体系提供了科学方法和依据。
1 仪器、试药与药品
SSI series 1500高效液相色谱仪(紫外检测器、CSChrom Plus色谱工作站、美国SSI公司);色谱柱Inertsil ODS-3(250 mm×4.6 mm,5 μm,GL Sciences lnc.); KQ-600DE型数控超声波清洗器(40 KHz,600 W,昆山市超声仪器有限公司);十万分之一电子天平(瑞士奥豪斯DV-215-CD);优普UPT系列超纯水器(成都优普电子产品有限公司)。
地榆升白片(批号141215、141111、140811、141208,由成都地奥制药集团有限公司提供);没食子酸对照品(批号:11083-201204,购于中国药品生物制品鉴定所),(+)-儿茶素对照品(批号:110877-201203,购于中国药品生物制品鉴定所)。液相用甲醇为色谱级(美国J.T.Baker),水为超纯水,其余试剂为市售分析级。
2 方法与结果
2.1 色谱条件
Inertsil ODS-3色谱柱(250 mm×4.6 mm,5 μm;GL Sciences Inc.);流动相为甲醇-0.05%磷酸,梯度洗脱(0~18 min,5%~14%;18~50 min,14%~21%;50~53 min,21%~55%;53~55 min,55%~5%;55~65 min,5%);检测波长280 nm;体积流量1 mL.min-1;柱温30 ℃;进样量20 μL。理论塔板数分别按没食子酸和(+)-儿茶素峰计算均应不低于20000。在此色谱条件下,没食子酸和(+)-儿茶素均与样品中其他组分色谱峰达到基线分离,分离度均大于1.5,见图1。
2.2 对照品溶液的制备
分别精密称取没食子酸、(+)-儿茶素对照品适量,置同一量瓶中,5%甲醇稀释至刻度,摇匀,即得混合对照品储备溶液,分别为没食子酸1.041 mg.mL-1、(+)-儿茶素1.045 mg.mL-1。
2.3 供试品溶液的制备
取地榆升白片(批号:141215)40片,除去包衣,精密称定,研细,取约3.0 g,精密称定,精密加入50%甲醇25 mL,称定重量,加热回流1 h,放冷至室温,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
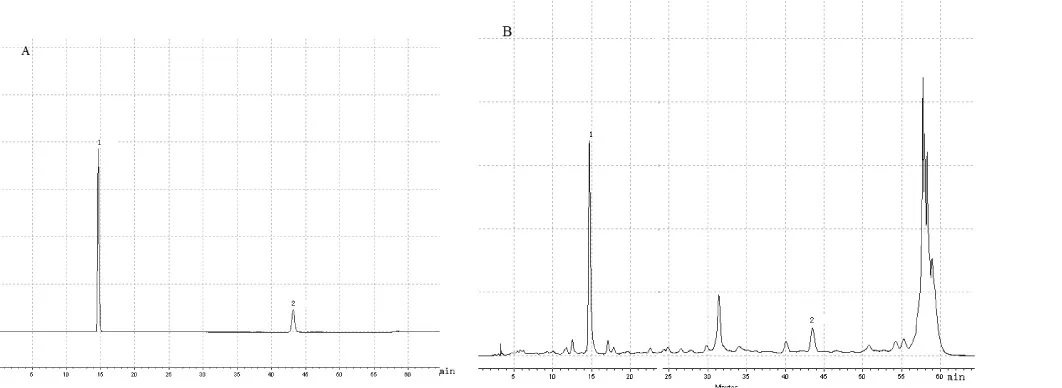
图1 对照品及制剂的HPLC图(1.没食子酸;2. (+)-儿茶素)
2.4 线性关系
检测限和定量限 分别精密吸取“2.2”项下制备的混合对照品贮备溶液适量,加5%甲醇稀释,分别配制成含没食子酸对照品20.82、41.64、83.28、104.10、166.56、187.38 μg.mL-1,含(+)-儿茶素对照品20.90、41.80、83.60、104.50、167.20、188.10 μg .mL-1的混合对照品溶液,在“2.1”项下色谱条件下平行3次测定峰面积,以质量浓度X(μg.mL-1)为横坐标,峰面积值Y为纵坐标,进行线性回归,得混合对照品的标准曲线和各对照品回归方程。将对照品溶液用甲醇不断进行稀释后分析,分别得到没食子酸和(+)-儿茶素的检测限LOD值(S/N≈3)和定量限LOQ值(S/N≈10)。目标化合物的回归方程、相关系数(r)、线性范围、检测限和定量限见表1。结果表明,没食子酸和(+)-儿茶素在线性范围内浓度与峰面积线性关系良好,方法灵敏度高。

表1 地榆升白片中没食子酸和(+)-儿茶素的线性关系(n=3)
2.5 精密度试验
精密吸取同一对照品溶液20 μL,重复进样6次,记录峰面积,结果显示,没食子酸和(+)-儿茶素的峰面积RSD值分别为1.19%、1.44%,说明方法精密度良好。
2.6 稳定性试验
取本品适量,按“2.3”项下方法制备供试品溶液,分别于配制后0、2、4、6、8、12、24、48 h照“2.1”项下色谱条件测定,由峰面积计算稳定性,没食子酸和(+)-儿茶素的RSD分别为1.36%、1.64%。结果表明供试品溶液在48 h内稳定性良好。
2.7 重复性试验
称取同一批地榆升白片(批号:141215)6份,按“2.3”项下方法平行制备6份供试品溶液,按“2.1”项下色谱条件测定,将测定没食子酸和(+)-儿茶素的峰面积代人“2.5”项下的回归方程,计算。结果显示,没食子酸和(+)-儿茶素的RSD分别为1.06%、1.21%,表明方法重复性良好。
2.8 加样回收率试验
精密称取已知含量的样品(批号:141215)共6份各约1.8 g,加入1.2 mL的含没食子酸对照品1.046 mg.mL-1、含(+)-儿茶素对照品1.045 mg.mL-1的对照品溶液,照2.3项下制备,按2.1项色谱条件进行测定,计算回收率,结果见表2。结果表明,没食子酸平均回收率98.99%,RSD为1.88%;(+)-儿茶素平均回收率为101.09%,RSD为0.58%。

表2 没食子酸、(+)-儿茶素的加样回收率(n=6)
2.9 含量测定
取4批地榆升白片制剂,按“2.3”项下方法制备供试品溶液,按“2.1”项色谱条件测定,每批样品平行测定3次,取平均值计算每片地榆升白片的含量,结果见表3。

表3 地榆升白片含量测定结果(n=3)
3 讨论
由于本制剂仅含一味药材,且为原粉入药,预实验发现制剂赋形剂不影响测定,所以供试品溶液的制备考虑采用中成药标准中地榆升白片供试品溶液的制备工艺[1]。
本研究经DAD全波长扫描,(+)-儿茶素除末端吸收外,还有一强吸收带,对应的λ值为280 nm+,与此同时,没食子酸在此条件下也有较好的吸收,故选择280 nm作为同时测定两种成分的检测波长。预实验结果表明HPLC采用等度洗脱的分离效果不理想,故采用梯度洗脱。没食子酸、(+)-儿茶素峰计算理论塔板数均大于20000,没食子酸和(+)-儿茶素与其它杂质峰达到基线分离,分离度大于1.5,可满足定量要求;按此色谱条件选三根不同色谱柱(Inertsil ODS-3,250 mm×4.6 mm;Alltima C18,4.6 mm×250 mm;Kromasil C18,200 mm×4.6 mm)分别测定理论塔板数,结果表明Inertsil ODS-3色谱柱的分离效果较好。分别对2个对照品的检测限和定量限进行测定,结果显示没食子酸和(+)-儿茶素线性范围的下限和测定样品中的量均远高于此定量限,说明此分析方法合理,具有灵敏的定量检测能力。
本文采用高效液相色谱法操作简便,重现性好,能有效控制质量,可作为地榆升白片内控标准的测定方法。
参考文献
[1]国 家药品监督管理局.国家中成药标准汇编(口腔肿瘤儿科分册)[S].标准号:WS-11020(ZD-1020)-2002.
[2]刘 扬帆.地榆升白片预防放疗性白细胞减少症的临床观察[J]. 中国现代药物应用, 2011,5(10):88.
[3]顾冬云.地榆升白片对抗精神病药所致白细胞减少疗效观察[J].中国现代医生,2012,50(36):92.
[4]董 红筠,宓余强,王敬,等.地榆升白片预防性治疗干扰素所致白细胞减少的临床观察[J].中成药,2010,32(2):182.
[5]国 家药典委员会.中华人民共和国药典[S].二部.北京:中国医药科技出版社,2010:117.
[6]曹爱民,张东方,沙明,等.地榆中皂苷类化合物分离、鉴定及其含量测定[J].中草药,2003,34(5):397.
[7]Nonaka G,Tanaka T,Nita M,et al.A dimeric hydrolyzable tannin,sanguiin H-6 from Sanguisorba officinalis L.[J].Chem Pharm Bull,1982,30(6): 2255.
[8]Nonaka G,Tanaka T, Nishioka I.Tannins and related compounds. Part 3. A newphenolic Acid, sanguisorbic acid dilactone, and three new ellagitannins, saguiins H-1, H-2,and H-3 from Sanguisorba officinalis[J].Chem Soc Pekin Trans,1982, 4:1067.
[9]李木涵,殷美琦,冯靖涵,等.没食子酸抗肿瘤作用研究进展[J].中医药信息,2011,28(1):109.
[10]Kusum R,Shambhunath C,Agricola O,et al.Green tea catechin intervention of reactive oxygen species-mediated ERK pathway activation and chronically induced breast cell c arcinogenesis[J].2012,33(1):174.
[11]Takano F,Tanaka T,Aoi J,et al.Protective effect of (+)-catechin against 5-fluorouracil-induced myelosuppression in mice[J]. Toxicology,2004,7:133.
[12]石卫民,赵新萍,芦婷.儿茶素对小鼠的辐射防护作用[J].南方医科大学学报,2006,26(11):1621.
(责任编辑:李芸霞)
·药理毒理·
Simultaneous determination of the contents of gallic acid and (+)-catechin in Diyu Shengbai tablet by HPLC
HUJia1, WANG Ze-yu1, GUANG Bing2, KANG Min1, LI Hong-xiang1, DENG Yun1//(1. School of Pharmacy, Chengdu University of Traditional Chinese Medicine; Key Laboratory of Standardization for Chinese Herbal Medicine, Ministry of Education; National Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan; 2. Chengdu Di'ao Pharmaceutical Group Co. Ltd. Chengdu 610041, Sichuan)
[Abstract]Objective: To establish a method for the simultaneous determination of gallic acid and (+)-catechin in Diyu Shengbai tablet by HPLC. Method: Determination was carried out on Inertsil ODS-3 column (250 mm×4.6 mm, 5 μm, GL Sciences lnc.) with methanol- 0.05 phosphoric acid as mobile phase. The flow rate maintained at 1 mL.min-1. The column temperature was set at 30 ℃. Result: The calibration curve for gallic acid was linear in the range of 20.82~187.38 μg.mL-1, and for (+)-catechin was linear in the range of 20.90~188.10 μg.mL-1. The average recovery of gallic acid was 98.99% (RSD=1.88%),and (+)-catechin was 101.09% (RSD=0.58%). Conclusion: This method is simple, sensitive and accurate which can be used for the quality control of Diyu Shengbai tablet.
[Key words]Diyu Shengbai tablet; gallic acid; (+)-catechin; HPLC; content determination
[中图分类号]R 284.1
[文献标识码]A
[文章编号]1674-926X(2016)02-016-03
[基金项目]国 家科技部新药创制重大专项(2014ZX0920102-008);国家自然基金国家基础科学人才培养项目(J13100340-12);四川省科技厅中药种质资源库建设关键技术研究及示范 2014SZ0156
[作者简介]胡 佳(1991-),女,在读硕士,主要从事中药活性成分方向研究
[通讯作者]李 鸿翔,男,实验师,主要从事中药化学成分物质基质研究
[收稿日期]2015-08-31
